(1z,3z)-4-арил-4-гидрокси-1-(3,3-диалкил-3,4-дигидроизохинолин-1(2н)-илиден)-бут-3-ен-4-оны и способ их получения
Иллюстрации
Показать всеНастоящее изобретение относится к области органической химии, а именно к новым производным 3,4-дигидроизохинолина общей формулы III, где III: R=H, Alk1=Alk2=Me, Ar=Ph (a), Ar=C6H4Me-n (б), Alk1=Me, Alk2=Bu, Ar=Ph (в), Ar=C6H4Me-n (г), R=OMe, Alk1=Alk2=Ме, Ar=Ph (д), Ar=С6Н4Ме-n (e), R=OEt, Alk1=Alk2=Me, Ar=Ph (ж). Также изобретение относится к способу получения соединений общей формулы III, заключающемуся во взаимодействии 6-арил-2,2-диметил-4Н-1,3-диоксин-4-онов с 3,3-диалкил-3,4-дигидроизохинолинами в среде абсолютного толуола при температуре 108-110°С с последующим выделением целевого продукта. Технический результат: получены новые производные 3,4-дигидроизохинолина общей формулы III, проявляющие флуоресцентные свойства, которые устойчивы в УФ-свете. 2 н. и 2 з.п. ф-лы.
Реферат
Изобретение относится к области органической химии, а именно к новым индивидуальным соединениям класса 3,4-дигидроизохинолина, которые проявляют флуоресцентные свойства и могут быть использованы в качестве продуктов для синтеза новых гетероциклических систем, а также в качестве веществ для маркировки образцов и добавок для светоотражающих красок и способу их получения.
Известны различные решения защиты денежных документов, акций, чеков, кредитных карточек, удостоверений личности, паспортов с использованием специальных красок, в частности красок с изменяющимся эффектом, позволяющих, например, переходить от голубого к зеленому цвету в зависимости от наклона документа, или же красок, которые начинают светиться только при определенном облучении, например под действием ультрафиолетового излучения (см. патент США №4175776, МПК B42D 15/00, приоритет 27.11.78 г.). Однако ассортимент этих красок в настоящее время невелик.
Известно использование специальной краски, содержащей отражающую субстанцию и в случае необходимости алюминиевый порошок (см. патент США №4066280, МПК B42D 15/00, приоритет 03.01.78 г.). Недостатком применения этой краски является трудоемкость нанесения на документ, что приводит к ограничению зон ее использования относительно общей площади документа.
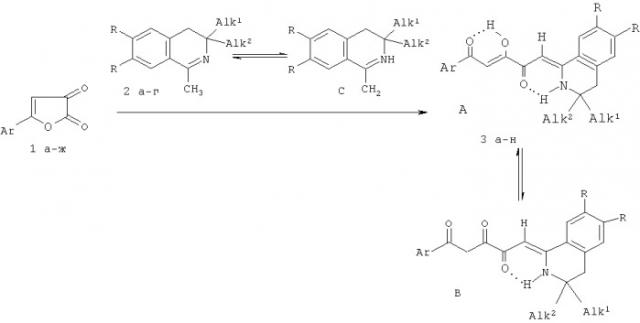
Из литературы известны ближайшие аналоги заявленных соединений - (2Z,5Z)-1-арил-3-гидрокси-5-(3,3-диалкил-3,4-дигидроизохинолин-1(2H)-илиден)-пент-2-ен-1,4-дионы (3а-н), не обладающие флуоресцентными свойствами. Способ получения данных соединений заключается во взаимодействии 5-арилфуран-2,3-дионов (1а-ж) с 3,3-диалкил-1-метил-3,4-дигидроизохинолинами (2а-г) в абсолютном бензоле или абсолютном хлороформе в течение 2-30 минут (В.В.Халтурина, Ю.В.Шкляев, З.Г.Алиев, А.Н.Масливец. ЖОрХ, 2009, 45, 743-748):
1: Ar=Ph (а), С6Н4Ме-n (б), C6H4Cl-n (в), С6Н4ОМе-n (г), C6H4NO2-n (д), C6H4F-n (е), C6H4Br-n (ж); 2: R=Н, Alk1=Alk2=Me (a), Alk1=Me, Alk2=Bu (б), R=OMe, Alk1=Alk2=Me (в), R+R=OCH2CH2O, Alk1=Alk2=Me (г); 3: R=H, Alk1=Alk2=Me, Ar=Ph (a), Ar=С6Н4Ме-n (б), Ar=C6H4Cl-n (в), Ar=C6H4F-n (г), Ar=C6H4Br-n (д), Alk1=Me, Alk2=Bu, Ar=С6Н4Ме-n (e), R=OMe, Alk1=Alk2=Me, Ar=Ph (ж), Ar=С6Н4Ме-n (з), Ar=C6H4Cl-n (и), Ar=С6Н4ОМе-n (к), Ar=C6H4NO2-n (л), Ar=C6H4F-n (м), R+R=OCH2CH2O, Alk1=Alk2=Me, Ar=Ph (н).
К недостаткам данного способа относится невозможность получения аналогичных соединений с боковой цепью из четырех атомов углерода.
Задачей изобретения является разработка способа синтеза (1Z,3Z)-4-арил-4-гидрокси-1-(3,3-диалкил-3,4-дигидроизохинолин-1(2H)-илиден)-бут-3-ен-4-онов (IIIa-ж), проявляющих флуоресцентные свойства, а также расширение арсенала средств, используемых в качестве меток для защиты документов от копирования и добавок в светоотражающие краски.
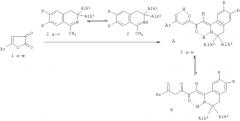
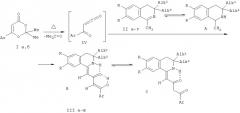
Поставленная задача осуществляется путем кипячения 6-арил-2,2-диметил-4H-1,3-диоксин-4-онов (Ia, б) с 1-метил-3,4-дигидроизохинолинами (IIa-г), взятыми в соотношении 1:1 по схеме:
I: Ar=Ph (a), C6H4Me-n (б); II: R=H, Alk1=Alk2=Me (a), Alk1=Me, Alk2=Bu (б), R=OMe, Alk1-Alk2=Me (в), R=OEt, Alk1=Alk2=Me (г); III: R-H, Alk1=Alk2=Me, Ar=Ph (a), Ar=C6H4Me-n (6), Alk1=Me, Alk2=Bu, Ar=Ph (в), Ar=C6H4Me-n (г), R=OMe, Alk1=Alk2=Me, Ar=Ph (д), Ar=С6Н4Ме-n (e), R=OEt, Alk1=Alk2=Me, Ar=Ph (ж).
Процесс ведут при температуре 108-110°C, а в качестве растворителя используют абсолютный толуол.
Вышеперечисленная совокупность существенных признаков позволяет получить следующий технический результат: простым способом из доступных веществ получены не описанные в литературе соединения класса 3,4-дигидроизохинолина, которые проявляют флуоресцентные свойства и могут быть использованы в качестве продуктов для синтеза новых гетероциклических систем, а также в качестве веществ для маркировки образцов и добавок для светоотражающих красок.
В патентной и технической литературе не были выявлены полезные свойства (3Z)-4-арил-4-гидрокси-1-(1,3,3-триметилиндолин-2-илиден)бут-3-ен-2-онов, а именно не были описаны их флуоресцентные свойства, на основании чего можно сделать вывод о соответствии заявленного технического решения критерию патентоспособности «новизна», «изобретательский уровень» и «промышленная применимость».
Изобретение иллюстрируется следующими примерами.
Пример 1. (1Z,3Z-4-Гидрокси-1-(3,3-диметил-3,4-дигидроизохинолин-1(2H)-илиден)-4-фенилбут-3-ен-2-он (IIIa).
Раствор 2.0 ммоль 2,2-диметил-6-фенил-4H-1,3-диоксин-4-она (Ia) и 2.0 ммоль изохинолина (IIa) в 20 мл абсолютного толуола кипятили 60 мин, охлаждали, выпавший осадок соединения (IIIa) отфильтровывали. Выход 85%, масло.
Найдено, %: C 78.82; H 6.75; N 4.20. C21H21NO2.
Вычислено, %: C 78.97; H 6.63; N 4.39.
Пример 2. (1Z,3Z)-4-Гидрокси-1-(3,3-диметил-3,4-дигидроизохинолин-1(2H)-илиден)-4-(4-толил)бут-3-ен-2-он (IIIб).
Раствор 2.0 ммоль 2,2-диметил-6-(4-толил)-4H-1,3-диоксин-4-она (Iб) и 2.0 ммоль изохинолина (IIa) в 20 мл абсодютного толуола кипятили 60 мин, охлаждали, выпавший осадок соединения (IIIб) отфильтровывали. Выход 86%, масло.
Найдено, %: C 79.24; H 7.15; N 4.02. C22H23NO2.
Вычислено, %: C 79.25; H 6.95; N 4.20.
Пример 3. (1Z,3Z)-4-Гидрокси-1-(3-бутил-3-метил-3,4-дигидроизохинолин-1(2H)-илиден)-4-фенилбут-3-ен-2-он (IIIв).
Раствор 2.0 ммоль 2,2-диметил-6-фенил-4H-1,3-диоксин-4-она (Ia) и 2.0 ммоль изохинолина (IIб) в 20 мл абсолютного толуола кипятили 60 мин, охлаждали, выпавший осадок соединения (IIIв) отфильтровывали. Выход 84%, масло.
Найдено, %: C 79.68; H 7.53; N 3.70. C24H27NO2.
Вычислено, %: С 79.74; H 7.53; N 3.87.
Пример 4. (1Z,3Z)-4-Гидрокси-1-(3-бутил-3-метил-3,4-дигидроизохинолин-1(2H)-илиден)-4-(4-толил)бут-3-ен-2-он (IIIг).
Раствор 2.0 ммоль 2,2-диметил-6-(4-толил)-4H-1,3-диоксин-4-она (Iб) и 2.0 ммоль изохинолина (IIб) в 20 мл абсолютного толуола кипятили 60 мин, охлаждали, выпавший осадок соединения (IIIг) отфильтровывали. Выход 85%. Т.пл. 164-166°C (разл.).
Найдено, %: C 79.85; H 7.83; N 3.59. C25H29NO2.
Вычислено, %: C 79.96; H 7.78; N 3.73.
Пример 5. (1Z,3Z)-4-Гидрокси-1-(3,3-диметил-6,7-диметокси-3,4-дигидроизохинолин-1(2H)-илиден)-4-фенилбут-3-ен-2-он (IIIд).
Раствор 2.0 ммоль 2,2-диметил-6-фенил-4H-1,3-диоксин-4-она (Ia) и 2.0 ммоль изохинолина (IIв) в 20 мл абсолютного толуола кипятили 60 мин, охлаждали, выпавший осадок соединения (IIIд) отфильтровывали. Выход 87%. Т.пл. 142-143°C (разл.).
Найдено, %: C 72.68; H 6.84; N 3.67. C23H25NO4.
Вычислено, %: C 72.80; H 6.64; N 3.69.
Пример 6. (1Z,3Z)-4-Гидрокси-1-(3,3-диметил-6,7-диметокси-3,4-дигидроизохинолин-1(2H)-илиден)-4-(4-толил)бут-3-ен-2-он (IIIе).
Раствор 2.0 ммоль 2,2-диметил-6-(4-толил)-4H-1,3-диоксин-4-она (16) и 2.0 ммоль изохинолина (IIв) в 20 мл абсолютного толуола кипятили 60 мин, охлаждали, выпавший осадок соединения (IIIе) отфильтровывали. Выход 88%. Т.пл. 139-141°C (разл.).
Найдено, %: C 73.25; H 6.94; N 3.53. C24H27NO4.
Вычислено, %: C 73.26; H 6.92; N 3.56.
Пример 7. (1Z,3Z)-4-Гидрокси-1-(3,3-диметил-6,7-диэтокси-3,4-дигидроизохинолин-1(2H-илиден)-4-фенилбут-3-ен-2-он (IIIж).
Раствор 2.0 ммоль 2,2-диметил-6-фенил-4H-1,3-диоксин-4-она (Ia) и 2.0 ммоль изохинолина (IIг) в 20 мл абсолютного толуола кипятили 60 мин, охлаждали, выпавший осадок соединения (IIIж) отфильтровывали. Выход 89%. Т.пл. 133-135°C (разл.).
Найдено, %: C 73.61; H 7.25; N 3.43. C23H29NO4.
Вычислено, %: C 73.69; H 7.17; N 3.44.
В ИК-спектрах (вазелиновое масло) соединений (IIIa-ж) присутствуют полосы валентных колебаний енольной группы ОН и группы NH, участвующих в образовании внутримолекулярных водородных связей (BBC), в виде широкой полосы в области 3384-3417 см-1, карбонильной группы в положении 2, участвующей в образовании ВВС, в виде широкой полосы в области 1582-1591 см-1.
В спектрах ЯМР 1H соединений (IIIa-ж) кроме сигналов протонов ароматических колец и связанных с ними групп присутствуют синглет шести протонов двух метильных групп в положении 3 изохинолинового фрагмента в области 1.27-1.28 м.д. [у соединений (IIIa, б, д-ж)], синглет трех протонов метильной группы при 1.27 м.д. и группа сигналов девяти протонов бутильной группы в положении 3 изохинолинового фрагмента в области 0.96-1.22 м.д. [у соединений (IIIв, г)], синглет двух протонов группы CH2 в положении 4 изохинолинового фрагмента в области 2.82-2.91 м.д., синглет протона группы C1H в области 5.67-5.77 м.д., синглет протона группы C3H в области 6.18-6.28 м.д., синглет протона группы NH в области 10.42-10.57 м.д., синглет протона енольной группы OH в области 16.04-16.07 м.д., относящиеся к кетоенольной форме В соединений (IIIa-ж). Кроме того, в спектрах ЯМР 1H соединений (IIIa-ж) имеются минорные наборы сигналов дикетонной формы С: сигналы протонов ароматических колец и связанных с ними групп, синглет шести протонов двух метильных групп в положении 3 изохинолинового фрагмента в области 1.19-1.20 м.д. [у соединений (IIIa, б, д-ж)], синглет трех протонов метильной группы при 1.24 м.д. и группа сигналов девяти протонов бутильной группы в положении 3 изохинолинового фрагмента в области 0.90-1.16 м.д. [у соединений (IIIв, г)], синглет двух протонов группы CH2 в положении 4 изохинолинового фрагмента в области 2.76-2.86 м.д., синглет двух протонов группы C3H2 в области 4.00-4.10 м.д., синглет протона группы C1H в области 5.76-5.87 м.д., синглет протона группы NH в области 10.95-11.08 м.д. Спектральные характеристики соединений (IIIa-ж) свидетельствуют о их существовании в растворе в ДМСО-d6 в виде смеси кето-енольной формы В и дикетонной формы С в соотношении ~9:1.
Пример 8. Соединения (IIIa-ж) в твердом состоянии обладают устойчивой флуоресценцией (излучение в области зеленого света при λ=530-545 нм) при облучении УФ-лампой, λ 254 нм. Флуоресценция сохраняется при хранении образцов в обычных условиях в течение длительного времени.
Оптическая активность предлагаемых соединений позволяет использовать их в индивидуальном виде и в составах для нанесения флуоресцирующих меток, невидимых при обычном освещении, на денежных купюрах или документах, требующих защиты от кодирования.
В смеси с красителями они могут использоваться для изготовления флуоресцентных красок, свечение которых вызывается УФ и коротковолновым видимым излучением.
Из описания и практического применения настоящего изобретения специалистам будут очевидны и другие частные формы его выполнения. Данное описание и примеры рассматриваются как материал, иллюстрирующий изобретение, сущность которого и объем патентных притязаний определены в нижеследующей формуле изобретения совокупностью существенных признаков и их эквивалентами.
1. (1Z,3Z)-4-Арил-4-гидрокси-1-(3,3-диалкил-3,4-дигидроизохинолин-1(2Н)-илиден)-бут-3-ен-4-оны общей формулы III: R=H, Alk1=Alk2=Me, Ar=Ph (a), Ar=C6H4Me-n (б), Alk1=Me, Alk2=Bu, Ar=Ph (в), Ar=C6H4Me-n (г), R=OMe, Alk1=Alk2=Ме, Ar=Ph (д), Ar=C6H4Me-n (e), R=OEt, Alk1=Alk2=Me, Ar=Ph (ж).
2. Способ получения (1Z,3Z)-4-арил-4-гидрокси-1-(3,3-диалкил-3,4-дигидроизохинолин-1(2Н)-илиден)-бут-3-ен-4-онов общей формулы III: R=H, Alk1=Alk2=Me, Ar=Ph (a), Ar=C6H4Me-n (б), Alk1=Me, Alk2=Bu, Ar=Ph (в), Ar=C6H4Me-n (r), R=OMe, Alk1=Alk2=Me, Ar=Ph (д), Ar=С6Н4Ме-n (е), R=OEt, Alk1=Alk2=Me, Ar=Ph (ж), характеризующийся тем, что 6-арил-2,2-диметил-4Н-1,3-диоксин-4-оны подвергают взаимодействию с 3,3-диалкил-3,4-дигидроизохинолинами в среде абсолютного толуола с последующим выделением целевого продукта.
3. Способ по п.2, отличающийся тем, что процесс ведут при температуре 108-110°С.
4. Способ по п.2, отличающийся тем, что в качестве растворителя используют абсолютный толуол.