Способ повышения точности прогнозирования атриовентрикулярной блокады
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к кардиологии. Выполняют чреспищеводное электрофизиологическое исследование. На левое предсердие наносят серию из девяти импульсов. Восемь из них базовые, St1 отстоят друг от друга на 600 мс. Девятый - экстрастимул, St2, - подают с программируемым интервалом сцепления St1St2. Измеряют время проведения восьмого St1R1 и девятого St2R2 импульсов на желудочки. Далее строят кривую атриовентрикулярного проведения со значениями Y=St2R2-St1R1 и X=St1St2; проводят секущую между точкой с координатами 600:0 и точкой графика с минимальной абсциссой; рассчитывают площадь, ограниченную графиком и секущей. Ширину графика определяют как разность абсцисс крайних его точек, высоту - как ординату точки с наименьшей абсциссой. Вычисляют индекс площади над кривой (ИПК) по оригинальной математической формуле. По полученной величине ИПК прогнозируют наличие атриовентрикулярной блокады. Способ позволяет повысить точность прогнозирования атриовентрикулярной блокады, причем чувствительность метода составляет 81,9%, а специфичность 95,5%. 2 ил.
Реферат
Изобретение относится к медицине, а именно к кардиологии.
Известен способ прогнозирования атриовентрикулярной (АВ) блокады, заключающийся в анализе стандартной электрокардиограммы, выявлении на ней пограничных величин интервала PQ, блокад ножек и ветвей (Орлов В.Н. Руководство по электрокардиографии. М.: Медицина 1983; 526). Для количественной оценки свойств АВ-соединения используют чреспищеводные электрофизиологические исследования (ЧП ЭФИ), в ходе которых определяется его эффективный рефрактерный период (ЭРП) и точка Венкебаха (ТВ) (Чирейкин Л.В., Шубик Ю.Л., Медведев М.М. Чреспищеводная электрокардиография и электрокардиостимуляция. СПб.: ИНКАРТ, 1999; 150). При выявлении величин указанных параметров более 340 мс и менее 120 имп/мин соответственно делают заключение о нарушении атриовентрикулярного проведения.
Недостатки данного способа: недостаточная чувствительность и специфичность, несовпадение результатов определения ЭРП и ТВ, отсутствие общепринятых пороговых значений.
Наиболее близким к заявляемому является способ расчета индекса рефрактерности атриовентрикулярного узла (ИРАВУ) (патент на изобретение №2300311 (RU) “Способ оценки электрических свойств атриовентрикулярного соединения”, от 15.07.2004). Он предусматривает измерение в ходе ЭФИ эффективного и относительного рефрактерных периодов (ЭРП и ОРП) АВ-соединения, минимального и максимального времени проведения (ВПмин и ВПмакс) по нему. Индекс рассчитывается по формуле:
ИРАВУ=(ВПмакс-ВПмин)/(ОРП-ЭРП).
Недостаток этого метода заключается в том, что учитываются только крайние точки АВ-кривой. Две кривые могут существенно отличаться по форме и в то же время иметь сходные значения вышеуказанных параметров, что приводит к потере информации. Кроме того, на графике не всегда удается однозначно выделить ОРП, а ВПмакс не всегда совпадает с последней его точкой.
Техническим результатом изобретения является повышение точности прогнозирования АВ-блокады.
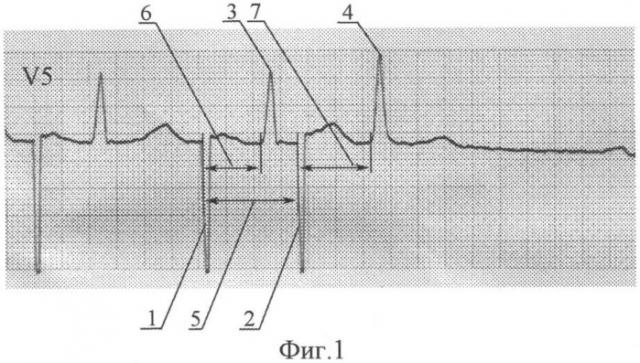
Технический результат достигается тем, что проводимость в атриовентрикулярном соединении оценивают с помощью чреспищеводного электрофизиологического исследования (ЧП ЭФИ) путем вычисления специального разработанного нами индекса. Программированная электрокардиостимуляция левого предсердия с одним экстрастимулом проводится по общепринятой методике (Чирейкин Л.В., Шубик Ю.Л., Медведев М.М. Чреспищеводная электрокардиография и электрокардиостимуляция. СПб.: ИНКАРТ, 1999; 150). После установки зонда в пищевод наносится серия из девяти импульсов, восемь из которых (базовые, St1 - Фиг.1.1), отстоят друг от друга на 600 мс, а девятый (экстрастимул, St2 - Фиг.1.2) подается преждевременно, с программируемым интервалом сцепления (St1St2 - Фиг.1.5). На ЭКГ измеряют время проведения восьмого (St1R1 - Фиг.1.6) и девятого (St2R2 - Фиг.1.7) импульсов на желудочки. Вычитая St1R1 из St2R2, получают корригированное время проведения для конкретного St1St2. В ходе исследования наносят несколько серий (обычно 25 - 35) с постепенно уменьшаемым интервалом сцепления, начиная от 600 мс до минимального эффективного (то есть проводимого на желудочки), с шагом в 10 мс. Получаемые корригированные St2R2 в декартовой системе координат (ось Y) соотносят с St1St2 (ось X).
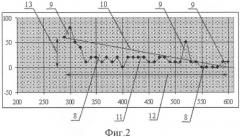
После построения графика полного (Фиг.2.11) проводят секущую (Фиг.2.10), соединяющую начало кривой (точку 600:0) с ее концом (ответ на экстрастимул с самым коротким интервалом сцепления). С помощью разработанной нами компьютерной программы рассчитывают площадь, очерченную кривой и секущей. При этом площадь между графиком снизу и прямой сверху (Фиг.2.8) соответствует положительной части изучаемого параметра. Фрагменты кривой, находящиеся выше секущей (Фиг.2.9), образуют негативную часть и вычитаются из основного значения. Полученная величина делится на ширину графика (Фиг.2.12) и на его высоту (Фиг.2.13) и выражается в процентах. Нормальные значения указанного индекса площади над кривой (ИПК) лежат выше уровня 10%. Обнаружение у пациента более низких значений ИПК позволяет прогнозировать в дальнейшем выявление атриовентрикулярной блокады I-II степени с чувствительностью 81.9% и специфичностью 95.5%.
Пример использования методики
Больной К. 1956 года рождения госпитализирован в кардиологическое отделение с диагнозом: Гипертоническая болезнь II стадии, риск ССО III. Ожирение алиментарно-конституциональное 2 степени. Жаловался на тяжесть в голове, эпизодическое головокружение, при осмотре отмечено повышение АД до уровня 160/100-170/100 мм рт. ст., частота пульса 60-65 уд/мин. Больной принимал конкор 5 мг на ночь, престариум 4 мг на ночь. На ЭКГ синусовый ритм, нормограмма, ЧСС 61 уд/мин, величина интервала PQ=180 мс. Выполнено ЧП ЭФИ. Тип АВ-проведения непрерывный, ЭРП АВ-соединения 330 мс, точка Венкебаха 120 имп/мин. Площадь над кривой составила 2150 мс2 при ширине зоны стимуляции 260 мс и высоте графика 90 мс, ИПК 9.2%. При дальнейшем суточном мониторировании ЭКГ выявлено 15 случаев АВ-блокады II степени с периодикой Венкебаха, паузами до 2400 мс. По результатам обследования конкор был отменен, что привело к улучшению самочувствия.
Больная П. 1945 года рождения госпитализирована в кардиологическое отделение с диагнозом: ИБС, стабильная стенокардия ФК2, кардиосклероз диффузный, Н2А ФК2. Жаловалась на слабость, эпизодическое головокружение, при осмотре АД 150/90-130/80, ЧСС 55-60 уд/мин. Принимала арифон 2.5 мг утром, тромбо-асс 100 мг утром, диротон 5 мг вечером. На ЭКГ синусовый ритм, ЭОС горизонтальная, ЧСС 57 уд/мин, величина интервала PQ=200 мс. Выполнено ЧП ЭФИ. Тип АВ-проведения непрерывный, ЭРП АВ=350 мс, точка Венкебаха 120 имп/мин. Площадь над кривой составила 1650 мс2 при ширине зоны стимуляции 240 мс и высоте графика 80 мс, ИПК=8.6%. В ходе суточного мониторирования выявлена АВ-блокада I степени с PQ до 240 мс, блокированная наджелудочковая экстрасистолия с максимальной паузой 2450 мс. Продолжено консервативное лечение. При повторном ЭФИ через 6 месяцев площадь над кривой - 4600 мс2 при ширине графика 250 мс и высоте 100 мс, ИПК=-18.4%. Во время суточного мониторирования выявлена АВ-блокада II степени 2:1, блокированная наджелудочковая экстрасистолия, максимальная пауза 3150 мс. В связи с появлением предобморочных состояний больная направлена на имплантацию электрокардиостимулятора.
Использование предложенного способа прогнозирования позволяет рационально использовать лекарственные препараты, влияющие на АВ-проводимость; проводить динамическое наблюдение за кондуктивными свойствами АВ-соединения у конкретного больного; обоснованно выбирать место стимуляции при имплантации электрокардиостимулятора.
АВТОРЫ: Глуховский Михаил Леонидович, Злуникин Геннадий Евгеньевич.
Описание к фигурам “Способ повышения точности прогнозирования атриовентрикулярной блокады”
Фигура 1. “Элементы ЭКГ, получаемые в ходе электрофизиологического исследования”. Отведение V5, вольтаж 10 мм/мВ, скорость записи 50 мм/с.
1.1. Восьмой стимул (St1).
1.2. Экстрастимул (St2).
1.3. Желудочковый ответ на восьмой стимул (R1).
1.4. Желудочковый ответ на экстрастимул (R2).
1.5. Интервал сцепления экстрастимула (St1St2).
1.6. Время проведения базового стимула (St1R1).
1.7. Время проведения экстрастимула (St2R2).
Фигура 2. “Элементы кривой атриовентрикулярного проведения”. По оси Y интервалы сцепления в мс, по оси Y корригированные интервалы АВ-проведения в мс.
2.8. Площадь над кривой, положительные части.
2.9. Площадь над кривой, отрицательные части.
2.10. Секущая.
2.11. Кривая атриовентрикулярного проведения.
2.12. Ширина кривой.
2.13. Высота кривой.
Способ повышения точности прогнозирования атриовентрикулярной блокады, включающий выполнение чреспищеводного электрофизиологического исследования, отличающийся тем, что на левое предсердие наносят серию из девяти импульсов, восемь из которых базовые St1 отстоят друг от друга на 600 мс, а девятый - экстрастимул St2 подают с программируемым интервалом сцепления St1St2, измеряют время проведения восьмого St1R1 и девятого St2R2 импульсов на желудочки, строят кривую атриовентрикулярного проведения со значениями St2R2-St1R1 по оси Y и St1St2 по оси X; проводят секущую между точкой с координатами 600:0 и точкой графика с минимальной абсциссой; рассчитывают площадь над кривой, вычитая из площади между графиком и секущей фрагменты кривой, находящиеся выше секущей; ширину графика определяют как разность абсцисс крайних его точек, а высоту - как ординату точки с наименьшей абсциссой; индекс площади над кривой (ИПК) вычисляют по формуле: при полученной величине менее 10% прогнозируют наличие атриовентрикулярной блокады с чувствительностью 81,9% и специфичностью 95,5%.