Косметическое средство
Иллюстрации
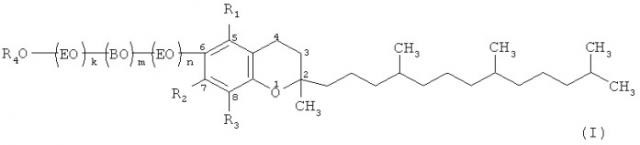
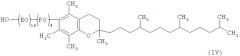
Показать всеИзобретение относится к косметологии и представляет собой косметическое средство, содержащее производное витамина Е в качестве солюбилизирующего агента, представленное приведенной ниже формулой (I), или его соль:
где R1, R2 и R3 независимо представляют собой атом водорода или метильную группу; R4 представляет собой атом водорода, алканоильную группу, имеющую от 1 до 6 атомов углерода, алкильную группу, имеющую от 1 до 6 атомов углерода, группу SO3H, группу Р(O)(ОН)2, группу СН2СООН или группу СОСН2CH(SO3H)COOH; ЕО представляет собой этиленоксидную группу; ВО представляет собой бутиленоксидную группу; k и n независимо представляют собой любое из чисел от 0 до 30 (однако k и n одновременно не принимают значение 0); и m представляет собой любое из чисел от 0 до 30 и компоненты, которые обычно применяются в косметических средствах. Изобретение обеспечивает отсутствие липкости во время высыхания после нанесения на кожу, а также улучшение солюбилизирующей и эмульгирующей способностей. 2 н. и 5 з.п. ф-лы, 5 табл., 1 ил.
Реферат
СООТВЕТСТВУЮЩИЕ ЗАЯВКИ
В данной заявке испрашивается приоритет на основании Японской патентной заявки №2006-350365, поданной 26 декабря 2006, которая включена в данное описание посредством ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к косметическим средствам, содержащим производное витамина Е или его соль. Более конкретно настоящее изобретение относится к косметическим средствам, которые не обладают липкостью (в частности, липкостью во время высыхания после нанесения на кожу) и вызывают великолепные ощущения при применении и которые могут содержать большое количество и разнообразие смешиваемых масляных компонентов в результате улучшения солюбилизирующей способности и эмульгирующей способности.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
В последние годы синтезированы различные производные витамина Е, и они предложены в качестве антиоксидантного компонента и компонента, сохраняющего влагу. Конкретные примеры включают сложные эфиры витамина Е с серной кислотой (см. публикацию выложенной патентной заявки (Kokai) №55-13214), полиэтоксилированный витамин Е (см. публикацию выложенной патентной заявки (Kokai) №5-194474 и №11-35577), полиоксипропилен-полиоксиэтилен-витамин Е (см. публикацию выложенной патентной заявки (Kohyo) №2002-517389) и полиоксипропилен-полиоксиэтилен-витамин Е с присоединенной функциональной группой (см. публикацию выложенной патентной заявки (Kokai) №2003-277392). В литературе (Kokai №2003-277392) это соединение было также предложено в качестве солюбилизирующего агента, в котором часть, включающая витамин Е, и полиоксипропиленовая часть являются гидрофобными группами, а полиоксиэтиленовая часть является гидрофильной группой.
Эти общепринятые производные витамина Е удовлетворительно функционируют в качестве антиоксидантного компонента или компонента, удерживающего влагу. Однако их функции в качестве солюбилизирующего агента или эмульгатора все же неудовлетворительны, и реально их нельзя применять в качестве косметического сырья.
Кроме того, желательно, чтобы жидкое косметическое средство и т.д. не вызывало ощущения липкости во время высыхания после нанесения на кожу и вызывало наилучшие ощущения при применении.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ПРОБЛЕМА, КОТОРАЯ ДОЛЖНА БЫТЬ РЕШЕНА ИЗОБРЕТЕНИЕМ
Авторы настоящего изобретения провели тщательные исследования по решению вышеописанных общепринятых проблем и по разработке производного витамина Е, обладающего как антиоксидантной активностью, так и великолепным свойством удерживания влаги, а также значительно лучшей эмульгирующей способностью и солюбилизирующей способностью. В результате авторы настоящего изобретения обнаружили, что производные витамина Е, имеющие гидрофобные группы бутиленоксида и гидрофильные группы этиленоксида в качестве заместителя в положении 6 хроманового каркаса витамина Е, обладают равной или более высокой антиоксидантной активностью и свойством удерживания влаги по сравнению с вышеописанными общепринятыми производными витамина Е. По сурфактантным качествам, таким как эмульгирующая способность и солюбилизирующая способность, они также обладают значительно более высокой активностью и эффектом по сравнению с общепринятыми производными витамина Е. Кроме того, авторы настоящего изобретения обнаружили, что они обладают в высшей степени превосходным эффектом в жидком косметическом средстве и т.д., который заключается в уменьшении ощущения липкости на коже (в частности, ощущения липкости во время высыхания после нанесения на кожу), что, таким образом, приводит к выполнению настоящего изобретения.
СПОСОБЫ РЕШЕНИЯ ПРОБЛЕМЫ
Таким образом, в настоящем изобретении предложены косметические средства, содержащие производное витамина Е или его соль, которое представлено приведенной ниже формулой (I):
где R1 R2 и R3 независимо представляют собой атом водорода или метильную группу; R4 представляет собой атом водорода, алканоильную группу, имеющую от 1 до 6 атомов углерода, алкильную группу, имеющую от 1 до 6 атомов углерода, группу SO3H, группу Р(O)(ОН)2, группу CH2COOH или группу СОСН2СН(SO3H)СООН; ЕО представляет собой этиленоксидную группу; ВО представляет собой бутиленоксидную группу; k и n независимо представляют собой любое из чисел от 0 до 30 (однако k и n одновременно не принимают значение 0); и m представляет собой любое из чисел от 1 до 30.
В настоящем изобретении предложены вышеописанные косметические средства, в которых R1, R2 и R3 в формуле (I) представляют собой метильные группы.
В настоящем изобретении предложены вышеописанные косметические средства, в которых R1 и R3 в формуле (I) представляют собой метильные группы и R2 представляет собой атом водорода.
В настоящем изобретении предложены вышеописанные косметические средства, в которых R1 в формуле (I) представляет собой атом водорода, a R2 и R3 представляют собой метильные группы.
В настоящем изобретении предложены вышеописанные косметические средства, в которых R1 и R2 в формуле (I) представляют собой атомы водорода, а R3 представляет собой метильную группу.
В настоящем изобретении предложены вышеописанные косметические средства, в которых R4 в формуле (I) представляет собой атом водорода.
В настоящем изобретении предложены вышеописанные косметические средства, в которых R4 в формуле (I) представляет собой алканоильную группу, имеющую от 1 до 6 атомов углерода, алкильную группу, имеющую от 1 до 6 атомов углерода, группу SO3H, группу Р(O)(ОН)2, группу СН2СООН или группу СОСН2СН(SO3 Н)СООН.
Кроме того, в настоящем изобретении предложен солюбилизирующий агент, который включает производное витамина Е, представленное вышеописанной формулой (I), или его соль.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
В соответствии с настоящим изобретением ощущение липкости на коже (в частности, ощущение липкости во время высыхания после нанесения на кожу) может быть заметно уменьшено при поддержании значительно лучшей эмульгирующей способности и солюбилизирующей способности, а также сохранении как антиоксидантной активности, так и отличных свойств удерживания влаги. Кроме того, могут быть предложены косметические средства, вызывающие великолепные ощущения при применении, такие как ощущение легкой свежести, ощущение впитывания и сродства к коже.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Чертеж представляет собой график, который иллюстрирует сравнение эффекта удерживания влаги для примеров продукции 1, 3 и 6 и сравнительных примеров 1, 2 и 3, которые были использованы в примерах.
ЛУЧШИЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Далее настоящее изобретение описано подробно.
Косметические средства по настоящему изобретению содержат производное витамина Е, представленное приведенной ниже формулой (I), или его соль.
В вышеописанной формуле (I) соответствующие заместители являются такими, как описано ниже. В формуле ЕО представляет собой этиленоксидную группу и ВО представляет собой бутиленоксидную группу.
R1, R2 и R3 независимо представляют собой атом водорода или метильную группу. В качестве предпочтительной комбинации R1, R2 и R3 можно перечислить комбинацию, в которой R1, R2 и R3 представляют собой метильные группы (5,7,8-триметильная форма, в случае которой исходный витамин Е представляет собой α-токоферол); комбинацию, в которой R1 и R3 представляют собой метильные группы и R2 представляет собой атом водорода (5,8-диметильная форма, в случае которой исходный витамин Е представляет собой β-токоферол); комбинацию, в которой R1 представляет собой атом водорода, a R2 и R3 представляют собой метильные группы (7,8-диметильная форма, в случае которой исходный витамин Е представляет собой γ-токоферол), и комбинацию, в которой R1 и R2 представляют собой атомы водорода и R3 представляет собой метильную группу (8-метильная форма, в случае которой исходный витамин Е представляет собой δ-токоферол).
R4 представляет собой атом водорода, алканоильную группу, имеющую от 1 до 6 атомов углерода, алкильную группу, имеющую от 1 до 6 атомов углерода, группу SO3H, группу Р(O)(ОН)2, группу СН2СООН или группу СОСН2СН(SO3H)СООН.
Вышеописанная алканоильная группа, имеющая от 1 до 6 атомов углерода, может быть либо нормальной, либо разветвленной. Конкретные примеры включают ацетильную группу, пропаноильную группу, бутирильную группу, изобутирильную группу и пивалоильную группу. Среди них предпочтительны ацетильная группа, пропаноильная группа и пивалоильная группа, а ацетильная группа более предпочтительна с точки зрения синтеза.
Вышеописанная алкильная группа, имеющая от 1 до 6 атомов углерода, может быть либо нормальной, либо разветвленной. Конкретные примеры включают метильную группу, этильную группу, пропильную группу, бутильную группу, изобутильную группу, трет-бутильную группу, пентильную группу и гексильную группу. Среди них предпочтительны метильная группа, этильная группа, пропильная группа и бутильная группа, а метильная группа и этильная группа более предпочтительны с точки зрения синтеза.
Группа SO3H, группа Р(O)(ОН)2, группа СН2СООН или группа COCH2 СН(SO3H)СООН может образовать соль с основанием. Основание не имеет особых ограничений, если токсичность является низкой, а антиоксидантная активность и свойство удерживания влаги производного витамина Е, представленного вышеописанной формулой (I), не подвергнуты воздействию. Примеры таких солей включают соли щелочных металлов, такие как натриевая соль, калиевая соль и литиевая соль; соли щелочноземельных металлов, такие как кальциевая соль и магниевая соль; соли металлов, такие как алюминиевая соль, железная соль, цинковая соль, медная соль, никелевая соль и кобальтовая соль; и неорганические соли, такие как аммонийная соль; соли органических аминов, такие как соль трет-октиламина, соль дибензиламина, соль морфолина, соль глюкозамина, соль алкилового эфира фенилглицина, соль этилендиамина, соль N-метилглюкамина, соль гуанидина, соль диэтиламина, соль триэтиламина, соль дициклогексиламина, соль N,N′-дибензилэтилендиамина, соль хлорпрокаина, соль прокаина, соль диэтаноламина, соль N-бензилфенетиламина, соль пиперазина, соль тетраметиламмония и соль трис(гидроксиметил)аминометана. Однако основание не ограничено этими примерами. Среди них соли щелочных металлов, соли щелочноземельных металлов и аммонийная соль предпочтительны с точки зрения синтеза. Более предпочтительными солями являются натриевая соль, калиевая соль, полумагниевая соль, полукальциевая соль и аммонийная соль, а натриевая соль и аммонийная соль более предпочтительны.
В настоящем изобретении, с точки зрения солюбилизирующей способности, наиболее предпочтительно, чтобы R4 в формуле (I) представлял собой группу SO3Н или группу Р(O)(ОН)2 и чтобы они находились в солевой форме.
Символы k и n соответственно представляют собой любое из чисел от 0 до 30. Предпочтительно они равны от 0 до 25 и более предпочтительно от 0 до 20 (однако k и n одновременно не принимают значение 0). Символ m представляет собой любое из чисел от 1 до 30, предпочтительно от 1 до 10 и более предпочтительно от 1 до 5. Наиболее предпочтительной комбинацией k, m и n является комбинация, в которой k и n соответственно равны от 0 до 20 (однако k и n одновременно не принимают значение 0) и m равно от 1 до 5.
В настоящем изобретении соединение, представленное вышеописанной формулой (I), имеет асимметрический атом углерода в молекуле, и существуют стереоизомеры, а именно D-форма и L-форма. Каждый из них и все их произвольные смеси включены в настоящее изобретение.
Когда соединению, представленному вышеописанной формулой (I), дают возможность стоять в атмосфере, оно может абсорбировать воду, адсорбировать воду или образовать гидрат. Эти случаи также включены в настоящее изобретение.
Кроме того, соединение, представленное вышеописанной формулой (I), может абсорбировать некоторые другие растворители и образовать сольват. Эти случаи также включены в настоящее изобретение.
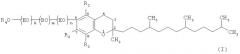
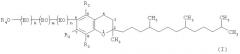
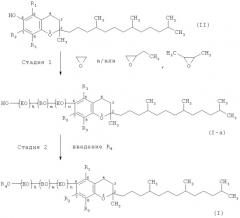
Производные витамина Е или их соли, представленные вышеописанной формулой (I), могут быть получены, например, способом, представленным на приведенной ниже схеме реакций.
(Стадия 1) На стадии 1 производное витамина Е (спиртовую форму), представленное вышеописанной формулой (I-а), получают путем присоединения этиленоксида и/или бутиленоксида в присутствии основного катализатора к витамину Е, представленному вышеописанной формулой (II) [в этой формуле R1, R2 и R3 соответственно являются такими, как определено для вышеописанной формулы (I)].
Что касается витамина Е, можно использовать либо синтетические, либо натуральные витамины Е. Конкретные примеры включают α-токоферол (5,7,8-триметильную форму), в котором R1, R2 и R3 представляют собой метильные группы в вышеописанной формуле (II); β-токоферол (5,8-диметильную форму), в котором R1 и R3 представляют собой метильные группы, a R2 представляет собой атом водорода; γ-токоферол (7,8-диметильную форму), в котором R2 и R3 представляют собой метильные группы, а R1 представляет собой атом водорода; и δ-токоферол (8-метильную форму), в котором R3 представляет собой атом водорода, а R1 и R2 представляют собой метильные группы. В настоящем изобретении предпочтительно можно использовать имеющиеся в продаже продукты, например натуральный витамин Е (например, D-α-токоферол, изготавливаемый фирмой Sigma-Aldrich Japan K.K.) и синтетический витамин Е (например, DL-α-токоферол, изготавливаемый фирмой Wako Pure Chemical Industries, Ltd.).
Примеры основных катализаторов (= щелочных катализаторов), используемых в реакции присоединения, включают гидроксиды щелочных металлов, такие как гидроксид натрия и гидроксид калия; алкоксиды щелочных металлов, такие как метоксид натрия и трет-бутоксид калия; гидриды металлов, такие как гидрид натрия и гидрид алюминия; и гидроксиды четвертичного аммония, такие как гидроксиды четвертичного триметиламмония. Среди них предпочтительно используют гидроксид калия, гидроксид натрия и т.д. из-за того, что с ними проще обращаться.
Количество основного катализатора варьирует в зависимости от условий реакции и не ограничено конкретно. В целях подавления побочных реакций, однако, предпочтительно обычно использовать от 0,05 до 10 масс.% по отношению к витамину Е, который является исходным веществом, и более предпочтительно использовать от 0,05 до 5 масс.%.
Вышеописанную реакцию присоединения проводят в присутствии или в отсутствие растворителя. Реакция в присутствии растворителя более предпочтительна с точки зрения уменьшения вязкости всей реакционной системы.
Используемый растворитель не ограничен конкретными веществами, поскольку он не участвует в реакции присоединения. Примеры включают ароматические углеводороды, такие как толуол, ксилол и бензол; алифатические углеводороды, такие как гексан, гептан и октан; алициклические углеводороды, такие как циклогексан и циклогептан; циклические эфиры, такие как тетрагидрофуран и диоксан; эфиры, такие как диэтиловый эфир, диизопропиловый эфир, этиленгликоля диметиловый эфир, этиленгликоля диэтиловый эфир и диэтиленгликоля диметиловый эфир; амиды, такие как диметилформамид и диметилацетамид; и сульфоксиды, такие как диметилсульфоксид. Однако растворитель не ограничен этими примерами. Среди них предпочтительно используют ароматические углеводороды, алициклические углеводороды, циклические эфиры, эфиры и т.д.
Этиленоксид и/или бутиленоксид обычно впрыскивают. Бутиленоксид, предпочтительно используемый в настоящем изобретении, представляет собой 1,2-бутиленоксид или 2,3-бутиленоксид.
Температура впрыска и температура реакции (температура выдерживания) обычно составляет от комнатной температуры до 200°С, предпочтительно от 50 до 200°С и более предпочтительно от 80 до 180°С. Время реакции (время выдерживания) варьирует в зависимости от температуры реакции; обычно оно составляет от 1 до 24 часов, предпочтительно от 1 до 12 часов и более предпочтительно от 1 до 10 часов.
После реакции реакционный раствор охлаждают, и использованное основание (катализатор) нейтрализуют кислотой. Примеры кислот включают минеральные кислоты, такие как соляная кислота, серная кислота, азотная кислота, бромисто-водородная кислота и фосфорная кислота; и органические кислоты, такие как метансульфоновая кислота, этансульфоновая кислота, уксусная кислота и пара-толуолсульфоновая кислота. Однако кислота не ограничена этими примерами. Среди них предпочтительно используют соляную кислоту, серную кислоту, фосфорную кислоту, метансульфоновую кислоту, уксусную кислоту и т.д., и более предпочтительно соляную кислоту, фосфорную кислоту, метансульфоновую кислоту, уксусную кислоту и т.д.
После нейтрализации желаемый продукт получают путем общепринятой обработки, например, путем добавления воды и нерастворимого в воде органического растворителя, экстрагирования, высушивания и последующего удаления органического растворителя. Когда образовавшаяся соль нерастворима, желаемый продукт может быть также получен путем фильтрования соли и удаления органического растворителя. При необходимости полученное желаемое соединение, а именно соединение, представленное формулой (I-а), можно очистить путем перекристаллизации, переосаждения или разделения хроматографией на силикагеле и т.д.
(Стадия 2) Соединение, полученное, как описано выше, и представленное формулой (I-а), представляет собой производное витамина Е (спиртовую форму), в котором R4 представляет собой атом водорода в формуле (I) настоящего изобретения.
Соединение, представленное вышеописанной формулой (I-а), может быть преобразовано путем введения по желанию заместителя R4 (однако R4 является иным, чем атом водорода) в производное, в которое вводят алканоильную группу, имеющую от 1 до 6 атомов углерода, алкильную группу, имеющую от 1 до 6 атомов углерода, группу SO3H, группу Р(O)(ОН)2, группу СН2СООН, группу СОСН2СН(SO3H)СООН или ее соль. Введение вышеописанного заместителя R4 можно проводить в соответствии с описанными ниже способами (1)-(6). Однако способ не ограничен этими примерами.
(1) Алканоильную группу, имеющую от 1 до 6 атомов углерода, вводят путем взаимодействия с хлорангидридом или ангидридом в присутствии основания и либо в присутствии, либо в отсутствие растворителя.
Предпочтительные примеры оснований включают органические основания, такие как триэтиламин, диизопропилэтиламин, пиридин, 4-диметиламинопиридин, 1-метилпиперазин, 4-метилморфолин, 1,4-диметилпиперазин и 1-метилпирролидин.
Растворитель не ограничен конкретными веществами, поскольку он не участвует в реакции присоединения. Примеры включают ароматические углеводороды, такие как толуол, ксилол и бензол; алифатические углеводороды, такие как гексан, гептан и октан; алициклические углеводороды, такие как циклогексан и циклогептан; циклические эфиры, такие как тетрагидрофуран и диоксан; эфиры, такие как диэтиловый эфир, диизопропиловый эфир, этиленгликоля диметиловый эфир, этиленгликоля диэтиловый эфир и диэтиленгликоля диметиловый эфир; амиды, такие как диметилформамид и диметилацетамид; и сульфоксиды, такие как диметилсульфоксид. Однако растворитель не ограничен этими примерами. Среди них предпочтительно используют ароматические углеводороды, алициклические углеводороды, циклические простые эфиры, простые эфиры и т.д.
Примеры хлорангидридов включают миристиновый хлорангидрид, пальмитиновый хлорангидрид и стеариновый хлорангидрид. Примеры ангидридов включают малеиновый ангидрид и уксусный ангидрид. Однако примеры не ограничены хлорангидридом и ангидридом.
Температура реакции варьирует в зависимости от используемых хлорангидридов и ангидридов; обычно она составляет от -20°С до 100°С, предпочтительно от 0 до 100°С и более предпочтительно от 0 до 50°С.
Время реакции варьирует в зависимости от температуры реакции; обычно оно составляет от 1 до 24 часов, предпочтительно от 1 до 8 часов и более предпочтительно от 1 до 4 часов.
После завершения реакции желаемый продукт получают путем общепринятой обработки, например, путем добавления воды и нерастворимого в воде растворителя, нейтрализации по необходимости, экстракции, высушивания и последующего удаления растворителя. Когда образовавшаяся соль нерастворима, желаемый продукт может быть также получен путем фильтрования соли и удаления растворителя. При необходимости полученное желаемое соединение может быть очищено путем перекристаллизации, переосаждения или разделения хроматографией на силикагеле и т.д.
(2) Алкильную группу, имеющую от 1 до 6 атомов углерода, вводят путем взаимодействия с алкилгалогенидом в присутствии основания и либо в присутствии, либо в отсутствие растворителя.
Предпочтительные примеры оснований включают гидроксиды щелочных металлов, такие как гидроксид натрия и гидроксид калия; алкоксиды щелочных металлов, такие как метоксид натрия и трет-бутоксид калия; гидриды металлов, такие как гидрид натрия и гидрид алюминия; и гидроксиды четвертичного аммония, такие как гидроксиды четвертичного триметиламмония.
Растворитель не ограничен конкретными веществами, поскольку он не участвует в реакции присоединения, и предпочтительно можно использовать растворители, перечисленные в вышеописанном параграфе (1).
Примеры алкилгалогенидов включают метилхлорид и этилбромид. Однако алкилгалогениды не ограничены этими примерами.
Температура реакции варьирует в зависимости от используемого алкилгалогенида; обычно она составляет от -20°С до 100°С, предпочтительно от 0 до 100°С и более предпочтительно от 0 до 50°С.
Время реакции варьирует в зависимости от температуры реакции; обычно оно составляет от 1 до 24 часов, предпочтительно от 1 до 8 часов и более предпочтительно от 1 до 4 часов.
После завершения реакции желаемый продукт получают путем общепринятой обработки, например, путем добавления воды и нерастворимого в воде растворителя, нейтрализации по необходимости, экстрагирования, высушивания и последующего удаления растворителя. Когда образовавшаяся соль нерастворима, желаемый продукт может быть также получен путем фильтрования соли и удаления растворителя. При необходимости полученное желаемое соединение может быть очищено путем перекристаллизации, переосаждения или разделения хроматографией на силикагеле и т.д.
(3) Группу SO3H вводят путем взаимодействия с сульфаминовой кислотой или серным ангидридом в присутствии мочевины и либо в присутствии, либо в отсутствие растворителя.
Растворитель не ограничен конкретными веществами, поскольку он не участвует в реакции присоединения, и можно использовать растворители, перечисленные в вышеописанном параграфе (1).
Температура реакции обычно составляет от -20°С до 100°С, предпочтительно от 0 до 100°С и более предпочтительно от 0 до 50°С.
Время реакции варьирует в зависимости от температуры реакции; обычно оно составляет от 1 до 24 часов, предпочтительно от 1 до 8 часов и более предпочтительно от 1 до 4 часов.
После завершения реакции желаемый продукт получают путем общепринятой обработки, например, путем добавления воды и нерастворимого в воде растворителя, нейтрализации по необходимости, экстрагирования, высушивания и последующего удаления растворителя. Когда образовавшаяся соль нерастворима, желаемый продукт может быть также получен путем фильтрования соли и удаления растворителя. При необходимости полученное желаемое соединение может быть очищено путем перекристаллизации, переосаждения или разделения хроматографией на силикагеле и т.д.
(4) Группу Р(O)(ОН)2 вводят путем взаимодействия с пентаоксидом дифосфора (= фосфорным ангидридом) или полифосфорной кислотой либо в присутствии, либо в отсутствие растворителя.
Растворитель не ограничен конкретными веществами, поскольку он не участвует в реакции присоединения, и можно предпочтительно использовать растворители, перечисленные в вышеописанном параграфе (1).
Температура реакции варьирует в зависимости от того, используют ли пентаоксид дифосфора или полифосфорную кислоту; обычно она составляет от комнатной температуры до 200°С, предпочтительно от комнатной температуры до 150°С.
Время реакции варьирует в зависимости от температуры реакции; обычно оно составляет от 1 до 24 часов, предпочтительно от 1 до 8 часов и более предпочтительно от 1 до 4 часов.
После завершения реакции желаемый продукт получают путем общепринятой обработки, например, путем добавления воды и нерастворимого в воде растворителя, нейтрализации по необходимости, экстрагирования, высушивания и последующего удаления растворителя. Когда образовавшаяся соль нерастворима, желаемый продукт может быть также получен путем фильтрования соли и удаления растворителя. При необходимости полученное желаемое соединение может быть очищено путем перекристаллизации, переосаждения или разделения хроматографией на силикагеле и т.д.
(5) Группу СН2СООН вводят путем взаимодействия с алкилмонохлорацетатом или алкилмонобромацетатом в присутствии основания либо в присутствии, либо в отсутствие растворителя, и путем последующего щелочного гидролиза эфирной группы.
Примеры оснований включают гидроксиды щелочных металлов, такие как гидроксид натрия и гидроксид калия; алкоксиды щелочных металлов, такие как метоксид натрия, метоксид калия, этоксид натрия, этоксид калия и трет-бутоксид калия; и гидриды металлов, такие как гидрид натрия и гидрид алюминия. Более предпочтительно используют алкоксиды щелочных металлов.
Растворитель не ограничен конкретными веществами, поскольку он не участвует в реакции присоединения. Однако предпочтительны спирты, такие как метанол, этанол, пропанол, бутанол, трет-бутанол; циклические эфиры, такие как тетрагидрофуран и диоксан; и амиды, такие как диметилформамид и диметилацетамид. Растворитель, однако, не ограничен этими примерами. Среди них более предпочтительны спирты, такие как метанол, этанол, пропанол, бутанол и трет-бутанол.
Температура реакции конкретно не ограничена; обычно она составляет от комнатной температуры до 100°С, предпочтительно от комнатной температуры до 80°С и более предпочтительно от комнатной температуры до 50°С.
Время реакции варьирует в зависимости от температуры реакции; обычно оно составляет от 1 до 24 часов, предпочтительно от 1 до 12 часов и более предпочтительно от 1 до 8 часов.
Стадию, на которой эфирную группу преобразуют в карбоновую кислоту или карбоксилатную соль путем щелочного гидролиза, можно осуществить с использованием водного раствора гидроксида щелочного металла, такого как гидроксид натрия или гидроксид калия.
После завершения реакции рН доводят до 2-4 с использованием кислоты, такой как соляная кислота, серная кислота или фосфорная кислота. Карбоновая кислота может быть получена путем экстракции растворителем, высушивания и удаления растворителя.
В качестве экстракционного растворителя предпочтительны галогенированные углеводороды, такие как метиленхлорид и хлороформ; ароматические углеводороды, такие как толуол, ксилол и бензол; сложные эфиры, такие как этилацетат и метилацетат; и простые эфиры, такие как диэтиловый эфир и диизопропиловый эфир. Среди них даже более предпочтительны галогенированные углеводороды.
Полученное желаемое соединение можно использовать как таковое на следующей стадии. Однако, если необходимо, соединение может быть очищено общепринятым способом, таким как перекристаллизация, переосаждение или разделение хроматографией на силикагеле и т.д.
(6) Группу СОСН2СН(SO3H)СООН вводят путем реакции этерификации с малеиновым ангидридом в присутствии каталитического количества ацетата натрия и путем последующего взаимодействия с водным раствором сульфита натрия.
Температура реакции этерификации обычно составляет от 50 до 200°С, предпочтительно от 60 до 150°С и более предпочтительно от 70 до 100°С.
Температура реакции с водным раствором сульфита натрия обычно составляет от 50 до 200°С, предпочтительно от 60 до 150°С и более предпочтительно от 70 до 100°С.
Соединения, полученные в вышеописанных п.п.(3), (4), (5) и (6), могут быть преобразованы по необходимости в желаемую соль с использованием основания общепринятым способом.
Свойство удержания влаги и антиоксидантная активность производных витамина Е по настоящему изобретению сравнимы с таковыми для витамина Е или общепринятых производных витамина Е, предложенных в патентной литературе 1-5, или являются более высокими. Однако свойства в качестве сурфактанта, такие как свойства эмульгирующего или солюбилизирующего агента, лучше, чем для общепринятых производных витамина Е, благодаря введению гидрофобных бутиленоксидных групп. Соответственно, когда производное витамина Е, представленное вышеописанной формулой (I), смешивают с косметическими средствами, можно повысить разнообразие и количественный уровень смешиваемых дополнительных масляных компонентов. Конкретно смешиваемое количество масляного компонента можно повысить примерно в 1,2-1,5 раза по сравнению с количеством в случае использования общепринятого производного витамина Е.
Следует также отметить великолепный эффект, состоящий в отсутствие ощущения липкости (в частности, в отсутствие ощущения липкости во время высыхания после нанесения на кожу). Потребность в этом эффекте давно ощущалась в прошлом, в частности, для жидкого косметического средства и т.д. Продукт по настоящему изобретению можно также применять в качестве эмульгатора или солюбилизирующего агента в фармацевтических препаратах, косметических изделиях и т.д.
Смешиваемое количество производного витамина Е, представленного вышеописанной формулой (I), или его соли в косметических продуктах конкретно не ограничено. Однако при его применении в качестве эмульгатора или солюбилизирующего агента предпочтительно смешиваемое количество, сравнимое с таковым для неионного сурфактанта или ионного сурфактанта, обычно используемого в качестве эмульгатора или солюбилизирующего агента. Более конкретно, предпочтительно количество от 0,01 до 5,0 масс.% по отношению к суммарному количеству косметического изделия, и более предпочтительно оно составляет от 0,05 до 3,0 масс.%.
При изготовлении косметических средств с применением производного витамина Е, представленного вышеописанной формулой (I), или его соли возможно произвольно смешивать другие дополнительные компоненты, которые обычно можно смешивать в косметических средствах в такой мере, чтобы эффект настоящего изобретения не был подвергнут негативному влиянию. Конкретные примеры таких компонентов включают сурфактанты, масла, загустители, увлажнители, поглотители ультрафиолетовых лучей, рассеиватели ультрафиолетовых лучей, лекарства, ароматизаторы, красители и стабилизирующие агенты. Однако дополнительные компоненты не ограничены этими примерами.
Неионные сурфактанты включают алкиловые эфиры ПОЭ (= полиоксиэтилен), такие как ПОЭ цетиловый эфир (ПОЭ 7), ПОЭ цетиловый эфир (ПОЭ 10), ПОЭ олеиловый эфир (ПОЭ 6), ПОЭ олеиловый эфир (ПОЭ 10), ПОЭ стеариловый эфир (ПОЭ 6), ПОЭ олеиловый эфир (ПОЭ 8), ПОЭ лауриловый эфир (ПОЭ 5), ПОЭ гексилдециловый эфир (ПОЭ 5), ПОЭ изостеариловый эфир (ПОЭ 5), ПОЭ октилдодециловый эфир (ПОЭ 5), ПОЭ децилпентадециловый эфир (ПОЭ 10), ПОЭ бегениловый эфир (ПОЭ 10), ПОЭ децилтетрадециловый эфир (ПОЭ 10) и ПОЭ холестериловый эфир (ПОЭ 10); алкилфениловые эфиры ПОЭ, такие как ПОЭ нонилфениловый эфир (ПОЭ 5), ПОЭ октилфениловый эфир (ПОЭ 5) и т.д.; слеараты алкиловых эфиров ПОЭ, такие как ПОЭ стеарилового эфира стеарат (ПОЭ 12), ПОЭ лаурилового эфира стеарат (ПОЭ 10), ПОЭ лаурилового эфира стеарат (ПОЭ 15) и ПОЭ лаурилового эфира изостеарат (ПОЭ 10); эфиры этиленгликоля с жирной кислотой/полиэтиленгликоль, такие как этиленгликоля дилаурат/полиэтиленгликоль (ПОЭ 8), этиленгликоля дилаурат/полиэтиленгликоль (ПОЭ 12), этиленгликоля моностеарат/полиэтиленгликоль (ПОЭ 5), этиленгликоля дистеарат/полиэтиленгликоль (ПОЭ 12) и этиленгликоля диолеат/полиэтиленгликоль (ПОЭ 12); эфиры полиэтиленгликоля и жирной кислоты, такие как полиэтиленгликоля изостеарат (ПОЭ 6), полиэтиленгликоля диизостеарат (ПОЭ 12) и полиэтиленгликоля моноолеат (ПОЭ 6); ПОЭ глицериловые эфиры жирных кислот, такие как ПОЭ глицерилизостеарат (ПОЭ 5), ПОЭ глицерилизостеарат (ПОЭ 6) и ПОЭ глицерилизостеарат (ПОЭ 8); ПОЭ глицериловые эфиры с тремя жирными кислотами, такие как ПОЭ глицерилтриизостеарат (ПОЭ 20), ПОЭ глицерилтриолеат (ПОЭ 20) и ПОЭ глицерилтриизостеарат (ПОЭ 7); ПОЭ эфиры триметилолпропана с тремя жирными кислотами, такие как ПОЭ триметилолпропантримиристат (ПОЭ 20), ПОЭ триметилолпропантриизостеарат (ПОЭ 20), ПОЭ триметилолпропантриизостеарат (ПОЭ 20), ПОЭ триметилолпропантриизостеарат (ПОЭ 25) и ПОЭ триметилолпропантриизостеарат (ПОЭ 30); ПОЭ-гидрогенизированные касторовые масла и их производные, такие как ПОЭ-гидрогенизированное касторовое масло (ПОЭ 20), ПОЭ касторовое масло (ПОЭ 20), ПОЭ-гидрогенизированного касторового масла лаурат (ПОЭ 20), ПОЭ-гидрогенизированного касторового масла изостеарат (ПОЭ 20), ПОЭ-гидрогенизированного касторового масла изостеарат (ПОЭ 30), ПОЭ-гидрогенизированного касторового масла триизостеарат (ПОЭ 40) и ПОЭ-гидрогенизированного касторового масла триизостеарат (ПОЭ 50); ПОЭ глицеринмоностеарат (ПОЭ 5); сорбитан-моноизостеарат; глицеринмоностеарат (самоэмульгирующий); диглицерилмоностеарат и цетостеарилглицозид.
Ионные сурфактанты включают алкилфосфат, такой как натрия лаурилфосфат и лаурилфосфат; ПОЭ алкиловых эфиров фосфаты, такие как ПОЭ (1) лаурилового эфира фосфат и натрия лаурилфосфат; соли N-ацилтаурина, такие как натрия N-кокоил N-метилтаурат, натрия N-лауроил N-метилтаурат, натрия N-миристоил N-метилтаурат, натрия N-пальмитоил N-метилтаурат и натрия N-стеароил N-метилтаурат; алкилсульфаты, такие как аммония лаурилсульфат, калия лаурилсульфат, натрия лаурилсульфат, триэтаноламина лаурилсульфат, натрия миристилсульфат и натрия цетилсульфат; ПОЭ алкилового эфира сульфат, такой как натрия ПОЭ (3 моль) алкил (C12-15) эфира сульфат, триэтаноламина ПОЭ (3 моль) алкил (C12-15) эфира сульфат, аммония ПОЭ (2 моль) лаурилового эфира сульфат, натрия ПОЭ (2 моль) лаурилового эфира сульфат, триэтаноламина ПОЭ (2 моль) лаурилового эфира сульфат, натрия ПОЭ (3 моль) лаурилового эфира сульфат и натрия ПОЭ (2 моль) лаурилового эфира сульфат; и сульфонаты, такие как натрия лаурилсульфоацетат, натрия тетрадеценсульфонат и диоктилнатрия сульфосукцинат.
Амфолитические сурфактанты включают амфолитические сурфактанты бетаинацетатного типа, такие как лаурилдиметиламиноуксусной кислоты бетаин, кокосового масла жирной кислоты амид пропилдиметиламиноуксусной кислоты бетаин кокосового масла жирной кислоты амид пропилдиметиламиноуксусной кислоты бетаин; и амфолитические сурфактанты имидазолинового типа, такие как натрия N-кокосового масла жирной кислоты ацил-N-карбоксиметил-N-гидроксиэтилэтилендиамин.
Масла включают эфирные масла, такие как трипропиленгликоля динеопентаноат, изодецилбензоат, пропиленгликоля дикаприлат, изононилизононаноат, цетил-2-этилгексаноат, глицерил-три-2-этилгексаноат, пентаэритрит-тетра-2-этилгексаноат, ди-2-этилгексилсукцинат и 2-этилгексил-2-этилгексаноат; углеводородные масла, такие как жидкий вазелин, озоцерит, сквалан, пристан, парафин, церезин, сквален, вазелин, микрокристаллический воск, полиэтиленовый воск и воск Фишера-Тропша; силиконовые масла, такие как цепочечные полисилоксаны (например, диметилполисилоксан, метилфенилполисилоксан, дифенилполисилоксан и т.д.), циклические полисилоксаны (например, декаметилциклопентаполисилоксан, додекаметилциклогексаполисилоксан и т.д.), силиконовые смолы, имеющие трехмерную сетчат