3,5-дизамещенные фенилпиперидины в качестве модуляторов нейротрансмиссии допамина
Иллюстрации
Показать всеИзобретение относится к новым соединениям формулы 1:
,
где R выбран из группы, состоящей из C1-С3алкилов, и к их фармацевтически приемлемым солям.
Изобретение также относится к фармацевтической композиции.
Технический результат - получение новых биологически активных соединений, которые обладают активностью модулятора нейротрансмиссии допамина. 2 н. и 14 з.п. ф-лы, 2 табл.
Реферат
Область изобретения
Настоящее изобретение относится к новым модуляторам нейротрансмиссии допамина и, более конкретно, к новым дизамещенным фенил-пиперидинам и их применению.
Предшествующий уровень техники
Допамин является нейротрансмиттером в мозге. После этого открытия, сделанного в 1950-х годах, функцию допамина в мозге активно исследовали. В настоящее время окончательно установлено, что допамин жизненно важен в нескольких аспектах функции мозга, включая моторную, когнитивную, сенсорную, эмоциональную и автономную функции (например, регуляция аппетита, температура тела, сон). Таким образом, модулирование допаминергической функции полезно в лечении множества разных расстройств, поражающих функции мозга. В действительности лекарственные средства, которые прямо или опосредованно действуют на центральные рецепторы допамина, широко применяются в лечении неврологических и психиатрических расстройств, например болезни Паркинсона и шизофрении. Однако доступные в настоящее время допаминергические фармацевтические препараты могут оказывать тяжелые побочные эффекты. Например, известно, что антагонисты допамина вызывают как моторные (эктрапирамидные побочные эффекты, EPS), так и ментальные побочные эффекты (например ангедонию, дисфорию и ухудшение когнитивной способности), и известно, что допаминергические агонисты вызывают дискинезии и психозы (Goodman and Gilman's the Pharmacological Basis of Therapeutics, 9th ed./McGraw-Hill, USA. Chapter 18, pp.407-416, Chapter 22, pp.509-512, pp.515-516).
Подход, выбранный многими исследователями для повышения эффективности и снижения побочных эффектов допаминергических фармацевтических препаратов, состоит в разработке новых лигандов рецепторов допамина, проявляющих селективность в отношении конкретных подтипов рецепторов допамина или региональную селективность. Еще один класс соединений, действующих через допаминовые системы мозга, составляют допаминергические стабилизаторы, которые, как было показано, полезны в лечении как неврологических, так и психиатрических расстройств (А.Ekesbo, PhD Thesis, Uppsala University, Sweden: Functional consequences of dopaminergic degeneration; clinical and experimental studies using a novel stabilizer of dopaminergic systems: Ekesbo et al., (-)-OSU6162 inhibits levodopa-induced dyskinesias in a monkey model of Parkinson's disease, Neuroreport, 8, 2567, 1997; Tedroff et al. Long-lasting improvement in motor function following (-)-OSU6162 in a patient with Huntington's disease. Neurology, 22:53:1605-6, 1999; Gefvert O. et al., (-)-OSU6162 induces a rapid onset of antipsychotic effect after a single dose. A double-blind placebo-controlled pilot study. Scandinavian Society for Psychopharmacology, 41st Annual Meeting, Copenhagen Denmark Nordic Journal of Psychiatry 54/2 93-94, April 2000: Carlsson et al., Annu. Rev. Pharmacol. Toxicol., 41, 237, 2001; Carlsson et al. Current Medicinal Chemistry, 11, 267, 2004).
Другим допаминергическим соединением, о котором сообщалось как о стабилизаторе допамин-серотониновой системы, а также как о частичном агонисте DA D2-рецепторов, является недавно выпущенное антипсихотическое соединение арипипразол (Burris et al., Pharm. Exp.Ther, vol. 302, 381, 2002). Соединения, являющиеся допаминергическими стабилизаторами, описаны также в WO 01/46145; WO 01/46146; Pettersson et al. The development of ACR16. A new class of dopaminergic stabilizers. Society for Neuroscience 32nd Annual Meeting, Abstract 2002, Vol.28 part 1 1028, Orlando USA, 2002, и Nyberg et al., Efficacy and tolerability of the new dopamine stabiliser ACR16 a randomised placebo-controlled add-on study in patients with schizophrenia, 12th BIENNIAL WINTER WORKSHOP ON SCHIZOPHRENIA, 7-13 February 2004, Davos, Switzerland.
Типичные фармакологические эффекты, характерные для допаминергических стабилизаторов, описанных в WO 01/46145, WO 01/46146 and Pettersson et al. 2002, можно суммировать как 1) усиление обратного захвата допамина в терминальных областях восходящих допаминергических проекций мозга млекопитающего, 2) отсутствие или только слабые поведенческие эффекты у крыс, не подвергавшихся лечению иным способом, и 3) ингибирование у крыс поведенческих эффектов, индуцированных психостимуляторами или психотомиметическими соединениями. В настоящем изобретении это называется профилем допаминергического стабилизатора.
Известно, что некоторые фармацевтически активные соединения, которые применяются в лечении неврологических и психиатрических расстройств (особенно антипсихотические соединения и соединения-антидепрессанты), могут оказывать нежелательные эффекты на те сердечные калиевые каналы, которые вовлечены в электрическую реполяризацию клеток сердца и которые обычно называются hERG-каналами (потенциал-зависимый калиевый канал, кодируемый геном ether-a-go-go человека) или 1 кг (быстро активируемый калиевый ток задержанного выпрямления). Лекарственные средства, которые блокируют эти каналы, могут вызывать желудочковую аритмию (двунаправленную желудочковую тахикардию, TdP), приводящую к внезапной смерти у здоровых во всех других отношениях субъектов. Признаком того, что лекарственное средство, возможно, оказывает нежелательные эффекты на реполяризацию сердца, является удлинение интервала QT на электрокардиограмме, которое считают суррогатным маркером риска TdP. Многие лекарственные средства были изъяты из продажи из-за неприемлемых побочных эффектов, относящихся к сердечной аритмии (J. Cardiovasc. Electrophysiol. 15, 475, 2004.; Eur. J. Pharm., 450, 37, 2002.; Cardiovascular Research, 58, 32, 2003).
Данное изобретение относится к области лечения млекопитающих, страдающих расстройствами ЦНС, у которых симптомы могут быть обусловлены допаминергическими функциями, где лечение включает введение указанному млекопитающему определенного количества соединения нового типа с профилем допаминергического стабилизатора. Кроме того, указанные соединения проявляют низкую аффинность к сердечным калиевым каналам, снижая риск серьезных кардиотонических побочных эффектов.
Описание предшествующего уровня техники
Ранее сообщалось о соединениях класса замещенных 4-(фенил)-N-алкил-пиперидинов. Среди этих соединений некоторые неактивны в ЦНС, некоторые проявляют серотонинергические или смешанные серотонинергические/допаминергические фармакологические свойства, а некоторые являются полными или неполными агонистами или антагонистами допаминовых рецепторов с высокой аффинностью к допаминовым рецепторам.
Известен целый ряд производных 4-фенил-пиперидина. В ЕР 0369887 раскрыты замещенные 4-(мета-трифторметилфенил)-1,2,3,6-тетрагидропиридины для лечения тревоги. В WO 00/03713 раскрыт способ лечения шизофрении и других дисфункций допаминовой системы с использованием замещенных 1-метил-4-фенил-1,2,3,6-тетрагидропиридинов.
Glennon et al. (патент США 6057371) заявляют способ лечения связанного с сигма-рецепторами расстройства ЦНС, включающий введение ариламинов, в том числе арилпиперидинов, которые либо не замещены, либо моно-замещены по арильному кольцу. Соединения проявляют высокую аффинность связывания с сигма-рецепторами. В WO 91/095954 утверждается, что термин «высокая аффинность» означает, что соединение демонстрирует IC50 менее 100 нМ в анализе против 3Н-DTG, описанном в Weber et al. Proc. Natl. Acad. Sci. (USA) 83: 8784-8788. В частности, в WO 91/095954 раскрыты композиции, относящиеся к «открытию, что определенные производные фенилалкил-амина, аминотетралина, пиперазина, пиперидина и родственных соединений проявляют высокую степень связывания с сигма-рецептором и неожиданно низкую степень связывания с РСР (фенциклидиновым) и DA (допаминовым) рецепторами» (смотри с.11, строки 33-36).
И в WO 91/095954, и в WO 93/00313 указано, что соединения должны иметь высокую аффинность связывания с сигма-рецептором, но не сообщается, что соединения фамакологически активны в отсутствие аффинности к сигма-рецепторам. Кроме того, клинические испытания, направленные на исследование свойств лигандов сигма-рецепторов у пациентов с шизофренией, не свидетельствуют ни об антипсихотической активности, ни об активности при любом другом расстройстве ЦНС. Два из наиболее всесторонне исследованных селективных антагонистов сигма-рецепторов, BW234U (Римказол) и BMY14802, не прошли клинические испытания у пациентов с шизофренией (Borison et al., 1991, Psychopharmacol Bull 27(2): 103-106; Gewirtz et al., 1994, Neuropsychopharmacology 10:37-40).
В WO 97/23216 раскрыты аналоги 4-замещенного пиперидина формулы:
в которой R5 может быть выбран из ОН, а Ar1 может быть замещенным. Такие соединения применяют для лечения травм ЦНС, психоза и нейродегенеративных расстройств посредством, среди прочего, селективной блокады подтипов рецепторов NMDA (N-метил-D-аспарагиновая кислота).
В US 4485109 раскрыты соединения формулы:
которые применяются в качестве психотерапевтических агентов, в частности в качестве антидепрессантов.
В ЕР 1177792 среди прочих раскрыты соединения, имеющие структуру:
,
обладающие допаминергической активностью, в частности активностью лигандов D4-рецепторов, и полезны для лечения расстройств, характеризующихся поиском новизны.
В WO 98/51668 раскрыты производные замещенного пиперидина формулы:
,
которые обладают свойствами ингибиторов обратного захвата моноаминного нейротрансмиттера, то есть допамина, серотонина, норадреналина. Указано, что эти соединения полезны в лечении паркинсонизма, депрессии, псевдодеменции, ожирения, нарколепсии, наркомании и/или злоупотребления лекарственными средствами, синдрома дефицита внимания с гиперактивностью, сенильной деменции или нарушений памяти.
Известно также, что соединения формул II (WO 01/46145) и III (WO 01/46146) обладают свойствами допаминергических стабилизаторов.
В формуле I:
Х представляет собой, среди прочего, СН; R1 выбран из группы, состоящей из OSO2CF3, OSO2CH3, SOR3, SO2R3, COR3, CN, NO2, CONHR3, CF3 (при условии, что Х представляет собой СН или С), F, Cl, Br, I (где R3 определен ниже);
R2 выбран из группы, состоящей из С1-С4алкила, аллила, CH2SCH3, CH2CH2OCH3, CH2CH2CH2F, CH2CF3, 3,3,3-трифторпропила, 4,4,4-трифторбутила или -(CH2)-R4 (где R4 определен ниже);
R3 выбран из группы, состоящей из С1-С3алкила, CF3 или N(R2)2;
R4 выбран из группы, состоящей из С3-С6циклоалкила, 2-тетрагидрофурана, 3-тетрагидрофурана.
В формуле II:
Х представляет собой, среди прочего, СН; R1 выбран из группы, состоящей из OSO2CF3, OSO2CH3, SOR7, SO2R7, COR7, CN, NO2, CONHR3, CF3, F, Cl, Br, I (где R3 определен ниже), 3-тиофена, 2-тиофена, 3-фурана, 2-фурана;
R2 выбран из группы, состоящей из F, Cl, Br, I, CN, CF3, СН3, ОСН3, ОН, NH2;
R3 и R4 независимо представляют собой Н или С1-C4алкил;
R5 выбран из группы, состоящей из С1-С4алкила, аллила, CH2SCH3, CH2CH2OCH3, CH2CH2CH2F, CH2CF3, 3,3,3-трифторпропила, 4,4,4-трифторбутила или -(CH2)-R6;
R6 выбран из группы, состоящей из С3-С6циклоалкила, 2-тетрагидрофурана, 3-тетрагидрофурана;
R7 выбран из группы, состоящей из C1-С3алкила, CF3 или N(R4)2.
Однако ни в WO 01/46145 (Формула I), ни в WO 01/46146 (Формула II) не приведены фармакологические данные для 3,5-дизамещения в фенольном кольце, раскрытого в настоящем изобретении. Приведенная ниже структура известна из примера синтеза, приведенного в WO 01/46146 (Пример 44. 4-[3-фтор-5-(трифторметил)фенил-]1-пропилпиперидин):
Кроме того, ни в WO 01/46145 (Формула I), ни в WO 01/46146 (Формула II) нет никаких указаний для получения эффективных допаминергических стабилизаторов.
Сохраняется потребность в новых фармацевтически активных соединениях, в частности полезных в лечении расстройств центральной нервной системы, обладающих повышенной эффективностью в качестве допаминергических стабилизаторов. Желательно также, чтобы любое такое фармацевтически активное соединение оказывало меньше побочных эффектов, в частности, относящихся к сердечной аритмии.
Краткое описание сущности изобретения
Задача настоящего изобретения заключается в том, чтобы предоставить новые фармацевтически активные соединения, в частности, полезные в лечении расстройств центральной нервной системы, обладающие повышенной эффективностью в качестве допаминергических стабилизаторов (смотри Таблицу 1, колонка 1) с низкой склонностью к блокированию hERG-канала (смотри Таблицу 1, колонка 2). Эти соединения имеют определенные преимущества, относящиеся к уменьшению побочных эффектов, в частности сердечных побочных эффектов.
Согласно настоящему изобретению 3,5-дизамещение неожиданно повышает силу действия и эффективность по сравнению с альтернативными картинами замещения (например, 3,4-дизамещение, где в положении 4 находится галоген) или монозамещением (в положении 3). Кроме того, соединения по настоящему изобретению проявляют пониженную аффинность к hERG-каналу по сравнению с соединениями предшествующего уровня техники.
Вещества по настоящему изобретению были испытаны в биологических тестах на крысах, и было обнаружено, что они действуют преимущественно на допаминергические системы в мозге. Они воздействуют на биохимические показатели в мозге с характерными признаками антагонистов допамина. Однако вещества по изобретению не оказывают ингибирующего воздействия на спонтанную двигательную активность в широком диапазоне доз. Кроме того, вещества по изобретению могут вызывать легкую поведенческую активацию, особенно когда исходная двигательная активность незначительна. Однако вещества по настоящему изобретению ингибируют поведенческую активацию, вызванную психостимуляторами и психотомиметиками.
Вещества по настоящему изобретению проявляют низкую эффективность ингибирования hERG-канала, которую определяли по значениям IC50 в анализе Rapid ICE (подробности изложены в экспериментальном разделе), что указывает на низкий риск удлинения интервала QT и аритмии у человека.
Подробное описание изобретения
Настоящее изобретение относится к новым пиперидинам в форме свободного основания или их фармацевтически приемлемых солей, к фармацевтическим композициям, содержащим указанные соединения, и к применению указанных соединений в изготовлении фармацевтических препаратов, являющихся нейротрансмиттерами допамина, и в терапии.
Более точно, настоящее изобретение относится к соединениям пиперидина формулы 1;
,
где R выбран из группы, состоящей из C1-С3алкилов и аллила, и их фармацевтически приемлемым солям.
В конкретных воплощениях R выбран из группы, состоящей из н-пропила и этила.
Еще один аспект изобретения относится к способу лечения расстройств центральной нервной системы путем введения терапевтически активного количества соединения формулы 1 или его фармацевтически приемлемой соли млекопитающему, включая человека, страдающему расстройством центральной нервной системы. Дополнительно, настоящее изобретение относится к способу лечения любых расстройств, перечисленных в данном описании, путем введения терапевтически активного количества соединения формулы 1 или его фармацевтически приемлемой соли млекопитающему, включая человека, страдающему указанным расстройством.
Наличие двух заместителей на арильном кольце таких соединений - одного в положении 3 (мета 1), а другого в положении 5 (мета 2) - повышает их эффективность модулирования нейротрансмиссии допамина. Беспрецедентное увеличение эффективности этих 3,5-дизамещенных соединений по сравнению с монозамещенными или 3,4-дизамещенными соединениями иллюстрируется в Таблице 1.
Обнаружено также, что 3,5-дизамещение в соединениях по настоящему изобретению снижает побочные эффекты, относящиеся к сердечной аритмии, которые определяют по воздействию этих соединений на hERG калиевый канал (Rapid Ice). Беспрецедентное снижение побочных эффектов таких замещенных соединений иллюстрируется в Таблице 1.
| Таблица 1 | ||
| Влияние соединений по настоящему изобретению на снижение индуцированной амфетамином гиперлокомоции (значения ED50) и афинность к hERG ионного канала (значения IC50). Включены также примеры из предшествующего уровня техники. Методы и статистические вычисления смотри в прилагаемых тестах | ||
| ED50 амф* мкмоль/кг | Rapid ICE (IC50, нМ) | |
| Сравнительные примеры | ||
| 52 | Не тестировали | |
| 34 | 610 | |
| 14 | 1500 | |
| Примеры | ||
| 12 | 9800 | |
| 28 | 21670 | |
| * Эффекты соединений по настоящему изобретению, относящиеся к снижению вызванной амфетамином гиперлокомоции. Включены также примеры из предшествующего уровня техники. Методы и статистические вычисления смотри в прилагаемых тестах |
Важным наблюдением является то, что присутствие заместителей F и SO2CH3 в положениях мета 1 и мета 2 в фенильном кольце повышает эффективность и силу действия допаминергического стабилизатора по сравнению с моно- или 3,4-дизамещением (например Пример 6 из WO 01/46145 и Пример 9 из WO 01/46146), а также снижает аффинность к hERG-каналу. Такой результат не мог быть предсказуемым как общее правило.
Задача настоящего изобретения заключается в том, чтобы предоставить новые соединения для терапевтического применения и, более точно, соединения для модулирования допаминергических систем в мозге млекопитающих, включая мозг человека. Предпочтительно такие соединения оказывают меньше побочных эффектов, относящихся к ингибированию калиевых каналов сердца.
Задача изобретения также заключается в том, чтобы предоставить соединения, обладающие терапевтическими эффектами после перорального введения.
Предпочтительными замещенными структурами являются:
1-этил-4-[3-фтор-5-(метилсульфонил)фенил]пиперидин,
4-[3-фтор-5-(метилсульфонил)фенил]-1-пропилпиперидин,
1-аллил-4-[3-фтор-5-(метилсульфонил)фенил]пиперидин.
Соединения и композиции по настоящему изобретению обладают допамин-модулирующими свойствами и полезны в лечении многих расстройств центральной нервной системы, включая как психиатрические, так и неврологические расстройства. В частности, соединения и содержащие их фармацевтические композиции можно применять в лечении расстройств ЦНС, при которых функция допаминергической системы нарушена по прямым или косвенным причинам.
Соединения и композиции по настоящему изобретению можно применять для улучшения состояния при всех формах психоза, включая шизофрению и шизофреноформные расстройства, а также психотические расстройства, вызванные лекарственными средствами, и биполярное расстройство. Их можно применять также в лечении состояния, выбранного из группы, состоящей из ятрогенных и неятрогенных психозов и галлюцинозов.
Расстройства настроения и тревожные расстройства, включая депрессию и обсессивно-компульсивное расстройство, также можно лечить соединениями и композициями по изобретению.
Соединения, обладающие модулирующими эффектами в отношении допаминергических систем, можно применять также для улучшения когнитивных функций и для лечения эмоциональных нарушений, связанных со старением, нейродегенеративных расстройств (например, деменции и возрастного ухудшения когнитивной функции) и расстройств развития (таких как расстройства типа аутизма, ADHD, корковый паралич, синдром Жиля де ля Туретта), а также после повреждения мозга. Такое повреждение мозга может быть вызвано травматическими, воспалительными, инфекционными, неопластическими, сосудистыми, гипоксическими или метаболическими факторами или токсическими реакциями на экзогенные химические вещества, где экзогенные химические вещества выбраны из группы, состоящей из веществ, которыми злоупотребляют, фармацевтических соединений и токсинов окружающей среды. Соединения и содержащие их фармакологические композиции полезны для лечения состояния, выбранного из группы, состоящей из расстройств сна, сексуальных расстройств, расстройств приема пищи, ожирения, а также головных болей и других болей при состояниях, характеризующихся повышенным мышечным тонусом. Их также можно применять в лечении болезни Альцгеймера или родственных расстройств с деменцией.
Соединения и композиции по изобретению можно применять также при поведенческих расстройствах, обычно впервые диагностированных в младенческом, детском или пубертатном возрасте, а также при расстройствах контроля мотивации.
Их можно применять также для лечения расстройств, связанных со злоупотреблением веществами, а также расстройств, характеризующихся злоупотреблением пищи.
Неврологические показания включают применение соединений и содержащих их композиций для улучшения ментальной и моторной функции при болезни Паркинсона, дискинезиях (включая дискинезии, вызванные L-DOPA) и родственных паркинсонических синдромах. Их также можно применять для улучшения состояния при тиках и треморе различного происхождения. Более того, их можно применять для снятия боли при состояниях, характеризующихся повышенным мышечным тонусом.
Их можно применять также в лечении болезни Гентингтона и других двигательных расстройств, а также двигательных расстройств, вызванных лекарственными средствами. Синдром беспокойных ног и родственные расстройства, а также нарколепсию тоже можно лечить соединениями по изобретению.
Настоящее изобретение также относится к применению соединения формулы 1, указанной выше, где R выбран из группы, состоящей из С1-С3алкилов и аллила, или его фармацевтически приемлемой соли в изготовлении фармацевтически активных препаратов для лечения расстройства центральной нервной системы. Расстройство центральной нервной системы может быть одним или более чем одним расстройством, описанным выше. В конкретном воплощении этого применения R выбран из группы, состоящей из н-пропила и этила.
Было показано, что соединения по настоящему изобретению проявляют свойства допаминергического стабилизатора с улучшенной эффективностью (Таблица 1). Они оказывают эффекты на биохимические показатели в мозге с характерными признаками антагонистов допамина, например, продуцируя увеличение концентрации допаминных метаболитов. У крыс соединение Примера 1 повышает концентрацию 3,4-дигидроксифенилуксусной кислоты (DOPAC) в полосатом теле до 318% по сравнению с контролем при 100 мкмоль/кг п.к. (подкожно). Соединение Примера 2 повышает концентрацию DOPAC до 292% при 100 мкмоль/кг п.к.
Соединения по данному изобретению не оказывают влияния на спонтанную двигательную активность в широком диапазоне доз (1-100 мкмоль/кг п.к.).
В некоторых случаях, в частности когда исходная активность низкая, они могут вызывать незначительную поведенческую активацию. Поведенческая активация ограничивается, не достигая полного повышения активности, вызванного прямыми или непрямыми допаминергическими агонистами. С другой стороны, предпочтительные вещества снижают повышение активности, вызванное прямыми или непрямыми допаминергическими агонистами, то есть d-амфетамином и представителями того же класса соединений (Таблица 1).
Таким образом, соединения по данному изобретению проявляют свойства допаминергического стабилизатора с повышенной или сохраненной эффективностью (Таблица 1) по сравнению с соединениями формулы I и II. Кроме того, за счет конкретного характера замещения снизилась эффективность ингибирования HERG-канала.
Учитывая вовлечение допамина в большое количество функций ЦНС и клинические недостатки доступных в настоящее время фармацевтических препаратов, действующих на допаминергические системы, новый класс допаминергических модуляторов, представленных в этом изобретении, может превзойти известные в настоящее время допаминергические соединения в лечении некоторых расстройств, связанных с дисфункциями ЦНС, по показателям эффективности, а также по сниженным побочным эффектам.
Было показано, что соединения по настоящему изобретению проявляют высокую метаболическую стабильность в микросомах печени крыс, измеренную как обновление за 15 минут (Пример 1-5%, Пример 2-0%), и высокую пероральную биодоступность у крыс, подтвержденную Примером 2 (приблизительно 85%).
Таким образом, эти соединения подходят для изготовления фармацевтических препаратов для перорального введения. В предшествующем уровне техники отсутствует информация по получению соединений с таким воздействием на поведение и допаминергические системы в мозге.
Фармакология
Имеется доказательство того, что при психиатрических и неврологических заболеваниях нарушается допаминергическая нейротрансмиссия в ЦНС. Во многих случаях, например при шизофрении, болезни Паркинсона, болезни Гентингтона, биполярном расстройстве и при деменции, фармакотерапии, основанные на антагонизме или агонизме рецепторов допамина, полезны, но не являются оптимальными.
В последние годы было предпринято много попыток поиска новых и селективных в отношении подтипов рецепторов допамина (D1, D2, D3, D4, D5) соединений с целью повышения эффективности и снижения побочных эффектов.
Настоящее изобретение предлагает другой принцип для новых терапевтических средств, основанный на взаимодействиях с допаминергической системой. Согласно изобретению предложены соединения, оказывающие, в качестве их главной особенности, стабилизирующее воздействие на допаминергическую систему в мозге.
Описание животных моделей, использованных в изобретении
Соединения по изобретению оказывают эффекты на нейрохимию мозга, подобные эффектам антагонистов D2-рецепторов допамина (то есть дозозависимо повышают концентрацию метаболита допамина DOPAC в кортикальной, стриарной и лимбической областях мозга). Соединения по изобретению не оказывают или оказывают только ограниченное ингибирующее воздействие на спонтанную двигательную активность. При определенных условиях они могут вызывать поведенческую активацию. Поведенческая активация ограничивается, не достигая полного увеличения активности, вызываемого прямыми или непрямыми агонистами рецепторов допамина. Однако предпочтительные вещества снижают повышение активности, вызванное непрямым допаминергическим агонистом d-амфетамином. Повышение активности после лечения d-амфетамином представляет собой стандартную модель гипердопаминергии (Таблица 1). В этой модели допаминергическая нейротрансмиссия повышается в результате системного введения d-амфетамина в дозе, которая достаточно высока для того, чтобы вызвать значительное повышение двигательной активности. Способность соединения противодействовать этой гиперактивности отражает антидопаминергические свойства, которые составляют часть профиля допаминергического стабилизатора. Кроме того, антагонизм гиперактивности, вызванной d-амфетамином, широко используется в качестве стандартного анализа антипсихотической активности (смотри Psychopharmacology, 4th Generation of progress, Chapter 68, p.793-795).
Другая животная модель антипсихотической активности основана на введении глутаматного антагониста МK-801. Глутаматные антагонисты (то есть антагонисты NMDA) могут вызывать психозы у человека (смотри Psychopharmacology, 4th Generation of progress, Chapter 101, p.1205 and 1207) и вызывать поведенческие аберрации у животных. Так, способность лекарственного средства воздействовать на шизофрению и психотические состояния может быть измерена с использованием поведенческих моделей, основанных на экспериментально вызванных гипоглутаматергических состояниях. В этом исследовании, чтобы вызвать гипоглутаматергическое состояние, при котором крысы демонстрируют атипичное гиперактивное поведение, использовали антагонист NMDA МK-801 (0,7 мг/кг в.б. (внутрибрюшинно)). Соединения по настоящему изобретнию дозозависимо реверсируют поведенческую аберрацию, вызванную МK-801 (смотри Таблицу 2).
Известно, что допаминергические системы мозга интенсивно взаимодействуют с другими медиаторными системами (смотри Psychopharmacology, 4th Generation of progress, Chapter 101, pages 1208-1209). Такие взаимодействия могут объяснить мощное воздействие допаминергических стабилизаторов на поведенческие аберрации, вызванные глутаматным антагонистом МK-801, несмотря на то что эти аберрации первоначально не основаны на или не вызваны изменениями в допаминергической трансмиссии.
| Таблица 2 | |||
| Воздействие соединений по настоящему изобретению на двигательную активность у крыс, предварительно подвергнутых лечению МK-801 (0,7 мг/кг в.б. за 90 минут до введения тестируемого соединения). Животных помещали в измерители подвижности сразу после введения тестируемого соединения и двигательную активность регистрировали в период времени от 30 до 60 минут после введения (отсчеты/30 минут ± SEM (среднеквадратическая ошибка)) | |||
| Контрольная группа | МK-801 0.7 мг/кг в.б. | МK + соединение 100 мкмоль/кг | |
| 47±12 | 58630±9344 | 20858±4638 (Р=0,01) | |
| 31±9,6 | 58753±10982 | 24012±5511 (Р=0,03) |
Терапевтическое применение допаминергических стабилизаторов
Согласно изобретению предложены соединения, обладающие, в качестве их главного признака, стабилизирующим воздействием на допаминергическую систему в мозге. Эти соединения полезны для лечения расстройств ЦНС, на симптомы которых могут влиять допаминергические функции. Подтверждение этого утверждения можно найти в следующих источниках информации:
- Подтверждение для шизофрении и психоза можно найти в Psychopharmacology, 4th Generation of progress, Chapter 26, p.295-301;
- Болезнь Паркинсона (Psychopharmacology, 4th Generation of progress, Chapter 26, p.295, Chapter 1479-1482);
- Тревожные расстройства (Psychopharmacology, 4th Generation of progress, Chapter 21, p.227 and 237, Chapter 111, p.1317-1318 and 1320);
- Расстройства настроения (Psychopharmacology, 4th Generation of progress, Chapter 80, p.921-928) и
- Злоупотребление веществами (Psychopharmacology, 4th Generation of progress, Chapter 25, p.283 and 292, Chapter 66, p.759-760, Chapter 147, p.1725 (смотри также Nisell et al., "Systemic Nicotine-Induced Dopamine Release in the Rat Nucleus Accumbens is Regulated by Nicotinic receptors in the Ventral Tegmental Area; Synapse (1994) 16: 36-44), Chapter 149, p.1745-1747 and 1751-1752). Лекарственные средства, злоупотребляемые людьми, преимущественно повышают синаптические концентрации допамина в мезолимбической системе свободно двигающихся крыс (Di Chiara et al. Proc Natl Acad Sci USA 85, 5274, 1988. Drug addiction as a disorder of associative learning. Role of nucleus accumbens shell/extended amygdala dopamine Ann N.Y. Acad Sci 877, 461, 1999).
Как показано в этих источниках информации, указанные состояния признаны в известном уровне техники как заболевания, которые имеют отношение к допаминергической нейротрансмиссии.
Кроме того, общепризнано, что фармакологическое взаимодействие с допаминергической нейротрансмиссией полезно в лечении ряда расстройств ЦНС, которые обычно не считаются прямо вызванными нарушениями допаминергической нейротрансмиссии. Например, симптомы болезни Гентингтона и других двигательных расстройств можно лечить допаминергическими агентами за счет вовлечения допамина в моторные функции (смотри Psychopharmacology, 4th Generation of progress, Chapter 26, p.295-301). Известно также, что когнитивные расстройства (смотри Psychopharmacology, 4th Generation of progress, Chapter 25, p.292, Chapter 120, p.1417 and 1420, Chapter 123, p.1447 and 1452 and 1455-1457), аутизм (смотри Psychopharmacology, 4th Generation of progress, Chapter 142, p.1653 and 1661), синдром дефицита внимания с гиперактивностью (смотри Psychopharmacology, 4th Generation of progress, Chapter 141, p.1643 and 1649-1650), сексуальные расстройства (смотри Psychopharmacology, 4th Generation of progress, Chapters 65, p.743-746 and Chapter 22, p.245 and 254) и расстройства приема пищи (смотри Psychopharmacology, 4th Generation of progress, Chapters 137, p.1600, Chapter 138, p.1609-1610 and 1612) можно лечить агентами, усиливающими допаминергическую трансмиссию. Таким образом, вышеизложенные ссылки являются подтверждением тому, что соединения по изобретению можно применять для лечения таких заболеваний.
В данной области признано, что ингибирование hERG-канала может иметь тяжелые побочные эффекты со стороны сердца, в том числе летальную аритмию (J.Cardiovasc. Electrophysiol. 15, 475, 2004; Eur. J. Pharm., 450, 37, 2002; Cardiovascular Research, 58, 32, 2003). Таким образом, при разработке новых лекарственных средств, действующих на ЦНС, искомыми являются соединения с минимальной аффинностью к hERG-каналу и, следовательно, с широкими пределами безопасности.
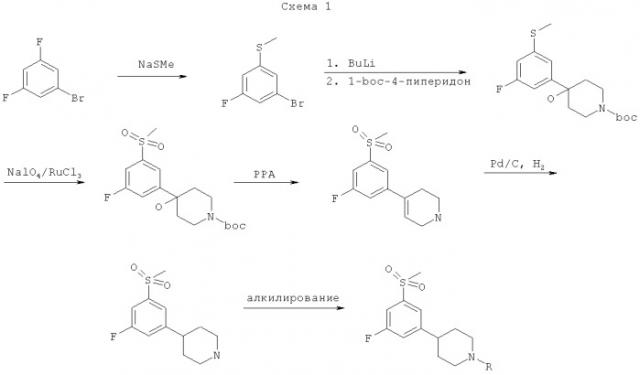
Способы получения
Соединения по изобретению могут быть получены, как в общем показано на Схеме 1. Однако изобретение не ограничивается этими способами. Соединения могут быть также получены способами, описанными для структурно родственных соединений в предшествующем уровне техники. Реакции можно проводить по стандартным методикам1,2 или как описано в рабочих примерах. Исходные вещества для процессов, описанных в настоящей заявке, известны или без труда могут быть получены общепринятыми способами из коммерчески доступных химических веществ.
Специалистам в данной области очевидно, что для получения соединений по изобретению альтернативным или в некоторых случаях более удобным способом отдельные стадии способа, упомянутые выше, можно выполнять в другом порядке и/или отдельные реакции можно осуществлять на другой стадии общего пути синтеза (т.е. химические превращения можно осуществлять с промежуточными соединениями, которые отличаются от промежуточных соединений, которые здесь выше ассоциированы с конкретными реакциями).
Ссылки:
1. Comprehensive Organic Transformations: A Guide to Functional Group Preparations
Richard C. Larock, 22 October, 1999 Wiley-VCH
ISBN: 0471190314
2. March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, 5th Edition.
Michael B. Smith, Jerry March, January 15, 2001 Wiley-lnterscience
ISBN: 0471585890
Используемый здесь термин "C1-С3алкил" относится к алкилу, содержащему 1-3 атома углерода, в любой изомерной форме. Различные углеродные группировки определены следующим образом: алкил относится к алифатическому углеводородному радикалу и включает неразветвленные формы, такие как метил, этил, н-пропил. Термин «аллил» относится к группе -CH2-CH=CH2.
Используемый здесь термин «пациент» относится к индивидууму, нуждающемуся в лечении согласно изобретению.
Используемый здесь термин «лечение» относится как к лечению с целью излечения или облегчения симптомов заболевания или состояния, так и к лечению с целью предупреждения развития заболевания или состояния. Можно проводить либо экстренное, либо длительное лечение.
Для образования нетоксичных фармацевтически приемлемых солей присоединения кислоты соединений по изобретению могут быть использованы как органические, так и неорганические кислоты. Подходящие соли присоединения кислоты соединений по настоящему изобретению включают фармацевтически приемлемые соли, такие как толуолсульфонат, метансульфонат, фумарат, гидрохлорид, гидробромид, гидройодид, нитрат, ацетат, лактат, цитрат, кислый цитрат, тартрат, битартрат, алифатический, алициклический, ароматический или гетероциклический карбоксилат, сукцинат, малеат, фумарат, глюконат, гликолят, сахарат, аскорбат, ацетат, пропионат, бензоат, пируват, памоат [то есть 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)], фосфат, кислый фосфат, сульфат или бисульфат. Эти соли получают способами, известными в уровне техники. Понятно также, что соединения по настоящему изобретению могут существовать как в сольватированной, так и в несольватированной форме, например в гидратированной форме.
Фармацевтическая композиция, содержащая соединение по изобретению, также может содержать вещества, используемые для облегчения изготовления фармацевтического препарата или введения препаратов. Такие вещества общеизвестны специалистам в данной области и могут представлять собой, например, фармацевтически приемлемые адъюванты, носители и консерванты.
В клинической практике соединения, применяемые согласно настоящему изобретению, будут вводить, как правило, перорально, ректально, интраназально или инъекцией в форме фармацевтических препаратов, содержащих активный ингредиент либо в виде свободного основания, либо в виде фармацевтически приемлемой нетоксичной соли присоединения кислоты, такой как гидрохлорид, лактат,