Водорастворимое соединение бензоазепина и содержащая его фармацевтическая композиция
Иллюстрации
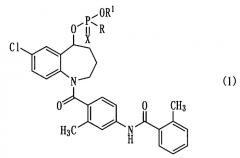
Показать всеИзобретение относится к соединению бензоазепина, представленному следующей общей формулой (I):
или к его соли, где R представляет собой атом водорода, гидрокси-группу, необязательно защищенную защитной группой, выбранной из низшей алкильной группы, фенил(низшей)алкильной группы, меркапто-группу или амино-группу, необязательно защищенную одной или двумя защитными группами, выбранными из низшей алкильной группы, необязательно содержащей гидрокси-группу, R1 представляет собой атом водорода или гидрокси-защитную группу, где защитная группа включает низшую алкильную группу, фенил(низшую)алкильную группу, циано низшую алкильную группу и низшую алкилоксикарбонил низшую алкильную группу, а Х представляет собой атом кислорода или атом серы. Изобретение также относится к фармацевтической композиции, обладающей антагонистической активностью к вазопрессину, на основе указанного соединения. Данное соединение бензоазепина обладают высокой растворимостью в воде и могут быть использованы в качестве сосудорасширяющего, гипотензивного, акваретического агента, ингибитора агрегации тромбоцитов или для лечения болезни поликистоза почек (PKD). 3 н. и 10 з.п. ф-лы, 2 ил., 6 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к новому соединению бензоазепина и содержащей его фармацевтической композиции.
Уровень техники
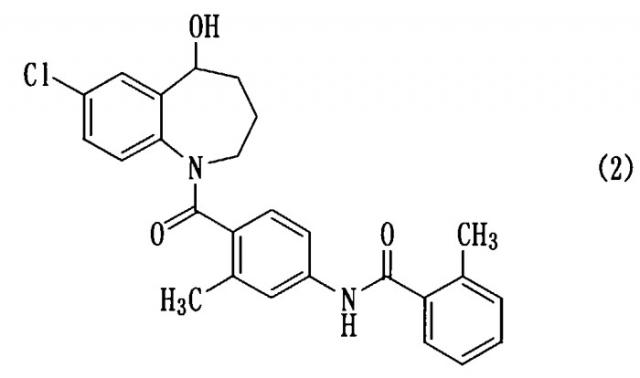
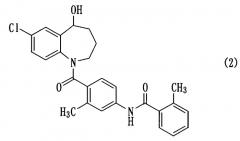
Толваптан, представленный следующей формулой (2), является известным соединением, и описан, например, в описании патента США №5258510 (пример 1199).
Известно, что толваптан применяется в качестве антагониста вазопрессина, обладающего акваретической активностью (Circulation, 107, pp.2690-2696 (2003)). Однако вследствие его низкой растворимости в воде проблема, связанная с толваптаном, заключается в том, что он плохо всасывается в кишечном канале, его дозировки и способы введения ограничены, и так далее. Несмотря на то, что предпринимались попытки решить данные проблемы, так что, например, толваптан можно вводить в виде препарата с композицией на основе аморфного твердого вещества (нерассмотренная японская патентная публикация №1999-21241), при использовании толваптана его дозировка и способ введения все еще остаются ограниченными.
Описание изобретения
Задачей настоящего изобретения является создание нового соединения бензоазепина для улучшения растворимости толваптана в воде.
Для решения упомянутой выше проблемы авторами настоящего изобретения проведено всестороннее исследование, в результате которого найдено, что когда толваптан находится в виде соединения эфира фосфорной кислоты, его растворимость в воде можно существенно повысить.
Настоящее изобретение основано на данном открытии.
Более конкретно, в настоящем изобретении предложены следующие соединения бензоазепина и содержащие их композиции, описанные в приведенных далее пунктах с 1 по 13.
Пункт 1. Соединение бензоазепина, представленное общей формулой (1)
или его соль,
в котором R представляет собой атом водорода, гидрокси-группу, необязательно защищенную защитной группой, меркапто-группу, необязательно защищенную защитной группой, или амино-группу, необязательно защищенную одной или двумя защитными группами, R1 представляет собой атом водорода, или гидрокси-защитную группу, а Х представляет собой атом кислорода, или атом серы.
Пункт 2. Соединение бензоазепина по пункту 1, или его соль, в котором Х представляет собой атом кислорода.
Пункт 3. Соединение бензоазепина по пункту 1, или 2, или его соль, в котором R представляет собой гидрокси-группу, необязательно защищенную защитной группой.
Пункт 4. Соединение бензоазепина по пункту 1, или 2, или его соль, в котором R представляет собой атом водорода, меркапто-группу, необязательно защищенную защитной группой, или амино-группу, необязательно защищенную одной или двумя защитными группами.
Пункт 5. Соединение бензоазепина по любому из пунктов 1, 2, 3 и 4, или его соль, в котором R1 представляет собой гидрокси-защитную группу.
Пункт 6. Соединение бензоазепина по любому из пунктов 1, 2, 3 и 4, или его соль, в котором R1 представляет собой атом водорода.
Пункт 7. Соединение бензоазепина по пункту 1, или его соль, в котором Х представляет собой атом серы.
Пункт 8. Соединение бензоазепина по пункту 1, или его соль, в котором Х представляет собой атом кислорода, R представляет собой гидрокси-группу, а R1 представляет собой атом водорода.
Пункт 9. Фармацевтическая композиция, содержащая соединение бензоазепина по пункту 1, или его фармацевтически приемлемую соль, вместе с фармацевтически приемлемым разбавителем и/или носителем.
Пункт 10. Фармацевтическая композиция по пункту 9 для использования в качестве сосудорасширяющего, гипотензивного, акваретического агента, PKD, или ингибитора агрегации тромбоцитов.
Пункт 11. Композиция в виде водного раствора, содержащего соединение бензоазепина по пункту 1, или его фармацевтически приемлемую соль.
Пункт 12. Композиция в виде водного раствора по пункту 11, содержащего соединение бензоазепина по пункту 1, или его фармацевтически приемлемую соль, вместе с буфером, агентом для придания изотоничности и растворителем для инъекции, и которая имеет форму препарата для инъекций.
Пункт 13. Композиция в виде водного раствора по пункту 12, дополнительно содержащего регулятор рН.
Использованный в настоящем описании термин «низший» означает С1-6, если не обозначено иначе.
Примеры защитных групп для «гидрокси-группы, необязательно защищенной защитной группой», «меркапто-группы, необязательно защищенной защитной группой» и «гидрокси-защитной группы» включают в себя низшие алкильные группы, фенил(низшие)алкильные группы, циано низшие алкильные группы и низшие алкилоксикарбонил низшие алкильные группы.
Примеры защитных групп для «амино-группы, необязательно защищенной одной или двумя защитными группами», включают в себя низшие алкильные группы, необязательно содержащие гидрокси-группу(ы).
Примеры низших алкильных групп и низших алкильных групп в фенил(низших)алкильных группах, циано низших алкильных группах и низших алкилоксикарбонил низших алкильных группах и низших алкильных групп, необязательно содержащих гидрокси-группу(ы), включают в себя С1-6 линейные или разветвленные алкильные группы, например, метил, этил, н-пропил, изопропил, н-бутил, изобутил, третбутил, втор-бутил, н-пентил, изопентил, неопентил, н-гексил, изогексил, 3-метилпентил и так далее.
Предпочтительными фенил(низшими)алкильными группами являются, например, бензил, фенетил, 3-фенилпропил, тритил и так далее.
Предпочтительными циано низшими алкильными группами являются С1-6 линейные или разветвленные алкильные группы, содержащие от одной до трех циано-групп, например, цианометил, 2-цианоэтил, 1-, 2-, или 3-циано-н-пропил, 1-, 2-, или 3-цианоизопропил, 1-, 2-, 3- или 4-циано-н-бутил, 1-, 2-, 3- или 4-цианоизобутил, 1-, 2-, 3- или 4-цианотретбутил, 1-, 2-, 3- или 4-циано-втор-бутил, 1-, 2-, 3-, 4- или 5-циано-н-пентил, 1-, 2-, 3-, 4- или 5-цианоизопентил, 1-, 2-, 3-, 4- или 5-цианонеопентил, 1-, 2-, 3-, 4-, 5- или 6-циано-н-гексил, 1-, 2-, 3-, 4-, 5- или 6-циано-изогексил, 1-, 2-, 3-, 4-, 5- или 6-циано-3-метилпентил, и так далее.
Предпочтительными низшими алкилоксикарбонил низшими алкильными группами являются алкилоксикарбонилалкильные группы, в которых алкилокси-фрагмент представляет собой С1-6 линейную, или разветвленную алкилокси-группу, а алкильный фрагмент представляет собой С1-6 линейную, или разветвленную алкильную группу, например, метоксикарбонилметил, этоксикарбонилметил, н-пропоксикарбонилметил, изопропоксикарбонилметил, н-бутоксикарбонилметил, изобутоксикарбонилметил, н-пентоксикарбонилметил, н-гексилоксикарбонилметил, 2-метоксикарбонилэтил, 3-метоксикарбонилпропил, 4-метоксикарбонилбутил, 5-метоксикарбонилпентил, 6-метоксикарбонилгексил и так далее.
Предпочтительными низшими алкильными группами, необязательно замещенными гидрокси-группой(группами), являются С1-6 линейные, или разветвленные алкильные группы, необязательно содержащие от одной до трех гидрокси-групп, например, метил, этил, н-пропил, изопропил, н-бутил, изобутил, третбутил, втор-бутил, н-пентил, изопентил, неопентил, н-гексил, изогексил, 3-метилпентил, гидроксиметил, 2-гидроксиэтил, 1-, 2-, или 3-гидрокси-н-пропил, 1-, 2-, или 3-гидроксиизопропил, 1-, 2-, 3-, или 4-гидрокси-н-бутил, 1-, 2-, 3-, или 4-гидрокси-изобутил, 1-, 2-, 3-, или 4-гидрокси-третбутил, 1-, 2-, 3-, или 4-гидрокси-вторбутил, 1-, 2-, 3-, 4-, или 5-гидрокси-н-пентил, 1-, 2-, 3-, 4-, или 5-гидрокси-изопентил, 1-, 2-, 3-, 4-, или 5-гидрокси-неопентил, 1-, 2-, 3-, 4-, 5-, или 6-гидрокси-н-гексил, 1-, 2-, 3-, 4-, 5-, или 6-гидрокси-изогексил, 1-, 2-, 3-, 4-, 5-, или 6-гидрокси-3-метилпентил и так далее.
Предпочтительными амино-группами, необязательно замещенными одной или двумя защитными группой(группами), являются амино-группы, необязательно содержащие одну или две С1-6 линейных, или разветвленных алкильных группы, необязательно содержащих от одной до трех гидрокси-групп, например, амино, метиламино, диметиламино, этиламино, диэтиламино, н-пропиламино, ди-н-пропиламино, изопропиламино, диизопропиламино, н-бутиламино, ди-н-бутиламино, изобутиламино, диизобутиламино, третбутиламино, дитретбутиламино, н-пентиламино, ди-н-пентиламино, н-гексиламино, ди-н-гексиламино, гидроксиметиламино, 2-гидроксиэтиламино, диэтиламино, ди-(2-гидроксиэтил)амино, 3-гидроксипропиламино, 4-гидроксибутиламино и так далее.
В ряду соединений бензоазепина, представленных приведенной выше общей формулой (1), предпочтительными являются следующие соединения и их соли:
в случае, когда Х является атомом кислорода,
(1) соединения, в которых R представляет собой гидрокси-группу, а R1 представляет собой атом водорода,
(2) соединения, в которых R представляет собой гидрокси-группу, а R1 представляет собой гидрокси-защитную группу,
(3) соединения, в которых R представляет собой меркапто-группу, а R1 представляет собой гидрокси-защитную группу, и
(4) соединения, в которых R представляет собой амино-группу, а R1 представляет собой гидрокси-защитную группу, и
в случае, когда Х является атомом серы,
(1) соединения, в которых R представляет собой гидрокси-группу, а R1 представляет собой атом водорода, или гидрокси-защитную группу.
Особенно предпочтительным из них является соединение, в котором Х является атомом кислорода, R представляет собой гидрокси-группу, а R1 представляет собой атом водорода; или его соль.
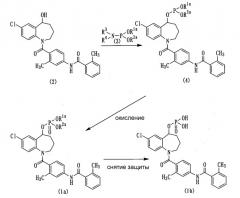
Соединения бензоазепина, представленные приведенной выше общей формулой (1), можно получить различными способами, и их примером является способ, представленный на следующих схемах реакций с 1 по 7:
Схема реакции-1
в которой R3 и R4 независимо представляют собой низшую алкильную группу, или необязательно замещенную фенильную группу, или вместо этого R3 и R4 могут быть связаны друг с другом через один, или более дополнительных гетероатомов, или без них, с образованием, вместе с атомом азота, с которым они связаны, 5-8-членного насыщенного, или ненасыщенного цикла, а R1а и R2а могут быть одинаковыми, или различными, и каждый из них представляет собой гидрокси-защитную группу.
Примерами низших алкильных групп являются упомянутые выше группы, включая С1-6 линейные, или разветвленные алкильные группы, например, метил, этил, н-пропил, изопропил, н-бутил, изобутил, третбутил, втор-бутил, н-пентил, изопентил, неопентил, н-гексил, изогексил, 3-метилпентил и так далее.
Примеры заместителей для необязательно замещенных фенильных групп включают в себя упомянутые выше низшие алкильные группы, С1-6 линейные, или разветвленные алкокси-группы, например, метокси, этокси, пропокси, изопропокси, бутокси, третбутокси, пентилокси, гексилокси и так далее, и атомы галогена, например, фтор, хлор, бром, йод и так далее.
Предпочтительные примеры необязательно замещенных фенильных групп включают в себя фенил, 2-, 3-, или 4-метилфенил, 2-, 3-, или 4-хлорфенил, 2-, 3-, или 4-метоксифенил и так далее.
Примеры 5-8-членных насыщенных, или ненасыщенных циклов, образованных связанными друг с другом R3 и R4, включают в себя морфолиновый цикл и так далее.
Соединение (4) можно получить, вводя соединение (2) во взаимодействие с соединением (3) в подходящем растворителе в присутствии кислоты.
Примеры растворителей включают в себя галогенсодержащие углеводородные растворители, например, хлористый метилен, хлороформ, 1,2-дихлорэтан, четыреххлористый углерод и так далее, сложные эфиры, например, этилацетат и так далее, ароматические углеводороды, например, бензол, толуол, ксилол и так далее, ацетонитрил и так далее.
Примеры кислот включают в себя мягкие кислоты, например, 1Н-тетразол, 5-метилтетразол, гидробромид пиридиния и так далее.
Количество кислоты обычно составляет, по меньшей мере, около 1 моль, а предпочтительно, от около 1 до около 10 моль на моль соединения (2).
Количество соединения (3) обычно составляет от 0,5 до 2 моль, а предпочтительно, от 0,7 до 1,5 моль на моль соединения (2).
Температура реакции обычно составляет от -20 до 50°С, предпочтительно, от 0 до 50°С, а более предпочтительно, от 0°С до комнатной температуры. Продолжительность реакции обычно составляет от 15 минут до 24 часов, предпочтительно, от 30 минут до 6 часов, а более предпочтительно, от 1 до 3 часов.
Соединение (1а) можно получить, вводя соединение (4) во взаимодействие с окисляющим агентом в подходящем растворителе.
Примеры растворителей включают в себя галогенсодержащие углеводородные растворители, например, хлористый метилен, хлороформ, 1,2-дихлорэтан, четыреххлористый углерод и так далее, сложные эфиры, например, этилацетат и так далее, ароматические углеводороды, например, бензол, толуол, ксилол и так далее, ацетонитрил и так далее.
Примеры окисляющих агентов включают в себя надкислоты, например, перекись водорода и метахлорпербензойную кислоту, надуксусную ксилоту, надмалеиновую кислоту и так далее.
Количество окисляющего агента обычно составляет, по меньшей мере, около 1 моль, а предпочтительно, от около 1 до около 3 моль на моль соединения (4).
Температура реакции обычно составляет от -100 до 50°С, предпочтительно, от -40°С до комнатной температуры, а более предпочтительно, от -40 до 0°С. Продолжительность реакции обычно составляет от 15 минут до 24 часов, предпочтительно, от 30 минут до 6 часов, а более предпочтительно, от 30 минут до 2 часов.
Соединение (1b) можно получить путем снятия защиты с защищенных гидрокси-групп соединения (1а) стандартными методами.
Например, в том случае, когда гидрокси-защитные группы представляют собой низшие алкильные группы, снятие защиты можно осуществить в стандартных условиях гидролиза.
Подобный гидролиз предпочтительно проводят в присутствии основания или кислоты (включая кислоту Льюиса).
В качестве подобного основания можно использовать широкий ряд известных неорганических и органических оснований. Предпочтительными неорганическими основаниями являются, например, щелочные металлы (например, натрий, калий и так далее), щелочноземельные металлы (например, магний, кальций и так далее) и их гидроксиды, карбонаты и гидрокарбонаты. Предпочтительными органическими основаниями являются, например, триалкиламины (например, триметиламин, триэтиламин и так далее), пиколин и 1,5-диазабицикло[4,3,0]нон-5-ен.
В качестве подобной кислоты можно использовать широкий ряд известных неорганических и органических кислот. Предпочтительными органическими кислотами являются жирные кислоты, например, муравьиная кислота, уксусная кислота, пропионовая кислота и так далее, и тригалогенуксусные кислоты, например, трихлоруксусная кислота, трифторуксусная кислота и так далее. Предпочтительными неорганическими кислотами являются, например, хлористоводородная кислота, бромистоводородная кислота, серная кислота, хлористый водород, бромистый водород и так далее. Примеры кислот Льюиса включают в себя эфирный комплекс трехфтористого бора, трехбромистый бор, хлорид алюминия, хлорид железа и так далее.
При использовании тригалогенуксусной кислоты, или кислоты Льюиса, гидролиз предпочтительно проводят в присутствии ловушки для катионов (например, анизола, фенола и так далее).
Количество основания или кислоты не ограничено, пока оно удовлетворяет требованиям гидролиза.
Температура реакции обычно составляет от -20 до 100°С, предпочтительно, от 0 до 50°С, а более предпочтительно, от 0°С до комнатной температуры. Продолжительность реакции обычно составляет от 5 минут до 24 часов, предпочтительно, от 15 минут до 6 часов, а более предпочтительно, от 15 минут до 3 часов.
В том случае, когда, например, гидрокси-защитные группы представляют собой фенил(низшие)алкильные группы, снятие защиты можно осуществить стандартным методом каталитического восстановления.
Катализаторы, подходящие для подобного каталитического восстановления, представляют собой платиновые катализаторы (например, платиновую пластину, губчатую платину, платиновую чернь, коллоидную платину, оксид платины, платиновую проволоку и так далее), палладиевые катализаторы (например, губчатый палладий, палладиевую чернь, оксид палладия, палладий на угле, палладий/сульфат бария, палладий/карбонат бария и так далее), никелевые катализаторы (например, восстановленный никель, оксид никеля, никель Ренея и так далее), кобальтовые катализаторы (например, восстановленный кобальт, кобальт Ренея и так далее), железные катализаторы (например, восстановленное железо и так далее) и так далее. При использовании катализатора палладия на угле, каталитическое восстановление предпочтительно проводят в присутствии бромида цинка.
Количество катализатора, используемого при каталитическом восстановлении, не ограничено и может представлять собой стандартное количество.
Температура реакции обычно составляет от 0 до 100°С, предпочтительно, от 0 до 50°С, а более предпочтительно, от комнатной температуры до 50°С. Продолжительность реакции обычно составляет от 5 минут до 24 часов, предпочтительно, от 5 минут до 3 часов, а более предпочтительно, от 5 минут до 1 часа.
Схема реакции-2
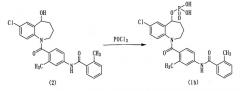
Соединение (2) вводят во взаимодействие с хлорокисью фосфора, а затем гидролизуют, получая соединение (1b).
Количество хлорокиси фосфора обычно составляет от 1 моль до большого избытка, а предпочтительно, от 1 до 5 моль на моль соединения (2).
Упомянутую выше реакцию проводят в присутствии основного соединения в подходящем растворителе. Примеры растворителей для реакции с хлорокисью фосфора включают в себя простые эфиры, например, диэтиловый эфир, диоксан, тетрагидрофуран, моноглим, диглим и так далее, галогенсодержащие углеводородные растворители, например, хлористый метилен, хлороформ, 1,2-дихлорэтан, четыреххлористый углерод и так далее, сложные эфиры, например, этилацетат и так далее, ароматические углеводороды, например, бензол, толуол, ксилол и так далее, ацетонитрил и так далее.
Примеры основных соединений включают в себя карбонаты, например, карбонат натрия, карбонат калия, гидрокарбонат натрия, гидрокарбонат калия, карбонат цезия и так далее, гидроксиды щелочных металлов, например, гидроксид натрия, гидроксид калия и так далее, гидроксиды щелочноземельных металлов, например, гидроксид кальция и так далее, фосфаты, например, фосфат натрия, фосфат калия и так далее; органические основания, например, пиридин, имидазол, N-этилдиизопропиламин, диметиламинопиридин, триэтиламин, триметиламин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU), 1,4-диазабицикло[2.2.2]октан (DABCO) и так далее, и их смеси.
Количество основного соединения обычно составляет, по меньшей мере, около 3 моль, а предпочтительно, от около 3 до около 10 моль на моль соединения (2). Температура реакции обычно составляет от -100 до 50°С, предпочтительно, от -50°С до комнатной температуры, а более предпочтительно, от -30°С до комнатной температуры. Продолжительность реакции обычно составляет от 15 минут до 24 часов, предпочтительно, от 30 минут до 6 часов, а более предпочтительно, от 1 до 3 часов.
Гидролиз можно осуществить, добавляя воду к упомянутой выше реакционной смеси или прибавляя реакционную смесь к воде.
Поскольку это обычно сопровождается избыточным разложением реагентов и, в результате этого, выделяется теплота, гидролиз предпочтительно проводят при охлаждении. Для завершения реакции нагревание предпочтительно осуществляют после замедления первоначальной реакции.
Продолжительность реакции обычно составляет от 15 минут до 24 часов, предпочтительно, от 30 минут до 6 часов, а более предпочтительно, от 1 до 3 часов.
Схема реакции-3
в которой R1 аналогичен указанному выше.
Соединение (2) вводят во взаимодействие с дифенилфосфитом, а затем вводят во взаимодействие со спиртом (R1ОН), получая соединение (1с).
Количество дифенилфосфита составляет обычно от 1 моль до большого избытка, а предпочтительно, от 1 до 5 моль на моль соединения (2). Количество спирта (R1ОН) составляет обычно от 1 моль до большого избытка, а предпочтительно, от 1 до 10 моль на моль соединения (2).
Упомянутую выше реакцию проводят в присутствии основного соединения в подходящем растворителе.
Примеры растворителей включают в себя простые эфиры, например, диэтиловый эфир, диоксан, тетрагидрофуран, моноглим, диглим и так далее, галогенсодержащие углеводородные растворители, например, хлористый метилен, хлороформ, 1,2-дихлорэтан, четыреххлористый углерод и так далее, сложные эфиры, например, этилацетат и так далее, ароматические углеводороды, например, бензол, толуол, ксилол и так далее, и ацетонитрил.
Примеры основных соединений включают в себя карбонаты, например, карбонат натрия, карбонат калия, гидрокарбонат натрия, гидрокарбонат калия, карбонат цезия и так далее, гидроксиды щелочных металлов, например, гидроксид натрия, гидроксид калия и так далее, гидроксиды щелочноземельных металлов, например, гидроксид кальция и так далее, фосфаты, например, фосфат натрия, фосфат калия и так далее; органические основания, например, пиридин, имидазол, N-этилдиизопропиламин, диметиламинопиридин, триэтиламин, триметиламин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU), 1,4-диазабицикло[2.2.2]октан (DABCO) и так далее, и их смеси.
Количество основного соединения обычно составляет, по меньшей мере, около 1 моль, а предпочтительно, от около 1 до около 10 моль на моль соединения (2). В качестве растворителя можно также использовать органические растворители.
Температура реакции обычно составляет от -100 до 50°С, предпочтительно, от -50°С до комнатной температуры, а более предпочтительно, от -30°С до комнатной температуры. Продолжительность реакции обычно составляет от 15 минут до 24 часов, предпочтительно, от 30 минут до 6 часов, а более предпочтительно, от 1 до 3 часов.
Схема реакции-4
в которой R1 аналогичен указанному выше.
Окисление фосфита можно осуществить при использовании от около 1 до около 3 эквивалентов агента, окисляющего фосфористую кислоту, при температуре в интервале от около 0°С до 50°С. Предпочтительно реакцию проводят при использовании от около 5 до около 15% избытка агента, окисляющего фосфористую кислоту, в интервале от 0°С до комнатной температуры.
Агент, окисляющий фосфористую кислоту, представляет собой реагент, окисляющий фосфит до фосфата. Его примеры включают в себя перекиси, например, перекись водорода, метахлорпербензойную кислоту и так далее, йод в воде, бром, четырехокись азота и так далее. Предпочтительным является йод в воде.
Указанную выше реакцию проводят в подходящем растворителе.
Примеры растворителей включают в себя простые эфиры, например, диэтиловый эфир, диоксан, тетрагидрофуран, моноглим, диглим и так далее, галогенсодержащие углеводородные растворители, например, хлористый метилен, хлороформ, 1,2-дихлорэтан, четыреххлористый углерод и так далее, сложные эфиры, например, этилацетат и так далее, ароматические углеводороды, например, бензол, толуол, ксилол и так далее, ацетонитрил и пиридин.
Температура реакции обычно составляет от -100 до 50°С, предпочтительно, от -50°С до комнатной температуры, а более предпочтительно, от -30°С до комнатной температуры. Продолжительность реакции обычно составляет от 15 минут до 24 часов, предпочтительно, от 15 минут до 6 часов, а более предпочтительно, от 15 минут до 3 часов.
Схема реакции-5
в которой R1 аналогичен указанному выше, а R11 и R12 могут быть одинаковыми или различными и каждый из них представляет собой атом водорода, или низшую алкильную группу, необязательно содержащую гидрокси-группу(группы).
Амин (R11R12NH) и четыреххлористый углерод вводят во взаимодействие с диэфиром фосфористой кислоты (1с), получая амидофосфат (1е).
Вместо четыреххлористого углерода можно также использовать гипохлорит натрия.
Количество четыреххлористого углерода обычно составляет от 1 моль до большого избытка, а предпочтительно, от 1 до 5 моль на моль соединения (1с). Количество амина (R11R12NH) обычно составляет от 1 моль до большого избытка, а предпочтительно, от 1 до 10 моль на моль соединения (1с).
Указанную выше реакцию проводят в присутствии основного соединения в подходящем растворителе.
Примеры растворителей включают в себя простые эфиры, например, диэтиловый эфир, диоксан, тетрагидрофуран, моноглим, диглим и так далее, галогенсодержащие углеводородные растворители, например, хлористый метилен, хлороформ, 1,2-дихлорэтан, четыреххлористый углерод и так далее, сложные эфиры, например, этилацетат и так далее, ароматические углеводороды, например, бензол, толуол, ксилол и так далее, ацетонитрил и так далее.
Примеры основных соединений включают в себя карбонаты, например, карбонат натрия, карбонат калия, гидрокарбонат натрия, гидрокарбонат калия, карбонат цезия и так далее, гидроксиды щелочных металлов, например, гидроксид натрия, гидроксид калия и так далее, гидроксиды щелочноземельных металлов, например, гидроксид кальция и так далее, фосфаты, например, фосфат натрия, фосфат калия и так далее; органические основания, например, пиридин, имидазол, N-этилдиизопропиламин, диметиламинопиридин, триэтиламин, триметиламин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU), 1,4-диазабицикло[2.2.2]октан (DABCO) и так далее, и их смеси. Количество основного соединения обычно составляет, по меньшей мере, около 1 моль, а предпочтительно, от около 1 до около 10 моль на моль соединения (2). В качестве растворителя можно также использовать органические растворители.
Температура реакции обычно составляет от -100 до 50°С, предпочтительно, от -50°С до комнатной температуры, а более предпочтительно, от -30°С до комнатной температуры. Продолжительность реакции обычно составляет от 1 минуты до 24 часов, предпочтительно, от 1 минуты до 6 часов, а более предпочтительно, от 1 минуты до 3 часов.
Схема реакции-6
в которой R1 аналогичен указанному выше.
Диэфир фосфористой кислоты (1с) вводят во взаимодействие с серой, получая диэфир тиофосфорной кислоты (1f).
Количество серы обычно составляет от 1 моль до большого избытка, а предпочтительно, от 1 до 5 моль на моль соединения (1с).
Указанную выше реакцию проводят в присутствии основного соединения в подходящем растворителе.
Примеры растворителей включают в себя простые эфиры, например, диэтиловый эфир, диоксан, тетрагидрофуран, моноглим, диглим и так далее, галогенсодержащие углеводородные растворители, например, хлористый метилен, хлороформ, 1,2-дихлорэтан, и так далее, сложные эфиры, например, этилацетат и так далее, ароматические углеводороды, например, бензол, толуол, ксилол и так далее, ацетонитрил и пиридин.
Примеры основных соединений включают в себя карбонаты, например, карбонат натрия, карбонат калия, гидрокарбонат натрия, гидрокарбонат калия, карбонат цезия и так далее, гидроксиды щелочных металлов, например, гидроксид натрия, гидроксид калия и так далее, гидроксиды щелочноземельных металлов, например, гидроксид кальция и так далее, фосфаты, например, фосфат калия, фосфат натрия и так далее, гидриды щелочных металлов, например, гидрид натрия, гидрид калия и так далее, щелочные металлы, например, калий, натрий и так далее, амид натрия, алкоголяты металлов, например, метилат натрия, этилат натрия, н-бутилат натрия, третбутилат натрия, третбутилат калия и так далее; органические основания, например, пиридин, имидазол, N-этилдиизопропиламин, диметиламинопиридин, триэтиламин, триметиламин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU), 1,4-диазабицикло[2.2.2]октан (DABCO) и так далее, и их смеси. Количество основного соединения обычно составляет, по меньшей мере, около 1 моль, а предпочтительно, от около 1 до около 10 моль на моль соединения (2). В качестве растворителя можно также использовать органические растворители.
Температура реакции обычно составляет от -100 до 50°С, предпочтительно, от -50°С до комнатной температуры, а более предпочтительно, от -30°С до комнатной температуры. Продолжительность реакции обычно составляет от 15 минут до 24 часов, предпочтительно, от 30 минут до 6 часов, а более предпочтительно, от 1 до 3 часов.
Схема реакции-7
в которой R1' представляет собой гидрокси-защитную группу.
Защитную группу в соединении (1g), которое представляет собой соединение (1f), полученной по схеме реакции 6, в которой R1 представляет собой гидрокси-защитную группу, снимают, получая соединение (1h).
Если R1 представляет собой цианоэтильную группу, данную защитную группу можно удалить действием основного соединения.
Указанную выше реакцию проводят в присутствии основного соединения в подходящем растворителе.
Примеры растворителей включают в себя воду, спирты, например, метанол, этанол, изопропиловый спирт и так далее, простые эфиры, например, диэтиловый эфир, диоксан, тетрагидрофуран, моноглим, диглим и так далее, галогенсодержащие углеводородные растворители, например, хлористый метилен, хлороформ, 1,2-дихлорэтан, четыреххлористый углерод и так далее, сложные эфиры, например, этилацетат и так далее, ароматические углеводороды, например, бензол, толуол, ксилол и так далее, апротонные полярные растворители, например, диметилформамид (ДМФА), диметилсульфоксид (ДМСО) и так далее, кетоны, например, ацетон, метилэтилкетон, метилизобутилкетон и так далее, ацетонитрил, и их смеси.
Примеры основных соединений включают в себя карбонаты, например, карбонат натрия, карбонат калия, гидрокарбонат натрия, гидрокарбонат калия, карбонат цезия и так далее, гидроксиды щелочных металлов, например, гидроксид натрия, гидроксид калия и так далее, гидроксиды щелочноземельных металлов, например, гидроксид кальция и так далее, фосфаты, например, фосфат калия, фосфат натрия и так далее, гидриды щелочных металлов, например, гидрид натрия, гидрид калия и так далее, щелочные металлы, например, калий, натрий и так далее, амид натрия, алкоголяты металлов, например, метилат натрия, этилат натрия, н-бутилат натрия, третбутилат натрия, третбутилат калия и так далее; органические основания, например, пиридин, имидазол, N-этилдиизопропиламин, диметиламинопиридин, триэтиламин, триметиламин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU), 1,4-диазабицикло[2.2.2]октан (DABCO) и так далее, и их смеси. Количество основного соединения обычно составляет, по меньшей мере, около 1 моль, а предпочтительно, от около 1 до около 10 моль на моль соединения (2). В качестве растворителя можно также использовать органические растворители.
Температура реакции обычно составляет от -100 до 50°С, предпочтительно, от -50°С до комнатной температуры, а более предпочтительно, от -30°С до комнатной температуры. Продолжительность реакции обычно составляет от 15 минут до 24 часов, предпочтительно, от 30 минут до 6 часов, а более предпочтительно, от 1 до 3 часов.
Соединения (2), (3), (4), (1а), (1b), (1c), (1d), (1e), (1f), (1g) и (1h) в приведенных выше схемах реакций могут представлять собой свои подходящие соли. Примеры подобных подходящих солей включают в себя те же типы солей, что и для соединения (1).
Соединения, полученные по приведенным выше схемам реакций, можно выделить и очистить из реакционной смеси обычными способами, например, после охлаждения реакционной смеси, выделения сырого продукта фильтрованием, концентрированием, экстракцией, или подобным способом выделения, а затем очисткой полученного продукта колоночной хроматографией, перекристаллизацией, или подобным стандартным способом очистки.
Соединения, представленные общей формулой (1) настоящего изобретения, включают в себя стереоизомеры, оптические изомеры и их сольваты (гидраты, этаноляты и так далее).
Примеры солей соединений, представленных общей формулой (1) настоящего изобретения, включают в себя фармацевтически приемлемые соли, например, соли металлов, например, соли щелочных металлов (например, соли натрия, соли калия и так далее), соли щелочноземельных металлов (например, соли кальция, соли магния и так далее), аммониевые соли, соли органических оснований (например, соли триметиламина, соли триэтиламина, соли пиридина, соли пиколина, соли дициклогексиламина, соли этилендиамина, соли N,N'-дибензилэтилендиамина, соли трис(гидроксиметил)аминометана, соли этаноламина и так далее) и так далее. В их ряду предпочтительными являются соли щелочных металлов, а более предпочтительными являются соли натрия.
Подобные соли можно легко получить, действуя на соединение настоящего изобретения соответствующим фармацевтически приемлемым основным соединением. Примеры применимых основных соединений включают в себя гидроксид натрия, гидроксид калия, гидроксид кальция, карбонат натрия, гидрокарбонат калия и так далее.
Соединение настоящего изобретения обладает, например, антагонизмом по отношению к вазопрессину, сосудорасширяющей активностью, гипотензивной активностью, активностью ингибирования выделения сахаридов в печени, активностью ингибирования роста мезангиальных клеток, акваретической активностью, и ингибирующей активностью к агрегации тромбоцитов. Соединение применимо в качестве сосудорасширяющего агента, гипотензивного агента, акваретического агента и ингибитора агрегации тромбоцитов и эффективно для предотвращения и лечения гипертензии, отека (например, сердечного отека, отека печени, почечного отека, церебрального отека), асцита, сердечной недостаточности (например, тяжелой сердечной недостаточности), почечной дисфункции, синдрома несоответствующей секреции вазопрессина (SIADH), цирроза печени, гипонатриемии, гипокалиемии, диабета, циркуляторной недостаточности, болезни поликистоза почек (PKD), инфаркта мозга, инфаркта миокарда и так далее.
При введении в организм человека в форме лекарственного средства соединение настоящего изобретения можно использовать одновременно, или отдельно с другими антагонистами вазопрессина, ингибиторами АСЕ, β-блокирующими агентами, акваретическими агентами, антагонистами ангиотензина II (ARB) и/или подобными фармацевтическими лекарственными средствами.
Соединение настоящего изобретения обычно используют в виде общей фармацевтической композиции. Такую фармацевтическую композицию можно получить стандартным способом при использовании обычно используемых разбавителей и/или эксципиентов, например, наполнителей, расширителей, связывающих веществ, увлажняющих агентов, разрыхлителей, поверхностно-активных веществ, смазывающих веществ и так далее.
Форму фармацевтической композиции, содержащей соединение настоящего изобретения, можно выбрать подходящим образом в зависимости от цели лечения. Например, она может быть в форме таблетки, пилюли, порошка, раствора, суспензии, эмульсии, капсулы, суппозитория, мази или гранул. В особенности предпочтительна композиция в виде водного раствора, например, препарат для инъекции, вливания и так далее.
Например, при получении препарата для инъекций с использованием соединения настоящего изобретения, подобный препарат для инъекций предпочтительно получают в виде раствора, эмульсии или суспензии, которую стерилизуют и которая изотонична крови. Для получения подобного раствора, эмульсии или суспензии с использованием соединения настоящего изобретения можно использовать любые обычно применяемые в данной области разбавители. Примеры подобных разбавителей включают в себя воду, водные растворы молочной кислоты, этиловый спирт, пропиленгликоль, этоксилированный изостеариловый спирт, полиоксиэтилированный изостеариловый спирт и полиоксиэтиленовые сложные эфиры сорбита и жирных кислот. Кроме того, в данном случае к фармацевтической композиции можно добавить хлорид натрия, глюкозу, маннит, глицерин и подобные агенты, придающие изотоничность, в количествах, достаточны