Противораковая фармацевтическая композиция
Иллюстрации
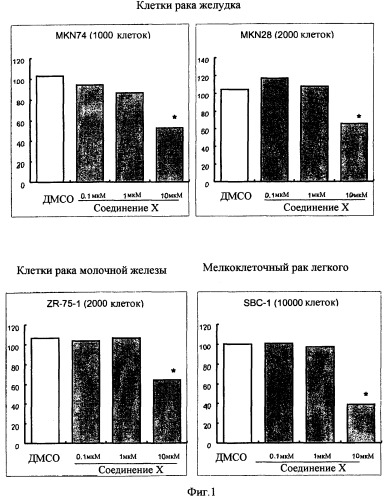
Показать всеИзобретение относится к области фармацевтики и медицины и касается противораковой фармацевтической композиции или комбинации для профилактики или рака легкого, или почки, содержащая в качестве активных ингредиентов лекарственное средство, выбранное из гефитиниба, эрлотиниба и сорафениба, и дигидрохлорид 5-(4-(6-(4-амино-3,5-диметилфенокси)-1-метил-1Н-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион. Изобретение обеспечивает повышенную эффективность лечения. 2 н. и 14 з.п. ф-лы, 5 ил., 4 табл.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к противораковой фармацевтической композиции, которая в качестве активного ингредиента содержит тиазолидиндионовое соединение, обладающее активирующим действием в отношении рецептора активатора пролиферации пероксисом (PPAR) γ, и к противораковой фармацевтической композиции для профилактики или лечения карциномы, саркомы или рака крови, которая в качестве активных ингредиентов содержит соединение, обладающее активирующим действием в отношении PPARγ, и ингибитор рецептора эпидермального фактора роста (EGFR), ингибитор фактора роста эндотелия сосудов (VEGFR) или ингибитор Raf-киназы.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Широко известно, что активаторы PPARγ применимы в качестве лекарственных средств для терапии сахарного диабета 2 типа, представленных такими примерами, как розиглитазон и пиоглитазон. Считается, что PPARγ выполняет различные физиологические функции, такие как индукция дифференцировки для превращения в адипоциты и корректировка энергетического обмена биогенных веществ (например, см. непатентные документы 1 и 2). С другой стороны, сообщалось, что активаторы PPARγ индуцируют дифференцировку, ингибируют клеточный цикл или индуцируют апоптоз у различных типов раковых клеток, и обусловливают ингибирование роста раковых клеток (например, см. непатентные документы 3, 4 и 5). В дополнение к этим открытиям было высказано предположение, что поскольку при раке щитовидной железы часто наблюдается хромосомная транслокация PAX8-PPARγ, и работа PPARγ инактивирована, и поскольку при раке толстой кишки наблюдается, хотя и с невысокой частотой, обусловливающая дисфункцию точечная мутация, то PPARγ действует как ингибитор онкогенной трансформации (например, см. патентные документы 6 и 7). Исходя из этих открытий, было высказано предположение о возможности использования активаторов PPARγ для лечения рака, и у больных раком были проведены немногочисленные клинические испытания с использованием розиглитазона. Однако значимого эффекта не наблюдалось (например, см. патентный документ 8). На сегодняшний день причина такого результата не установлена; тем не менее, весьма вероятно, что противораковое действие розиглитазона было недостаточно сильным. Соответственно, считается, что обнаружение активатора PPARγ, который обладает более сильным эффектом, внесет значительный вклад в лечение рака в будущем.
С другой стороны, в современных методах лечения рака предпринят подход, при котором для усиления эффективности лекарственных средств и для снижения побочных эффектов по сравнению со способом, при котором каждое из лекарственных средств вводят по отдельности, сочетанно используют несколько противораковых лекарственных средств. В качестве типов противораковых лекарственных средств, использованных при комбинированном лечении, могут быть упомянуты разрушающие раковые клетки химиотерапевтические лекарственные средства и различные молекулярно направленные лекарственные средства, которые недавно были представлены на рынке. В частности, молекулярно направленные лекарственные средства, как правило, обладают слабыми побочными эффектами по сравнению с используемыми ранее лекарственными средствами, и что касается комбинированного введения, то для предупреждения усиления побочных эффектов часто нет необходимости в снижении количества используемого ранее лекарственных средств. Поэтому, поскольку при комбинированной терапии может быть достигнута максимальная эффективность разрушающих раковые клетки химиотерапевтических лекарственных средств, и поскольку их эффект может быть усилен за счет эффективности молекулярно направленных лекарственных средств, то в настоящее время ведется активная разработка различных лекарственных средств, которые обладают молекулярно направленным действием. Примерами молекулярно направленных лекарственных средств, которые привлекают внимание в настоящее время, являются бевацизумаб (название продукта Авастин), который представляет собой лекарственное средство на основе антитела, обладающее антиангиогенетической активностью, и гефитиниб (название продукта Иресса) и эрлотиниб (название продукта Тарцева), которые представляют собой ингибиторы рецептора эпидермального фактора роста (EGFR). Кроме того, считается, что сорафениб, который обладает антиангиогенетической (ингибирующей рецептор фактора роста эндотелия сосудов (VEGFR)) активностью в сочетании с ингибирующей активностью в отношении Raf-киназы и находится в настоящее время на стадии клинических испытаний, также эффективен в клинических испытаниях и привлекает внимание. Описанное выше указание на то, что противораковые эффекты могут быть усилены путем комбинированного введения с указанными молекулярно направленными лекарственными средствами, делает возможным проведение различных вариантов лечения рака у пациента, и тем самым вносят значительный вклад в улучшение результата лечения. Так, повышение противораковой эффективности путем комбинированного введения, как правило, указывает на то, что полученный путем комбинированного введения эффект выше эффекта, полученного путем отдельного введения каждого лекарственного средства (например, см. непатентный документ 9), и считается, что клиническая значимость является высокой даже если синергический усиливающий эффект и не был достигнут.
В патенте Японии №3488099 (для других, см. патентные документы 1 и 2) раскрыто тиазолидиндионовое соединение, обладающее новым химическим строением. Представленное общей формулой (I) соединение, которое содержится в качестве активного ингредиента противораковой фармацевтической композиции по настоящему изобретению, представляет собой соединение, которое охватывается объемом соединений, относящихся к тиазолидиндионовому соединению, раскрытому в изобретении. В патенте Японии № 3488099 показано, что раскрытое в опубликованном патенте тиазолидиндионовое соединение обладает способностью активировать PPARγ и может быть использовано в качестве противоракового лекарственного средства. Тем не менее, в патенте не раскрыты какие-либо конкретные результаты испытаний, которые показывают, что тиазолидиндионовое соединение действительно обладает противораковым действием.
Кроме того, сообщалось о фармацевтических композициях, которые содержат указанное тиазолидиндионовое соединение и другое лекарственное средство.
Например, сообщалось о фармацевтической композиции, содержащей тиазолидиндионовое соединение и ингибитор MAP-киназы (см. патентные документы 3 и 4), и было раскрыто, что указанная фармацевтическая композиция применима в качестве профилактического средства, лекарственного средства или в качестве ингибитора пролиферации клеток при раке, таком как рак желудка, рак легких, рак молочной железы, рак толстой кишки, рак предстательной железы, рак поджелудочной железы, рак печени, лейкоз, рак головы и шеи или липосаркома.
Кроме того, сообщалось о фармацевтической композиции для профилактики или лечения рака, которая содержит некоторые из соединений, подпадающих под объем соединений и относящихся к упомянутому выше тиазолидиндионовому соединению, и активатор RXR (рецептора ретиноидов X) (см. патентные документы 5 и 6), и было раскрыто, что указанная фармацевтическая композиция применима в качестве лекарственного средства или в качестве профилактического средства, в особенности при раке легких, раке желудка и раке толстой кишки.
Сообщалось о фармацевтической композиции, содержащей упомянутое выше тиазолидиндионовое соединение и антиметаболит фторурацилового ряда или комплекс платины (см. патентные документы 7 и 8), и было раскрыто, что указанная фармацевтическая композиция особенно применима в качестве профилактического средства, лекарственного средства или в качестве ингибитора пролиферации клеток при раке, таком как рак желудка, рак легких, рак молочной железы, рак толстой кишки, рак предстательной железы, рак поджелудочной железы, рак печени, лейкоз, рак головы и шеи или липосаркома.
Сообщалось о фармацевтической композиции, содержащей упомянутое выше тиазолидиндионовое соединение и диуретик (см. патентные документы 9 и 10), и было раскрыто, что указанная фармацевтическая композиция может предупреждать или лечить побочные эффекты, обусловленные введением активатора PPARγ, такие как гипертрофия сердца, отек, задержка жидкости и задержка плеврального выпота, и особенно применима в качестве профилактического средства, лекарственного средства или в качестве ингибитора пролиферации клеток при раке, таком как рак желудка, рак легких, рак молочной железы, рак толстой кишки, рак предстательной железы, рак поджелудочной железы, рак печени, лейкоз, рак головы и шеи или липосаркома.
Сообщалось о фармацевтической композиции, содержащей упомянутое выше тиазолидиндионовое соединение и новое сульфамидное соединение, обладающее ингибирующей активностью в отношении MEK (см. патентные документы 11 и 12), и было раскрыто, что указанная фармацевтическая композиция особенно применима в качестве профилактического средства, лекарственного средства или в качестве ингибитора пролиферации клеток при раке, таком как рак желудка, рак легких, рак молочной железы, рак толстой кишки, рак предстательной железы, рак поджелудочной железы, рак печени, лейкоз, рак головы и шеи или липосаркома.
[Патентный документ 1] Патент США №6432993.
[Патентный документ 2] Европейский патент №1022272.
[Патентный документ 3] Заявка на выдачу патента Японии (Kokai) №2003-192592.
[Патентный документ 4] Брошюра международной публикации № WO 03/032988.
[Патентный документ 5] Заявка на выдачу патента Японии (Kokai) №2003-238406.
[Патентный документ 6] Брошюра международной публикации № WO 03/053440.
[Патентный документ 7] Заявка на выдачу патента Японии (Kokai) №2004-83558.
[Патентный документ 8] Брошюра международной публикации № WO 03/082865.
[Патентный документ 9] Заявка на выдачу патента Японии (Kokai) №2004-83574.
[Патентный документ 10] Брошюра международной публикации № WO 2004/000356.
[Патентный документ 11] Заявка на выдачу патента Японии (Kokai) №2005-162727.
[Патентный документ 12] Брошюра международной публикации № WO 2004/083167.
[Непатентный документ 1] Spiegelman B.M. PPAR-γ: Adipogenic regulator and thiazolidinedione receptor. Diabetes, 1998; 47: 507-14.
[Непатентный документ 2] Lehmann J.M., Moore L.B. et al. An antidiabetic thiazolidinedione is a high affinity ligand for peroxisome proliferator-activated receptor gamma. J. Biol. Chem. 1995; 270: 12953-6.
[Непатентный документ 3] Mueller E., Sarraf P. et al. Terminal differentiation of the human breast cancer through PPAR gamma. Mol. Cell. 1998; 1: 465-70.
[Непатентный документ 4] Yoshizume T., Ohta T. et al. Thiazolidinedione, a peroxisome proliferator-activated receptor gamma ligand, inhibits growth and metastasis of HT-29 human colon cancer cells through differentiation-promoting effects. Int. J. Oncol. 2004; 25: 631-9.
[Непатентный документ 5] Ray D.M., Bernstein S.H. et al. Human multiple myeloma cells express peroxisome proliferator-activated receptor γ and undergo apoptosis upon exposure to PPARγ ligands. Clin. Immunology, 2004; 113: 203-13.
[Непатентный документ 6] Dwight T., Thoppe S.R., et al. Involvement of the PAX8/peroxisome proliferator-activated receptor gamma rearrangement in follicular thyroid tumors. J. Clin. Endocrinol. Metab. 2003; 88: 4440-5.
[Непатентный документ 7] Sarraf P., Mueller E. et al. Loss-of-function mutations in PPAR gamma associated with human colon cancer. Mol. Cell. 1999; 3: 799-804.
[Непатентный документ 8] Debrock G., Vanhentenrijk V. et al. A phase II trial with rosiglitazone in liposarcoma patients. Br. J. Cancer. 2003; 89: 1409-12.
[Непатентный документ 9] Tatsuo Saito ed., Development of Drug Therapy for Cancer and Evaluation of Efficiency, Realize inc., pp. 128-138 (1985).
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Проблемы, требующие решения настоящим изобретением
Соответственно, авторы настоящего изобретения отобрали соединение, представленное общей формулой (I), представляющее собой активный ингредиент противораковой фармацевтической композиции по настоящему изобретению, из соединений, подпадающих под объем упомянутого выше тиазолидионового соединения, и исследовали противораковые эффекты соединения, представленного общей формулой (I) по настоящему изобретению, при использовании только самого соединения.
В результате было обнаружено, что соединение, представленное общей формулой (I), или его фармакологически приемлемая соль по настоящему изобретению обладает превосходным противораковым эффектом в отношении конкретного типа рака.
В результате проведения обширных исследований по обнаружению сочетания лекарственных средств, обладающих лучшим противораковым действием, авторы настоящего изобретения обнаружили, что путем введения соединения, способного активировать PPARγ (в особенности соединения, представленного общей формулой (I) по настоящему изобретению), или его фармацевтически приемлемой соли, в сочетании с ингибитором рецептора эпидермального фактора роста (EGFR), ингибитором рецептора фактора роста эндотелия сосудов (VEGFR) или ингибитором Raf-киназы, противораковые эффекты могут быть усилены по сравнению со случаем, когда они вводятся по отдельности, оформив тем самым настоящее изобретение.
Средства решения проблем
Настоящее изобретение представляет собой
(1) противораковую фармацевтическую композицию для профилактики или лечения рака желудка, рака толстой кишки, рака легких, рака молочной железы, рака поджелудочной железы, рака почки, рака предстательной железы, медуллобластомы, рабдомиосаркомы, саркомы Юинга, липосаркомы, множественной миеломы или лейкоза, содержащую в качестве активного ингредиента соединение, представленное следующей общей формулой (I):
[в которой
R представляет собой фенильную группу, замещенную 1-5 группами, выбранными из группы заместителей α, и
X представляет собой атом кислорода или атом серы;
<группа заместителей α>: атом галогена, гидроксигруппа, C1-C6алкильная группа, галогенC1-C6алкильная группа, C1-C6алкоксигруппа, C1-C6алкилтиогруппа, аминогруппа, которая может быть замещена 1 или 2 группами, выбранными из группы заместителей γ, C3-C10циклоалкильная, C6-C10арильная, C7-C16аралкильная, C6-C10арилокси, C7-C16аралкилокси или C6-C10арилтио группа, которая может быть замещена 1-3 группами, выбранными из группы заместителей β, C1-C7алифатическая ацилоксигруппа, 4-7-членная насыщенная гетероциклическая группа, содержащая атом(ы) азота, 5-6-членная ароматическая гетероциклическая группа, содержащая атом(ы) азота, нитрогруппа и цианогруппа;
<группа заместителей β>: атом галогена, гидроксигруппа, C1-C6алкильная группа, галогенC1-C6алкильная группа, C1-C6алкоксигруппа, аминогруппа, которая может быть замещена 1 или 2 группами, выбранными из группы заместителей γ, C6-C10арильная группа и нитрогруппа;
<группа заместителей γ>: C1-C10алкильная группа, C6-C10арильная группа, C7-C16аралкильная группа, C1-C7алифатическая ацильная группа, C7-C11ароматическая ацильная группа, C8-C12ароматическоалифатическая ацильная группа, C4-C11циклоалкилкарбонильная группа и 5-6-членная ароматическая гетероциклическая карбонильная группа, содержащая атом(ы) азота], или его фармацевтически приемлемую соль,
(2) фармацевтическую композицию в соответствии с упомянутым выше п.(1), в которой
R представляет собой фенильную группу, замещенную 1-5 группами, выбранными из группы заместителей α, и
группа заместителей α представляет собой группу, состоящую из атома галогена, C1-C6алкильной группы, галогенC1-C6алкильной группы, аминогруппы, которая может быть замещена 1 или 2 группами, выбранными из группы заместителей γ, 4-7-членной насыщенной гетероциклической группы, содержащей атом(ы) азота, и 5-6-членной ароматической гетероциклической группы, содержащей атом(ы) азота,
(3) фармацевтическую композицию в соответствии с упомянутым выше п.(1), в которой R представляет собой фенильную группу, замещенную одной аминогруппой, которая может быть замещена 1 или 2 заместителями (заместители могут быть одинаковыми или разными, и каждый представляет собой группу, выбранную из группы, состоящей из C1-С10алкильной группы, С6-С10арильной группы и C7-С16аралкильной группы), и может быть дополнительно замещена 1-3 заместителями (каждый заместитель представляет собой группу, выбранную из группы, состоящей из атома галогена, C1-С6алкильной группы и галогенС1-С6алкильной группы),
(4) фармацевтическую композицию в соответствии с упомянутым выше п.(1), в которой R представляет собой фенильную группу, замещенную аминогруппой или моно- или ди-С1-С10алкиламиногруппой, и которая может быть дополнительно замещена 1 или 2 C1-С6алкильными группами,
(5) фармацевтическую композицию в соответствии с любым из упомянутых выше п.(1)-(4), в которой Х представляет собой атом кислорода,
(6) фармацевтическую композицию в соответствии с упомянутым выше п.(1), в которой соединение, представленное общей формулой (I), представляет собой соединение, выбранное из следующих соединений:
5-(4-(6-(3-изопропиламинофенокси)-1-метил-1Н-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(3-(изобутилметиламино)фенокси)-1-метил-1Н-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(4-(изобутилметиламино)фенокси)-1-метил-1Н-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(3-(этилизопропиламино)фенокси)-1-метил-1Н-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(4-изопропиламинофенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(4-втор-бутиламинофенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(4-изобутиламинофенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион и
5-(4-(6-(4-амино-3,5-диметилфенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
(7) фармацевтическую композицию в соответствии с упомянутым выше п.(1), в которой соединение, представленное общей формулой (I), или его фармацевтически приемлемая соль представляет собой дигидрохлорид 5-(4-(6-(4-амино-3,5-диметилфенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-диона,
(8) фармацевтическую композицию в соответствии с упомянутым выше п.(1), в которой соединение, представленное общей формулой (I), или его фармацевтически приемлемая соль представляет собой дигидрохлорид 5-(4-(6-(3-изопропиламинофенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-диона,
(9) противораковую фармацевтическую композицию для профилактики или лечения карциномы, саркомы или рака крови, содержащую в качестве активных ингредиентов
по меньшей мере, одно противораковое лекарственное средство, выбранное из группы, состоящей из ингибитора рецептора эпидермального фактора роста (EGFR), ингибитора рецептора фактора роста эндотелия сосудов (VEGFR) и ингибитора Raf-киназы; и
по меньшей мере, одно соединение, выбранное из группы, состоящей из химических соединений, представленных следующей общей формулой (I):
[в которой
R представляет собой фенильную группу, замещенную 1-5 группами, выбранными из группы заместителей α, и
X представляет собой атом кислорода или атом серы;
<группа заместителей α>: атом галогена, гидроксигруппа, C1-C6алкильная группа, галогенC1-C6алкильная группа, C1-C6алкоксигруппа, C1-C6алкилтиогруппа, аминогруппа, которая может быть замещена 1 или 2 группами, выбранными из группы заместителей γ, C3-C10циклоалкильная, C6-C10арильная, C7-C16аралкильная, C6-C10арилокси, C7-C16аралкилокси или C6-C10арилтиогруппа, которая может быть замещена 1-3 группами, выбранными из группы заместителей β, C1-C7алифатическая ацилоксигруппа, 4-7-членная насыщенная гетероциклическая группа, содержащая атом(ы) азота, 5-6-членная ароматическая гетероциклическая группа, содержащая атом(ы) азота, нитрогруппа и цианогруппа;
<группа заместителей β>: атом галогена, гидроксигруппа, C1-C6алкильная группа, галогенC1-C6алкильная группа, C1-C6алкоксигруппа, аминогруппа, которая может быть замещена 1 или 2 группами, выбранными из группы заместителей γ, C6-C10арильная группа и нитрогруппа;
<группа заместителей γ>: C1-C10алкильная группа, C6-C10арильная группа, C7-C16аралкильная группа, C1-C7алифатическая ацильная группа, C7-C11ароматическая ацильная группа, C8-C12ароматическоалифатическая ацильная группа, C4-C11циклоалкилкарбонильная группа и 5-6-членная ароматическая гетероциклическая карбонильная группа, содержащая атом(ы) азота],
или его фармакологически приемлемую соль,
где активные ингредиенты предназначены для одновременного введения или введения по отдельности в разное время,
(10) фармацевтическую композицию в соответствии с упомянутым выше п.(9), в которой противораковое лекарство выбирают, по меньшей мере, из группы, состоящей из ингибитора рецептора эпидермального фактора роста (EGFR) (лекарственное средство представляет собой цетуксимаб, панитумумаб, гефитиниб, эрлотиниб или лапатиниб), ингибитора рецептора фактора роста эндотелия сосудов (VEGFR) (лекарственное средство представляет собой бевацизумаб, сорафениб, SU11248 или ваталаниб) и ингибитора Raf-киназы (лекарственное средство представляет собой сорафениб),
(11) фармацевтическую композицию в соответствии с упомянутым выше п.(9), в которой противораковое лекарственное средство выбирают, по меньшей мере, из группы, состоящей из гефитиниба и сорафениба,
(12) фармацевтическую композицию в соответствии с любым из упомянутых выше пп.(9)-(11), где карцинома представляет собой рак желудка, рак толстой кишки, рак легких, рак молочной железы, рак поджелудочной железы, рак почки или рак предстательной железы,
(13) фармацевтическую композицию в соответствии с любым из упомянутых выше пп.(9)-(12), где саркома представляет собой медуллобластому, рабдомиосаркому, саркому Юинга или липосаркому,
(14) фармацевтическую композицию в соответствии с любым из упомянутых выше пп.(9)-(13), где рак крови представляет собой множественную миелому или лейкоз,
(15) фармацевтическую композицию в соответствии с любым из упомянутых выше пп.(9)-(14), в которой
R представляет собой фенильную группу, замещенную 1-5 группами, выбранными из группы заместителей α, и
группа заместителей α представляет собой группу, состоящую из атома галогена, C1-C6алкильной группы, галогенC1-C6алкильной группы, аминогруппы, которая может быть замещена 1 или 2 группами, выбранными из группы заместителей γ, 4-7-членной насыщенной гетероциклической группы, содержащей атом(ы) азота, и 5-6-членной ароматической гетероциклической группы, содержащей атом(ы) азота,
(16) фармацевтическую композицию в соответствии с любым из упомянутых выше пп.(9)-(14), в которой R представляет собой фенильную группу, замещенную одной аминогруппой, которая может быть замещена 1 или 2 заместителями (заместители могут быть одинаковыми или разными, и каждый представляет собой группу, выбранную из группы, состоящей из C1-C10алкильной группы, C6-C10арильной группы и C7-C16аралкильной группы), и может быть дополнительно замещена 1-3 заместителями (каждый заместитель представляет собой группу, выбранную из группы, состоящей из атома галогена, C1-C6алкильной группы и галогенC1-C6алкильной группы),
(17) фармацевтическую композицию в соответствии с любым из упомянутых выше пп.(9)-(14), в которой R представляет собой фенильную группу, замещенную аминогруппой или моно- или ди-C1-C10алкиламиногруппой, и которая может быть дополнительно замещена 1 или 2 C1-C6алкильными группами,
(18) фармацевтическую композицию в соответствии с любым из упомянутых выше пп.(9)-(17), в которой X представляет собой атом кислорода,
(19) фармацевтическую композицию в соответствии с упомянутым выше п.(9), в которой соединение, представленное общей формулой (I), представляет собой соединение, выбранное из следующих соединений:
5-(4-(6-(3-изопропиламинофенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(3-(изобутилметиламино)фенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(4-(изобутилметиламино)фенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(3-(этилизопропиламино)фенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(4-изопропиламинофенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(4-втор-бутиламинофенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
5-(4-(6-(4-изобутиламинофенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион и
5-(4-(6-(4-амино-3,5-диметилфенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-дион,
(20) фармацевтическую композицию в соответствии с упомянутым выше п.(9), в которой, по меньшей мере, одно соединение, выбранное из группы, состоящей из соединений, представленных общей формулой (I), или его фармацевтически приемлемая соль представляет собой дигидрохлорид 5-(4-(6-(4-амино-3,5-диметилфенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-диона, и
(21) фармацевтическую композицию в соответствии с упомянутым выше п.(9), в которой соединение, выбранное из группы, состоящей из соединений, представленных общей формулой (I), или его фармацевтически приемлемая соль представляет собой дигидрохлорид 5-(4-(6-(3-изопропиламинофенокси)-1-метил-1H-бензимидазол-2-илметокси)бензил)тиазолидин-2,4-диона.
Кроме того, настоящее изобретение относится к способу профилактики или лечения рака желудка, рака толстой кишки, рака легких, рака молочной железы, рака поджелудочной железы, рака почки, рака предстательной железы, медуллобластомы, рабдомиосаркомы, саркомы Юинга, липосаркомы, множественной миеломы или лейкоза, который включает введение фармацевтической композиции, описанной в любом из упомянутых выше пп.(1)-(8), теплокровному животному (предпочтительно, человеку).
Кроме того, настоящее изобретение относится к способу профилактики или лечения карциномы (в особенности, рака желудка, рака толстой кишки, рака легких, рака молочной железы, рака поджелудочной железы, рака почки или рака предстательной железы), саркомы (в особенности, медуллобластомы, рабдомиосаркомы, саркомы Юинга или липосаркомы) или рака крови (в особенности, множественной миеломы или лейкоза), который включает одновременное введение активных ингредиентов фармацевтической композиции или введение каждого из ингредиентов в различное время, причем активные ингредиенты описаны в упомянутых выше пп.(9)-(21).
В настоящем изобретении в определении групп заместителей α и β «атом галогена» представляет собой атом фтора, атом хлора, атом брома или атом йода, предпочтительно атом фтора или атом хлора, и более предпочтительно атом фтора.
В определении групп заместителей α и β «C1-C6алкильная группа» представляет собой неразветвленную или разветвленную алкильную группу, содержащую 1-6 атомов углерода, и представляет собой, например, метильную, этильную, пропильную, изопропильную, бутильную, изобутильную, втор-бутильную, трет-бутильную, пентильную, изопентильную, 2-метилбутильную, неопентильную, 1-этилпропильную, гексильную, 4-метилпентильную, 3-метилпентильную, 2-метилпентильную, 1-метилпентильную, 3,3-диметилбутильную, 2,2-диметилбутильную, 1,1-диметилбутильную, 1,2-диметилбутильную, 1,3-диметилбутильную, 2,3-диметилбутильную или 2-этилбутильную группу. В отношении группы заместителей α она предпочтительно представляет собой метильную или трет-бутильную группу, а в отношении группы заместителей β она предпочтительно представляет собой C1-C4алкильную группу, и более предпочтительно метильную или этильную группу.
В определении групп заместителей α и β «галогенC1-C6алкильная группа» представляет собой группу, в которой с упомянутой выше C1-C6алкильной группой связаны от 1 до 3 из упомянутых выше атомов галогена, и представляет собой, например, трифторметильную, трихлорметильную, трибромметильную, дифторметильную, дихлорметильную, дибромметильную, фторметильную, 2,2,2-трихлорэтильную, 2,2,2-трифторэтильную, 2-бромэтильную, 2-хлорэтильную, 2-фторэтильную, 2-йодэтильную, 3-хлорпропильную, 4-фторбутильную, 6-йодгексильную или 2,2-дибромэтильную группу, предпочтительно галогенC1-C2алкильную группу, и более предпочтительно трифторметильную группу.
В определении групп заместителей α и β «C1-C6алкоксигруппа» представляет собой группу, в которой упомянутая выше C1-C6алкильная группа связана с атомом кислорода, и представляет собой, например, метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, пентокси, изопентокси, 2-метилбутокси, неопентокси, 1-этилпропокси, гексилокси, 4-метилпентокси, 3-метилпентокси, 2-метилпентокси, 3,3-диметилбутокси, 2,2-диметилбутокси, 1,1-диметилбутокси, 1,2-диметилбутокси, 1,3-диметилбутокси, 2,3-диметилбутокси или 2-этилбутокси группу, предпочтительно C1-C4алкоксигруппу, более предпочтительно C1-C2алкоксигруппу, и особенно предпочтительно метоксигруппу.
В определении группы заместителей α «C1-C6алкилтиогруппа» представляет собой группу, в которой упомянутая выше C1-C6алкильная группа связана с атомом серы, и представляет собой, например, метилтио, этилтио, пропилтио, изопропилтио, бутилтио, изобутилтио, втор-бутилтио, трет-бутилтио, пентилтио, изопентилтио, 2-метилбутилтио, неопентилтио, 1-этилпропилтио, гексилтио, 4-метилпентилтио, 3-метилпентилтио, 2-метилпентилтио, 1-метилпентилтио, 3,3-диметилбутилтио, 2,2-диметилбутилтио, 1,1-диметилбутилтио, 1,2-диметилбутилтио, 1,3-диметилбутилтио, 2,3-диметилбутилтио или 2-этилбутилтио группу, предпочтительно C1-C4алкилтиогруппу, более предпочтительно C1-C2алкилтиогруппу, и особенно предпочтительно метилтиогруппу.
В определении групп заместителей α и β «аминогруппа, которая может быть замещена 1 или 2 группами, выбранными из группы заместителей γ» представляет собой аминогруппу, которая может быть замещена одной или двумя группами, которые могут быть одинаковыми или разными, причем группу выбирают из группы заместителей γ, состоящей из C1-C10алкильной группы, C6-C10арильной группы, C7-C16аралкильной группы, C1-C7алифатической ацильной группы, C7-C11ароматической ацильной группы, C8-C12ароматическоалифатической ацильной группы, C4-C11циклоалкилкарбонильной группы и 5- или 6-членной ароматической гетероциклической карбонильной группы, содержащей атом(ы) азота.
В представленном выше определении группы заместителей γ «C1-C10алкильная группа» представляет собой неразветвленную или разветвленную алкильную группу, содержащую 1-10 атомов углерода, и представляет собой, например, упомянутую выше C1-С6алкильную, гептильную, 1-метилгексильную, 2-метилгексильную, 3-метилгексильную, 4-метилгексильную, 5-метилгексильную, 1-пропилбутильную, 4,4-диметилпентильную, октильную, 1-метилгептильную, 2-метилгептильную, 3-метилгептильную, 4-метилгептильную, 5-метилгептильную, 6-метилгептильную, 1-пропилпентильную, 2-этилгексильную, 5,5-диметилгексильную, нонильную, 3-метилоктильную, 4-метилоктильную, 5-метилоктильную, 6-метилоктильную, 1-пропилгексильную, 2-этилгептильную, 6,6-диметилгептильную, децильную, 1-метилнонильную, 3-метилнонильную, 8-метилнонильную, 3-этилоктильную, 3,7-диметилоктильную или 7,7-диметилоктильную группу, и предпочтительно представляет собой неразветвленную или разветвленную алкильную группу, содержащую 1-4 атома углерода.
В представленном выше определении группы заместителей γ «C6-С10арильная группа» представляет собой ароматическую углеводородную группу, содержащую 6-10 атомов углерода, и группа может быть замещена нитрогруппой, упомянутыми выше атомами галогена, гидроксигруппой, упомянутой выше C1-С6алкильной группой, C1-С6алкилкарбонилоксигруппой или C1-С6алкоксигруппой. Такая группа представляет собой, например, фенильную, нафтильную, пара-нитрофенильную, пара-хлорфенильную, пара-фторфенильную, пара-гидроксифенильную, пара-ацетоксифенильную, пара-метилфенильную, пара-этилфенильную, пара-пропилфенильную, пара-метоксифенильную, пара-этоксифенильную или пара-пропоксифенильную группу, и
предпочтительно представляет собой фенильную, пара-нитрофенильную или пара-пропоксифенильную группу.
В представленном выше определении группы заместителей γ «C7-C16аралкильная группа» представляет собой группу, в которой упомянутая выше C6-C10арильная группа связана с упомянутой выше C1-C6алкильной группой, и представляет собой, например, бензильную, нафтилметильную, инденилметильную, дифенилметильную, 1-фенетильную, 2-фенетильную, 1-нафтилэтильную, 2-нафтилэтильную, 1-фенилпропильную, 2-фенилпропильную, 3-фенилпропильную, 1-нафтилпропильную, 2-нафтилпропильную, 3-нафтилпропильную, 1-фенилбутильную, 2-фенилбутильную, 3-фенилбутильную, 4-фенилбутильную, 1-нафтилбутильную, 2-нафтилбутильную, 3-нафтилбутильную, 4-нафтилбутильную, 5-фенилпентильную, 5-нафтилпентильную, 6-фенилгексильную или 6-нафтилгексильную группу, предпочтительно аралкильную группу, в которой фенильная группа связана с C1-C4алкильной группой, и более предпочтительно бензильную группу.
В представленном выше определении группы заместителей γ «C1-C7алифатическая ацильная группа» представляет собой группу, в которой атом водорода или насыщенная или ненасыщенная неразветвленная C1-C6углеводородная группа связана с карбонильной группой, и представляет собой, например, формильную, ацетильную, пропионильную, бутирильную, изобутирильную, валерильную, изовалерильную, пивалоильную, гексаноильную, акрилоильную, метакрилоильную или кротоноильную группу, предпочтительно ацетильную, пропионильную или пивалоильную группу, и более предпочтительно ацетильную группу.
В представленном выше определении группы заместителей γ «C7-C11ароматическая ацильная группа» представляет собой группу, в которой C6-C10арильная группа связана с карбонильной группой, и представляет собой, например, бензоильную, 1-инданкарбонильную, 2-инданкарбонильную или 1- или 2-нафтоильную группу, и предпочтительно представляет собой бензоильную или нафтоильную группу.
В представленном выше определении группы заместителей γ «C8-C12ароматическоалифатическая ацильная группа» представляет собой группу, в которой фенильная группа связана с C2-C6алифатической ацильной группой, и представляет собой, например, фенилацетильную, 3-фенилпропионильную, 4-фенилбутирильную, 5-фенилпентаноильную или 6-фенилгексаноильную группу, и предпочтительно представляет собой фенилацетильную группу.
В представленном выше определении группы заместителей γ «C4-C11циклоалкилкарбонильная группа» представляет собой группу, в которой C3-C10циклоалкильная группа (которая представляет собой 3-10-членную насыщенную циклическую углеводородную группу, которая может быть конденсированной, и представляет собой, например, циклопропильную, циклобутильную, циклопентильную, циклогексильную, циклогептильную, норборнильную или адамантильную группу, и предпочтительно C3-C6циклоалкильную группу) связана с карбонильной группой, и представляет собой, например, циклопропаноильную, циклобутирильную, циклопентаноильную, циклогексаноильную, циклогептилкарбонильную, норборнилкарбонильную или адамантилкарбонильную группу, предпочтительно C4-C7циклоалкилкарбонильную группу, и особенно предпочтительно циклопентаноильную или циклогексаноильную группу.
В представленном выше определении группы заместителей γ «5- или 6-членная ароматическая гетероциклическая карбонильная группа, содержащая атом(ы) азота» представляет собой группу, в которой 5- или 6-членное ароматическое гетероциклическое кольцо, которое содержит, по меньшей мере, один атом азота и может дополнительно содержать гетероатом, выбранный из группы г