Фармацевтические композиции для лечения хронической сердечной недостаточности, включающие соединение - производное пиразолопиримидинона
Иллюстрации
Показать всеИзобретение относится к области фармацевтики и медицины и касается фармацевтической композиции для лечения хронической сердечной недостаточности, включающей в качестве эффективного ингредиента 5-[2-пропилокси-5-(1-метил-2-пирролидинил-этил-амидосульфонил)фенил]-1-метил-3-пропил-1,6-дигидро-7Н-пиразоло(4,3-d)пиримидин-7-он, способа лечения хронической сердечной недостаточности и применения указанного соединения для получения фармацевтической формы для лечения хронической сердечной недостаточности. Изобретение обеспечивает смягчение симптомов хронической сердечной недостаточности, предотвращение дилатации левого желудочка, уменьшение истончения стенки желудочка, сдерживание желудочкового фиброза и уменьшение побочных эффектов. 3 н. и 2 з.п. ф-лы, 1 табл., 3 ил.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к фармацевтической композиции для лечения хронической сердечной недостаточности (ХСН), включающей в качестве эффективного ингредиента 5-[2-пропилокси-5-(1-метил-2-пирролидинил-этил-амидосульфонил)фенил]-1-метил-3-пропил-1,6-дигидро-7H-пиразоло(4,3-d)пиримидин-7-он.
УРОВЕНЬ ТЕХНИКИ
Сердце состоит из четырех камер, двух предсердий (верхние камеры) и двух желудочков (нижние камеры), и четырех главных клапанов. При биении сердца правое предсердие принимает венозную кровь тела. Затем кровь проходит через трикуспидальный клапан в правый желудочек. В то же время кровь, насыщенная в легких кислородом, втекает в левое предсердие и затем проходит через митральный клапан в левый желудочек. Сокращение правого желудочка проталкивает кровь, собранную в правом предсердии, в легкое, в котором венозная кровь принимает кислород. Насыщенная кислородом кровь возвращается в левое предсердие и стекает в левый желудочек. Левый желудочек сокращается, накачивая кровь в тело. Из четырех сердечных клапанов два клапана предотвращают обратное течение крови между предсердием и желудочком, а другие два клапана предотвращают обратное течение крови между желудочком и артерией. Сердце бьется, чтобы доставить кровь ко всем частям тела. Кровь, накачиваемая из сердца, циркулирует в теле, доставляя кислород и питательные вещества к тканям и унося продукты жизнедеятельности из тканей. Объем крови, выталкиваемой сердцем с каждым биением, изменяется в зависимости от физической активности. Относительно малый объем крови требуется во время отдыха, тогда как большой объем крови необходим при упражнениях. Таким образом, сердце бьется медленнее или быстрее в соответствии с потребностями в крови, что приводит к расслаблению и сокращению кровеносных сосудов.
Сердечная недостаточность представляет собой патофизиологическое состояние, при котором сердце теряет способность накачивать достаточное количество крови, чтобы удовлетворить потребностям тканей тела, и вызывается несколькими факторами. Когда сердечная мышца не способна достаточно сильно сокращаться или расслабляться, кровообращение затрудняется, и большой объем крови накапливается в каждой камере сердца и в легких. Если это имеет место, сердце пытается компенсировать снижение насосной функции за счет своего увеличения, чтобы накачивать больше крови в ткани или органы. Если данное состояние длится в течение долгого времени, компенсаторное напряжение достигает своего предела, вызывая более тяжелые проблемы. В частности, если насосная способность сердца ослабевает постепенно, данное состояние называется хронической сердечной недостаточностью. Способы компенсации данного состояния, которыми располагает организм, включают повышенную частоту сердечных сокращений, увеличение сердца (дилатацию) и задержку жидкости. Поскольку сердечная декомпенсация сопровождается застоем, хроническую сердечную недостаточность также называют застойной сердечной недостаточностью.
Согласно данным Американской сердечной ассоциации сердечной недостаточностью страдают примерно пять миллионов американцев, и примерно 550000 новых случаев диагностируются каждый год. Также примерно 1% людей в возрасте 50 лет или старше и примерно 5% людей в возрасте 75 лет или старше страдают сердечной недостаточностью. Примерно 10% пациентов с диагностированной сердечной недостаточностью умирают от сердечной недостаточности в течение одного года, и 50% пациентов умирают в течение пяти лет после установления диагноза.
Хроническая сердечная недостаточность может быть вызвана некоторыми заболеваниями, и такие заболевания считаются основными причинами сниженной сердечной функции. Однако другие факторы могут способствовать развитию сердечной недостаточности у пациентов, которые жили относительно благополучно в течение долгого времени, несмотря на то, что они страдали заболеванием, вызывающим сердечную недостаточность. Общие причины сердечной недостаточности включают чрезмерную постнагрузку и преднагрузку, ухудшенный кровоток в желудочках, несовершенную сердечную функцию, вызванную ишемией миокарда, и первичное заболевание миокарда. Факторы, способствующие сердечной недостаточности, включают инфекционный эндокардит, острый миокардит, неконтролируемую гипертензию, острый инфаркт миокарда, легочную эмболию, различные инфекции, анемию, гипертироидизм, беременность, физическое и умственное напряжение, чрезмерное потребление алкоголя и переедание.
Симптомы сердечной недостаточности изменяются в зависимости от тяжести заболевания, но наиболее общим симптомом является затруднение дыхания. На ранних стадиях затруднение дыхания наблюдается только при упражнениях, но с прогрессированием сердечной недостаточности оно наблюдается даже в отсутствии физической активности. При принятии лежачего положения дыхание становится более затрудненным вследствие различия в объеме крови, поступающей в сердце. Другие симптомы включают кашель, одышку, сердцебиение, тошноту, замешательство, энурез, олигурию, системный отек, асцит, дискомфорт в верхнем отделе брюшной полости, боль и припухлость, быструю утомляемость и общую слабость.
Сердечная недостаточность диагностируется при медицинском осмотре, на основе личного и семейного анамнеза, или определением отклонений в левом желудочке или клапанах. Проводят электрокардиографию, эхокардиографию и катетеризацию сердца, чтобы оценить сердечную функцию и обнаружить заболевание коронарной артерии и инфаркт миокарда.
Лечение хронической сердечной недостаточности проводят путем устранения способствующих факторов, лечения заболеваний, являющихся ее основными причинами, уменьшения содержания соли в диете, уменьшения преднагрузки, используя диуретики, и уменьшения постнагрузки, используя вазодилаторы. Дигоксин или симпатомиметические амины, которые действуют, повышая сократительную способность миокарда, также пригодны для лечения хронической сердечной недостаточности.
Вазодилаторы, такие как ингибиторы ангиотензинпревращающего фермента (АПФ), нитраты и гидралазин, используются в первую очередь для лечения хронической сердечной недостаточности. Тиазид или петлевые диуретики могут быть назначены на ранних стадиях терапии, поскольку они могут уменьшить задержку жидкости. Гликозиды дигиталиса также использовались для лечения сердечной недостаточности. Сообщалось, что бета-блокаторы, такие как карведилол, метопролол и бисопролол, эффективны при хронической сердечной недостаточности.
Ингибиторы АПФ активируют цГМФ, который индуцирует расслабление гладкой мускулатуры сосудов, расширяя артериальные кровеносные сосуды. Из ингибиторов АПФ эналаприл, каптоприл и лизиноприл увеличивают выживаемость пациентов, имеющих хроническую сердечную недостаточность, а квинаприл и фозиноприл облегчают симптомы у пациентов, имеющих левожелудочковую дисфункцию. Таким образом, ингибиторы АПФ уменьшают появление осложнений у пациентов с сердечной недостаточностью и их смертность вследствие левожелудочковой дисфункции и соответственно применяются для лечения хронической сердечной недостаточности. Так, предполагалось, что лозартан, действующий на ренинангиотензиновую систему (РАС), имеет терапевтические эффекты в отношении сердечной недостаточности, и на сегодняшний день клинические испытания подтвердили его терапевтическую эффективность в отношении хронической сердечной недостаточности. Однако применение лозартана ограничено в случае пациентов с гипотензией и может воздействовать на функцию почек и содержания калия в крови. Хронический кашель наблюдается у 10% пациентов. Также другие побочные эффекты включают головокружение вследствие низкого кровяного давления, кожную сыпь и внезапное опухание губ и щек.
Блокаторы рецепторов ангиотензина II используются у пациентов, которые не могут переносить побочные эффекты ингибиторов АПФ. Они облегчают симптомы сердечной недостаточности по механизму действия, схожему с механизмом действия ингибиторов АПФ. В настоящее время проводятся испытания по исследованию того, могут ли быть использованы блокаторы рецепторов ангиотензина II в сочетании с ингибиторами АПФ. Блокаторы рецепторов ангиотензина II не вызывают серьезных побочных эффектов при их введении в виде однократной дозы в сутки, но изредка вызывают ухудшение функции почек.
Известно, что бета-блокаторы утяжеляют симптомы сердечной недостаточности, но их также рассматривают, как оказывающие полезные терапевтические эффекты. Они способствуют расслаблению сердечной мышцы, ослабляют сократительную способность миокарда и уменьшают дополнительное сердечное напряжение. Наиболее часто применяемыми бета-блокаторами являются карведилол и метопролол, которые оказывают полезные действия, предотвращая прогрессирование сердечной недостаточности, укорачивая период пребывания в стационаре и снижая смертность. Бета-блокаторы следует вводить, начиная с малой дозировки, и дозировку следует увеличивать постепенно в течение длительного периода нескольких месяцев. В течение нескольких недель после введения симптомы часто ухудшаются, поскольку доставка кислорода в организм уменьшается. Другие побочные эффекты включают гипотензию, затруднение дыхания и тошноту.
Кроме вышеупомянутых лекарственных средств для лечения сердечной недостаточности применяются ингибиторы фосфодиэстеразы III, антиаритмические средства III класса, такие как амиодарон, имплантируемые кардиовертерные дефибрилляторы (ИКД) и блокаторы кальциевых каналов (БКК), такие как амлодипин и фелодипин. ИКД, которые все еще исследуются, одобрены только для применения в группе высокого риска, а БКК используются только у пациентов, имеющих другие показания для терапии БКК.
Показано, что ингибиторы фосфодиэстеразы V (ФДЭ-5) сдерживают увеличение, перестройку и фиброз желудочковой мышцы у мышей, у которых перегрузка давлением была вызвана силденафилом (Nature medicine 2005 11(2): 214-222). Известно, что эффекты ингибиторов ФДЭ-5 достигаются посредством механизма, который включает блокировку активности ФДЭ-5, катализирующей разрушение циклической гуанозинмонофосфатазы (цГМФ), спаренной с внутренней сигнальной системой сердца, сдерживая, таким образом, пролиферативные реакции миокарда (Journal of Biological Chemistry 2003, 278: 47694-47699).
Авторы настоящего изобретения до данной заявки разработали 5-[2-пропилокси-5-(1-метил-2-пирролидинил-этил-амидосульфонил)фенил]-1-метил-3-пропил-1,6-дигидро-7H-пиразоло(4,3-d)пиримидин-7-он, назвали соединение “уденафил” и сообщили, что данное соединение обладает эффектом ингибирования активности ФДЭ-5 (патент Кореи, регистрационный № 0353014).
Авторы данной заявки провели дополнительное исследование данного соединения, и это исследование дало новые данные о том, что соединение уденафил (также названное здесь “производным пиразолопиримидинона”) предотвращает увеличение желудочковой полости и утолщение стенки желудочка при хронической сердечной недостаточности. Данные дополнительно включают обнаружение того, что производное пиразолопиримидинона подавляет желудочковую экспрессию мРНК атриального натрийуретического пептида (АНП) и уменьшает количество коллагенового отложения, которое является маркером желудочкового фиброза, в желудочках, тем самым, приводя к настоящему изобретению.
ОПИСАНИЕ
Техническая проблема
Задача настоящего изобретения, следовательно, состоит в том, чтобы предоставить фармацевтическую композицию, включающую производное пиразолопиримидинона в качестве активного ингредиента для нового применения данного соединения в лечении хронической сердечной недостаточности.
Другая задача настоящего изобретения состоит в том, чтобы предоставить фармацевтическую композицию для улучшения угнетенной сердечной функции путем подавления морфологических изменений в сердцах в состоянии хронической недостаточности, снижения содержаний атриального натрийуретического пептида (АНП) и сдерживания желудочкового фиброза.
Дополнительная задача настоящего изобретения состоит в том, чтобы предоставить фармацевтическую композицию для лечения хронической сердечной недостаточности, включающую в качестве активного ингредиента производное пиразолопиримидинона, которое имеет хорошие профили фармакокинетики и безопасности в сравнении с традиционными ингибиторами фосфодиэстеразы-5 (ФДЭ-5).
Техническое решение
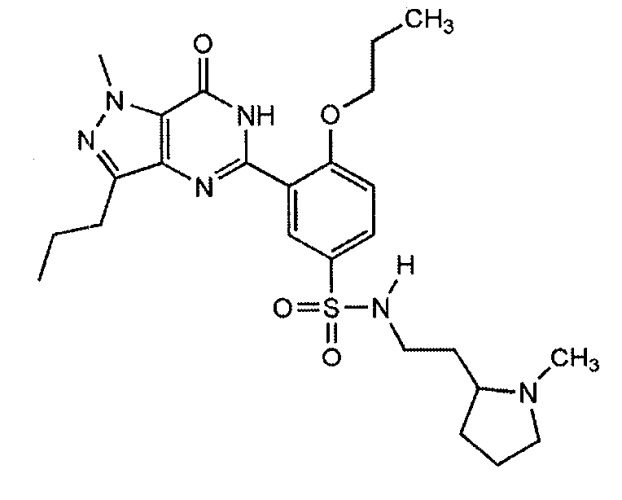
Для решения вышеназванных задач настоящее изобретение предоставляет фармацевтическую композицию, включающую в качестве эффективного ингредиента 5-[2-пропилокси-5-(1-метил-2-пирролидинил-этил-амидосульфонил)фенил]-1-метил-3-пропил-1,6-дигидро-7H-пиразоло(4,3-d)пиримидин-7-он (здесь далее названный “производным пиразолопиримидинона”), представленный ниже химической формулой 1, для нового применения данного соединения в лечении хронической сердечной недостаточности.
Химическая формула 1
Обеспечивающие преимущество эффекты
В соответствии с настоящим изобретением фармацевтическая композиция, включающая производное пиразолопиримидинона в качестве эффективного ингредиента, подавляет морфологические изменения в сердцах в состоянии хронической недостаточности. Также настоящая композиция снижает содержания циркулирующего атриального натрийуретического пептида (АНП), которые повышены при патофизиологическом состоянии хронической сердечной недостаточности, и подавляет кардиальную экспрессию мРНК АНП, тем самым, являясь подходящей в качестве терапевтического агента для лечения сердечной недостаточности. Дополнительно настоящая композиция сдерживает кардиофиброз, тем самым, улучшая систолическую и диастолическую функции сердца.
Также производное пиразолопиримидинона имеет длительный период полувыведения in vivo, что позволяет проводить введения с меньшей частотой, достигает максимального содержания в плазме за короткое время, обладает меньшим числом присущих ему побочных эффектов, влечет малую опасность взаимодействия с другими лекарственными средствами и имеет широкий безопасный диапазон доз.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
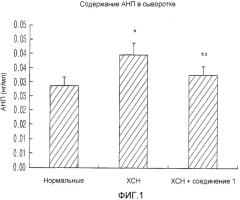
Фиг.1 представляет собой диаграмму, показывающую, что производное пиразолопиримидинона по настоящему изобретению снижает содержания АНП в сыворотке.
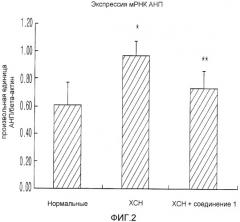
Фиг.2 представляет собой диаграмму, показывающую, что производное пиразолопиримидинона по настоящему изобретению снижает содержания мРНК АНП в ткани желудочка.
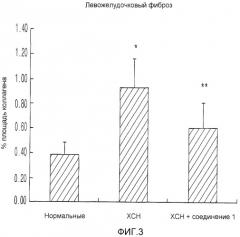
Фиг.3 представляет собой диаграмму, показывающую, что производное пиразолопиримидинона по настоящему изобретению снижает количество коллагенового отложения в ткани желудочка.
НАИЛУЧШИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
Производное пиразолопиримидинона по настоящему изобретению, которое представляет собой ингибитор фосфодиэстеразы 5 (ФДЭ-5), демонстрирует сильную и селективную ингибирующую активность в отношении ФДЭ-5, быстро абсорбируется благодаря своей повышенной растворимости, обладает высокой биодоступностью и большим объемом распределения, а также имеет период полувыведения in vivo в 3 раза больший, чем лекарственное средство силденафил, действующее по тому же механизму.
Производное пиразолопиримидинона имеет следующие физико-химические свойства: оно труднорастворимо в воде, но легкорастворимо в уксусной кислоте, метаноле и хлороформе; имеет температуру плавления 158-161°C; имеет значение pKa1 примерно 6,5 и значение pKa2 примерно 12,5; и не является гидратом или сольватом, а представляет собой белый или легкий белый порошок.
Производное пиразолопиримидинона синтезируют трехстадийным способом, как изложено ниже.
Вкратце, на первой стадии получают 4-[2-пропилокси-5-(хлорсульфонил)бензамидо]-1-метил-3-пропил-5-карбамоилпиразол. 4-[2-Пропилоксибензамидо]-1-метил-3-пропил-5-карбамоилпиразол смешивают с заданным количеством хлорсульфоновой кислоты, предварительно охлажденной до 0°C. Смесь фильтруют, и фильтрат промывают и высушивают с получением 4-[2-пропилокси-5-(хлорсульфонил)бензамидо]-1-метил-3-пропил-5-карбамоилпиразола.
Вторая стадия состоит в получении 4-[2-пропилокси-5-(1-метил-2-пирролидинилэтиламидосульфонил)бензамидо]-1-метил-3-пропил-5-карбамоилпиразола из пиразольного соединения, полученного на первой стадии. Заданное количество дихлорметанового раствора 4-[2-пропилокси-5-(хлорсульфонил)бензамидо]-1-метил-3-пропил-5-карбамоилпиразола, полученного на первой стадии, смешивают с заданным количеством 2-(2-аминоэтил)-1-метилпирролидином при перемешивании при 0°C. По завершении реакции реакционную смесь разбавляют дихлорметаном. Органическую фазу промывают, высушивают, концентрируют и фильтруют, получая 4-[2-пропилокси-5-(1-метил-2-пирролидинилэтиламидосульфонил)бензамидо]-1-метил-3-пропил-5-карбамоилпиразол.
Третья стадия состоит в получении соединения настоящего изобретения, 5-[2-пропилокси-5-(1-метил-2-пирролидинил-этил-амидосульфонил)фенил]-1-метил-3-пропил-1,6-дигидро-7H-пиразоло(4,3-d)пиримидин-7-она, из соединения, полученного на второй стадии. Заданное количество пиразольного соединения, синтезированного на второй стадии, растворяют в трет-бутаноле и смешивают с заданным количеством трет-бутоксида калия при кипячении с обратным холодильником в течение заданного периода времени. По завершении реакции реакционную смесь охлаждают, разбавляют, промывают и высушивают. Высушенный продукт подвергают перегонке при пониженном давлении, удаляют из него растворитель и подвергают колоночной хроматографии на силикагеле, получая чистое производное пиразолопиримидинона по настоящему изобретению.
Настоящее изобретение относится к фармацевтической композиции для лечения хронической сердечной недостаточности и может быть подробно описано следующим образом.
1) Настоящее изобретение предоставляет терапевтический агент, который подавляет морфологические изменения сердца, вызванные сердечной недостаточностью.
2) Настоящее изобретение предоставляет терапевтический агент, который подавляет экспрессию атриального натрийуретического пептида (АНП), которая повышена в сердцах с недостаточностью функции, с целью нормализации содержаний АНП, и который сдерживает желудочковый фиброз.
3) Настоящее изобретение предоставляет терапевтический агент для лечения хронической сердечной недостаточности, который обладает лучшими фармакокинетическими свойствами и более безопасен, чем традиционные ингибиторы фосфодиэстеразы-5 (ФДЭ-5).
Терапевтический агент, включающий производное пиразолопиримидинона по настоящему изобретению в качестве эффективного ингредиента, может быть использован в обычных фармацевтических лекарственных формах. То есть при клиническом применении производное пиразолопиримидинона по настоящему изобретению может быть введено с использованием широкого разнообразия пероральных и парентеральных лекарственных форм, причем в настоящем изобретении пероральное введение является предпочтительным. Форма может быть получена с обычно используемыми разбавителями или эксципиентами, такими как наполнители, загустители, связующие, увлажнители, дезинтеграторы и поверхностно-активные вещества.
Твердые формы для перорального введения могут включать таблетки, пилюли, порошки, гранулы и капсулы, и их получают смешением соединения-производного пиразолопиримидинона с одним или более эксципентами, такими как крахмал, карбонат кальция, сахароза, лактоза и желатин. Также твердые формы кроме простого эксципиента могут включать смазывающее, такое как стеарат магния или тальк.
Жидкие формы для перорального введения могут включать суспензии, внутренние растворы, эмульсии и сиропы. Жидкие формы могут включать кроме обычно используемых простых разбавителей, таких как вода и жидкий парафин, различные эксципиенты, примерами которых являются увлажнители, подсластители, ароматизаторы и консерваторы. Формы для парентерального введения могут включать стерильные водные растворы, неводные растворы, суспензии, эмульсии, лиофилизированные препараты и суппозитории. Неводные растворы и суспензии могут быть получены с использованием пропиленгликоля, полиэтиленгликоля, растительных масел, таких как оливковое масло, и инъецируемых сложных эфиров, таких как этилолеат. В качестве основы для суппозиториев могут быть использованы витепсол, макрогол, твин 61, масло какао, лауриновое масло и глицеринированный желатин.
Дозировка фармацевтической композиции настоящего изобретения, включающей производное пиразолопиримидинона в качестве эффективного ингредиента, может изменяться в зависимости от массы, возраста, пола и диеты пациента, времени и способа введения, скорости экскреции и тяжести заболевания. Предпочтительно, настоящее соединение может быть введено взрослому пациенту в суточной дозировке от 50 до 100 мг. Суточная дозировка может быть принята в виде единственной дозы или может быть поделена на несколько доз.
СПОСОБ ИЗОБРЕТЕНИЯ
Лучшее понимание настоящего изобретения может быть достигнуто рассмотрением следующих примеров, которые приведены для иллюстрации, но не должны истолковываться как ограничение настоящего изобретения.
Пример. Оценка терапевтических эффектов производного пиразолопиримидинона на животной модели сердечной недостаточности
Производное пиразолопиримидинона химической формулы 1 по настоящему изобретению оценивали, чтобы определить обладает ли оно терапевтическим эффектом в отношении сердечной недостаточности следующим образом.
Самцов крыс Sprague-Dawley массой 220-240 г рандомизированно делили на три группы: нормальную контрольную группу (нормальные), контрольную группу с сердечной недостаточностью (ХСН) и группу, получающую лечение (ХСН плюс соединение 1), причем каждая группа состояла из семи крыс. Производное пиразолопиримидинона вводили перорально животным с развитой сердечной недостаточностью группы, получающей лечение, в дозе 30 мг/кг.
Нормальных контрольных животных подвергали имитационной операции. Животным контрольной группы с сердечной недостаточностью и группы, получающей лечение, проводили хирургическое рассечение брюшной стенки, чтобы создать фистулу, соединяющую брюшную аорту с нижней полой веной, чтобы искусственно увеличить кровоток из нижней полой вены в правое предсердие. Спустя 8 недель 5 мл/кг растворителя вводили перорально нормальной контрольной группе и контрольной группе с сердечной недостаточностью в течение 8 недель, а производное пиразолопиримидинона вводили перорально группе, получающей лечение, в дозе 30 мг/кг в течение 8 недель. Затем крыс анестезировали пентобарбиталом (50 мг/кг, внутрибрюшинно) и подвергали эхокардиографии в M-режиме, чтобы оценить толщину стенки межжелудочковой перегородки (IWT) в конечную систолу (S) и конечную диастолу (D) левого желудочка, толщину задней стенки левого желудочка (PWT), размер левого желудочка в конечную систолу (LVESD) и размер левого желудочка в конечную диастолу (LVEDD). Относительную толщину стенки (RWT) рассчитывали по следующему уравнению: [IWT(D)+PWT(D)]/LVEDD, и она приведена ниже в Таблице.
После эхокардиографических измерений образцы крови отбирали из брюшной аорты для получения образцов сыворотки. Определяли сывороточные содержания атриального натрийуретического пептида (АНП), и они показаны на Фиг.1. 100 мг каждого образца ткани левого желудочка хранили в жидком азоте и затем подвергали полимеразной цепной реакции с обратной транскрипцией (RT-PCR), чтобы оценить содержания мРНК АНП. Измеренные содержания мРНК АНП показаны на Фиг.2. Оставшиеся части тканей фиксировали в 10% формалине и окрашивали Masson's trichrome для обнаружения коллагенового волокна, чтобы оценить левожелудочковый фиброз, и результаты приведены на Фиг.3. Все значения выражены как среднее ±SD.
Как показано в Таблице, эхокардиографические изображения в M-режиме короткой оси показывают, что крысы с индуцированной хронической сердечной недостаточностью (группа ХСН) имели значительно большие конечно-диастолические и конечно-систолические размеры левого желудочка, чем нормальные контрольные крысы, то есть увеличение, указывающее на желудочковую дилатацию, которая является типичным признаком сердечной недостаточности. Толщина стенки межжелудочковой перегородки в конечную систолу и систолическая и диастолическая толщина задней стенки левого желудочка были значительно меньше, и данное уменьшение является результатом расширения желудочковой полости, ведущего к истончению стенки желудочка, указывая на клинически значимое изменение сердца. Относительная толщина стенки, вычисленная с использованием приведенного выше уравнения, также значительно уменьшилась, и данные результаты согласуются с упомянутыми выше изменениями.
У крыс с аортокавальной фистулой, которые принимали производное пиразолопиримидинона в течение 8-недельного периода (группа, получающая лечение) конечно-диастолические и конечно-систолические размеры левого желудочка были значительно уменьшены по сравнению с контрольными крысами с сердечной недостаточностью (группа ХСН). Данные результаты показывают, что желудочковая дилатация, обнаруживаемая при хронической сердечной недостаточности, сдерживалась путем введения производного пиразолопиримидинона. Также по сравнению с контрольной группой с сердечной недостаточностью были значительно увеличены толщина стенки межжелудочковой перегородки в конечную систолу и конечную диастолу и толщина задней стенки левого желудочка, а также была значительно увеличена относительная толщина стенки. Данные результаты показывают, что производное пиразолопиримидинона сдерживают желудочковую дилатацию и уменьшение толщины стенки желудочка.
На Фиг.1 показаны сывороточные содержания атриального натрийуретического пептида (АНП). Контрольная группа с хронической сердечной недостаточностью обнаруживала значительно повышенные сывороточные содержания АНП (0,040±0,004 нг/мл) по сравнению с нормальной контрольной группой (0,029±0,003 нг/мл). Данное повышение было значительно понижено у крыс, принимавших производное пиразолопиримидинона (0,033±0,003 нг/мл).
На Фиг.2 показаны содержания мРНК АНП в тканях левого желудочка. Контрольная группа с хронической сердечной недостаточностью обнаруживала значительно повышенные содержания мРНК АНП (0,963±0,114) по сравнению с нормальной контрольной группой (0,607±0,169). Повышенные содержания мРНК АНП были значительно понижены у крыс, принимавших производное пиразолопиримидинона (0,739±0,120) по сравнению с контрольной группой с сердечной недостаточностью. Данные результаты показывают, что содержания АНП, увеличенные за счет патофизиологических изменений, были понижены до нормальных содержаний путем введения производного пиразолопиримидинона.
На Фиг.3 показано количество коллагенового отложения, как маркера желудочкового фиброза. Контрольная группа с хронической сердечной недостаточностью обнаруживала значительно повышенное коллагенового отложения (0,928±0,228) по сравнению с нормальной контрольной группой (0,384±0,103). Повышенное коллагеновое отложение было значительно понижено путем введения производного пиразолопиримидинона (0,604±0,214). Данные результаты показывают, что желудочковый фиброз, вызывающий желудочковую систолическую и диастолическую дисфункцию, был уменьшен производным пиразолопиримидинона, что тем самым улучшает желудочковую систолическую и диастолическую функцию.
| Таблица | |||
| Эхокардиографические измерения в M-режиме для оценки индукции хронической сердечной недостаточности у SD-крыс и терапевтических эффектов производного пиразолопиримидинонав отношении данного заболевания | |||
| Нормальные | ХСН | ХСН + соединение 1(30 мг/кг) | |
| IWT(D) (мм) | 1,81±0,20 | 1,56±0,09* | 1,74±0,13** |
| LVEDD (мм) | 8,69±0,56 | 9,75±0,85* | 8,45±0,62** |
| PWT(D) (мм) | 1,83±0,13 | 1,64±0,11* | 1,78±0,04** |
| IWT(S) (мм) | 2,83±0,17 | 2,56±0,11* | 2,74±0,11** |
| LVESD (мм) | 5,43±0,31 | 6,20±0,70* | 4,68±0,38** |
| PWT(S) (мм) | 2,89±0,15 | 2,54±0,18* | 2,80±0,10** |
| RWT | 0,42±0,05 | 0,34±0,02* | 0,42±0,05** |
| *: Группа ХСН обнаруживает значимое различие по сравнению с нормальной группой (p<0,05).**: Группа ХСН + соединение 1 обнаруживает значимое различие по сравнению с нормальной группой ХСН (p<0,05). |
Примеры форм. Получение фармацевтических форм для перорального введения
1. Получение порошков
| Соединение формулы | 12 г |
| Лактоза | 1 г |
Вышеназванные компоненты смешивали и помещали в воздухонепроницаемую упаковку, получая порошки.
2. Получение таблеток
| Соединение формулы 1 | 100 мг |
| Кукурузный крахмал | 100 мг |
| Лактоза | 100 мг |
| Стеарат магния | 2 мг |
Вышеприведенные компоненты смешивали и таблетировали согласно обычному способу получения таблеток, получая таблетки.
3. Получение капсул
| Соединение формулы 1 | 100 мг |
| Кукурузный крахмал | 100 мг |
| Лактоза | 100 мг |
| Стеарат магния | 2 мг |
Вышеприведенные компоненты смешивали и загружали в желатиновые капсулы согласно обычному способу получения капсул, получая капсулы.
1. Фармацевтическая композиция для лечения хронической сердечной недостаточности, содержащая производное пиразолопиримидинона, представленное ниже химической формулой 1, в качестве эффективного ингредиента
2. Фармацевтическая композиция по п.1, которая сдерживает морфологические изменения в сердце при хронической сердечной недостаточности.
3. Фармацевтическая композиция по п.1, которая сдерживает расширение желудочковой полости и изменение толщины стенки желудочка при хронической сердечной недостаточности.
4. Способ лечения хронической сердечной недостаточности, включающий введение производного пиразолопиримидинона, представленного ниже химической формулой 1, пациенту, нуждающемуся в таком лечении, в терапевтически эффективном количестве
5. Применение производного пиразолопиримидинона, представленного ниже химической формулой 1, для получения фармацевтической формы для лечения хронической сердечной недостаточности