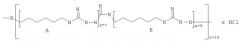
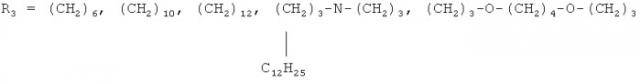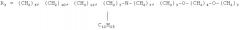Способ получения биоцидного полигуанидина и биоцидный полигуанидин
Иллюстрации
Показать всеИзобретения относятся к области медицины, ветеринарии, сельского хозяйства и фармакологии и касается биоцидного полигуанидина формулы (1), способа его получения и биоцидной композиции на его основе. Изобретения позволяют получить биоцидный полигуанидин с высокой антимикробной активностью широкого спектра действия. 3 н.п. ф-лы, 14 табл.
или
Реферат
Изобретения относятся к антисептическим средствам и способу их получения и могут быть использованы в качестве дезинфекционного средства широкого спектра действия в медицине, ветеринарии, сельском хозяйстве и т.д.
Согласно современным представлениям основной причиной порчи практически всех материалов (древесина, металл, кожа, краски, штукатурка, пищевых продуктов и т.п.), большей части болезней человека, животных и растений являются микробы - бактерии, грибы, вирусы и простейшие. Актуальность борьбы с ними постоянно возрастает во всех отраслях промышленности, в медицине, ветеринарии, сельском хозяйстве. Наибольшее значение в профилактике распространения микробных поражений во всех отраслях играют антисептики. Число общедоступных антисептиков для промышленности, медицины, ветеринарии и сельского хозяйства является явно недостаточным. Большая часть существующих препаратов имеет ряд выраженных недостатков, и, прежде всего, токсичность, неприятный запах, малую эффективность. Повсеместно наблюдается формирование и распространение микробов, устойчивых к существующим антисептикам (Fidel P.L. Jr, Vazquez J.A., Sobel J.D. Candida glabrata: review of epidemiology, pathogenesis and clinical disease with comparison to C.albicans 1999, 1:80-96. White T. Antifungal drug resistance in Candida albicans, ASM News 8:427-433). В промышленности многие антисептики представляют собой побочные продукты нефтехимической переработки и, как следствие, токсичны, имеют выраженный запах или содержат повышенное количество металлов, например меди, что также является серьезным недостатком.
В настоящее время существует потребность в новых антисептиках, особенно ввиду постоянного изменения видового состава патогенной микрофлоры и появления форм, резистентных к препарату. Как правило, поиски направлены на получение препаратов с заданными физико-химическими (растворимость, гидролитическая устойчивость и др.) и биологическими свойствами (широта действия, специфичность применительно к тем или иным микроорганизмам, активность к резистентным штаммам и др.).
Известен способ получения биоцидного гуанидина путем поликонденсации смеси гексаметилендиамина, додекаметилендиамина и гуанидингидрохлорида. После окончания процесса поликонденсации к раствору полученного сополимера добавляют гидразингидрат в тройном избытке и нагревают (обратным холодильником до прекращения выделения аммиака).
Раствор высушивают в вакууме, смешивают с 1 молем изоникотиновой кислоты и греют на масляной бане при 150°C до прекращения выделения влаги, RU 2176523.
Полученный продукт представляет собой гидрофобный полигуанидин, его водный раствор является биоцидным средством, предназначенным для использования в качестве дезинфицирующего вещества при туберкулезе.
Обработка гидразином полученного полигуанидина не позволяет ввести гидразиновый фрагмент в полимерную цепочку, поскольку при этом либо не происходит разрыв этой цепочки (при непродолжительном нагревании), либо происходит полное разрушение полимерной цепочки (при продолжительном и/или более интенсивном нагревании). В любом случае сохранить цепочку с введением в нее гидразинового фрагмента при реализации способа по RU 2176523 невозможно. Полученный по данному способу биоцидный полигуанидин имеет низкую биологическую активность и узкий спектр действия.
Известен способ получения биоцидного полигуанидина, включающий поликонденсацию α,ω-диамина с солью гуанидина; при этом используют гидрофобный α,ω-диамин в смеси с гексаметилендиамином или в смеси с 4,9-диоксадодекадимином H2N-(CH2)3-O-(CH2)4-O-(CH2)3-NH2 при следующих соотношениях, мас.%:
гидрофобный α,ω-диамин 16-60
гексаметилендиамин или
4,9-диоксадодекандиамин 84-40,
причем в качестве гидрофобного α,ω-диамина используют 1,10-декаметилендиамин H2N-(CH2)10-NH2 или 1,12-додекаметилендиамин (H2N-(CH2)12-NH2 или N,N-бис-(3-аминопропил)додециламин
В результате реализации способа получают биоцидный полигуанидин со следующей формулой:
где n=30-50;
R1 и R2 = H, CH3, C2H5, C4H9, C8H17, CH2C6H5, RU 2324478.
Данный способ, принятый в качестве прототипа настоящего изобретения, не обеспечивает достаточной степени полимеризации исходных компонентов (n=30-50) и не позволяет получить биоцидное средство с высокой биологической активностью.
Биоцидные полигуанидины указанного выше типа («метацид» и его аналоги) применяются более 50 лет, в результате чего возникло большое количество разнообразных резистентных штаммов патогенных микроорганизмов.
Задачей настоящих изобретений является получение биоцидного полигуанидина и композиции на его основе с высокой антимикробной активностью широкого спектра действия.
Согласно изобретению в части способа в способе получения биоцидного полигуанидина, включающем поликонденсацию гексаметилендиамина с солью гуанидина, в процессе поликонденсации дополнительно используют гидразингидрат при следующем соотношении компонентов, мас.%:
| гексаметилендиамин | 20-50 |
| соль гуанидина | 45-65 |
| гидразингидрат | остальное, |
при этом процесс ведут при температуре 190-200°С до прекращения выделения аммиака.
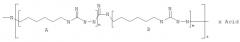
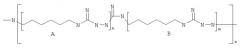
Согласно изобретению в части вещества заявлен биоцидный полигуанидин, полученный способом по п.1, с формулой:
или
где n - количество звеньев А в единичном фрагменте полимерной цепочки, n=1-3;
m - количество звеньев В в единичном фрагменте полимерной цепочки, m=2-10;
z - количество единичных фрагментов в полимерной цепочке, z=4-20;
Acid - HCl, или H2SO4, или СН3СООН, или С6Н5СООН.
Согласно изобретению в части биоцидной композизии заявлена композиция, представляющая собой водный раствор, содержащий биоцидный полигуанидин по п.2 и 0,5-20,0% водный раствор алгината натрия, или крахмала, или поливинилпирролидона, или карбоксиметилцеллюлозы, или пектина, или поливинилового спирта при следующем соотношении компонентов, мас.%:
| биоцидный полигуанидин | 0,01-10,0 |
| 0,5-20,0% водный раствор | |
| алгината натрия, | |
| или крахмала, | |
| или поливинилпирролидона, | |
| или карбоксиметилцеллюлозы, | |
| или пектина, | |
| или поливинилового спирта | остальное. |
Получение биоцидного полигуанидина заявленным способом поясняется примерами.
Пример 1. В колбу вместимостью 1 л, снабженную газоотводной трубкой и термометром, загружали 95,5 г гуанидина гидрохлорида (48,7 мас.%), 95,5 г гексаметилендиамина (48,7 мас.%) и 5 г гидразингидрата (2,6 мас.%). Содержимое колбы перемешивали и помещали в воздушный термостат, а газоотводную трубку подсоединяли к приемнику для улавливания аммиака; нагревали реакционную смесь до 200°С с постепенной отгонкой воды и аммиака и выдерживали 2 ч при этой температуре до прекращения выделения аммиака. После этого горячую сиропообразную массу выливали на металлический противень, охлаждали и получили 179 г продукта в виде твердого, практически бесцветного прозрачного стекловидного вещества с формулой:
Общее количество звеньев А и В в среднестатистической полимерной цепочке (n+m)z=100.
Пример 2. Способ осуществляли так же, как в примере 1, при этом использовали, мас.%:
Гуанидина гидрохлорида 65
Гексаметилендиамина 20
Гидразингидрата 15
Получено вещество с формулой
Общее количество звеньев А и В в среднестатистической полимерной цепочке (n+m)z=60.
Пример 3. Способ осуществляли так же, как в примере 1, при этом использовали, мас.%:
Гуанидина гидрохлорида 40
Гексаметилендиамина 55
Гидразингидрата 5,5
Получено вещество с формулой
Общее количество звеньев А и В в среднестатистической полимерной цепочке (n+m)z=48.
Пример 4. Способ осуществляли так же, как в примере 1, при этом использовали, мас.%:
Гуанидина сульфата 50
Гексаметилендиамина 45
Гидразингидрата 5
Получено вещество с формулой
Общее количество звеньев А и В в среднестатистической полимерной цепочке (n+m)z=100.
Пример 5. Способ осуществляли так же, как в примере 1, при этом использовали, мас.%:
Гуанидина карбоната 50
Гексаметилендиамина 45
Гидразингидрата 5
Получено вещество с формулой
.
Общее количество звеньев А и В в среднестатистической полимерной цепочке (n+m)z=80.
Пример 6. Способ осуществляли так же, как в примере 1, при этом использовали, мас.%:
Гуанидина ацетата 50
Гексаметилендиамина 37,5
Гидразингидрата 12,5
Получено вещество с формулой
Общее количество звеньев А и В в среднестатистической полимерной цепочке (n+m)z=100.
Пример 7. Способ осуществляли так же, как в примере 1, при этом использовали, мас.%:
Гуанидина бензоата 64,3
Гексаметилендиамина 33,9
Гидразингидрата 1,8
Получено вещество с формулой
Общее количество звеньев А и В в среднестатистической полимерной цепочке (n+m)z=99.
Элементный состав веществ по примерам 1-7, полученных согласно заявленному способу, приведен в таблице 1.
| Таблица 1 | ||||||||
| Пример № | × Acid | n | m | z | Данные элементного анализа, % | |||
| С | Н | N | Cl (S) | |||||
| 1 | HCl | 1 | 9 | 10 | 46,91 | 9,06 | 24,25 | 19,78 |
| 2 | HCl | 3 | 2 | 12 | 45,05 | 9,12 | 26,27 | 19,56 |
| 3 | HCl | 2 | 10 | 4 | 46,60 | 9,20 | 23,97 | 20,23 |
| 4 | H2SO4 | 1 | 9 | 10 | 43,60 | 9,02 | 22,11 | 8,44 |
| 5 | нет | 1 | 9 | 8 | 58,0 | 10,67 | 30,45 | - |
| 6 | СН3СООН | 2 | 3 | 20 | 45,87 | 8,69 | 21,94 | - |
| 7 | С6Н5СООН | 1 | 10 | 9 | 63,26 | 8,71 | 15,91 | - |
Антимикробная активность заявляемого вещества по примерам 1-7 в составе биоцидной композиции в сравнении с прототипом подтверждается следующими примерами. Минимальная подавляющая (биоцидная) концентрация активного компонента - биоциодного полигуанидина зависит от типа микроорганизма и конкретного штамма и находится в указанных в п.3 формулы изобретения пределах. При этом установлено, что существенного влияния на биологическую активность биоцидной композиции характер водного раствора указанных в п.3 формулы изобретения вспомогательных веществ не оказывает.
Пример 8.
Определение противогрибковой активности заявляемого вещества по отношению к спорам грибов.
В экспериментах использованы различные грибы - вегетативные формы и споры, вызывающие заболевания людей и животных, а также порчу сельскохозяйственных продуктов продуктов и различных промышленных материалов - древесины, кожи и др.
Биоцидные свойста испытаны на спорах культур грибов, предусмотренных ГОСТ 9.050-75. Оптическая плотность посевной суспензии спор Е=0,310. Суспензия содержала в равных пропорциях споры следующих микромицетов:
Aspergillis niger
Aspergillis terreus
Alternaria alternata
Fusarium moniliforme
Penicillium brevicompactum
Penicillium chrysogenum
Penicillium ochrochloron
Penicillium martensii
Trichoderma viride
Определение антисептических свойств заявляемых веществ проводили через 7 суток выращивания микромицетов методом бумажных дисков и методом лунок (таблица 2).
| Таблица 2 | ||||||||
| Споры грибов (смесь) | Минимальная подавляющая (биоцидная) концентрация (МПК) вещества в водном растворе, мкг/мл | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | Прототип | |
| А.niger | ||||||||
| A.terreus | ||||||||
| A.alternata | ||||||||
| F.moniliforme | 1,0 | 1,5 | 0,5 | 0,5 | 1,0 | 1,5 | 2,0 | 3,5 |
| Р.brevicompactum | ||||||||
| Р.chrysogenum | ||||||||
| Р.ochrochloron | ||||||||
| Р.martensii |
Зона ингибирования составила от 16 до 38 мм. Вещество по примерам 3, 4 проявляет биоцидные свойства уже в концентрации 0,1%.
Пример 9.
Оценка эффективности воздействия вещества на дрожжи и дрожжеподобные грибы.
Активность против дрожжей и дрожжеподобных грибов определяли методом серийных разведений.
Испытуемые вещества растворяли в воде и титровали в среде N-1, RPMI, Сабуро так, что заявленное вещество содержалось в отдельных пробирках со средой в различных концентрациях.
| Таблица 3 | |||||||||
| Гриб | Штамм | Минимальная подавляющая концентрация (МПК) (мкг/мл) в водном растворе (примеры 1-7 и прототип) | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | Прототип | ||
| Saccharomyces cervisiae | VT-2 | 0,5 | 0,7 | 0,4 | 0,5 | 0,5 | 0,7 | 0,8 | 12000 |
| Candida albicans | 21 | 0,8 | 0,7 | 0,5 | 0,5 | 0,7 | 0,8 | 0,9 | 10000 |
| Candida albicans | 372 | 0,9 | 0,7 | 0,3 | 0,3 | 0,6 | 0,9 | 1,0 | 12000 |
| Candida albicans | 80 | 1,0 | 0,8 | 0,3 | 0,4 | 0,5 | 0,6 | 0,7 | 12000 |
| Candida glabrata | 382 | 0,8 | 0,8 | 0,7 | 0,8 | 1,0 | 1,1 | 1,2 | 14000 |
| Candida glabrata | 111 | 0,7 | 0,8 | 0,5 | 0,6 | 0,7 | 0,8 | 0,9 | 12000 |
| Candida glabrata | 160 | 0,8 | 0,9 | 0,6 | 0,7 | 0,8 | 0,8 | 1,0 | 12000 |
| Candida krusei | 21 | 0,9 | 1,0 | 0,7 | 0,8 | 1,0 | 1,1 | 1,2 | 12000 |
Данные таблицы 3 свидетельствуют о весьма высокой активности заявляемого вещества по отношению к дрожжам и одноклеточным грибам рода Candida в сравнении с прототипом.
Пример 10.
Определение эффективности вещества в отношении грамположительных и грамотрицательных бактерий (аэробных и анаэробных).
В экспериментах использованы стандартные коллекционные штаммы и бактерии, выделенные от больных. Оценку проводили методом серийных разведений с использованием питательных сред пригодных для культивирования соответствующих видов микроорганизмов.
Соединения растворяли в стерильной воде и титровали в концентрациях от 500 до 0,025 мг/л. Концентрация препарата в среде соседних пробирок отличалась в два раза. Результат учитывали после 72-часового культивирования бактерий при 37°С (таблица 4).
| Таблица 4 | ||||||||
| Микроорганизм | МПК (мкг/мл) | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | Прототип | |
| Escherichia coli АТСС922 | 0,7 | 0,9 | 0,5 | 0,5 | 1,0 | 1,5 | 2,0 | 2,0 |
| Salmonella typhimur. VT-191 | 1,5 | 2,0 | 1,0 | 1,1 | 2,0 | 3,0 | 4,0 | 10,1 |
| Enterococcus fecalis | 1,5 | 2,0 | 1,0 | 1,5 | 2,0 | 2,5 | 3,0 | 4,0 |
| Pseudomonas aeruginosa ATCC27853 | 0,1 | 0,2 | 0,1 | 0,1 | 0,1 | 0,1 | 0,2 | 0,1 |
| Klebsiella pneumoniae | 0,7 | 1,0 | 0,5 | 1,0 | 1,5 | 1,5 | 2,0 | 2,0 |
| Bacillus cereus | 2,5 | 3,0 | 2,0 | 2,0 | 2,5 | 2,5 | 3,0 | 12 |
| Staphylococcus aureus VT-209 | 2,5 | 3,0 | 2,0 | 2,5 | 2,5 | 3,0 | 3,0 | 5,0 |
| Fusobacterium nucleatum | 0,3 | 0,4 | 0,2 | 0,3 | 0,5 | 0,6 | 0,7 | 0,4 |
| Porfhiromonas gingivalis | 0,8 | 1,0 | 0,5 | 0,6 | 1,0 | 1,5 | 2,5 | 6,0 |
| Prevotella melaninogenica | 0,8 | 1,0 | 0,4 | 0,7 | 1,0 | 1,1 | 1,4 | 1,5 |
Таким образом, заявляемое вещество обладает выраженной антибактериальной активностью.
Пример 10.
Определение действия заявляемого вещества на микобактерии туберкулеза.
Для определения активности был использован стандартный штамм Mycobacterium tuberculosis H37Rv, чувствительный ко всем антимикробным препаратам. Оценку антимикобактериального действия проводили методом серийных разведений.
Вещества растворяли в стерильной воде и титровали так, чтобы препарат содержался в отдельных пробирках со средой в концентрациях от 200 до 0,025 мг/л. Концентрация препарата в среде соседних пробирок отличалась в два раза. Результат учитывали после 72-часового культивирования бактерий при 37°С (таблица 5).
| Таблица 5 | ||||||||
| Микроорганизм | МПК (мкг/мл) | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | Прототип | |
| Mycobacterium tuberculosis H37Rv | 10,0 | 10,0 | 10,0 | 10,0 | 10,0 | 10,0 | 10,0 | 2000 |
Таким образом, заявляемые соединения по активности против возбудителя туберкулеза значительно превосходят прототип.
Пример 11.
Определение антипротозойного действия вещества по отношению к трихомонадам (Trichomonas vaginalis).
В экспериментах использованы штаммы, выделенные от больных. Оценку проводили методом серийных разведений с использованием питательных сред пригодных для культивирования соответствующих видов микроорганизмов.
Вещества растворяли в стерильной воде и титровали в концентрациях от 500 до 0,025 мг/л. Концентрация препарата в среде соседних пробирок отличалась в два раза. Результат учитывали после 72-часового культивирования бактерий при 37°С (таблица 6).
| Таблица 6 | ||||||||
| Микроорганизм | Минимальная подавляющая (бактерицидная) концентрация (МПК) (мкг/мл) в водном растворе | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | Прототип | |
| Trichomonas vaginalis | 0,02 | 0,02 | 0,01 | 0,01 | 0,01 | 0,02 | 0,02 | 0,02 |
Результаты свидетельствуют о достаточно высокой активности заявляемого вещества против простейших на примере трихомонад.
Пример 12.
Определение действия заявляемого вещества на вирус простого герпеса.
Антивирусная активность изучалась по отношению к вирусу простого герпеса I типа (ВПГ-I/Ленинград/248/88) по общепринятому методу [Gentry G.A., Lawrency N., Lushbaugh N. Isolation and differentiation of Herpes simplex virus and Trichomonas vaginalis in cell culture, J. of Clinical Microbiology 1985, Vol.22, No.2, P.199-204]. Вирусы выращивали на перевиваемой культуре клеток Vero, полученной из банка клеточных культур Института цитологии РАН. Результаты оценивали по наличию цитопатогенного действия вируса на клетки через 36 часов культивирования при 37°С в СО2-инкубаторе. Для оценки цитопатического действия вируса подсчитывали число неизмененных клеток. Результаты приведены в таблице 7.
| Таблица 7 | ||||||||
| Вирус | МПК (мкг/мл) | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | Прототип | |
| ВПГ-I/Ленинград/248/88 | 80,0 | 100,0 | 50,0 | 70,0 | 100,0 | 140,0 | 150,0 | 1000 |
Полученные результаты указывают, что заявленное вещество обладает высокой активностью против вируса герпеса.
Пример 13.
Использование заявляемого вещества для борьбы со смешанной микробной инфекцией.
У лабораторных животных (морские свинки) выбривали часть волосяного покрова, наносили поверхностные царапины и втирали микробную смесь, состоящую из грибов рода Candida, стафилококка, кишечной палочки и энтерококка. Через 24 часа у всех животных возникал местный воспалительный процесс. Для лечения использовали мазь, приготовленную из вещества по примеру 3, или вещества-прототипа, приготовленного в виде мази на ланолине. Вещества были добавлены в количестве 100 мкг/мл. В контрольной группе наносили чистый ланолин. Каждая группа включала 5 животных. Критерием эффективности был срок полного заживления и восстановления кожного покрова. У животных в группах, леченных веществом по примеру 3, выздоровление наступило через 5 дней. В группах, получавших препарат-прототип в течение 6 дней, все животные были больны. Выздоровление этой группы наступило через 13 дней, а в контрольной группе с ланолином - через 15 дней.
Таким образом, полученные данные свидетельствуют, что заявленное вещество может быть эффективно использовано местно для борьбы со смешанными инфекциями, вызванными грамположительными и грамотрицательными бактериями и грибами.
Пример 14.
Использование заявленного вещества для придания антимикробных свойств краскам.
В работе использована белая водоэмульсионная краска завода «Кронос», в которую было добавлено заявленное вещество по примеру 5 в конечной концентрации 1,0%. В чашках Петри на питательную среду засевали тест-микробы (Е.coli ATCC 25922, S.aureus VT209, Candida ATCC 885-653, Aspergillus niger VT-7765) и после 15-минутного подсушивания поверх них накладывали бумажные диски диаметром 5 мм, пропитанные краской с заявленным веществом. После инкубации в течение 20-24 часов при 35-37°С определяли наличие и величину зоны угнетения роста микробов вокруг дисков. Во всех экспериментах было зарегистрировано выраженное угнетение роста тест штаммов использованных бактерий.
Таким образом, полученные данные свидетельствует, что заявленное вещество, введенное в водоэмульсионную краску, сохраняло антимикробные свойства и проявляло их по отношению к различным неродственным бактериям и грибам.
Пример 15.
Использование заявляемого вещества для обработки корневых каналов зубов.
Исследование выполнено на экстерпированных зубах. Зубы предварительно обрабатывали, удаляли посторонние вещества и очищали корневой канал. В обработанные таким образом зубы в канал вводили 0,05% вводный раствор вещества по примеру 7 или вещества-прототипа, после чего вход в канал закрывали временной пломбой, не пропускающей жидкость. Зуб помещали на 24 часа в стерильной пустой чашке Петри в термостат и инкубировали при температуре 37°С 20-24 часа. Во время этой инкубации могла происходить диффузия веществ в канальцы дентина. Известно, что именно канальцы дентина могут быть местом, где сохраняются вредные и опасные микробы после обработки корневых каналов, при этом общая протяженность таких канальцев в однокорневом зубе составляет около 5 километров. После инкубации зубы помещали в полужидкий агар, содержащий тест-микробы (Е.coli или S.aureus) в количестве 1,0-5,0×105 мл.
Чашки инкубировали еще 20-24 часа при 37°С. Результат учитывали по наличию и величине зоны угнетения роста, возникающей по периметру зуба. Наличие зоны угнетения роста свидетельствовало о проникновении препарата в дентин, его способности выходить по периметру зуба (в организме человека в ткани вокруг зуба) и сохранять антимикробные свойства.
Препарат во всех использованных концентрациях, начиная с 0,05, вызывал антимикробный эффект в поставленных экспериментах.
Пример 16.
Придание антимикробных свойств шовному материалу и эндопротезам.
В чашку Петри ⌀ 90 мм с тонкой (3 мм) подложкой из 1,5% МПА помещали образцы нитей длиной около 1 см по 2 кусочка на пробу, по 4 кусочка на чашку. Пробы заливали 6 мл 0,7% МПА, содержащего 0,6 мл тест-культуры в концентрации 5×105 микроорганизмов в 1 мл. Посевы инкубировали в термостате при 37°С в течение 24 ч (бактерии), 30°С - 24 ч (грибы).
Чашки с 1,5% МПА засевали газоном взвесью микроорганизмов в физиологическом растворе в концентрации 5×105, разведенной в 10 раз для бактерий, 5 ЕД, разведенной в 10 раз для грибов. Чашки подсушивали при комнатной температуре в течение 10-15 минут, далее на них раскладывали диски из фильтровальной бумаги ⌀ 6 мм, смоченные исследуемыми растворами, в количестве 2 диска на пробу, 4 диска на чашку. Пробы снова подсушивали в перевернутом виде в течение 10-15 мин и инкубировали в термостате при 37°С в течение 24 ч (бактерии), при 30°С - 24 ч (грибы).
Результаты оценивали по наличию или отсутствию зон задержки роста вокруг тестируемых объектов (таблица 8); использованы шовные нити и сетки (эндопротезы).
| Таблица 8. | |||||
| № | Тестируемый объектТест-культуры | Антимикробная активность (мм от края нити) | |||
| Е.coli АТСС 25922 | St. aureus 209 | Candida АТСС 885-653 | Aspergillus niger | ||
| 1 | Капроновая нить, обработанная водным раствором заявленного вещества (1,0 мг/1,0 мл) | 4 | 6 | 5 | 6 |
| 2 | Лавсановая нить, обработанная водным раствором заявленного вещества (1,0 мг/1,0 мл) | 5 | 4 | 4 | 5 |
| 3 | Сетка полипропиленовая заявленного вещества (1,0 мг/1,0 мл) | 5 | 6 | 5 | 4 |
| Продолжение Таблицы 8. | |||||
| № | Тестируемый объектТест-культуры | Антимикробная активность (мм от края нити) | |||
| Е.coli АТСС 25922 | St. aureus 209 | Candida АТСС 885-653 | Aspergillus niger | ||
| 4 | Сетка из ПВДФ волокна заявленного вещества (1,0 мг/1,0 мл) | 6 | 5 | 5 | 3 |
| 5 | Лавсановая сетка заявленного вещества (1,0 мг/1,0 мл) | 8 | 7 | 8 | 6 |
Полученные результаты свидетельствуют, что заявленное вещество (по примеру 2), нанесенное на шовный материал, смывается с него и сохраняет антимикробную активность с широким спектром действия и угнетает рост грамположительной и грамотрицательной бактериальной флоры, а также одно- и многоклеточных грибов, представляющих опасность для человека.
Пример 17.
Пролонгирование действия биоцидного полигуанидина.
Для пролонгирования действия и нанесения на поверхности большего количества биоцидного полигуанидина были приготовлены водные растворы алгината натрия, или крахмала, или поливинилпиролидона, или карбоксиметилцеллюлозы, или пектина, или поливинилового спирта. Готовили растворы, содержащие биоцидный полигуанидин - 0,01-10,0%, а остальное 0,5-20,0% водный раствор алгината натрия, или 0,5-20,0% водный раствор крахмала, или 0,5-20,0% водный раствор поливинилпиролидона, 0,5-20,0% водный раствор карбоксиметилцеллюлозы, или 0,5-20,0% водный раствор пектина, или 0,5- 20,0% водный раствор поливинилового спирта.
Для оценки длительности антимикробного действия приготовленные растворы наносили на стандартную, стерильную металлическую проволоку, давали высохнуть и помещали в стерильный изотонический раствор хлорида натрия при температуре 37°С. После экспозиций различной продолжительности в растворе хлорида натрия кусочки проволоки извлекали и для определения антимикробного действия помещали на плотную питательную среду, засеянную грамположительными бактериями S.aureus VT209. Антимикробное действие оценивали по наличию зоны угнетения роста после 24 часов культивирования при 37°С.
Определение антимикробного действия раствора биоцидный полигуанидин с алгинатом натрия после инкубации в изотоническом растворе хлорида натрия (таблица 9).
| Таблица 9 | ||
| Водный раствор алгината натрия, % | Продолжительность сохранения антимикробного действия, часы | |
| Биоцидный полигуанидин (№3) (0.01%) | биоцидный полигуанидин (№3) (10.0%) | |
| 0,5 | 5 | 48 |
| 20 | 20 | 72 |
Определение антимикробного действия раствора биоцидный полигуанидин с крахмалом после инкубации в изотоническом растворе хлорида натрия (таблица 10).
| Таблица 10 | ||
| Водный раствор крахмала, % | Продолжительность сохранения антмикробного действия, часы | |
| биоцидный полигуанидин (№3) (0.01%) | биоцидный полигуанидин (№3) (10.0%) | |
| 0,5 | 3 | 28 |
| 20 | 18 | 36 |
Определение антимикробного действия раствора биоцидный полигуанидин с поливинилпиролидоном после инкубации в изотоническом растворе хлорида натрия (таблица 11).
| Таблица 11 | ||
| Водный раствор поливинилпиролидона, % | Продолжительность сохранения антмикробного действия, часы | |
| биоцидный полигуанидин (№3) (0.01%) | биоцидный полигуанидин (№3) (10.0%) | |
| 0,5 | 6 | 48 |
| 20 | 24 | 72 |
Определение антимикробного действия раствора биоцидный полигуанидин с карбоксиметилцеллюлозой после инкубации в изотоническом растворе хлорида натрия (таблица 12).
| Таблица 12 | ||
| Водный раствор карбоксиметилцеллюлозы, % | Продолжительность сохранения антимикробного действия, часы | |
| биоцидный полигуанидин (№3) (0.01%) | биоцидный полигуанидин (№3) (10.0%) | |
| 0,5 | 10 | 54 |
| 20 | 24 | 78 |
Определение антимикробного действия раствора биоцидный полигуанидин с пектином после инкубации в изотоническом растворе хлорида натрия (таблица 13).
| Таблица 13 | ||
| Водный раствор пектина, % | Продолжительность сохранения антмикробного действия, часы | |
| биоцидный полигуанидин (№3) (0.01%) | биоцидный полигуанидин (№3) (10.0%) | |
| 0,5 | 4 | 40 |
| 20 | 16 | 72 |
Определение антимикробного действия раствора биоцидный полигуанидин с поливиниловым спиртом после инкубации в изотоническом растворе хлорида натрия (таблица 14).
| Таблица 14 | ||
| Водный раствор поливинилового спирта, % | Продолжительность сохранения антмикробного действия, часы | |
| биоцидный полигуанидин (№3) (0.01%) | биоцидный полигуанидин (№3) (10.0%) | |
| 0,5 | 5 | 48 |
| 20 | 20 | 72 |
Таким образом, полученные данные свидетельствуют, что приготовление композиций указанного состава приводит к пролонгации действия биоцидного полигуанидина. Эффективность пролонгации имеет дозозависимый характер.
1. Способ получения биоцидного полигуанидина, включающий поликонденсацию гексаметилендиамина с солью гуанидина, отличающийся тем, что в процессе поликонденсации дополнительно используют гидразингидрат при следующем соотношении компонентов, мас.%:
| гексаметилендиамин | 20-55 |
| соль гуанидина | 25-65 |
| гидразингидрат | остальное |
2. Биоцидный полигуанидин, полученный способом по п.1, формулы: или где n - количество звеньев А в единичном фрагменте полимерной цепочки, n=1-3;m - количество звеньев В в единичном фрагменте полимерной цепочки, m=2-10;z - количество единичных фрагментов в полимерной цепочке, z=4-20;Acid - НСl, или Н2SO4, или СН3СООН, или С6Н5СООН.
3. Биоцидная композизия, представляющая собой водный раствор, содержащий биоцидный полигуанидин по п.2 и 0,5-20,0%-ный водный раствор алгината натрия, или крахмала, или поливинилпирролидона, или карбоксиметилцеллюлозы, или пектина, или поливинилового спирта при следующем соотношении компонентов, мас.%:
| биоцидный полигуанидин | 0,01-10,0 |
| 0,5-20,0%-ный водный раствор | |
| алгинат натрия, | |
| или крахмала, | |
| или поливинилпирролидона, | |
| или карбоксиметилцеллюлозы, | |
| или пектина, | |
| или поливинилового спирта | остальное |