Способ извлечения ионов меди(ii) из аммиачных сред с использованием бета-n-оксиэтилгидразидов алифатических карбоновых кислот
Иллюстрации
Показать всеИзобретение относится к новому способу очистки воды от катионов меди(II) в присутствии аммиака, который основан на применении в качестве реагента для флотации β-N-оксиэтилгидразидов алифатических карбоновых кислот формулы (I), где R - радикал с прямой цепью, содержащей от 7 до 14 атомов углерода. Заявляемый способ обеспечивает высокую (до 99,0%) степень извлечения ионов меди(II) из аммиачных сред в одну ступень при относительно небольшом расходе реагента. 1 з.п. ф-лы, 3 табл., 2 ил.
Реферат
Изобретение относится к новым соединениям класса β-N-оксиэтилгидразидов алифатических карбоновых кислот и способу их использования в процессах очистки воды от ионов цветных металлов, например, сточных вод гальванических производств от катионов меди(II) в присутствии амиака.
Описания заявляемых соединений, их свойств и способа их применения в источниках информации не обнаружено.
Известны различные способы очистки воды от ионов цветных металлов электрохимическими, химическими и другими способами и их комбинациями. Извлечение ионов цветных металлов из аммиачных сред затруднено из-за образования аммиакатов.
Известен, например, способ флотационной очистки сточных вод гальванических производств от ионов цветных металлов, в том числе меди(II), включающий двухстадийную флотацию в импеллерном и пневматическом флотаторах с применением в щелочной среде при рН 9 в качестве флотореагента 2% мас., водного раствора хозяйственного мыла, играющего роль осадителя и флотационного собирателя [Скрылев Л.Д., Бабинец С.К., Костик В.В. и др. Флотационная очистка сточных вод гальванических производств. // Химия и технология воды, 1990, т.12, №2, с.168-170].
Известен также способ извлечения ионов меди и ионов других цветных металлов из щелочных растворов с использованием в качестве реагента симметричных 1,2-диацилгидразинов [пат. РФ №2135418, МКИ 8 C02F 1/62, 1/58. Способ очистки воды от ионов тяжелых металлов. Опубл. 27.08.1999].
К недостаткам обоих способов можно отнести то, что очистка воды осуществляется в щелочной среде, но нет данных о применении их для извлечения ионов цветных металлов из аммиачных сред. Кроме того, в вышеописанных способах очищению подвергается вода с достаточно большим содержанием меди (сотни - десятки мг/л). Использование этих способов для доочистки воды с содержанием 10 мг/л меди(II) и менее не описано.
Наиболее близким по технической сущности и достигаемому результату является способ извлечения малых количеств меди(II) из аммиачных растворов методом ионной флотации с использованием несимметричных 1,2-диацилгидразинов [Чеканова Л.Г., Ельчищева Ю.Б., Радушев А.В., Жданова Е.В. Флотация ионов цветных металлов из аммиачных растворов с несимметричными 1,2-диацилгидразинами. // Сб. докладов международной конференции «Техническая химия. От теории к практике. г.Пермь, 8-12 сентября 2008 г.». Ч.2. - Пермь: ИТХ УрО РАН, 2008. - С.336-340].
Недостатком данного способа является относительно низкое извлечение меди(II) при значительном расходе собирателя.
Задачей изобретения является расширение ассортимента флотореагентов для очистки воды, получение новых соединений из ряда β-N-гидроксиэтилгидразидов алифатических карбоновых кислот и разработка способа извлечения меди(II) из аммиачных растворов с их использованием.
Для решения поставленной задачи синтезированы β-N-оксиэтилгидразиды алифатических карбоновых кислот общей формулы
где R - радикал с прямой или разветвленной цепью, содержащей от 5 до 14 атомов углерода.
Синтезированы соединения общей формулы (I), где R=C5H11 (1) ; C7H15 (2); С4Н9СН(С2Н5) (3); C10H21 (4); С14Н29 (5). Соединения общей формулы (I) выделены в твердом виде. Соединения 1-4 - белые масла, 5 - белое кристаллическое вещество с tпл=67-68°C.
Синтез соединений общей формулы (I) проводили способом оксиалкилирования соответствующих ацилгидразидов с помощью β-Сl - этанола.
Строение соединений общей формулы (I) подтверждено данными элементного анализа, тонкослойной хроматографии, ИК-спектрами (снятыми на Фурье-спектрометре IFS 66/S Bruker, в вазелиновом масле), спектрами ЯМР 1H (полученными на спектрометре "MERCURY plus 300") и анализом на содержание основного вещества.
Спектральные характеристики заявляемых соединений представлены в таблица 1.
Предлагается способ извлечения ионов меди(II) из аммиачных сред, включающий обработку воды реагентами с последующим выделением ионов металлов в виде нерастворимых комплексов и извлечение их из растворов в пену флотацией, отличающийся тем, что в качестве реагента используют β-N-оксиэтилгидразиды алифатических карбоновых кислот общей формулы (I), где R-радикал с прямой или разветвленной цепью, содержащий от 5 до 14 атомов углерода.
Предлагается способ, отличающийся тем, что в качестве реагента применяют β-N-оксиэтилгидразиды алифатических карбоновых кислот общей формулы (I), где радикал R содержит от 10 до 14 атомов углерода.
Предлагается способ, отличающийся тем, что β-N-оксиэтилгидразиды алифатических карбоновых кислот общей формулы (I) применяют в мольном соотношении [Сu2+]:[реагент]=1:(0,75-1).
При большем, чем 14 атомов углерода в радикале R, уменьшается растворимость реагентов в этаноле. Получение и применение реагентов с количеством атомов углерода в радикале R менее 5 нецелесообразно, так как из экспериментальных данных прослеживается тенденция к уменьшению извлечения меди с уменьшением количества атомов углерода в радикале R. Степени извлечения меди(II) с применением реагента с неразветвленным (2) и разветвленным (3) радикалами при общем одинаковом числе атомов углерода в радикале одинаковы (таблица 3).
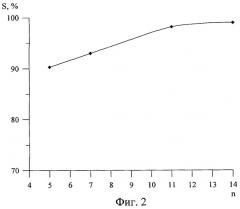
Наиболее высокая степень извлечения и, соответственно, наименьшее остаточное содержание меди(II) наблюдается при использовании реагента с количеством атомов углерода 10 и более (фиг.2).
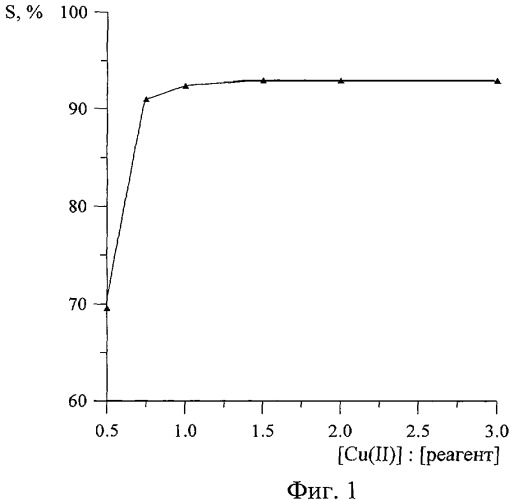
При использовании реагента в соотношении [Сu2+]:[реагент]=1:(менее 0,75) степень извлечения резко снижается, при соотношении [Cu2+]:[реагент]=1:(более 1) степень извлечения остается на одном уровне (фиг.1) и использование большего количества реагента нецелесообразно.
Сущность способа извлечения меди (II) иллюстрируется фиг.1, 2.
На фиг.1 представлена зависимость степени извлечения (S, %) меди(II) в пену от количества реагента (2).
На фиг. 2 представлена зависимость степени извлечения (S, %) меди(II) в пену от длины радикала R β-N-оксиэтилгидразида.
Методика извлечения Сu(II) из аммиачных растворов
В аммиачные растворы меди(II) добавляют растворы в этаноле гидроксиэтилгидразидов с длиной радикалов С5Н11-С14Н29 и перемешивают в течение 1-2 минут. Оптимальный диапазон рН флотационного извлечения Сu(II) равен 7-9. После кондиционирования раствор направляют во флотационную колонну. Взаимодействие ионов Сu(II) с реагентом в аммиачных средах сопровождается образованием флотоактивных осадков, которые переходят в пену и отделяются от водной фазы.
Результаты экспериментов по использованию соединений общей формулы (I) для извлечения меди(II) из аммиачных растворов приведены в примерах (1-11) и таблицах (2-3).
Пример 1. Влияние количества реагента на флотационное извлечение меди (II)
В колбу на 250 мл вносили 25 мл 10-3 моль/л раствора Сu2+ (начальная концентрация C°Cu(II)=6,44 мг/л), 2 мл 0,1 моль/л раствора аммиака (рНравн~9), 1,3 мл 10-2 моль/л раствора реагента (2) в этаноле и доводили до метки дистиллированной водой. Соотношение [Сu2+]:[реагент]=1:0,5. После 2 минут перемешивания смесь поступала на флотацию. Скорость подачи воздуха во флотационную колонну составляла 190 см3/мин, время флотации - 10 минут. Пенный продукт удаляли с поверхности воды с помощью вакуум-насоса.
Эксперименты в примерах 2-6 проводили аналогично примеру 1 с различными соотношениями [Сu2+]:[реагент].
Остаточное содержание меди (II) определяли атомно-абсорбционным методом. По полученным данным рассчитывали степень извлечения меди(II) в зависимости от количества реагента. Результаты приведены в таблице 2 и на фиг.1, из которых видно, что максимальная степень извлечения достигается уже при соотношении [Сu2+]:[реагент]=1:(0,75-1).
Пример 7. Влияние длины радикала R реагента на флотационное извлечение меди (II)
В колбу на 250 мл вносили 25 мл 10-3 моль/л раствора Cu2+(C°cu(II)=7,132 мг/л), 2 мл 0,1 моль/л раствора аммиака (рНравн~9), 2,5 мл раствора реагента (1) (10-2 моль/л) в этаноле и доводили до метки дистиллированной водой. После 2 минут перемешивания смесь поступала на флотацию. Скорость подачи воздуха во флотационную колонну составляла 190 см3 /мин, время флотации - 10 минут. Пенный продукт удаляли с поверхности воды с помощью вакуум-насоса.
Эксперименты в примерах 8-11 проводили аналогично примеру 7 с различными соединениями общей формулы (I).
Остаточное содержание меди(II) определяли атомно-абсорбционным методом. По полученным данным рассчитали степень извлечения меди(II) в зависимости от длины радикала R. Результаты приведены в таблице 3 и на фиг.2, из которых видно, что все предлагаемые соединения обеспечивают высокую степень извлечения меди(II) из аммиачных растворов. Наиболее высокая степень извлечения и, соответственно, наименьшее остаточное содержание меди(II) наблюдается при использовании в качестве реагента соединений с количеством атомов углерода 10 и более (фиг.2).
Таким образом, можно сделать вывод, что предлагаемые соединения проявляют сильные комплексообразующие и флотационные свойства и обеспечивают более высокую степень извлечения ионов меди(II) из аммиачных растворов по сравнению с прототипом при меньшем расходе реагента.
| Таблица 1 | |||||
| Спектральные характеристики соединений RCONHN (C2H5OH)2 | |||||
| №п/ п | ИК-спектры, ν/см-1 | ЯМР 1H, (м.д., J/Гц) | |||
| N-H | Амид I | Амид II | ОН | ||
| 1 | 3250 | 1660 | 1556 | 3440 | 0,88 (т.3Н, СН3, J=6,7), 1,31 (т. 6Н, 3СН2, J=3,4), 1,83 (м. 2Н, СН2СО), 2,17 (п.4Н, N(CH2)2, J=3,7), 2,93 (т.4Н, 2СН2), 3,65 (с.2Н, 2OН), 7,13 и 7,28 (оба c.1H, NH, Z и Е соотв.) |
| 2 | 3260 | 1660 | 1550 | 3420 | 0,82 (т.3Н, СН3, J=6,45), 1,22 (м. 8Н, 4СН2), 1,57 (м. 2Н, СН2), 2,1 (т.2Н, СОСН2, J=7,65), 2,87 (т.4Н, N(CH2)2, J=4,8), 3,55 (т.4Н, 2СН2, J=5), 4,02 (с.2Н, 2OН) 7,23 и 7,35 (оба с, 1Н, NH, Z и Е соотв.) |
| 3 | 3250 | 1650 | 1540 | 3400 | 0,83 (к. 6Н, 2СН3, J=7,6), 1,22 (д, 2Н, СН2, J=2,l), 1,4 (п.2Н, СН2, J=6,7), 1,57 (п.2Н, СН2, J=7,05), 1,87 (с.2Н, CH2, J=4,2), 2,18 (м. 1Н, СН), 2,9 (т.4Н, 2CH2, J=4,2), 3,57 (т.4Н, 2CH2, J=4,8), 4,0 (с.2Н, ОН), 7,02 (c.1H, NH) |
| 4 | 3250 | 1652 | 1556 | 3360 | 0,86 (т.3Н, СН3, J-6,6), 1,25 (м. 14Н, 7СН2), 1,61 (с, 2Н, СН2), 2,15 (т.2Н, СН2СО, J=7,4), 2,93 (т.4Н, N(CH2)2, J=4,5), 3,59 (т.4Н, 2СН2, J=4,6), 4,0 (с, 2Н, 20Н), 7,28 и 7,4 (оба с, 1Н, NH, Z и Е - изомеры) |
| 5 | 3250 | 1650 | 1556 | 3360 | 0,87 (т.3Н, СН3, J=6,6), 1,24 (с, 22Н, 11СН2), 1,62 (с, 2Н, СН2), 2,15 (т.2Н, СН2 СО, J=7,5), 2,91 (т.4Н, N(CH2)2, J=4,9), 3,6 (т.4Н, 2СН2, J=4,8), 4,0 (с, 2Н, 2OН), 7,25 (с, 1Н, NH) |
| Таблица 2 | |||
| Зависимость извлечения меди(II) из аммиачных растворов от количества реагента (соединение 2) | |||
| CCu(II)=6,44 мг/л; Среаг=10-4 моль/л | |||
| №примера | [Cu2+]:[реагент] | ССu(II)ост. | S, % |
| 1 | 1:0,5 | 1,957 | 69,60 |
| 2 | 1:0,75 | 0,560 | 91,10 |
| 3 | 1:1 | 0,502 | 92,20 |
| 4 | 1:1,5 | 0,464 | 92,80 |
| 5 | 1:2 | 0,461 | 92,84 |
| 6 | 1:3 | 0,462 | 92,82 |
| Прототип - | 1:1,5 | 0,655 | 87,8 |
| несимметричные | |||
| 1,2- | |||
| диацилгидразиныCСu(II)=5,37 мг/л Среаг=10-4 моль/л |
| Таблица 3 | ||||
| Зависимость извлечения меди(II) из аммиачных растворов от длины радикала R реагента | ||||
| CCu(II)=7,132 мг/л; Среаг=10-4 моль/л | ||||
| № примера | № соединения | R | CCu(II) ост. | S, % |
| 7 | 1 | C5H11 | 0,69 | 90,3 |
| 8 | 2 | C7H15 | 0,50 | 93,0 |
| 9 | 3 | С4Н9СН(С2Н5) | 0,49 | 93,1 |
| 10 | 4 | C10H21 | 0,13 | 98,2 |
| 11 | 5 | C14H29 | 0,07 | 99,0 |
| Прототип - | 0,655 | 87,8 | ||
| несимметричные | ||||
| 1,2- | ||||
| диацилгидразины | ||||
| С°Cu(II)=5,37 мг/л | ||||
| Среаг=10-4 моль/л |
1. Способ извлечения ионов меди (II) из аммиачных сред, включающий обработку среды реагентами с последующим выделением ионов металлов в виде нерастворимых комплексов и извлечение их из растворов в пену флотацией, отличающийся тем, что в качестве реагента используют β-N-оксиэтилгидразиды алифатических карбоновых кислот общей формулы где R - радикал с прямой цепью, содержащий от 7 до 14 атомов углерода.
2. Способ по п.1, отличающийся тем, что реагент общей формулы (I) применяют в мольном соотношении [Сu2+]:[реагент]=1:(0,75-1).