Лекарственное средство для лечения эндометриоза
Иллюстрации
Показать всеПредложено применение агониста дофамина (например, амантадина, бромокриптина, каберголина, хинаголида, лизурида, перголида, ропинирола и прамипексола) для изготовления лекарственного средства для лечения или предотвращения эндометриоза. Показано уменьшение числа активных эндометриоидных очагов, в пролеченных очагах наблюдали признаки атрофичной или дегенеративной ткани - т.е. снижение количества эндометриальных желез под действием каберголина. 13 з.п. ф-лы, 6 ил., 2 табл.
Реферат
Настоящее изобретение относится к лекарственным средствам для лечения эндометриоза.
Эндометриоз представляет собой доброкачественное хроническое гинекологическое заболевание. Его можно определить как присутствие эндометриальной ткани, содержащей как железистый эпителий, так и строму, вне полости матки. Он является доброкачественным гинекологическим расстройством, которое в субпопуляции пациентов женского пола может развиваться в агрессивное заболевание. Эндометриоз ассоциирован с различными болезненными симптомами, включая дисменорею, диспареунию, тазовую боль и сниженную фертильность.
Известно, что для развития эндометриоза может быть важен ангиогенез (процесс, посредством которого из ранее существовавших сосудов образуются новые кровеносные сосуды) и что в образовании сосудов играет роль фактор сосудистой проницаемости/фактор роста эндотелия сосудов (VP/VEGF), причем как в физиологическом, так и в патологическом ангиогенезе. Потенциальную эффективность антиангиогенной терапии для лечения эндометриоза оценивали с применением исследования с использованием человеческих эндометриальных тканей, трансплантированных бестимусным мышам с ослабленным иммунитетом. Четыре различных антиангиогенных ангента вводили через три недели после трансплантации эндометриальных эксплантатов (Nap et al, 2004). Все четыре ингибитора были способны уменьшать размер прижившихся эксплантатов, и образование новых кровеносных сосудов прекратилось. Тем не менее, известные антиангиогенные агенты высокотоксичны, и их довольно трудно внедрять в клиническую практику у человека.
Сейчас было неожиданно обнаружено, что композиции, содержащие агонист дофамина, могут быть использованы для лечения эндометриоза.
Таким образом, согласно настоящему изобретению предложено применение агониста дофамина в изготовлении лекарственного средства для лечения и/или предотвращения эндометриоза. Согласно настоящему изобретению также предложено применение агониста дофамина в лечении и/или предотвращении эндометриоза. Здесь термин «лечение эндометриоза» включает лечение для уменьшения количества (или удаления) эндометриальной ткани, присутствующей вне полости матки (например, уменьшение или удаление эндометриоидных очагов), и/или лечение для уменьшения и/или облегчения одного или более симптомов, ассоциированных с эндометриозом (например, лечение для облегчения и/или уменьшения симптомов дисменореи; лечение для облегчения и/или уменьшения симптомов диспареунии и/или лечение для облегчения и/или уменьшения тазовой боли). Термин «лечение эндометриоза» включает лечение для уменьшения числа элементов и/или уменьшение размеров элементов эндометриальной ткани, присутствующей вне полости матки (например, уменьшение числа и/или размера эндометриоидных очагов). Термин «лечение эндометриоза» включает лечение для уменьшения числа эндометриальных желез. Термин «лечение эндометриоза» включает лечение, приводящее к одному или более из: значительного уменьшения процента активных эндометриоидных очагов; значительной потери клеточности и организации в эндометриоидных очагах, что представляет собой характерные признаки атрофической или дегенеративной ткани; и значительного уменьшения числа новых кровеносных сосудов в эндометриоидных очагах. Термин «лечение эндометриоза» включает лечение для уменьшения числа и/или размеров эндометриоидных очагов в одном или более одном из яичника, маточно-прямокишечного углубления, крестцово-маточных связок, задних поверхностей матки, широкой связки, остальной тазовой брюшины, кишечника, мочевыводящих путей (включая, например, мочевой пузырь и/или мочеточники).
Термин эндометриоз включает, например, перитонеальный эндометриоз, эндометриоз яичников и глубокий эндометриоз.
Здесь термин агонист дофамина означает соединение, действующее подобно дофамину, например лекарственное средство, взаимодействующее с рецепторм дофамина (то есть специфично связывающее его) для имитации действия дофамина. Он не включает соединения, являющиеся исключительно «дофаминергическими веществами», то есть исключительно соединениями, которые, посредством различных механизмов действия, увеличивают уровни дофамина. Термин агонист дофамина не включает мостиковые инденопирролокарбазолы, раскрытые в US 6359130.
Ранее было обнаружено, что агонисты дофамина полезны в лечении или предотвращении синдрома гиперстимуляции яичников (OHSS) (WO 2006117608). Он представляет собой состояние, при котором значительно увеличивается сосудистая проницаемость капилляров. Было обнаружено, что агонисты дофамина способны реверсировать этот эффект. Тем не менее, состояние эндометриоза и потенциальная эффективность антиангиогенной терапии для лечения эндометриоза там не раскрыта.
В контексте данного изобретения агонисты дофамина включают, без ограничения, амантадин, бромокриптин, каберголин, хинаголид, лизурид, перголид, ропинирол и прамипексол. Предпочтительным агонистом дофамина для использования в настоящем изобретении является каберголин. Предпочтительным агонистом дофамина для использования в настоящем изобретении является хинаголид. Так называемые «частичные агонисты дофамина» (например, тергурид) также могут быть использованы в соответствии с изобретением. Тем не менее, предпочтительно применение агонистов дофамина.
Предпочтительно используют один агонист дофамина.
Агонист дофамина можно вводить в дозе (например, пероральной дозе пациенту-человеку) от 25 микрограмм в сутки до 80 мг/сутки, предпочтительно от 50 микрограмм в сутки до 5 мг/сутки, более предпочтительно от 300 микрограмм в сутки до 1 мг/сутки; подходящие дозы в пределах этого диапазона зависят от используемого агониста дофамина и очевидны для специалистов в данной области техники.
В предпочтительном воплощении агонист дофамина представляет собой каберголин. Предпочтительно каберголин вводят в дозе (например, пероральной дозе пациенту-человеку) 0,01-12,5 мг/неделя, предпочтительно 0,1-10 мг/неделя, более предпочтительно 0,5-5 мг/неделя, более предпочтительно в дозе 3,5 мг/неделя - 4 мг/неделя. Агонист дофамина может быть введен в виде, например, однократной суточной дозы (например, 0,1 мг/сутки - 5 мг/сутки, 0,2 мг/сутки - 1 мг/сутки, например 0,5 мг/сутки); или суточная доза может быть разделена на две или более субдозы для приема в разное время в течение 24-часового периода. Агонист дофамина (каберголин) может быть введен в виде суточной дозы в уровнях, указанных выше, или в виде эквивалентных доз, например, раз в неделю, два раза в неделю или каждые два дня. В одной схеме агонист дофамина (например, каберголин) вводят в суммарной дозе 3,5-12,5 мг в неделю (например, 4 мг в неделю, 7 мг в неделю, 10 мг/неделя).
В другом воплощении агонист дофамина представляет собой хинаголид. Предпочтительно хинаголид вводят в дозе (например, пероральной дозе пациенту-человеку) 25-1000 микрограмм/сутки, предпочтительно 25-500 микрограмм/сутки, более предпочтительно 25-300 микрограмм/сутки. Агонист дофамина может быть введен в виде, например, однократной суточной дозы; или суточная доза может быть разделена на две или более субдозы для приема в разное время в течение 24-часового периода. Агонист дофамина (хинаголид) может быть введен в виде суточной дозы в уровнях, указанных выше, или в виде эквивалентных доз, например, раз в неделю, два раза в неделю или каждые два дня.
В другом воплощении агонист дофамина представляет собой бромокриптин. Предпочтительно бромокриптин вводят в дозе (например, пероральной дозе пациенту-человеку) 10-80 микрограмм/сутки, предпочтительно 10-40 мг/сутки.
В одном воплощении агонист дофамина используют как единственное медикаментозное лечение эндометриоза. Иными словами, агонист дофамина может быть использован в отсутствие других медикаментозных или хирургических способов лечения (например, в отсутствие даназола).
В другом воплощении введение агониста дофамина может быть объединено с другими медикаментозными или хирургическими способами лечения эндометриоза (например, нестероидными противовоспалительными лекарственными средствами (НПВС) и/или гормональными лекарственными средствами (даназолом, пероральными контрацептивами (ОК), ацетатом медроксипрогестерона, другими прогестинами, агонистами и антагонистами гонадотропин-рилизинг-гормона (ГнРГ), ингибиторами ароматазы)). В другом воплощении хирургическое лечение или медикаментозное лечение могут быть использованы до, во время или после лечения агонистом дофамина. Эти воплощения обсуждены несколько более подробно в примерах ниже.
Также было обнаружено, что введение агониста дофамина пациенту, нуждающемуся в этом, может обеспечить существенные клинические преимущества, такие как, например, значительное уменьшение процента активных эндометриоидных очагов; значительная потеря клеточности и организации в эндометриоидных очагах, что представляет собой характерные признаки атрофической или дегенеративной ткани; и значительное уменьшение числа новых кровеносных сосудов в эндометриоидных очагах.
Лекарственные средства на основе агонистов дофамина также обладают преимуществом толерантности к высоким дозам, а также безопасности и хорошо документированных отчетов о клиническом применении.
Также было обнаружено, что агонист дофамина (например, каберголин) можно вводить в течение длительных периодов времени (например, 1-3 недель (например, 1-21 дня, например 1-14 дней), от 1 дня до 3 месяцев, от 1 дня до шести месяцев, от 1 дня до 12 месяцев, от 1 дня до 2 лет или дольше) с терапевтически полезным эффектом и низким риском побочных эффектов. Введение может быть непрерывным, например в виде суточной или недельной дозы, или может быть прервано одним или более перерывами продолжительностью, например, несколько (например 1-3) недель или несколько (например 1-3) месяцев. Агонист дофамина можно вводить пока сохраняется боль (или другой симптом).
Агонист дофамина (например, каберголин, хинаголид) можно вводить беременному субъекту.
Лечение или предотвращение эндометриоза может быть ассоциировано с уменьшением количества эндометриальных желез.
В примере изобретения на фактор роста эндотелия сосудов (VEGF) как на фактор развития эндометриоза может быть оказано направленное воздействие агонистом дофамина. По-видимому, в процесс ангиогенеза вовлечены главным образом изоформы VEGF121 и VEGF165 (Watkins, R.H., et al., Am. J. Physiol. 1999, vol. 276, pp.858-67). Были идентифицированы два специфичных мембранных эндотелиальных клеточных рецептора VEGF, рецептор VEGF 1 типа (VEGFR-1; Flt-1) и VEGFR-2 (Flk-1/KDR). По-видимому, в регуляцию ангиогенеза и образования и развития сосудов вовлечен главным образом VEGFR-2.
На VEGFR-2 (KDR) как на фактор развития эндометриоза может, таким образом, быть оказано направленное воздействие агонистом дофамина. На Notch-4 как на фактор развития эндометриоза может быть оказано направленное воздействие агонистом дофамина. На VEGF, VEGFR-2 и Notch-4 как на факторы развития эндометриоза может быть оказано направленное воздействие агонистом дофамина. Другие механизмы действия агониста дофамина входят в объем изобретения.
Агонист дофамина вводят в виде фармацевтически приемлемого препарата. Препараты могут быть введены в соответствии с изобретением в фармацевтически приемлемых композициях, которые могут, возможно, содержать фармацевтически приемлемые соли, буферные агенты, консерванты и эксципиенты. Фармацевтические препараты, содержащие агонист(ы) дофамина в качестве активных агентов, хорошо известны в данной области техники и имеются в продаже. Например, каберголин доступен под зарегистрированными товарными знаками Cabaser и Sogilen/Dostinex. Применение таких имеющихся в продаже препаратов агонистов дофамина в лечении эндометриоза входит в объем изобретения.
Выбор способа введения зависит от остроты и тяжести состояния, подлежащего лечению, и необходимой дозы. Любой способ введения, обеспечивающий желаемый терапевтический эффект без неприемлемых вредных эффектов, уместен при практическом осуществлении изобретения. Такие способы введения могут включать пероральный, ректальный, местный, трансдермальный, сублингвальный, внутримышечный, парентеральный, внутривенный, внутриполостной, вагинальный способ и введение с использованием адгезивной матрицы для применения во время хирургического вмешательства. Различные способы изготовления композиций для применения в соответствии с изобретением описаны в Handbook of Pharmaceutical Excipients, Third Edition, American Pharmaceutical Association, USA and Pharmaceutical Press UK (2000), и Pharmaceutics - The Science of Dosage Form Design, Churchill Livingston (1988).
В предпочтительном воплощении введение является пероральным. Композиции, подходящие для перорального введения включают капсулы, крахмальные облатки, таблетки, сиропы, эликсиры или лепешки.
Согласно настоящему изобретению, в другом аспекте, предложен способ лечения или предотвращения эндометриоза, включающий стадию введения пациенту, нуждающемуся в этом, агониста дофамина.
Предпочтительно агонист дофамина вводят в форме фармацевтического препарата, содержащего один или более чем один агонист дофамина в качестве активного ингредиента.
Агонист дофамина может быть введен в дозе (например, пероральной дозе пациенту-человеку) от 25 микрограмм в сутки до 80 мг/сутки, предпочтительно от 50 микрограмм в сутки до 5 мг/сутки, более предпочтительно от 300 микрограмм в сутки до 1 мг/сутки; подходящие дозы в пределах этого диапазона зависят от используемого агониста дофамина и очевидны для специалистов в данной области техники.
В предпочтительном воплощении агонист дофамина представляет собой каберголин. Предпочтительно каберголин вводят в дозе (например, пероральной дозе пациенту-человеку) 0,01-12,5 мг/неделя, предпочтительно 0,1-10 мг/неделя, более предпочтительно 0,5 мг - 5 мг/неделя, более предпочтительно в дозе 3,5 мг/неделя - 4 мг/неделя. Агонист дофамина может быть введен в виде, например, однократной суточной дозы (например, 0,1 мг/сутки - 5 мг/сутки, 0,2 мг/сутки - 1 мг/сутки, например, 0,5 мг/сутки); или суточная доза может быть разделена на две или более субдозы для приема в разное время в течение 24-часового периода. Агонист дофамина (каберголин) может быть введен в виде суточной дозы в уровнях, указанных выше, или в виде эквивалентных доз, например, раз в неделю, два раза в неделю или каждые два дня. В одной схеме агонист дофамина (например, каберголин) вводят в суммарной дозе 3,5-12,5 мг в неделю (например, 4 мг в неделю, 7 мг в неделю, 10 мг/неделя).
В другом воплощении агонист дофамина представляет собой хинаголид. Предпочтительно хинаголид вводят в дозе (например, пероральной дозе пациенту-человеку) 25-1000 микрограмм/сутки, предпочтительно 25-500 микрограмм/сутки, более предпочтительно 25-300 микрограмм/сутки. Агонист дофамина может быть введен в виде, например, однократной суточной дозы; или суточная доза может быть разделена на две или более субдозы для приема в разное время в течение 24-часового периода. Агонист дофамина (хинаголид) может быть введен в виде суточной дозы в уровнях, указанных выше, или в виде эквивалентных доз, например, раз в неделю, два раза в неделю или каждые два дня.
В другом воплощении агонист дофамина представляет собой бромокриптин. Предпочтительно бромокриптин вводят в дозе (например, пероральной дозе пациенту-человеку) 10-80 мг/сутки, предпочтительно 10-40 мг/сутки.
Введение агониста дофамина может быть объединено с другими медикаментозными или хирургическими способами лечения эндометриоза (например, нестероидными противовоспалительными лекарственными средствами (НПВС) и/или гормональными лекарственными средствами (даназолом, пероральными контрацептивами (ОК), ацетатом медроксипрогестерона, другими прогестинами, агонистами и антагонистами гонадотропин-рилизинг-гормона (ГнРГ), ингибиторами ароматазы)). В другом воплощении хирургическое лечение или медикаментозное лечение могут быть использованы до, во время или после лечения агонистом дофамина.
Авторы настоящей заявки обнаружили, что агонист дофамина (например, каберголин) можно вводить в течение длительных периодов времени (например, 1-3 недель (например, 1-21 дня, например 1-14 дней), от 1 дня до 3 месяцев, от 1 дня до шести месяцев, от 1 дня до 12 месяцев, от 1 дня до 2 лет или дольше) с терапевтически полезным эффектом и низким риском побочных эффектов. Введение может быть непрерывным, например, в виде суточной или недельной дозы, или может быть прервано одним или более перерывами продолжительностью, например, несколько (например, 1-3) недель или несколько (например, 1-3) месяцев. Агонист дофамина можно вводить пока сохраняется боль (или другой симптом).
Пациент может быть беременным.
Лечение или предотвращение эндометриоза может быть ассоциировано с уменьшением количества эндометриальных желез.
Настоящее изобретение теперь будет проиллюстрировано со ссылкой на примеры и прилагаемые графические материалы.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
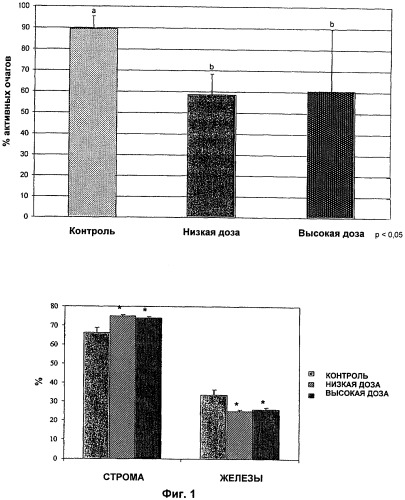
На Фиг.1 показан процент активных очагов согласно исследованию на животных, обсуждаемому ниже, для контрольной группы и групп, проходивших лечение низкой дозой (0,05 мг/кг/сутки) и высокой дозой (0,1 мг/кг/сутки) каберголина; на Фиг.1а показано соотношение железы/строма в трех установленных группах (как при низкой, так и при высокой дозе каберголина («Cb2») стромы было больше и желез было меньше, чем у контрольных животных (*р<0,05)).
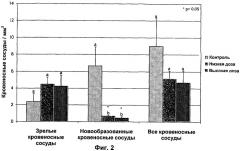
На Фиг.2 показаны кровеносные сосуды (мм3) для контрольной группы и групп низкой и высокой дозы.
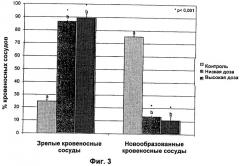
На Фиг.3 показан процент «зрелых» и «новообразованных» кровеносных сосудов у животных из контрольной группы и групп низкой и высокой дозы.
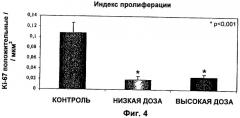
На Фиг.4 показан индекс пролиферации для контрольной группы и групп низкой и высокой дозы.
На Фиг.5 показана относительная экспрессия VEGF, VEGFR-2 (KDR), Notch-4, Ang 1 и Wnt-1 для контрольной группы и групп низкой и высокой дозы.
На Фиг.6а показано присутствие рецептора дофамина 2 типа (Dp-r2) и VEGF в эндометриальных имплантатах животных в трех установленных группах (контрольной группе и группах низкой и высокой дозы).
На Фиг.6б показана относительная экспрессия VEGF, VEGFR-2 (KDR) и D2R в эндометриоидных очагах (левая колонка) и в эндометрии (правая колонка).
Пример 1
Экспериментальная животная модель эндометриоза была разработана на бестимусных мышах посредством введения фрагментов человеческого эндометрия. Самок мышей (Hsd: Athimic Nude-nu, Harlan Iberica S.L, Barcelona, Spain) по отдельности содержали в автоклавируемых клетках на подстилке, в ламинарных боксах с фильтрами. В помещении для животных поддерживали температуру 26°С с циклом «12 часов света, 12 часов темноты» и мышей кормили ad libitum автоклавированным кормом для лабораторных грызунов и подкисленной водой. Все манипуляции проводили в ламинарных боксах с фильтрами. Смесь кетамина и медетомидина (75 мкг/г кетамина и 1 мкг/г медетомидина) (Ketolar®, Parke-Davis, Espana; Domtor®, Pfizer, Spain), вводимую внутрибрюшинно (i.p.), использовали для анестезирования мышей перед инвазивными процедурами и атипамезол (Antisedan®, SmithKline Beecham, Spain), вводимый i.p. в дозе 1 мкг/г для реверсирования эффектов анестезии, использовали после инвазивных процедур с использованием стерильного инструментария.
В возрасте 5 недель стерильные капсулы с высвобождением в течение 60 дней (60-d), содержащие 18 мг 17β-эстрадиола (Innovative Research of America, Sarasota, FL), помещали подкожно в шею каждого животного. В соответствии с информацией изготовителя капсулы обеспечивают длительное высвобождение гормона в сывороточных концентрациях 150-250 пмоль/л в диапазоне физиологических уровней у мышей в течение эстрального цикла. Этот стабильный физиологический уровень эстрогенов стимулирует рост трансплантированного человеческого эндометрия и нивелирует различия у разных мышей, обусловленные разными стадиями эстрального цикла.
Через четыре дня после введения эстрогеновой пилюли осуществляли доступ в брюшную полость по срединной линии внизу живота для введения свежего человеческого эндометрия от доноров после изъятия яйцеклетки. Эти фрагменты фиксировали клеем (Vetabond®, 3М Animal Care products, USA) к брюшине. Этот протокол позволяет имитировать патологическую ситуацию ретроградной менструации, происходящей у женщин с эндометриозом.
Через три недели после имплантации животных разделяли на три группы. Первая представляла собой контрольную группу; вторая представляла собой группу низкой дозы, проходившую лечение каберголином перорально в дозе 0,05 мг/кг/сутки; и группу высокой дозы, проходившую лечение каберголином перорально в дозе 0,1 мг/кг/сутки. Через две недели после лечения животных умерщвляли, брали образцы эндометриоидных очагов и анализировали их, как изложено ниже. Результаты показаны на Фиг.1, 1а и 2-6б.
Антиангиогенные эффекты агонистов дофамина оценивали посредством иммунофлуоресценции, при конфокальной микроскопии использовали антитела, выработанные против фактора фон Виллебранда (vWF моноклональный IgG1, DAKO Corp., Denmark), присутствующего в эндотелиальных клетках и гладкомышечных клетках сосудов (моноклональный IgG2 α-SMA-FITC конъюгированные, de Sigma, St Louis, USA). Кровеносные сосуды, не являющиеся новообразованными, окружены гладкомышечным слоем, придающим им зрелость. Идентификацию эндотелиальных клеток проводили с использованием vWF, в то время как зрелые сосуды идентифицировали положительным окрашиванием на α-SMA. Таким образом, vWF+/αSMA- кровеносные сосуды рассматривали как новые или незрелые, в то время как vWF+/αSMA+ сосуды классифицировали как старые или зрелые кровеносные сосуды.
Морфометрическое исследование проводили для измерения площади и клеточной плотности имплантатов. Иммуноцитохимию с использованием антитела Ki-67 (моноклональный IgG1 DAKO Corp., Denmark) проводили с целью оценки пролиферативной активности имплантатов. Гистопатологические и субклеточные ультраструктурные изменения выявляли с использованием оптического микроскопа (ОМ), трансмиссионного электронного микроскопа (ТЕМ) и гистохимического окрашивания. Оптическую микроскопию (ОМ), трансмиссионную электронную микроскопию (ТЕМ) и морфометрию проводили для обнаружения присутствия эндометриальных желез и стромы и исследования субклеточных ультраструктурных изменений, площади имплантатов и клеточной плотности.
TaqMan Real-time PCR (полимеразную цепную реакцию в реальном времени TaqMan) и способы 2-ΔΔCt применяли для анализа профилей экспрессии генов трех различных маркеров, стимулирующих ангиогенез (VEGF, VEGFR-2, Notch-4), ангиопоэтина-1 (Ang-1), маркера антиангиогенеза, стимулирующего увеличение существующих сосудов и сопротивление фильтрации, и Wnt-1. Присутствие экспрессии VEGF и рецептора дофамина 2 типа (Dp-r2) в экспериментальных имплантатах, человеческих перитонеальных эндометриоидных очагах и эндометрии демонстрировали с применением TaqMan Real-time PCR и способа 2-ΔΔCt (Фиг.6а, 6б). Сходным образом, этот способ применяли для демонстрации присутствия экспрессии VEGFR-2 в человеческих перитонеальных эндометриоидных очагах и эндометрии (Фиг.6б).
Статистический анализ проводили с использованием GraphPad Instat V3.0 (GraphPad Software, San Diego, CA, USA). Исследование было спланировано для выявления различий в различных анализируемых маркерах в группах лечения и контрольной группе. Категорийные данные выражали как число и процент и числовые данные выражали как среднее ± стандартная ошибка среднего (SEM), если не указано иное. Значимость определяли как р<0,05. Для статистического анализа использовали однофакторный дисперсионный анализ.
Токсичность
Ни одна из исследуемых мышей не умерла после введения каберголина. По-видимому, каберголин не влиял на общее состояние здоровья мышей, поскольку значимых различий массы тела мышей в различных группах лечения не было (результаты не показаны).
Результаты
На Фиг.1 показан процент активных очагов согласно исследованию на животных, обсужденному выше, для контрольной группы и групп, проходивших лечение низкой дозой (0,05 мг/кг/сутки) и высокой дозой (0,1 мг/кг/сутки) каберголина. У животных, проходивших лечение низкой (58,6±9,7%) и высокой (60,4±8,4%) дозами, было значительное уменьшение (р=0,0169) активных очагов по сравнению с контролями (89,6±5,7%). У животных, проходивших лечение каберголином (как в группе с низкой дозой, так и в группе с высокой дозой), было значительно меньше активных очагов по сравнению с контрольной группой. Иными словами, лечение каберголином, по-видимому, уменьшало число активных эндометриоидных очагов в этой модели. ОМ- и ТЕМ-исследования показали, что в контрольной группе эндометриоидные очаги имели высококлеточную строму и гистологический аспект полной реорганизации, и структуру, которую можно наблюдать в типичном человеческом эндометриоидном очаге. Тем не менее, в пролеченных очагах (высокой и низкой дозой каберголина) наблюдают рыхлую строму с потерей клеточности и организации; это является характерным признаком атрофичной или дегенеративной ткани. Человеческая эндометриальная строма, окружающая железистые области, была легко отличима от мышечно-соединительной мышиной ткани.
Эти гистологические результаты подтверждали морфометрическим анализом (Фиг.1а). Хотя по клеточной плотности статистического различия между группами не было, между группами было значительное (р=0,0093) различие по отношению железы/строма, как можно видеть на Фиг.1а; как низкая, так и высокая дозы каберголина имели больше стромы и меньше желез, чем контроли (*р<0,05). Это указывает на то, что лечение каберголином может быть ассоциировано с уменьшением или снижением количества эндометриальных желез.
На Фиг.2 показаны кровеносные сосуды (мм3) для контрольной группы и групп низкой и высокой дозы, с разделением между «зрелыми» кровеносными сосудами и «новообразованными» кровеносными сосудами. В контрольной группе больше была доля новообразованных кровеносных сосудов (что указывает на значительный ангиогенез), в то время как в группах низкой и высокой дозы значительно больше была доля зрелых кровеносных сосудов, что указывает на значительно сниженный ангиогенез. Это также было продемонстрировано гистологически (результаты не показаны). Эти результаты указывают на то, что каберголин значительно снижал образование новых кровеносных сосудов (ангиогенез) в этой модели.
На Фиг.3 показан процент кровеносных сосудов в контрольной группе и группах низкой и высокой дозы. В контрольной группе приблизительно 74% всех кровеносных сосудов являются новообразованными кровеносными сосудами, указывая на значительный ангиогенез. С другой стороны, в группах низкой и высокой дозы приблизительно 85-89% всех кровеносных сосудов являются зрелыми, указывая на то, что ангиогенез незначителен. Эти результаты указывают на то, что каберголин значительно снижал образование новых кровеносных сосудов (ангиогенез) в этой модели.
На Фиг.4 показаны результаты исследования пролиферации. Иммуноцитохимическое исследование с использованием антитела Ki-67 (то есть с анализом степени клеточной пролиферации с использованием антител против Ki-67) использовали для оценки пролиферативной активности имплантатов с применением способов, известных в данной области техники. Программное обеспечение для вычислений с изображения использовали для подсчета Ki-67-положительных клеток и таким образом вычисляли индекс пролиферации в каждой группе. В очагах у животных, прошедших лечение каберголином (как в группе низкой дозы, так и в группе высокой дозы), наблюдали значительное (р<0,001) уменьшение пролиферации по сравнению с контрольной группой.
Ангиогенный статус очагов сначала анализировали с применением иммунофлуоресценции с использованием антител для идентификации новых (vWF+/αSMA-) и старых сосудов (vWF+/αSMA+) и конфокальной микроскопии (Leica Confocal Software). Иммунофлуоресценцию с использованием антител, выработанных против фактора фон Виллебранда (vWF), присутствующего в эндотелиальных клетках и гладкомышечных клетках сосудов (α-SMA), можно использовать для исследования антиангиогенного действия Cb2. Кровеносные сосуды, не являющиеся новообразованными, окружены гладкомышечным слоем, придающим им зрелость. Идентификацию эндотелиальных клеток проводили с использованием vWF, в то время как зрелые сосуды идентифицировали положительным окрашиванием на α-SMA. Таким образом, vWF+/αSMA- кровеносные сосуды рассматривали как новые или незрелые, в то время как vWF+/αSMA+ сосуды классифицировали как старые или зрелые кровеносные сосуды.
В контрольной группе имплантаты имели высококлеточную строму и гистологический аспект полной реорганизации и структуру, обычно наблюдаемую в очаге эндометриоза, в то время как имплантаты у мышей, включенных в группы низкой и высокой дозы, демонстрировали рыхлую строму с потерей клеточности и организации, что является характерным признаком атрофичной/дегенеративной ткани. Морфометрия показала отсутствие различий среди групп в клеточной плотности, соотношении строма/железы и площади желез.
TaqMan Real-time PCR и способы 2-ΔΔCt использовали для анализа профилей экспрессии генов трех различных маркеров, стимулирующих ангиогенез (VEGF, VEGFR-2, Notch-4), ангиопоэтина-1 (Ang-1), маркера антиангиогенеза, стимулирующего увеличение существующих сосудов и сопротивление фильтрации, и Wnt-1. Конститутивная 18S рибосомальная РНК (рРНК) была использована для нормализации значений Ct целевого гена. Значение Ct в каждой группе выражали по отношению к значениям Ct в контрольной группе (калибратор) для вычисления относительной экспрессии способом 2-ΔΔCt. Комплементарную ДНК (кДНК), полученную из опухолевых клеток саркомы 180 (S-180), и эндотелиальные клетки пупочной вены человека (HUVEC) использовали в качестве отрицательного и положительного контроля соответственно, для экспрессии генов VEGF и VEGFR-2. Селезенку использовали как положительный контроль для Ang-1 и Wnt-1 и легкое использовали как положительный контроль для Notch-4.
В Таблице 1 показано, что профили экспрессии генов проангиогенных маркеров (VEGF, VEGFR-2 и Notch-4) в имплантатах, обработанных низкой и высокой дозами каберголина («Cb2»), были снижены по сравнению с контролями. Ang-1 и Wnt-1 рассматривают как антиангиогенные маркеры; профили их экспрессии в имплантатах мышей, пролеченных низкой и высокой дозами Cb2, были повышены по сравнению с контролями, показывая, что лечение каберголином ассоциировано с ингибированием ангиогенеза. Данные по относительной экспрессии из таблицы показаны графически на Фиг.5.
| Таблица 1 | |||||||
| Профили экспрессии ангиогенных генов | |||||||
| Маркер ангиогенеза | Ген | Контроль ± | Наполнитель | НИЗКАЯ ДОЗА (0,05 мг/кг/сутки) | ВЫСОКАЯ ДОЗА (0,1 мг/кг/сутки) | Значение р | Экспрессия |
| + | VEGF | HUVEC | 1,2±0,3 | 0,5±0,2 | 0,4±0,1 | <0,05 | Снижена в группах, пролеченных Cb2 |
| + | VEGFR-2 (KDR) | HUVEC | 1,0±0,1 | 0,4±0,1 | 0,3±0,1 | <0,05 | Снижена в группах, пролеченных Cb2 |
| + | Notch-4 | Легкое | 1,0±0,1 | 0,5±0,1 | 0,4±0,1 | <0,05 | Снижена в группах, пролеченных Cb2 |
| - | Ang-1 | Селезенка | 1,1±0,2 | 3,2±0,6 | 3,7±0,6 | <0,05 | Повышена в группах, пролеченных Cb2 |
| - | Wnt-1 | Селезенка | 1,0±0,1 | 3,4±0,2 | 3,3±0,6 | =0,07 | Повышена в группах, пролеченных Cb2 |
Данные выражены как среднее ± среднеквадратическое отклонение (SD)
Было исследовано присутствие рецепторов дофамина 2 типа в человеческой эндометриальной ткани и эндометриоидных имплантатах у женщин, подвергнутых хирургическому вмешательству (лапароскопии). TaqMan Real-time PCR и способы 2-ΔΔCt использовали для подтверждения присутствия рецептора дофамина 2 типа («Dp-r2», «D2R») и VEGF в человеческой эндометриальной ткани не только в имплантатах (Фиг.6а), но также в перитонеальных эндометриоидных очагах, полученных от 10 женщин при лапароскопии (Фиг.6б, также включающая данные no VEGF-R2). Положительными и отрицательными контролями для Dp-r2 была кДНК клеток HUVEC и S-180, соответственно. Для мышей контрольные значения Ct использовали в качестве калибратора, и для человеческих перитонеальных очагов значения Ct HUVEC использовали в качестве калибратора для вычисления относительной экспрессии способом 2-ΔΔCt.
На Фиг.6а показано присутствие VEGF и Dp-r2 в эндометриальных имплантатах животных в трех установленных группах. Была тенденция к увеличению экспрессии Dp-r2, по мере того как животных лечили увеличивающимися дозами каберголина. Имеется тенденция к уменьшению экспрессии VEGF, по мере того как животных лечили увеличивающимися дозами каберголина.
На Фиг.6б показана (левая колонка) относительная экспрессия VEGF, VEGFR-2 (KDR) и D2R («Dp-r2») в различных типах эндометриоидных очагов; красным, белым и черным. Имеется четкое различие в экспрессии VEGF, VEGFR-2 и Dp-r2 согласно типу очага.
На Фиг.6б также показана (правая колонка) относительная экспрессия VEGF, VEGFR-2 (KDR) и D2R («Dp-r2») в эндометрии. Относительная экспрессия VEGF и VEGFR-2 в эндометрии субъектов с эндометриозом выше, чем у субъектов без эндометриоза; относительная экспрессия Dp-r2 в эндометрии субъектов с эндометриозом ниже, чем у субъектов без эндометриоза.
Эти результаты показаны в Таблице 2 ниже.
| Таблица 2 | ||||||||
| Ген | Эндометрий | Эндометриоидные очаги | ||||||
| Без эндометриоза | Умеренный | Тяжелый | Значение р | Красный | Белый | Черный | Значение р | |
| VEGF | 1,0±0,1 | 2,2±0,7 | 2,1±0,4 | NS | 17,8±5,8 | 10,1±4,8 | 11,1±3,9 | NS |
| KDR | 1,0±0,1 | 2,1±0,6 | 1,9±0,3 | NS | 47,4±15,0 | 26,9±12,2 | 23,6±7,2 | NS |
| D2R | 1,0±0,1 | 0,3±0,1 | 0,2±0,1 | =0,07 | 0,2±0,1 | 0,3±0,2 | 0,6±0,3 | NS |
Результаты показывают, что агонист дофамина каберголин, вводимый в дозе 0,05 и 0,1 мг/кг/сутки, был способен:
(а) значительно уменьшать число активных эндометриоидных очагов;
(б) вызывать потерю клеточности и организации в эндометриоидных имплантатах, что представляет собой характерные признаки атрофичной или дегенеративной ткани;
(в) значительно снижать число новых кровеносных сосудов в эндометриоидных имплантатах;
(г) значительно уменьшать экспрессию маркеров ангиогенеза и клеточную пролиферацию и
(д) усиливать дегенерацию тканей и уменьшать эндометриоидные имплантаты.
Существует высокая степень гомологии между системами VEGF человека и грызунов, что указывает на то, что активность, показанная в описанной выше модели на грызунах, применима к человеческим моделям. Результаты показывают, что введение агонистов дофамина оказывает значительный эффект на эндометриоз, возможно связанный с действием на ангиогенез. Эти результаты могут быть связаны с присутствием рецепторов дофамина в эутопической и эктопической эндометриальной ткани.
Пример 2
Композиция в форме таблетки для перорального применения представляет собой 0,5 мг каберголина (имеется в продаже под названием Dostinex®, Pfizer, Spain).
Другие примеры
Пример А. Пациент с хронической тазовой болью проходит диагностическую лапароскопию, и у него диагностируют эндометриоз III типа. Во время этой же лапароскопии пациенту выполняют хирургическое вмешательство, такое как резекция доступных очагов, и начинают введение каберголина.
Пример Б. Ранее у пациента был диагностирован эндометриоз, проявлявшийся симптомами тазовой боли и дисменореи. Введение каберголина начинают без хирургического вмешательства.
Пример В. Пациенту, у которого диагностирован эндометриоз, проводят лечение агонистами ГнРГ (или даназолом, или ингибиторами ароматазы) и начинают введение каберголина (продолжая использовать агонист ГнРГ) в течение определенного периода. После следующих 3 или 6 месяцев отсутствия терапии пациенту вновь проводят лечение каберголином в течение дополнительного периода.
1. Применение агониста дофамина в изготовлении лекарственного средства для лечения или предотвращения эндометриоза.
2. Применение по п.1, где указанный агонист дофамина представляет собой одно из амантадина, бромокриптина, каберголина, хинаголида, лизурида, перголида, ропинирола и прамипексола.
3. Применение по п.1, где агонист дофамина представляет собой каберголин, вводимый в дозе 0,01-12,5 мг/нед.
4. Применение по п.1, где агонист дофамина представляет собой хинаголид, вводимый в дозе 25-1000 мг/сут.
5. Применение по п.1, где агонист дофамина представляет собой бромокриптин, вводимый в дозе 10-80 мг/сут.