Имплантируемое устройство и способ доставки текучего лекарственного препарата в ткань
Иллюстрации
Показать всеИзобретение относится к устройствам и способам для электростимулирования внутреннего уха. Устройство включает имплантируемый носитель электрода, имеющий внешнюю сторону, на которой расположена группа контактов для электростимуляции окружающей нервной ткани, расширяющийся резервуар текучей среды с диаметром, составляющим по меньшей мере одну третью часть от диаметра носителя электрода, расположенный внутри носителя электрода для текучего лекарственного препарата для продолжительного лечебного периода, и по меньшей мере один порт доставки текучей среды, связывающий указанный резервуар с внешней стороной носителя электрода для доставки текучего лекарственного препарата от указанного резервуара к указанной внешней стороне. Способ доставки текучего лекарственного препарата в ткань, окружающую имплантируемое устройство, заключается в использовании имплантируемого устройства. Использование изобретения позволяет минимизировать разрушение структур внутреннего уха и повысить качество стимуляции и эффективности доставки лекарственного средства. 2 н. и 16 з.п. ф-лы, 56 ил.
Реферат
Область, к которой относится изобретение
Изобретение относится к медицинской технике, а именно к имплантируемым устройствам для внутреннего уха, содержащим электроды кохлеарного имплантата, высвобождающим (элюирующим) в течение некоторого времени лекарственный препарат во внутреннее ухо.
Уровень техники
Электростимулирование внутреннего уха весьма успешно применяется при восстановлении слуха у пациентов, страдающих глухотой. Интракохлеарные электроды предназначены для восстановления некоторых слуховых ощущений путем непосредственного электростимулирования нервной ткани, находящейся вблизи контакта электрода. Электростимулирование осуществляется с помощью имплантируемого кохлеарного стимулятора, соединенного с электродом, введенным глубоко в полость барабанной лестницы (scala tympani) улитки. Но введение электрода в той или иной мере вызывает разрастание соединительной ткани и причиняет травмы. Степень травмирования очень трудно предсказуема и зависит от анатомии улитки, конструкции электрода и способа введения. Повреждения, причиняемые тканям, могут впоследствии вызывать утрату клеток (апоптоз) и/или некроз нервной ткани (то есть волосковых клеток и клеток спирального ганглия). Качество функционирования имплантата могут ограничивать такие факторы, как разрастание тканей и травмы. Кроме того, повреждения клеток спирального ганглия являются накапливающимися, и поврежденные ткани не могут быть восстановлены при данном уровне техники. Так как кохлеарные имплантаты получают все большее распространение среди пациентов, у которых в значительной мере сохранился остаточный слух, становится более актуальным, чем когда-либо ранее, применять минимально травмирующие электроды. Кроме того, поскольку все большему числу пациентов имплантат устанавливается в раннем возрасте и на протяжении жизни пациента будет неоднократно реимплантироваться, каждое новое введение электрода должно в минимальной степени травмировать клетки спирального ганглия.
Травмы обычно вызываются введением электрода в хрупкие и требующие осторожного обращения ткани внутреннего уха. При введении необходимо прилагать к электроду механические усилия, чтобы преодолеть трение между электродом и тканями улитки, что осложняется спиральной формой улитки. Чтобы снизить повреждения органа или тканей, электроды и катетеры должны быть мягкими и гибкими, а усилия при их введении минимальными. К сожалению, в настоящее время большинство электродов кохлеарных имплантатов, предлагаемых на рынке, при их введении требуют значительных усилий, даже для расстояний, намного меньших полной длины барабанной лестницы улитки.
Сила, необходимая для введения электродов или катетеров, связана с размерами, геометрией и материалами, из которых они изготовлены. Материалы, применяемые в таких устройствах, включают материалы проводов, контактов, функциональных сегментов, выполненных из металлов или полимеров, и материалы основы. Размер устройства, жесткость используемого материала, гидрофобность внешней оболочки матрицы электродов, энергия, тем или иным способом запасенная в электроде, и процесс введения устройства - все это влияет на локализацию и степень повреждения тканей, причиняемого введением электродов.
Повреждения и травмы вызывают кровотечение, воспалительные процессы, перфорацию мягких тканей, разрывы и перфорацию мембран и трещины в тонких костных структурах. Результирующие повреждения могут вызвать гибель сохранившихся волосковых клеток, ретроградную дегенерацию дендритов, иннервирующих кортиев орган, а в самых неблагоприятных случаях - гибель клеток спирального ганглия в спиральном канале улитки. Гибель клеток в количественном отношении означает, что меньше невральной ткани будет доступно для стимулирования, а в качественном отношении означает, что уменьшится число волокон, настроенных на определенные частоты, и, следовательно, способность воспринимать частотную информацию. Дальнейшая потеря волосковых клеток и дендритов, даже не сопровождающаяся потерей клеток спирального ганглия, означает, что акустическое стимулирование более невозможно и что не могут быть использованы никакие синергетические эффекты, обусловленные взаимодействием между акустической и электрической стимуляцией. Синергизм электрических и акустических воздействий может играть большую роль в надежном выделении полезного звукового сигнала в зашумленной акустической среде.
Другим неудобством, связанным с кохлеарными имплантатами, является увеличение наблюдаемого сопротивления электродов в послеоперационной период. Это увеличение, как считают, вызывается инкапсуляцией электрода плотной мембраной, которая снижает эффективность электрической стимуляции, создавая обедненную ионами область вокруг контактов. Имеет смысл в послеоперационный период вводить в улитку некоторые лекарственные препараты, способствующие сохранению величины сопротивления электрода на низком уровне. Было продемонстрировано, например, что введение кортикостероидов может замедлить увеличение сопротивления после операции. Это выполнялось способом осаждения препарата на электроде или натиранием электрода препаратом. Но когда электрод введен в жидкость барабанной лестницы улитки, жидкий препарат быстро растворяется и не может достичь той области, где он мог бы принести наибольшую пользу.
При лечении болезни Меньера, или вертиго, предпринимались попытки доставлять медицинский препарат во внутреннее ухо пациентам, которым имплантант не вводится внутрь улитки. Доставка препарата производится через проницаемую в некоторой степени мембрану круглого окна после инъекции болюса в среднее ухо. Одна из проблем, возникающих при доставке препарата через круглое окно, состоит в том, что проницаемость мембраны для молекул веществ изменяется на протяжении суток, а большие молекулы не могут проникнуть через плотную мембрану. Считается, что лишь очень небольшое количество фармакологически активного вещества достигает области улитки, расположенной далее нескольких первых миллиметров длины улитки.
Не существует никакого простого способа доставлять лекарственный (фармацевтический) препарат во внутреннее ухо после кохлеарной имплантации. Уже доступ к среднему уху не является легким, а внутреннее ухо представляет собой изолированную систему, что делает невозможным прямое депонирование или инъекцию препаратов, иначе как в ходе операции кохлеарной имплантации. После операции пространство улитки частично занято электродом, который не должен сдвигаться или удаляться.
Элюирующие кортикостероиды выводы электродов успешно применялись в прошлом с электродами кардиостимулятора с целью уменьшения сопротивления контакта. Кроме того, в нескольких областях, таких как предупреждение беременности, лечение сосудистых повреждений и применение стентов в качестве элюирующих структур, применялся силиконовый эластомер, содержащий фармакологический препарат. Электроды, элюирующие лекарственные препараты, совместно с кохлеарными имплантатами не применялись.
Цель изобретения - разработка имплантируемого устройства с матрицей кохлеарных электродов, обладающего высокой надежностью, минимизирующего разрушение структур внутреннего уха при вводе в него матрицы электродов, повышение качества стимуляции внутреннего уха, повышение эффективности доставки лекарственного препарата непосредственно во внутреннее ухо.
Раскрытие изобретения
Для достижения указанного технического результата разработано имплантируемое устройство, включающее матрицу кохлеарных электродов для электростимулирования тканей улитки, содержащую лекарственную элюирующую часть, состоящую из полимерного материала и связанного с ним фармацевтического препарата, при этом указанная часть выполнена с возможностью высвобождения фармацевтического препарата в течение заданного периода времени во внутреннее ухо в терапевтически эффективном количестве. Матрица электродов может быть снабжена участком, содержащим полимерный материал. Указанный участок может иметь заданные геометрические характеристики для обеспечения заданной скорости высвобождения фармацевтического препарата. Фармацевтический препарат может представлять собой гель или порошок, включенный в полимерный материал, а полимерный материал может являеться эластомером на основе силикона. Лекарственная элюирующая часть может представлять собой полимерный слой, размещенный между двумя слоями безлекарственного элюирующего материала. Масса лекарственной элюирующей части может составлять от 1% до 2% массы матрицы электродов. Лекарственная элюирующая часть размещена внутри безлекарственного элюирующего материала. Безлекарственный элюирующий материал может имеет заданную толщину для обеспечения заданной скорости высвобождения лекарственного препарата. Лекарственная элюирующая часть может начинаться по меньшей мере в 3 миллиметрах от места входа матрицы электродов во внутреннее ухо. Лекарственная элюирующая часть может иметь заданную концентрацию поперечных связей полимерного материала для обеспечения заданной скорости высвобождения лекарственного препарата. Лекарственная элюирующая часть может иметь заданную площадь поверхности контакта с жидкостью внутреннего уха для обеспечения заданной скорости высвобождения фармацевтического препарата. Лекарственная элюирующая часть может иметь заданный объем для обеспечения заданной скорости высвобождения фармацевтического препарата. Лекарственная элюирующая часть может включать первый и второй лекартвенные элюирующие участки, при этом фармацевтические препараты в каждом участке являются разными. Матрица электродов может снабжаться рядом электрических контактов для электростимулирования тканей улики, при этом по меньшей мере один из контактов покрыт лекарственным препаратом. Фармацевтический препарат может выполняться в виде твердых частиц с размером меньше 200 микрометров, включенных в соответствующий материал лекарственной элюирующей части. Фармацевтический препарат может выполняться в виде частиц с заданным распределением по размерам для обеспечения заданной скорости высвобождения лекарственного препарата. Фармацевтический препарат может содержать по меньшей мере 90% частиц размером меньше чем 200 микрометров. Фармацевтический препарат может содержать по меньшей мере 50% частиц с размером меньше чем 50 микрометров. Фармацевтический препарат может являеться кортикостероидом. Кортикостероид может выбираеться из группы, включающей бетаметазон, клобетазол, дифлоразон, флюоцинонид, триамцинолон, их соли и их смеси. Кортикостероидом может являеться дексаметазон. Матрица электродов может выполняться с возможностью высвобождения от 5 до 600 миллиграмм дексаметазона в течение первых 24 часов применения. Фармацевтический препарат может являеться противовоспалительным препаратом. В устройстве может содержаться физиологический раствор, который включает указанный противовоспалительный препарат с концентрацией в точке насыщения не менее 26,4 миллиграмм на миллилитр при 37°С. Матрица электродов может быть выполнена с возможностью высвобождения от 5 до 250 миллиграмм противовоспалительного препарата в течение первой недели после имплантации. Фармацевтический препарат может быть бактерицидом.
Краткое описание чертежей
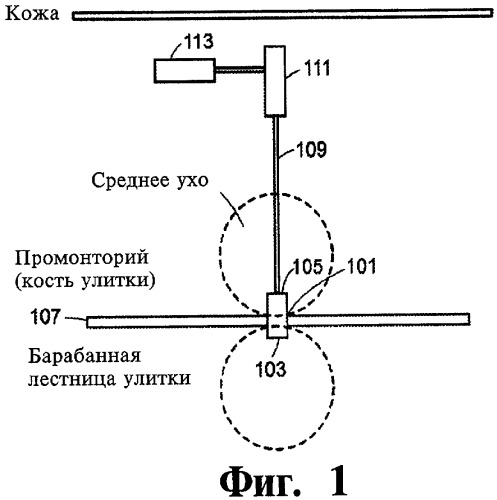
Фиг.1 графически представляет систему доставки жидкого препарата в соответствии с вариантом настоящего изобретения.
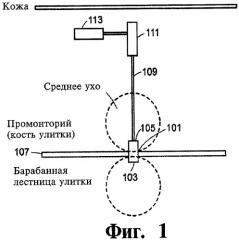
Фиг.2 - графическая иллюстрация системы доставки жидкого препарата, соединенной с кохлеарным имплантатом, в соответствии с другим вариантом изобретения.
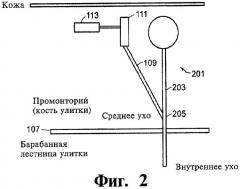
Фиг.3 графически представляет систему доставки жидкого препарата, имплантированную параллельно кохлеарному имплантату, в соответствии с вариантом изобретения.
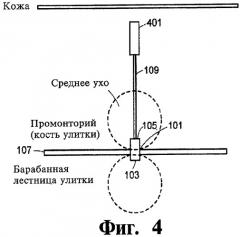
Фиг.4 графически представляет систему доставки жидкого препарата в соответствии с дополнительным вариантом изобретения.
Фиг.5 графически представляет систему доставки жидкого препарата в соответствии с другим вариантом изобретения.
Фиг.6 графически представляет систему доставки жидкого препарата, в которой имеется контейнер с жидким препаратом, в соответствии с вариантом изобретения.
Фиг.7 графически представляет переключатель, который может быть имплантирован под кожей, в соответствии с вариантами, показанными на фиг.1-5.
Фиг.8 графически представляет переключатель, который может быть имплантирован в среднее ухо пациента, в соответствии с вариантом, показанным на фиг.5.
Фиг.9 графически представляет пополняемый резервуар в соответствии с другим вариантом изобретения.
Фиг.10 графически представляет автоматически закрывающийся запорный клапан в соответствии с дополнительным вариантом изобретения.
Фиг.11 графически представляет систему доставки жидкого препарата, служащую для доставки жидкого препарата к внутреннему уху пациента, в соответствии с другим вариантом изобретения.
Фиг.12 графически представляет конфигурацию с имплантируемым микромембранным разъемом, применяемым совместно с насосом и доставляющим препарат катетером, в соответствии с другим вариантом настоящего изобретения.
Фиг.13 графически представляет конфигурацию с имплантируемым микромембранным разъемом, применяемым совместно с имплантируемым портом (порт - имплантируемый чрескожно или хирургически в резервуар, снабженный пунктируемой мембраной), имеющим резервуар и катетер доставки, в соответствии с дополнительным вариантом изобретения.
Фиг.14 графически представляет конфигурацию с имплантируемым микромембранным разъемом, применяемым совместно с электронным протезом, в соответствии с другим вариантом изобретения.
Фиг.15 графически представляет микромембранный разъем перед соединением имплантируемого разъема порта и имплантируемого пунктирующего разъема в соответствии с вариантами, показанными на фиг.12-14.
Фиг.16 графически представляет микромембранный разъем после соединения имплантируемого разъема порта и имплантируемого пунктирующего разъема в соответствии с вариантом, показанным на фиг.15.
Фиг.17 графически представляет устройство для доставки жидкого препарата к внутреннему уху пациента в соответствии с дополнительным вариантом изобретения.
Фиг.18 графически представляет катетер в соответствии с другим вариантом изобретения.
Фиг.19 - графически представляет катетер, показанный на фиг.18, имплантированный в ухо пациента.
Фиг.20 графически представляет имплантируемый электрод в соответствии с другим вариантом изобретения.
Фиг.21 графически представляет электрод, показанный на фиг.20, имплантированный во внутреннее ухо пациента.
Фиг.22 - графически представляет провода, соединенные с электродом, показанным на фиг.20 и 21.
Фиг.23 графически представляет имплантируемый электрод, используемый для доставки жидкого препарата в организм пациента, в соответствии с другим вариантом изобретения.
Фиг.24 графически представляет электрод, показанный на фиг.23, имплантированный во внутреннее ухо пациента, в соответствии с дополнительным вариантом изобретения.
Фиг.25 показывает поперечный разрез электрода, представленного на фиг.23.
Фиг.26 графически представляет электрод, используемый в соединении с имплантируемым корпусом, в соответствии с дополнительным вариантом изобретения.
Фиг.27 графически представляет имплантируемый электрод в соответствии с другим вариантом изобретения.
Фиг.28 показывает поперечный разрез электрода, представленного на фиг.27.
Фиг.29 графически представляет электрод, показанный на фиг.27, имплантированный во внутреннее ухо пациента.
Фиг.30 графически представляет электрод, показанный на фиг.27, с зажимом для соединения концов.
Фиг.31 графически представляет устройство для доставки жидкого препарата в организм пациента в соответствии с дополнительным вариантом изобретения.
Фиг.32 графически представляет иглу, которая имеется в варианте, показанном на фиг.31.
Фиг.33 графически представляет имплантируемый порт доступа в соответствии с другим вариантом изобретения.
Фиг.34 графически представляет устройство для доставки жидкого препарата в организм пациента в соответствии с фиг.31-33.
Фиг. с 35 по 41 показывают различные способы включения силиконового материала, элюирующего лекарственный препарат, в различные части имплантируемого кохлеарного электрода.
Фиг. с 42 по 45 показывают различные конкретные варианты кохлеарных электродов, содержащих силиконовый материал, элюирующий лекарственный препарат.
Фиг.46, 47 показывают вариант, в котором имеются элюирующий препарат силиконовый материал и элюирующий препарат силиконовый стержень, расположенный в щели электрода.
Фиг.48, 49 показывают альтернативные варианты включения в электрод элюирующего лекарственный препарат силикона.
Фиг.50 показывает имплантируемый носитель электрода, включающий резервуар, содержащий некоторый объем терапевтического раствора.
Фиг.51, 52, 53 показывают различные альтернативные детали носителя электрода, подобного представленному на фиг.50.
Фиг.54, 55 показывают двухканальный носитель электрода, содержащий резервуар.
Фиг.56 показывает в увеличенном масштабе секцию выходных отверстий в носителе электрода, показанного на фиг.54-55.
Осуществление изобретения
Фиг.1 графически представляет систему доставки жидкого препарата в соответствии с одним вариантом настоящего изобретения. В соответствии с целями данного варианта система доставки жидкого препарата применяется, например, для доставки фармацевтических препаратов во внутреннее ухо пациента. Однако системы доставки жидкого препарата и приспособления, здесь описанные, могут использоваться и для доставки жидкостей многих различных типов к одной или нескольким внутренним областям тела пациента. Система, показанная на фиг.1, включает биологически совместимый герметичный микроклапан 101, имеющий сторону 103, соответствующую внутреннему уху 103, и сторону 105, соответствующую среднему уху. Микроклапан 101 обеспечивает надежный проводящий путь между средним ухом и внутренним ухом через промонторий 107 улитки или через круглое окно. Соединение может, например, быть осуществлено как соединение с барабанной лестницей улитки, преддверием или протоком улитки. Микроклапан 101 обеспечивает постоянный доступ к внутреннему уху для доставки жидких препаратов различной вязкости и с разными лечебными функциями. Микроклапан 101 может быть изготовлен, например, из полимера, титана (инструментами особо точной лазерной микрообработки, например, производимыми компанией Kurtz GmbH, Германия), из сплава титана и никеля и в любом сочетании с биоматериалами. Для применения во внутреннем ухе микроклапан 101 может закрепляться на промонтории 107 улитки. Аналогично, микроклапан может быть размещен в круглом окне или полукружном канале внутреннего уха. Закрепление и обеспечение изоляции между изготовленным на основе металлов и/или полимеров микроклапаном 101 и промонторием 107 выполняется с применением, например, биосовместимого клея и/или механическим соединением с имеющим резьбу штифтом, а также сращиванием имплантата с костью (остеоинтеграцией). Соединение между микроклапаном 101 и промонторием 107 может осуществляться, например, через трубку, имеющую внутреннюю и внешнюю резьбу. Микроклапан 101 может быть сделан удаляемым из промонториума 107, когда это необходимо.
Для установки микроклапана 101 типично (но не обязательно) высверливание отверстия диаметром примерно от 0,8 до 2 мм или более в промонтории. Микроклапан 101 может быть, как показано на фиг.10, закрывающимся автоматически, когда на него не воздействует никакое давление жидкости из катетера, от резервуара или насоса. На поверхность микроклапана 101 может быть нанесено покрытие, или же она может быть обработана способом химического осаждения из газовой фазы или другими средствами с целью предотвращения разрастания ткани и возникающей через некоторое время окклюзии отверстия клапана в интракохлеарной области. Микроклапан 101 может включать также магнит и магнитную систему управления через тимпанопластику. Доставка жидкого препарата к микроклапану 101 может осуществляться через гибкий катетер 109, который может иметь внутренний диаметр от 0,5 до 2 мм (размеры не имеют ограничительного смысла). Один конец катетера 109 может быть надежно соединен, например, со стороной 105, соответствующей среднему уху, микроклапана 101. Соединение является достаточно плотным, чтобы предотвратить утечку жидкости из катетера в среднее ухо. Соединение может быть постоянным или допускающим отсоединение хирургическими средствами. Внутренняя поверхность катетера 109 может быть обработана таким образом, чтобы сообщить просвету гидрофильные свойства, поскольку гидрофильные свойства способствуют доставке вязкой жидкости. Другой конец катетера может быть соединен с источником жидкого препарата, например, насосом 111 с резервуаром 113. Аналогично, источник жидкого препарата может включать резервуар 401 с пассивной системой разгрузки, такой как поршень, приводимый в действие пружиной, или поршень, включающий магнит и приводимый в действие извне или изнутри магнитными силами, как показано на фиг.4. Катетер 109 может также быть соединен с осмотическим насосом. Насос 111 может быть активным насосом; это означает, что он может приводиться в действие с помощью энергии, передаваемой через кожу электронному блоку управления, например, применяемому в кохлеарных имплантатах и других имплантируемых протезах. Насос 111 может быть также пассивным насосом, энергия на который передается, например, газом или другим флюидом, введенным в камеру насоса.
Когда насос 111 обеспечен энергией, требуемой для перемещения жидкого препарата из резервуара 113 через катетер к внутреннему уху, или когда жидкость перемещается посредством сжатой пружины резервуара 401, давление оказывается достаточным для открытия микроклапана 101. Когда давление или энергия не воздействуют на микроклапан 101, он может закрываться автоматически, изолируя тем самым внутреннее ухо от среднего уха. Закрытие микроклапана 101 может осуществляться с помощью титанового шарика 1001, прикрепленного к пружине 1003 со стороны клапана, соответствующей внутреннему уху, как показано на фиг.10. Однако могут применяться и другие способы открытия и закрытия микроклапана 101, например с использованием давления жидкости/газа или с помощью пьезоэлектрических элементов.
В другом варианте изобретения микроклапан 101 может быть надежно соединен непосредственно, например, резьбовым соединением с контейнером 601, как показано на фиг.6. Это позволяет выполнить одноразовую доставку жидкого препарата. Контейнер 601 может быть удален и снова наполнен или заменен другим контейнером, способным выполнять пассивную функцию при доставке жидкого препарата.
Как отмечено выше, система доставки жидкого препарата в соответствии с изобретением может использоваться в сочетании с электронным протезом или имплантатом, например кохлеарным имплантатом. Это может быть выполнено двумя способами: способом объединения катетера с электродом, соединенным с протезом или имплантатом, или способом параллельной доставки жидкого препарата и электрического тока к данной области тела пациента. Фиг.2 - графическая иллюстрация системы доставки жидкого препарата, соединенной с кохлеарным имплантатом, в соответствии с вариантом изобретения. Катетер 109 системы доставки жидкого препарата связан с кохлеарным имплантатом 201 через электрод 203. Электрод 203 является полым на отрезке, начинающемся в точке соединения 203 катетера с электродом (отметим, что в этом варианте также можно применять клапан, как это было описано выше). Полый участок электрода 203 может заканчиваться в некоторой области внутри улитки. Полый электрод 203 функционирует как канал доставки жидкого препарата к внутреннему уху. На участке электрода внутри улитки имеется один или несколько каналов подходящего размера, сформированных в материале электрода 203; эти каналы обеспечивают доступ к жидкости внутреннего уха. Катетер 109, соединяющий источник жидкого препарата с имплантатом, может быть (или не быть) отсоединяемым от электрода 203. Когда он не является отсоединяемым, клапан или переключатель (не показан) предотвращает какой-либо обмен (это относится к жидкостям, тканям и воздуху) между внутренним ухом и другими структурами височной кости, включая среднее ухо.
Фиг.3 графически представляет систему доставки жидкого препарата, имплантированную параллельно кохлеарному имплантату, в соответствии с вариантом изобретения. Параллельная доставка состоит в том, что кохлеарный имплантат 301 и система доставки жидкого препарата 305 не соединяются друг с другом. Чтобы разместить раздельные ввод электрода 303 и канал системы 305 доставки жидкого препарата, можно использовать одну большую кохлеостому или две отдельных, но смежных кохлеостомы. Кохлеостомы могут находиться рядом друг с другом на промонтории. В этом случае электрод кохлеарного имплантата 303 и канал системы 305 доставки жидкого препарата могут быть введены во внутреннее ухо с помощью классической операции, которая включает заднюю тимпанотомию или одну расширенную кохлеостомию, позволяющую ввести как электрод, так и канал доставки жидкого препарата через одно и то же или через смежные отверстия промонтория. При типичном подходе требуется высверлить две кохлеостомы, следуя двум различным хирургическим тактикам доступа к промонторию. Первая хирургическая тактика является классической задней тимпанотомией.
Вторая хирургическая тактика является вариантом так называемого надпроходного (supra-meatal) доступа, описанного профессором
Кроненбергом (Kronenberg), профессором Хауслером (Hausler) и доктором Киратзидисом (Kiratzidis). Электрод или система доставки жидкого препарата могут быть введены классической кохлеостомией после задней тимпанотомии. Электрод или система доставки жидкого препарата могут быть введены в кохлеостому с использованием надпроходного доступа. Электрод или система доставки жидкого препарата могут также быть имплантированы через круглое окно. Возможны любые перестановки электрода и системы доставки жидкого препарата при двух кохлеостомах и при одной кохлеостоме и отверстии в круглом окне.
Фиг.5 графически представляет систему доставки жидкого препарата в соответствии с другим вариантом изобретения. В соответствии с этим вариантом катетер может быть введен непосредственно во внутреннее ухо, при этом клапан промонтория отсутствует. В этом случае высверливается кохлеостома, и катетер вводится в отверстие на некоторое расстояние. Катетер может быть надежно герметизирован, например, с помощью фибринового клея на промонтории. Фиг.7 графически представляет переключатель, который может быть имплантирован под кожу в соответствии с вариантами изобретения. В различных вариантах (резервуар с поршнем, резервуар и насос, контейнер с резьбой, с пополняемым или не пополняемым резервуаром, с резервуаром, включенным в систему кохлеарного имплантата, с системой доставки лекарственного средства при наличии клапана или без клапана на промонтории и т.д.) могут быть включены средства, позволяющие останавливать в любой момент доставку жидкого препарата, если пациент страдает от побочных эффектов. Поток жидкости может быть остановлен, например, телеметрически, если в конструкцию включен насос с приемником телеметрических сигналов. Поток жидкости может быть остановлен пассивным механическим переключателем 701 (обеспечивающим функции включения/выключения). Такой переключатель 701 может быть предусмотрен, например, на катетере, резервуаре или клапане. Переключатель 701 может быть включен или выключен вручную, если он доступен извне (если, например, он фиксирован на поверхности черепной кости непосредственно под кожей). Переключатель 701 может также приводиться в действие с помощью энергии магнитного поля, передаваемой через кожу или через барабанную перепонку 801, как показано на фиг.8. Переключатель может также включаться и выключаться через маленькое отверстие в барабанной перепонке (тимпанопластику) путем введения специально разработанного инструмента в клапан или воздействием на особым образом расположенный вблизи клапана переключатель в среднем ухе. Особым образом расположенный переключатель может представлять собой металлическую деталь, нависающую над промонторием и доступную посредством тимпанопластики.
В соответствии с различными вариантами системы доставки лекарственных препаратов резервуар или контейнер может допускать пополнение. На фиг.9 показано, что пополнение может осуществляться, например, с помощью инъекции жидкого лечебного препарата через толстую непроницаемую мембрану, находящуюся на верхней стороне резервуара, или с помощью специального выходного клапана. Такое пополнение может осуществляться под местной анестезией после разреза кожного покрова, закрывающего резервуар. Пополнение может также осуществляться через малый разрез на барабанной перепонке введением иглы в приемное гнездо резервуара. Если система доставки представляет собой резервуар со сжатой пружиной, то для пополнения резервуара может применяться, например, система с переключаемыми клапанами. После того, как доступ к устройству обеспечен, переключаемый клапан 901 закрывается, а переключаемый клапан 902 открывается. Жидкий препарат может вводиться через переключаемый клапан 902, например, с помощью иглы, что заставляет поршень 903 смещаться назад, что обеспечивает загрузку жидкого препарата в насос и сжатие пружины 905 насоса.
Фиг.11 графически представляет систему доставки жидкого препарата через барабанную перепонку пациента. Здесь насос и/или резервуар 111, 113 находится вне наружного уха, а катетер проходит через наружное ухо и барабанную перепонку. Конец катетера 1101 в среднем ухе соединяется с клапаном, фиксированным на промонтории, круглом окне или овальном окне. Присоединенный катетер 1101 может быть отсоединен, если приложить тянущее усилие к трубке катетера, в результате чего возникает сила, действующая в направлении от среднего уха к наружному уху. Как и в вариантах, описанных выше, насос/резервуар может содержать включаемый/выключаемый переключатель, а резервуар может быть пополнимым. На фиг.12-14 показано другое устройство для доставки жидкого препарата в организм пациента. Устройство включает источник жидкого препарата типа гидронасоса 1201 (как показано на фиг.12) или содержащий жидкий препарат порт или резервуар 1301 (как показано на фиг.13). Устройство, кроме того, включает микромембранный разъем 1203. Микромембранный разъем сообщается с питающим иглу катетером 1205 в его проксимальном конце, который, в свою очередь, сообщается с источником жидкого препарата. Микромембранный разъем 1203 также сообщается с катетером 1207 порта в дистальном конце. Катетер 1207 порта может сообщаться с другим катетером (не показан), или с одним или несколькими электродами, или с электронным протезом 1401, как показано на фиг.14. Каждый электрод или электронный протез 1401 может включать один или несколько жидкостных каналов 1403 с выходами такими, что каждый электрод или электронный протез 1401 действует, в свою очередь, как катетер с одним или несколькими выходами.
Как описано выше, микромембранный разъем 1203 сообщается с имплантируемым гидронасосом, или портом, или резервуаром 1301, или с осмотическим насосом через питающий иглу катетер 1205 и сообщается с телом пациента через катетер 1207 порта, который может быть соединен и может сообщаться с другим катетером, или электродом, или электронным протезом (таким как 1401). Устройство доставки жидкого препарата (например, катетер 1207 порта и электрод или электронный протез 1401) и устройство, приводящее в движение и доставляющее жидкий препарат (например, гидронасос 1201 или порт 1301 жидкого препарата), предназначены для имплантации в организм пациента (человека или животного) с помощью хирургической операции. Соединение между двумя устройствами осуществляется с помощью микромембранного разъема 1203.
На фиг.15 графически представлен микромембранный разъем согласно варианту изобретения. Микромембранный разъем включает имплантируемый разъем 1501 порта и имплантируемый пунктирующий разъем 1503 (показанный как соединенный на фиг.15 и как не соединенный на фиг.16). Имплантируемый разъем 1501 порта включает мембрану 1505 и может сообщаться с катетером 1207 порта, транспортирующим жидкий препарат к конкретной области тела пациента, к которой подходит дистальный конец (когда разъем 1501 порта сообщается с катетером 1207 порта, разъем порта находится вблизи проксимального конца катетера 1207 порта, как показано на фиг.12-14). Дистальный конец катетера 1207 порта может иметь одно или несколько отверстий, позволяющих жидкости распределяться в окружающей биологической ткани. Пунктирующий разъем 1503 включает иглу 1507 и может сообщаться с питающим иглу катетером 1205 в дистальном конце. К проксимальному концу питающего иглу катетера 1205 прикреплен источник жидкого препарата.
В одном варианте изобретения проксимальный конец разъема 1501 порта и дистальный конец пунктирующего разъема 1503 не соединяются плотно, "поверхность к поверхности". Это должно предотвратить образование мертвого пространства между плоскими поверхностями микромембранного разъема 1203 присоединении разъема 1501 порта и пунктирующего разъема 1503 посредством иглы 1507. В таком варианте игла 1507 пунктирующего разъема 1503 пронизывает мембрану 1505, но часть иглы 1507, оставшаяся вне мембраны 1505, оказывается в контакте с жидкостями и тканями тела. Такая ситуация способствует хорошей изоляции тканями тела в точке, где игла 1507 входит в мембрану 1505. Кроме того, в инкапсулирующую ткань поступает жидкость из окружающих тканей, а поэтому она может благоприятным образом отвечать на любое воспаление. Целесообразным является также введение в иглу 1507 тканей оболочки мышц или мышц, доходящих до торца пунктирующего разъема 1503. Введение тканей будет способствовать хорошему здоровому росту тканей между торцами разъема 1501 порта и пунктирующим разъемом 1503. Как можно видеть на фиг.16, когда разъем 1501 порта и пунктирующий разъем 1503 оказываются соединенными, они обеспечивают надежный транспорт жидкости, не сопровождающийся утечкой в окружающую биологическую среду.
Важной особенностью (признаком) разъема 1501 порта является мембрана 1505. Мембрана 1505 изготовляется предпочтительно из силиконового каучука. Разъем 1501 порта может также включать сжимающее кольцо 1511. Сжимающее кольцо 1511 (или другое сжимающее устройство) сжимает силикон, благодаря чему устройству придаются свойства изолирующей мембраны. Сжимающее кольцо 1511 изготовляется предпочтительно из титана медицинского качества, однако может применяться любой другой материал, который может сдавливать силикон, находящийся в цилиндрической части. Такие материалы могут быть металлами типа нитинола, который обладает свойством запоминать форму, или полимерами, обладающими аналогичным свойством. Сжимающее кольцо 1511 может заканчиваться на соединяющей стороне разъема 1501 порта какой-либо направляющей или направляющим механизмом 1513, упором или другим приспособлением 1515, служащим для блокирования дальнейшего перемещения, и фиксатором 1517. Можно, если желательно, ввести бактериальный фильтр 1509 между разъемом 1501 порта и катетером 1207 порта. Разъем 1501 порта может также включать резервуар 1521, который может быть выстлан титановым защитным слоем, или титановую оболочку, предотвращающую прокалывание иглой 1507. Проксимальный конец катетера 1207 порта может по желанию быть скреплен с разъемом порта силиконом. Слой силикона может быть нанесен на весь разъем 1501 порта, чтобы предотвратить контакт металла со средой и способствовать инкапсуляции. Нанесение слоя может быть выполнено способом погружения разъема 1501 порта в подходящий раствор силиконового каучука.
Пунктирующий разъем 1503 может быть изготовлен из силикона, эпоксидной смолы или любого другого биосовместимого материала, который будет выбран как необходимый или полезный для данного изобретения. Медицинская игла (