Производные индола как ингибиторы н3-рецептора гистамина для лечения когнитивных расстройств и нарушений сна, ожирения и других расстройств центральной нервной системы
Иллюстрации
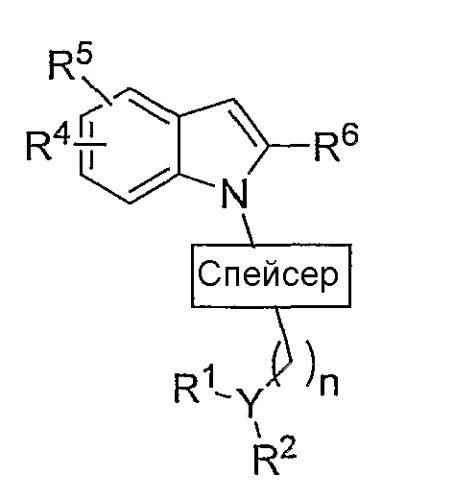
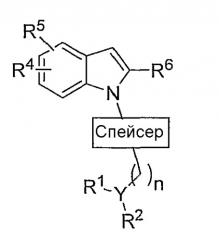
Показать всеИзобретение относится к соединениям формулы:
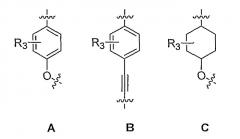
где спейсер представляет собой
Y представляет собой N;
R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют 5-6-членную гетероциклическую кольцевую систему, которая, необязательно, замещена 1-3 (С1-С5)алкильными группами; n равен 2-4; R3 представляет собой 0-2 группы, выбранные из атома галогена, (С1-С6)алкильной, (С1-С6)алкоксильной групп;
R4 и R5 независимо выбраны из Н, (С1-С5)алкильной, (C1-С8)алкоксильной группы, атома галогена;
R6 представляет собой Н, CONR7R8, -(СН2)х-О-R9, (С1-С4)алкильную группу, СООС2Н5, циклопропил;
х равен 1-4;
R7 и R8 независимо представляют собой водород, (С1-С5)алкильную группу, (С3-С7)-циклоалкильную группу, -СН2-циклогексил или
R7 и R8 вместе с атомом азота, к которому они присоединены, образуют 5-6-членную гетероциклическую кольцевую систему с 0-1 дополнительным гетероатомом, выбранным из О;
R9 представляет собой водород, (С1-С5)алкильную, (С3-С7)циклоалкильную группу;
и его фармацевтически приемлемым солям, и его индивидуальным стереоизомерам.
Соединения ингибируют Н3-рецептор гистамина, что позволяет использовать их для получения фармацевтических композиций. 4 н. и 2 з.п. ф-лы, 1 табл.
Реферат
ОПИСАНИЕ
Перекрестная ссылка на родственную заявку
Эта заявка заявляет на приоритет предварительной заявки на патент США с серийным номером 60/726793, поданной 14 октября 2005 года, описание которой включено в настоящее описание посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Это изобретение относится к соединениям, обладающим фармакологической активностью, композициям, содержащим эти соединения, и способу лечения, применяющего соединения и композиции. Более конкретно, это изобретение относится к некоторым производным индола и их солям и сольватам. Эти соединения изменяют активность Н3-рецептора гистамина. Это изобретение также касается фармацевтических композиций, содержащих эти соединения, и способа лечения расстройств, в которых полезно блокирование Н3-рецептора гистамина.
УРОВЕНЬ ТЕХНИКИ
Гистамин представляет собой химический мессенджер, участвующий во многих сложных биологических процессах. При высвобождении гистамин взаимодействует со специфическими макромолекулярными рецепторами на клеточной поверхности или внутри клетки-мишени, вызывая изменения многих различных функций организма. Разнообразные типы клеток, включая гладкую мускулатуру, клетки крови, клетки иммунной системы, эндокринные и экзокринные клетки, а также нейроны, откликаются на гистамин посредством модуляции формирования межклеточных сигналов, в том числе фосфатидилинозита или фермента аденилатциклазы. Очевидность того, что гистамин играет роль нейромедиатора, была обнаружена во второй половине 1970-х годов (Schwartz, 1975), Life Sci., 17: 503-518. Иммуногистохимические исследования выявили гистаминергические клеточные тела в туберомамиллярном ядре заднего гипоталамуса с распространенными проекциями в промежуточный и большой мозг (Inagaki et al., 1998), J. Comp. Neurol., 273: 283-300.
Два рецептора гистамина (Н1 и Н2) были описаны как посредники биохимических действий гистамина на нейроны. Впоследствии исследования выявили существование третьего подтипа рецептора гистамина, Н3-рецептора гистамина (Schwartz et al., 1986), TIPS, 8: 24-28. Разнообразные исследования теперь продемонстрировали, что Н3-рецепторы гистамина находятся на гистаминергических нервных окончаниях в мозге некоторых биологических видов, включая человека (Arrang et al., 1983), Nature, 302: 832-837. Н3-рецептор, найденный на гистаминергическом нервном окончании, был охарактеризован как авторецептор и мог бы непосредственно контролировать количество гистамина, выделяемого из нейронов. Гистамин, представляющий собой природное соединение, был способен стимулировать этот авторецептор, но тестирование известных агонистов и антагонистов Н1- и Н2-рецепторов привело к мысли, что Н3-рецептор имеет особый фармакологический профиль. Далее, Н3-рецепторы были идентифицированы на холинергических, серотонинергических и моноаминных нервных окончаниях в периферической нервной системе (PNS) и центральной нервной системе, включая кору головного мозга и кровеносные сосуды головного мозга. Эти наблюдения предполагают, что Н3-рецепторы размещаются единственно для модулирования высвобождения гистамина, а также прочих нейромедиаторов, и соединения, которые связывают Н3-рецепторы, могли бы быть важными медиаторами нейронной активности.
Как установлено, гистаминергические клеточные тела центральной нервной системы обнаруживаются в магноцеллюлярном ядре сосковой части гипоталамуса, и эти нейроны диффузно проецируются на большие области переднего мозга. Присутствие гистаминергических клеточных тел в туберомамиллярных ядрах заднего гипоталамуса, зоны мозга, вовлеченной в поддержание бодрствования, и их проекции на кору головного мозга свидетельствуют о роли в модулировании состояния активации или цикла сна-пробуждения. Гистаминергическая проекция на многие лимбические структуры, такие как гиппокампальная формация и амигдалоидный комплекс, свидетельствуют о роли в таких функциях, как автономная регуляция, контроль эмоций и мотивированное поведение, и процессы памяти.
Концепция, что гистамин является важным для состояния активации, на что указывает расположение гистаминергических путей, подтверждается другими типами фактов. Хорошо известно, что повреждения заднего гипоталамуса могут вызывать сон. Нейрохимические и электрофизиологические исследования также показали, что активность гистаминергических нейронов максимальна во время периодов бодрствования и подавляется барбитуратами и другими снотворными средствами. Внутрижелудочковый гистамин вызывает признаки картины пробуждения на электроэнцефалограмме кроликов и усиливает спонтанную двигательную активность, груминг и исследовательское поведение у крыс, получивших как физиологический раствор, так и пентобарбитал.
Напротив, высокоселективный ингибитор гистидиндекарбоксилазы, единственного фермента, ответственного за синтез гистамина, был показан как ухудшающий пробуждение крыс. Эти данные поддерживают гипотезу, что гистамин может быть эффективным в модулировании поведенческой активации. Была продемонстрирована роль Н3-рецептора в характеристиках сна-пробуждения (Lin et al., 1990), Brain Res., 592: 325-330. Пероральное введение препарата RAMHA, агониста Н3-рецептора, вызывало существенное усиление медленной волны глубокого сна у кошек. Наоборот, тиоперамид, антагонист/обратный агонист Н3-рецептора, усиливает бодрствование в зависимости от дозы. Тиоперамид был также показан усиливающим бодрствование и сокращающим медленную волну и быстрый сон у крыс. Эти факты согласуются с результатами исследований in vivo, демонстрирующих, что тиоперамид усиливает синтез и высвобождение гистамина. В совокупности эти данные демонстрируют, что селективные антагонисты Н3-рецептора или обратные агонисты могут быть полезными в лечении состояний активации и нарушений сна.
Было показано, что содержание как серотонина, так и гистамина и ацетилхолина в мозге снижается при болезни Альцгеймера (AD). Н3-рецептор гистамина был показан как регулятор высвобождения каждого из этих нейромедиаторов. Поэтому следовало бы ожидать, что антагонист или обратный агонист Н3-рецептора усиливал бы высвобождение этих нейромедиаторов в мозге. Поскольку было продемонстрировано, что гистамин важен для возбуждения ЦНС, антагонисты или обратные агонисты Н3-рецептора могли бы усилить возбуждение ЦНС благодаря повышению уровней высвобождения нейромедиаторов и тем самым улучшить познавательную способность. Так, применение соединений, которые подавляют функционирование Н3-рецептора при болезни Альцгеймера (AD), расстройствах концентрации внимания (ADD), связанных с возрастом нарушениях памяти и прочих расстройствах познавательных способностей, было бы обоснованным.
Антагонисты или обратные агонисты Н3-рецептора могут быть полезными в лечении некоторых прочих расстройств центральной нервной системы. Было высказано предположение, что гистамин может быть вовлечен в мозговое кровообращение, энергетический обмен и секрецию гипоталамических гормонов. Например, антагонисты или обратные агонисты Н3-рецептора были продемонстрированы влияющими на прием пищи и прирост веса тела у грызунов. Недавно полученные факты показали возможность применения антагонистов или обратных агонистов Н3-рецептора в лечении эпилепсии. Работа выявила обратную корреляцию между продолжительностью хронических конвульсий и уровнями гистамина в мозге. Тиоперамид был также показан в существенном и дозозависимом сокращении продолжительности каждой конвульсивной фазы после индуцированных электрическим током конвульсий и повышении электроконвульсивного порога.
Несмотря на свою низкую плотность, сайты связывания Н3-рецептора могут быть обнаружены вне мозга. Некоторые исследования выявили присутствие Н3-гетерорецепторов в желудочно-кишечном тракте, а также на нейронах дыхательных путей. Соответственно, соединение, связывающее Н3-рецептор, может быть полезным в лечении заболеваний и состояний, таких как астма, ринит, гиперемия дыхательных путей, воспаление, гиперкинезия и гипокинезия и секреция кислоты в желудочно-кишечном тракте. Блокирование периферических или центральных Н3-рецепторов также может содействовать изменениям кровяного давления, частоты сердечных сокращений и пропускной способности сердечно-сосудистой системы и могло бы быть использовано в лечении сердечно-сосудистых заболеваний и в лечении таких болезней или состояний, как ожирение, мигрень, воспаление, морская болезнь, боль, расстройства концентрации внимания с гиперактивностью (ADHD), слабоумие, депрессия, болезнь Паркинсона, шизофрения, эпилепсия, нарколепсия, острый инфаркт миокарда и астма.
Различные производные индола представлены в патентах США № 5631381 и 6630496 В1; WO 93/25524; WO 99/43672 и WO 2004/099192.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение, в своем главном аспекте, представляет соединения общей формулы:
в которой
спейсер представляет собой
Y представляет собой СН или N при условии, что если Y представляет собой СН, то n равен 0-2; если Y представляет собой N, то n равен 2-4;
если Y представляет собой СН, то R1 и R2, взятые вместе, представляют собой -(CH2)a-NR11-(CH2)2-, где а равен 1-2, который вместе с Y образует пиперидиновый или пирролидиновый цикл, который, необязательно, замещен 1-3 группами, выбранными из атома фтора, фторалкильной, (С1-С4)алкильной, алкоксильной, арильной, (С3-С7)циклоалкильной, гетероциклоалкильной группы, содержащей 1-2 гетероатома, выбранных из (О, S) и (С1-С5)алкил-О-(С1-С5)алкила; и
если Y представляет собой N, то R1 и R2 независимо представляют собой (С1-С5)алкильную или (С3-С6)циклоалкильную группу, или R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют 5-7-членную гетероциклическую кольцевую систему с 0-1 дополнительным гетероатомом, выбранным из О и S, которая, необязательно, замещена 1-3 (С1-С5)алкильными, фторалкильными или (С3-С6)циклоалкильными группами, или R1 и R2, взятые вместе, представляют собой -(CH2)a-NR11-(CH2)2-, где а равен 2-3, который вместе с Y образует пиперазиновый или гомопиперазиновый цикл, который, необязательно, замещен 1-3 группами, выбранными из атома фтора, фторалкильной, (С1-С4)алкильной, алкоксильной, арильной, (С3-С7)циклоалкильной, гетероциклоалкильной группы, содержащей 1-2 гетероатома, выбранных из (О, S) и (С1-С5)алкил-О-(С1-С5)алкила;
R3 представляет собой 0-2 из групп, выбранных из атома галогена, (С1-С6)алкильной, (С1-С6)алкоксильной, (С3-С7)циклоалкильной, (С3-С7)циклоалкил-(С1-С6)алкильной, гетероциклоалкильной групп, содержащих 1-3 гетероатома, выбранных из (О, S) и (С1-С3)алкил-О-(С1-С5)алкила;
R4 и R5 независимо выбраны из Н, (С1-С5)алкильной, (С1-С8)алкоксильной, (С1-С5)алкил-О-(С1-С5)алкильной, (С3-С6)циклоалкильной, арильной, СF3-группы и атома галогена;
R6 представляет собой CONR7R8, -(CH2)x-O-R9, алкильную, фторалкильную группу или SO2NR7R8;
х равен 1-4;
R7 и R8 независимо представляют собой водород, (С1-С5)алкильную или (С3-С6)циклоалкильную группу или R7 и R8 вместе с атомом азота, к которому они присоединены, образуют 5-7-членную гетероциклическую кольцевую систему с 0-1 дополнительными гетероатомами, выбранными из О, S и N(R10), в которой сформированное кольцо необязательно замещается 1-3 (С1-С5)алкильными или (С3-С6)циклоалкильными группами;
R9 представляет собой водород, (С1-С5)алкильную, (С3-С7)циклоалкильную или арильную группу;
R10 представляет собой (С1-С5)алкильную, (С1-С8)алкоксильную, (С1-С5)алкил-О-(С1-С5)алкильную, (С3-С6)циклоалкильную или арильную группу; и
R11 представляет собой (С1-С5)алкильную, фторалкильную или (С3-С6)циклоалкильную группу, и их фармацевтически приемлемые соли, и их индивидуальные стереоизомеры.
Настоящее изобретение также относится к фармацевтическим композициям, включающим фармацевтически приемлемый носитель в сочетании с эффективным количеством, по меньшей мере, одного соединения формулы (I).
Настоящее изобретение также относится к способу лечения состояний, в которых модуляция Н3-рецепторов гистамина может быть терапевтически важной, таких как воспаление, мигрень, морская болезнь, боль, болезнь Паркинсона, эпилепсия, сердечно-сосудистая болезнь (т.е. повышенное или пониженное кровяное давление, острый инфаркт миокарда), желудочно-кишечные расстройства (секреция кислоты, сократительная способность) и расстройства центральной нервной системы, включая расстройства концентрации внимания или познавательной способности (т.е. болезнь Альцгеймера, расстройство концентрации внимания, связанные с возрастом нарушения памяти, удар и т.д.), психиатрические расстройства (т.е. депрессия, шизофрения, обсессивно-компульсивные расстройства и т.д.); нарушения сна (т.е. нарколепсия, апноэ во сне, бессонница, нарушение биологического и околосуточного ритма, патологическая сонливость и инсомния), и такие расстройства, как ожирение, анорексия/булимия, терморегуляция, высвобождение гормонов), включающему введение эффективного количества соединения формулы (I) пациенту, нуждающемуся в таком лечении.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Предпочтительно для соединений формулы (I) R1-Y-R2 представляет собой (пирролидин-1-ильный остаток); R3 представляет собой Н; R4 представляет собой Н; 5-метоксильную, 5-фтор или метильную группу; R5 представляет собой Н; и R6 представляет собой -СН2ОСН3 или -(СН2)2ОСН3.
В настоящий момент предпочтительные соединения включают
2-метил-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
2-метил-1-[4-(3-пиперидин-1-илпропокси)фенил]-1Н-индол;
2-метил-1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол;
1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
5-метокси-2-метил-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
5-метил-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
5-бром-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
4-хлор-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
5-метокси-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
5-хлор-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
2,5-диметил-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
6-хлор-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
2-метил-5-фтор-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
1-[3-метокси-4-(3-пирролидин-1-илпропокси)фенил]-2-метил-1Н-индол;
1-[3-хлор-4-(3-пирролидин-1-илпропокси)фенил]-2-метил-1Н-индол;
2-пропил-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
5-метокси-2-метил-1-[4-(4-пирролидин-1-илбут-1-инил)фенил]-1Н-индол;
(5-метокси-1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол-2-ил)пирролидин-1-илметанон;
циклобутиламид 1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол-2-карбоновой кислоты;
циклопентиламид 1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол-2-карбоновой кислоты;
циклогексиламид 1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол-2-карбоновой кислоты;
циклогептиламид 1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол-2-карбоновой кислоты;
1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол-2-ил)пирролидин-1-илметанон;
2-(3-морфолин-4-илпропокси)-6,7,8,9-тетрагидропиридо[1,2-а]индол;
(1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол-2-ил)морфолин-4-илметанон;
бутиламид 1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол-2-карбоновой кислоты;
изобутиламид 1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол-2-карбоновой кислоты;
циклогексилметиламид 1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол-2-карбоновой кислоты;
циклогексиламид 5-метокси-1-{4-[3-(2R-метилпирролидин-1-ил)пропокси]фенил}-1Н-индол-2-карбоновой кислоты;
сложный этиловый эфир 1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол-2-карбоновой кислоты;
{1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол-2-ил}метанол;
2-метоксиметил-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
2-циклогексилоксиметил-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
2-изопропоксиметил-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
2-циклопентилоксиметил-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
{5-метокси-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол-2-ил}метанол;
2-циклопропил-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
2-пропил-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол;
2-циклопропил-1-[4-(3-пирролидин-1-илпропокси)циклогексил]-1Н-индол;
2-(2-метоксиэтил)-1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол и
2-{1-[4-(3-пирролидин-1-илпропокси)фенил]-1Н-индол-2-ил}этанол.
Некоторые соединения согласно изобретению могут существовать в различных изомерных (например, энантиомеры и диастереоизомеры) формах. Изобретение рассматривает все такие изомеры как в чистом виде, так и в смеси, включая рацемические смеси. Включены также енольные и таутомерные формы.
Соединения согласно изобретению могут существовать в несольватированных, а также сольватированных формах, включая гидратные формы, например полугидраты. В общем, сольватированные формы с фармацевтически приемлемыми растворителями, такими как вода, этанол и т.п., являются эквивалентными несольватированным формам в соответствии с изобретением.
Некоторые соединения согласно изобретению также образуют фармацевтически приемлемые соли, например соли присоединением кислот. Например, атомы азота могут образовывать соли с кислотами. Примерами применимых кислот для формирования солей являются соляная, серная, фосфорная, уксусная, лимонная, щавелевая, малоновая, салициловая, яблочная, фумаровая, янтарная, аскорбиновая, малеиновая, метансульфоновая и другие минеральные и карбоновые кислоты, хорошо известные специалисту в этой области. Соли готовятся путем контактирования формы свободного основания с достаточным количеством желаемой кислоты для образования соли общеупотребительным способом. Формы свободных оснований могут быть регенерированы путем обработки соли подходящим разбавленным водным раствором основания, такого как разбавленные водные растворы гидроксида, карбоната калия, аммиака и бикарбоната натрия. Формы свободных оснований до некоторой степени отличаются от своих соответствующих солевых форм некоторыми физическими свойствами, такими как растворимость в полярных растворителях, но соли кислот являются эквивалентными своим соответствующим формам свободных оснований в соответствии с изобретением (см., например, S.M. Berge, et al., “Pharmaceutical Salts”, J. Pharm. Sci., 66: 1-19 (1977), включено в описание посредством ссылки).
Используемые в описании и прилагаемых пунктах формулы изобретения термины имеют следующие значения:
Термин «алкил», как используется в описании, относится к радикалам с линейными или разветвленными цепями насыщенных углеводородов, при удалении одного атома водорода. Примерами алкильных групп являются метильная, этильная, н-пропильная, изопропильная, н-бутильная, втор-бутильная, изобутильная, трет-бутильная группы и т.п.
Термин «циклоалкил», как используется в описании, относится к алифатической циклической системе, имеющей от 3 до 10 атомов углерода и от 1 до 3 циклов, включая, но не ограничиваясь таковыми, циклопропильную, циклопентильную, циклогексильную, норборнильную и адамантильную группы, среди прочих. Циклоалкильные группы могут быть незамещенными или замещенными одним, двумя или тремя заместителями, независимо выбранными из низших алкильных, галогеналкильных, алкоксильных, тиоалкоксильных групп, аминогрупп, алкиламиногрупп, диалкиламиногрупп, гидроксильной группы, атомов галогенов, меркаптогруппы, нитрогруппы, карбоксальдегидной группы, карбоксильной группы, алкоксикарбонильных и карбоксимидных групп.
Термин «циклоалкил» включает цис- и транс-формы. Далее, заместители могут быть либо в эндо-, либо в экзоположениях в мостиковых бициклических системах.
Термин «галоген», как используется в настоящем описании, относится к атомам I, Br, Cl или F.
Термин «гетероатом», как используется в настоящем описании, относится, по меньшей мере, к одному из атомов N, О или S.
Термин «гетероциклический», как используется в настоящем описании, по отдельности или в сочетании, касается неароматического 3-10-членного цикла, содержащего, по меньшей мере, один эндоциклический атом N, О или S. Необязательно, гетероцикл может быть конденсированным с арильным кольцом. Гетероцикл также, необязательно, может быть замещен, по меньшей мере, одним заместителем, который независимо выбран из группы, состоящей из атома водорода, атомов галогенов, гидроксильной группы, аминогруппы, нитрогруппы, трифторметильной, трифторметоксильной, алкильной, арилалкильной, алкенильной, алкинильной, арильной групп, цианогруппы, карбоксильной, карбалкоксильной, карбоксиалкильной групп, оксогруппы, арилсульфонильной и арилалкиламинокарбонильной группы, среди прочих.
Как используется в описании, термин «композиция» предполагает продукт, включающий специфические ингредиенты в специфических количествах, а также любой продукт, который получается, непосредственно или косвенно, из комбинации специфических ингредиентов в специфических количествах.
Соединения согласно настоящему изобретению могут быть использованы в форме фармацевтически приемлемых солей, производных из неорганических или органических кислот. «Фармацевтически приемлемая соль» означает такие соли, которые, в объеме тщательного медицинского обследования, пригодны для применения в контакте с тканями человека и низших животных без чрезмерной токсичности, раздражения, аллергической реакции и т.п. и являются соразмерными с благоразумным соотношением польза/риск. Фармацевтически приемлемые соли хорошо известны в уровне техники. Например, S.M. Berge et al. подробно описывают фармацевтически приемлемые соли в J. Pharmaceutical Sciences, 1977, 66: с.1 и след. Соли могут быть приготовлены in situ во время окончательного выделения и очистки соединений согласно изобретению, или отдельно с помощью реакции функциональной группы свободного основания с подходящей органической кислотой. Представителями солей как продуктов присоединения кислоты являются, но не ограничиваются таковыми, ацетат, адипат, альгинат, цитрат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, камфорат, камфорсульфонат, диглюконат, глицерофосфат, гемисульфат, гептаноат, гексаноат, фумарат, гидрохлорид, гидробромид, гидроиодид, 2-гидроксиэтансульфонат (изотионат), лактат, малеат, метансульфонат, никотинат, 2-нафталинсульфонат, оксалат, пальмитат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат, тартрат, тиоцианат, фосфат, глутамат, бикарбонат, пара-толуолсульфонат и ундеканоат. Также, основные азотсодержащие группы могут быть кватернизованы действием таких средств, как низшие алкилгалогениды, такие как метил-, этил-, пропил- и бутилхлориды, -бромиды и -иодиды; диалкилсульфаты типа диметил-, диэтил-, дибутил- и диамилсульфатов; длинноцепочечные галогениды, такие как децил-, лаурил-, миристил- и стеарилхлориды, -бромиды и -иодиды; арилалкилгалогениды типа бензил- и фенетилбромидов и других. Таким образом получают продукты, растворимые или диспергируемые в воде или масле. Примеры кислот, которые могут быть применены для образования фармацевтически приемлемых солей как продуктов присоединения кислот, включают такие неорганические кислоты, как соляная кислота, бромистоводородная кислота, серная кислота и фосфорная кислота, и такие органические кислоты, как щавелевая кислота, малеиновая кислота, янтарная кислота и лимонная кислота.
Соли, получаемые присоединением оснований, могут быть приготовлены in situ во время окончательного выделения и очистки соединений согласно этому изобретению посредством реакции фрагмента, содержащего остаток карбоновой кислоты, с подходящим основанием, таким как гидроксид, карбонат или бикарбонат фармацевтически приемлемого металлического катиона, или аммиак, или органический первичный, вторичный или третичный амин. Фармацевтически приемлемые соли включают, но не ограничиваются таковыми, катионы, производные щелочных металлов или щелочноземельных металлов, таких как соли лития, натрия, калия, кальция, магния и алюминия и т.п., и нетоксичные четвертичные аммониевые и аминные катионы, включая аммоний, тетраметиламмоний, тетраэтиламмоний, метиламмоний, диметиламмоний, триметиламмоний, триэтиламмоний, диэтиламмоний и этиламмоний, среди прочих. Другими примерами органических аминов, используемых для формирования солей как продуктов присоединения оснований, являются этилендиамин, этаноламин, диэтаноламин, пиперидин, пиперазин и т.п.
Лекарственные формы для местного применения соединения согласно этому изобретению включают порошки, спреи, мази и средства для ингаляции. Активное соединение смешивают в стерильных условиях с фармацевтически приемлемым носителем и любыми требуемыми консервантами, буферами или пропеллентами, при необходимости. Офтальмические составы, глазные мази, порошки и растворы также рассматриваются в объеме настоящего изобретения.
Уровни дозировки активных ингредиентов в фармацевтических композициях согласно настоящему изобретению могут варьировать так, чтобы получить количество активного соединения, которое является эффективным для достижения желаемого терапевтического ответа для конкретного пациента, композиций и способа введения. Выбранный уровень дозировки будет зависеть от активности конкретного соединения, пути введения, серьезности состояния, которое лечат, и состояния и предшествующей истории болезни пациента, которого лечат. Однако специалисту в этой области свойственно начинать дозировку соединения с уровней, более низких, чем требуется для достижения желаемого терапевтического эффекта, и постепенно увеличивать дозировку до появления желаемого эффекта.
При использовании в вышеперечисленных или прочих видах лечения терапевтически эффективное количество одного из соединений согласно настоящему изобретению может быть использовано в чистой форме или, где такие формы существуют, в форме фармацевтически приемлемой соли, сложного эфира или пролекарства. Альтернативно, соединение может быть введено как фармацевтическая композиция, содержащая конкретное соединение в комбинации с одним или более фармацевтически приемлемыми наполнителями. Термин «терапевтически эффективное количество» соединения согласно изобретению означает количество соединения, достаточное для излечения заболеваний, при разумном соотношении польза/риск, применимом к любому медицинскому воздействию. Однако должно быть понятно, что общая суточная дозировка соединений и композиций согласно настоящему изобретению будет определяться лечащим врачом в пределах рамок тщательного медицинского обследования. Конкретный уровень терапевтически эффективной дозы для любого конкретного пациента будет зависеть от множества факторов, включающих излечиваемое расстройство и серьезность расстройства; активность конкретного применяемого соединения; конкретную применяемую композицию; возраст, массу тела, общее состояние здоровья, пол и режим питания пациента; время введения, путь введения и скорость выведения конкретного применяемого соединения; продолжительность лечения; лекарственные средства, употребляемые в комбинации или совпадающие с конкретным применяемым соединением; и подобных факторов, хорошо известных квалифицированному медицинскому работнику. Например, специалисту в этой области изначально свойственно начинать дозировку соединения с доз, более низких, чем требуется для достижения желаемого терапевтического эффекта, и постепенно увеличивать дозировку до появления желаемого эффекта.
Общая суточная доза соединений согласно настоящему изобретению, вводимая человеку или низшему животному, может варьировать от около 0,0001 до около 1000 мг/кг/день. Для перорального введения более предпочтительные дозы могут находиться в интервале от около 0,001 до около 5 мг/кг/день. При необходимости эффективная суточная доза может быть разделена на несколько доз для целей введения; следовательно, композиции разовой дозировки могут содержать такие количества или целые доли их, чтобы составить суточную дозу.
Настоящее изобретение также относится к фармацевтическим композициям, которые включают соединения согласно настоящему изобретению, введенные в состав вместе с одним или более нетоксичными фармацевтически приемлемыми носителями. Фармацевтические композиции могут быть специально составлены для перорального введения в твердой или жидкой форме, для парентеральной инъекции или для ректального введения.
Фармацевтические композиции согласно этому изобретению могут быть введены людям или прочим млекопитающим перорально, ректально, парентерально, интрацистернально, интравагинально, интраперитонеально, местно (в виде порошков, мазей или капель), буккально или в виде орального или назального спрея. Термин «парентерально», как используется в описании, относится к методам введения, которые включают внутривенную, внутримышечную, интраперитонеальную, внутригрудинную, подкожную и интраартикулярную инъекцию и инфузию.
В еще одном аспекте настоящее изобретение относится к фармацевтической композиции, включающей компонент согласно настоящему изобретению и физиологически приемлемый разбавитель. Настоящее изобретение включает одно или более соединений, описанных выше, введенных в состав композиций вместе с одним или более нетоксичными физиологически толерантными или приемлемыми разбавителями, носителями, вспомогательными лекарственными веществами или средами, которые в совокупности называются разбавители, для парентеральной инъекции, для интраназального введения, для перорального введения в твердой или жидкой форме, для ректального или местного введения, среди прочих.
Композиции могут быть также введены через катетер для местной доставки в назначенное место, через внутрикоронарный стент (трубчатое устройство, состоящее из тонкой проволочной сетки), или с помощью биоразлагаемого полимера. Соединения также могут образовывать комплекс с лигандами, такими как антитела, для целевой доставки.
Соединения, пригодные для парентеральной инъекции, могут включать физиологически приемлемые стерильные водные или неводные растворы, дисперсии, суспензии или эмульсии и стерильные порошки для разбавления в стерильные пригодные для инъекции растворы или дисперсии. Примеры пригодных водных и неводных носителей, разбавителей, растворителей или сред включают воду, этанол, полиолы (пропиленгликоль, полиэтиленгликоль, глицерин и т.п.), растительные масла (такие как оливковое масло), пригодные к инъекции органические сложные эфиры, такие как этилолеат, и их применимые смеси.
Эти композиции также могут содержать вспомогательные лекарственные вещества, такие как консерванты, смачивающие средства, эмульгаторы и диспергаторы. Защита от микроорганизмов может быть обеспечена с помощью разнообразных бактерицидных средств и противогрибковых препаратов, например парабенов, хлорбутанола, фенола, сорбиновой кислоты и т.п. Может быть также желательным включить изотонические агенты, например сахара, хлорид натрия и т.п. Пролонгированная абсорбция пригодной к инъекции фармацевтической формы может быть реализована применением агентов, замедляющих абсорбцию, например моностеарата алюминия или желатина.
Суспензии, в дополнение к активным соединениям, могут содержать суспендирующие средства, например, такие как этоксилированные изостеариловые спирты, полиоксиэтиленсорбит и сложные эфиры сорбитана, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, или их смеси, или подобные.
В некоторых случаях, чтобы пролонгировать действие лекарственного средства, желательно замедлить абсорбцию лекарственного средства при подкожной или внутримышечной инъекции. Это может быть выполнено с помощью жидкой суспензии кристаллического или аморфного материала с низкой растворимостью в воде. Скорость абсорбции лекарственного средства, кроме того, зависит от скорости его растворения, которая, в свою очередь, может зависеть от величины кристаллов или кристаллической формы. Альтернативно, замедленная абсорбция введенной парентерально лекарственной формы достигается растворением или суспендированием лекарственного средства в масляном наполнителе.
Пригодные для инъекции депо-формы изготавливаются формированием микроинкапсулированных матриц лекарственного средства в биоразлагаемых полимерах, таких как полилактид-полигликолид. В зависимости от отношения лекарственного средства к полимеру и природы конкретного применяемого полимера скорость высвобождения лекарственного средства может контролироваться. Примеры прочих биоразлагаемых полимеров включают полиортоэфиры и полиангидриды. Пригодные для инъекции депо-составы также готовят включением лекарственного средства в липосомы или микроэмульсии, которые являются совместимыми с тканями организма.
Составы для инъекций могут быть стерилизованы, например, фильтрованием через задерживающий бактерии фильтр, или введением стерилизующих средств в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или иной стерильной инъецируемой среде непосредственно перед употреблением.
Твердые лекарственные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых лекарственных формах активное соединение может быть смешано, по меньшей мере, с одним инертным, фармацевтически приемлемым наполнителем или носителем, таким как цитрат натрия или дикальцийфосфат, и/или а) наполнителями или добавками, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремниевая кислота; b) связующими средствами, такими как карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и гуммиарабик; с) увлажнителями, такими как глицерин; d) диспергаторами, такими как агар-агар, карбонат кальция, крахмал из картофеля или маниоки, альгиновая кислота, некоторые силикаты и карбонат натрия; е) замедлителями растворения, такими как парафин; f) ускорителями абсорбции, такими как четвертичные аммониевые соединения; g) смачивателями, такими как цетиловый спирт и моностеарат глицерина; h) абсорбентами, такими как каолин и бентонитовая глина, и i) смазывающими средствами, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси. В случае применения капсул, таблеток и пилюль лекарственные формы также могут включать буферные средства.
Твердые композиции подобного типа могут быть также применены в качестве наполнителей в желатиновых капсулах мягкого или твердого наполнения с использованием таких формообразующих средств, как лактоза или молочный сахар, а также полиэтиленгликоли с высокой молекулярной массой, и т.п.
Твердые лекарственные формы в виде таблеток, драже, капсул, пилюль и гранул могут быть приготовлены с покрытиями и оболочками, такими как энтеросолюбильные покрытия и прочие покрытия, хорошо известные в области приготовления фармацевтических составов. Необязательно, они могут содержать контрастные вещества и также могут состоять из композиции так, что они высвоб