Сульфированные поли(арилены) как гидролитически и термоокислительно устойчивые полимеры
Иллюстрации
Показать всеНастоящее изобретение относится к сульфированным поли(ариленам), их получению и использованию в мембранах, топливных элементах, электродиализе, увлажнении и осушении газов или для защиты от электромагнитного излучения. Предложенные сульфированные поли(арилены) содержат один или несколько структурных звеньев общей формулы -Х-Аr(SO3М)n-Y-, где Х и У выбраны из -SO2-, -SO-, -SO2O-, -СО-, -СОО-, -CONH-, -CONR- и -POR-, Аr выбран из фенилена, нафтилена, антрацена, фенантрена, бифенилена, фурана, тиофена, пиррола, тиазола, триазола, пиридина, имидазола и бензимидазола, которые помимо сульфокислотной группы и заместителей Х и У могут иметь заместители, которые не являются электронодонорными группами, М выбран из Li+, Na+, K+, NR4 +, PR4 + и Н+, n - целое число от 1 до 4, R означает алкил, который содержит исключительно повторяющиеся звенья формул -[Аr1(SO3М)n-Х-]- и -[Аr2(SO3М)n-Y-]-, где Ar1 и Ar2 означают ароматическую или гетероароматическую циклическую систему с 5-18 атомами в кольце, как определено выше для Аr, М и n такие, как определено выше. Технический результат - получение новых сульфированных поли(ариленов) и продуктов на их основе. 14 н. и 10 з.п. ф-лы, 23 ил.
Реферат
Применение материалов, обладающих ионной проводимостью, в области электрохимии, как, например, топливные элементы, диализный мешок, электролизеры и электрохимические методы разделения, ограничено из-за их гидролитических и термоокислительных областей устойчивости, которые часто находятся в области ниже 100°С. Однако в ряде применений, как, например, в случае топливных элементов, предпочтительно достигать более высоких рабочих температур (ок. 100-200°С). С одной стороны, требуется пониженное охлаждение топливного элемента, с другой стороны, при повышенных температурах повышается электрическая мощность ячейки как следствие ускоренных электродных реакций и уменьшенного отравления электродов (например, посредством CO из реформера).
Повышенные температуры, в особенности в среде, содержащей влагу и кислород, требуют химически, термически, термоокислительно и гидролитически стойких материалов.
В настоящее время, например, в области технологии топливных элементов, в основном используют перфторированные сульфированные полимеры (например, Nafion®), которые в целом обладают высокой химической, термической и термоокислительной устойчивостью, однако их дорого и затратно получать и утилизировать. Не требующей больших затрат альтернативой перфторированным полимерам являются мембранные материалы на основе сульфированных поли(ариленов), как, например, поли(ариленэфиркетоны), поли(ариленэфирсульфоны) и поли(арилентиоэфирсульфоны), которые в настоящее время испытывают для топливных элементов. (Общие сведения из уровня техники топливных элементов и мембранных материалов для них, а также для синтеза вышеназванных и других поли(ариленов) приведены в обзоре литературы.
Общим в структуре поли(ариленэфиркетонов), поли(ариленэфирсульфонов) и поли(арилентиоэфирсульфонов) является то, что к сульфированным ароматическим кольцам присоединена по меньшей мере одна электронодонорная мостичная группа (например, простая эфирная группа -O- или тиогруппа -S-). Так как гидролитическая устойчивость сульфокислотных групп в ароматическом кольце из-за электронодонорных заместителей (например, простой эфирной группы -O- или тиогруппы -S-) ухудшается, эти полимеры склонны к реакциям деструкции сульфокислотных групп при повышенных температурах. Кроме этого, в особенности эфирные мостики не достаточно устойчивы по отношению к кислородной атаке (например, пероксидные радикалы, тест Фентона (Fentons-Test)).
Поэтому задачей данного изобретения является создание новых гидролитически и термоокислительно устойчивых полимеров, которые в особенности предпочтительно могут использоваться в области технологий мембранных и топливных элементов и могут быть получены без особых затрат. Связанной с этим задачей является разработка нового способа получения таких полимеров.
Эти задачи согласно изобретению решаются путем получения сульфированных поли(ариленов) по пункту 1 формулы изобретения и способа получения этих поли(ариленов) по пунктам 22 и 24 формулы изобретения. Специальные и предпочтительные формы выполнения изобретения являются объектами зависимых пунктов.
Описание изобретения
Данное изобретение касается новых сульфированных поли(ариленов), характеризующихся структурным звеном -X-Ar(SO3M)n-Y-, где ароматическое кольцо, с которым связана сульфокислотная группа, замещено исключительно электроноакцепторными мостичными группами (сильно деактивирующими группами, например, сульфонной группой -SO2- или кетонной группой -CO-) X и Y, а также, в случае необходимости, другими не электронодонорными заместителями, а также их синтеза и применения.
По сравнению с ароматическими соединениями, замещенными электронодонорными группами (активирующими группами, например, сульфидной группой -S- или простой эфирной группой -O-) или электронодонорными и электроноакцепторными группами, гидролитическая устойчивость сульфокислоты в ароматическом соединении, замещенном электроноакцепторными группами, которое не имеет электронодонорных заместителей, должна быть значительно выше. Это следует из теоретических соображений о механизме гидролиза сульфированных ароматических соединений, или обратных реакций, электрофильного ароматического сульфирования. Эти реакции в общем обратимы, причем стадией, определяющей скорость, является образование σ-комплекса как промежуточной стадии электрофильного ароматического замещения. При повышенной температуре и высокой активности воды сульфокислотные группы относительно легко вновь отщепляются от ароматического соединения (инверсия сульфирования), что ограничивает пригодность сульфированных поли(ариленов) низкими температурами. Все заместители, которые дестабилизируют промежуточную стадию электрофильного ароматического замещения (σ-комплекс) как, например, деактивирующие электроноакцепторные заместители в орто- или параположении к сульфокислоте, затрудняют обратную реакцию (гидролиз) и тем самым стабилизируют сульфокислотную группу в ароматическом соединении. Однако, таким образом электрофильное сульфирование ароматических соединений, замещенных электроноакцепторами без дополнительных электронодонорных заместителей, также чрезвычайно затруднено или практически невозможно.
Решение этой проблемы достигается согласно изобретению с помощью способа, причем сначала получают сульфированный полимер, у которого ароматическое кольцо, замещенное одной сульфокислотной группой, имеет еще, по меньшей мере, один электронодонорный заместитель. Сначала присоединением химически превращают электронодонорный заместитель в электроноакцепторный заместитель. Это превращение может происходить, например, посредством окисления сульфидной группы -S- (электронодонор) до сульфоновой группы -SO2- (электроноакцептор).
Электроноакцепторными группами, которые здесь используют, являются оттягивающие электроны группы, которые как заместители понижают электронную плотность на ароматическом кольце (обозначаются также как деактивирующие группы). Оттягивающие электроны группы обладают -M и/или -I-эффектом.
Резонансный эффект (M-эффект, мезомерный эффект) в общем действует только когда группа связана непосредственно с ненасыщенной (например, ароматической) системой. Он действует через п-электроны, в противоположность эффекту поля (I-эффект, индуктивный эффект), который действует на систему через пространство, через молекулы растворителя или предпочтительно через σ-связи системы.
-M-эффект (отрицательный резонансный эффект): группа обладает -M-эффектом, если электронная плотность у этой группы больше, чем ожидаемая, и электронная плотность у ненасыщенной системы меньше, чем ожидаемая. Некоторыми, не ограничивающими примерами для мостичных групп с -M-эффектом являются -SO2-, -SO2O-, -CO-, -COO-, -CONH-, -CONR- и -POR-. Такие группы являются предпочтительными согласно изобретению.
Электронодонорными группами, которые здесь используют, соответственно являются группы, которые как заместители повышают электронную плотность на ароматическом кольце (обозначаются также как активирующие группы). Электронодонорные группы обладают +M и/или +I-эффектом. Примерами для таких мостичных групп являются простая эфирная группа -O- и сульфидная группа (тиоэфир) -S-.
Сульфированные поли(арилены) согласно изобретению содержат один или несколько структурных звеньев формулы -[X-Ar(SO3M)n-Y-]-, причем X и Y, одинаковые или отличающиеся друг от друга, соответственно обозначают электроноакцепторную группу, Ar представляет собой ароматическую или гетероароматическую циклическую систему предпочтительно с 5-18 атомами в кольце, M обозначает одновалентный катион, и n обозначает целое число от 1 до 4, и причем X, Y, Ar, M и n, независимо друг от друга, в различных структурных звеньях могут быть одинаковыми или разными.
Мостичные группы X и Y могут находиться в ароматическом кольце в пара-, мета- и ортоположении, причем параположение как правило предпочтительно. Пригодными, не ограничивающими примерами для электроноакцепторных мостичных групп X и Y являются -SO2-, -SO-, -SO2O-, -CO-, -COO-, -CONH-, -CONR- и -POR-, причем -SO2- и -CO- являются предпочтительными, и -SO2- является наиболее предпочтительной.
Специальными, не ограничивающими примерами для пригодных ароматических или гетероароматических циклических систем являются фенилен, нафтилен, антрацен, фенантрен, бифенилен, фуран, тиофен, пиррол, тиазол, триазол, пиридин, имидазол и бензимидазол.
Ароматические или гетероароматические кольца могут быть замещены одной - четырьмя сульфокислотными группировками -SO3M, т.е. в вышеприведенной формуле n=1-4, причем для Ar=фенилен n предпочтительно равно 1 или 2. Противоион M сульфонатной группы является или протоном, т.е. имеет место сульфокислота, или обычным одновалентным катионом. Типичными примерами таких катионов являются ионы металлов как Li+, Na+, K+, а также NR4 +, PR4 +, причем R обозначает органический остаток, предпочтительно алкил.
Ароматические или гетероароматические кольца кроме сульфокислотных групп и мостичных заместителей X и Y могут содержать еще другие не электронодонорные заместители. Некоторыми специальными, не ограничивающими примерами таких заместителей являются галогены, например, F, Cl, Br, или незамещенные или замещенные алкильные группы, например, -CH3 или -CF3.
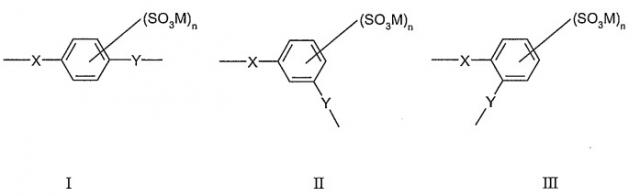
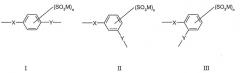
В одной предпочтительной форме выполнения Ar обозначает фенилен, и сульфированный поли(арилен) содержит один или несколько следующих структурных звеньев I, II или III
где X и Y определены, как указано выше, являются одинаковыми или разными.
В типичной форме выполнения структурное звено или звенья общей формулы -X-Ar(SO3M)n-Y- образован(ы) повторяющимися звеньями формул -[-Ar1(SO3M)n-X-]- или -[-Ar2(SO3M)n-Y-]-, причем X и Y, одинаковые или отличающиеся друг от друга, соответственно обозначают электроноакцепторные группы, Ar1 и Ar2, одинаковые или отличающиеся друг от друга, представляют собой выше определенную ароматическую или гетероароматическую циклическую систему Ar предпочтительно с 5-18 атомами в кольце, M обозначает одновалентный катион, как определено выше, и n обозначает целое число от 1 до 4, и причем X, Y, Ar1, Ar2, M и n, независимо друг от друга, в различных структурных звеньях могут быть одинаковыми или разными, и причем сульфированные ароматические или гетероароматические циклические системы Ar1(SO3M)n или Ar2(SO3M)n не замещены электронодонорными группами. Звенья -[-Ar1(SO3M)n-X-]- или -[-Ar2(SO3M)n-Y-]- могут быть одинаковыми или различаться типом ароматического кольца и/или степенью замещения и/или положениями заместителей.
В специальной форме выполнения данного изобретения сульфированный поли(арилен) содержит только повторяющиеся звенья формул -[-Ar1(SO3M)n-X-]- или -[-Ar2(SO3M)n-Y-]-. В особенном случае сульфированный поли(арилен) содержит только одно или несколько вышеуказанных структурных звеньев I, II или III.
Особенно предпочтительно сульфированные поли(арилены) обозначают сульфированные поли(ариленсульфоны), в особенности поли(сульфокислота-фениленсульфоны) и их сополимеры. Другими не ограничивающими примерами сульфированных поли(ариленов) согласно изобретению являются поли(сульфокислота-фениленэфиркетоны), поли(сульфокислота-фениленсульфонкетоны) и их сополимеры.
Однако данное изобретение включает также такие сополимерные поли(арилены), которые кроме звеньев, образующих структурное звено или звенья общей формулы -X-Ar(SO3M)n-Y-, содержат одно или несколько звеньев формулы -[Ar3-Z-]-, причем Z может быть электронодонорной или электроноакцепторной группой, или ни одной из них, Ar3 представляет собой ароматическую или гетероароматическую циклическую систему предпочтительно с 5-18 атомами в кольце без SO3M-заместителей, и группы Ar3 и Z в различных звеньях -[Ar3-Z-]- могут быть одинаковыми или разными, с оговоркой, что группа Z только тогда может быть связана с сульфированной ароматической или гетероароматической циклической системой формулы Ar(SO3M)n, если Z не является электронодонором.
Некоторыми пригодными, не ограничивающими примерами мостичных групп Z являются -SO2-, -SO-, -SO2O-, -CO-, -COO-, -CONH-, -CONR- и -POR-, -S-, -O- и алкилен. Другие пригодные группы для специалиста в области полимерной химии являются очевидными.
Специальными, не ограничивающими примерами для пригодных ароматических или гетероароматических циклических систем Ar3 являются фенилен, нафтилен, антрацен, фенантрен, бифенилен, фуран, тиофен, пиррол, тиазол, триазол, пиридин, имидазол, бензимидазол и т.д. Эти циклические системы помимо мостичных заместителей при желании могут содержать и другие заместители.
Также объектами данного изобретения являются сополимеры, которые кроме повторяющихся звеньев сульфированного поли(арилена), как описано выше, содержат еще (предпочтительно повторяющиеся) звенья, по меньшей мере, одного другого мономера или макромономера.
В качестве другого мономера или макромономера в принципе пригодно каждое соединение, которое способно сополимеризоваться с арильными мономерами, используемыми согласно изобретению. Обычно при этом речь идет о α,ω-дигидрокси-соединении или о α,ω-дигалогензамещенном соединении. Предпочтительно α,ω-дигидрокси-соединение характеризуется формулой HO-W-OH, и α,ω-дигалогензамещенное соединение - формулой Hal-W-Hal, причем W выбрано из группы, состоящей из -(CH2)n-, -(CF2)n-, -(CF2CH2)n-, -(CH2-CH2-O)n-CH2-CH2-, -(CH(CH)3-CH2-O)n-CH(CH3)-CH2-, -(CF2-CF2-O)n-CF2-CF2-, полиариленэфирсульфонов, полиариленэфиркетонов, полисилоксанов (например, -(SiR2-O)n-). Hal в дигалогензамещенном соединении обозначает галогенный остаток, например, F, Cl, Br и I.
Чистые сульфированные поли(арилены) согласно изобретению или сополимеры могут быть также смешаны с одним или несколькими обычными полимерами известным образом, чтобы получить полимерную смесь, которая соединяет в себе благоприятные свойства своих отдельных компонентов. Например, согласно изобретению могут быть смешаны полимеры на основе сульфированного поли(арилена) с «пластифицирующими компонентами», чтобы придать полученной в результате полимерной смеси большую гибкость и/или пластичность. Пригодные полимеры известны специалисту и могут быть, например, выбраны из группы: PBI (полибензимидазол), PTFE (политетрафторэтилен), PVDF (поливинилиденфторид), PSU (полисульфоны), PES (полиэфирсульфоны), PEK (полиэфиркетоны), PPO (полифениленоксиды), PPS (полифениленсульфиды), PA (полиимиды), PC (поликарбонаты), PMMA (полиметилметакрилаты), полифосфазены.
В специальной форме выполнения согласно изобретению чистые сульфированные поли(арилены) или сополимеры, или полимерные смеси могут быть заделаны в инертную пористую матрицу, например, органическую (пористый PE (ПЭ), PP (ПП), PVDF (ПВДФ), PTFE (ПТФЭ) и др.) или неорганическую матрицу (пористый нитрид бора, диоксид кремния и др.).
В следующей форме выполнения согласно изобретению чистые сульфированные поли(арилены) или сополимеры, или полимерные смеси могут быть усилены волокнистыми материалами, например, стекловолокном, керамическими волокнами, текстильными волокнами, углеволокном, микропористым полипропиленом или политетрафторэтиленом и т.д.
Кроме этого согласно изобретению чистые сульфированные поли(арилены) или сополимеры, или вышеназванные полимерные смеси могут быть комбинированы с активными или неактивными наполнителями, включая, однако не ограничиваясь этим, частицы TiO2, ZrO2 или SiO2, фосфат и фосфонат циркония, вольфрамовую или молибденовую кислоту и т.д., чтобы образовать соответствующий композитный материал. Также возможна комбинация с другими традиционными добавками без другого.
Сульфированные поли(арилены) согласно изобретению имеют молекулярный вес в области от 2000 до 2000000, обычно в области от 2000 до 1000000, наиболее часто в области от 10000 до 1000000, предпочтительнее в области от 2000 до 200000, еще предпочтительнее в области от 10000 до 100000.
Синтез сульфированных поли(ариленов) согласно изобретению осуществляют путем многостадийной реакции, причем сначала получают сульфированный полимер, имеющий еще, по меньшей мере, один электронодонорный заместитель в сульфированном ароматическом кольце, который затем переводят в электроноакцепторный заместитель.
В специальной форме выполнения на первой стадии уже существующий, электронодонорно замещенный полиарилен, полученный традиционным способом или коммерчески доступный, сульфируют самим по себе известным способом, например, превращением с SO3 и/или H2SO4 (смотри пример 11).
Однако чаще получение сульфированного полимера включает поликонденсацию уже сульфированных мономеров. Таким образом состав и свойства получаемого в результате сульфированного полимера могут устанавливаться по желанию.
В целом такой способ получения включает стадии:
а) получение сульфированного арильного мономера F1-AS-F2, причем AS обозначает арильную систему из одного или нескольких ароматических колец, причем, по меньшей мере, одно ароматическое кольцо замещено сульфокислотной группой, и арильная система которого характеризуется функциональными группами F1 и F2, которые могут быть одинаковыми или разными и могут вступать в реакцию конденсации, или несколько таких различных арильных мономеров;
b) поликонденсация сульфированного арильного мономера или сульфированных арильных мономеров из стадии a) с образованием сульфированного поли(арилена), который содержит, по меньшей мере, один электронодонорный заместитель в сульфированном ароматическом кольце;
с) перевод, по меньшей мере, одного электронодонорного заместителя в электроноакцепторный заместитель с образованием сульфированного поли(арилена), который характеризуется только электроноакцепторными заместителями в сульфированном ароматическом кольце.
При одном варианте этого способа в поликонденсации, кроме одного или нескольких сульфированных арильных мономеров F1-AS-F2, как определено выше, участвуют еще один или несколько арильных мономеров F1-ANS-F2, причем ANS обозначает арильную систему из одного или нескольких ароматических колец, которые не замещены сульфокислотной группой, и арильная система которого характеризуется функциональными группами F1 и F2, как определено выше, которые могут быть одинаковыми или разными. При этом образуется частично сульфированный поли(арилен), характеризующийся по меньшей мере одним электронодонорным заместителем в сульфированном ароматическом кольце, и у которого по меньшей мере один электронодонорный заместитель затем переводят в электроноакцепторный заместитель, причем образуется частично сульфированный поли(арилен), характеризующийся исключительно электроноакцепторными заместителями в сульфированном ароматическом кольце.
Специальная форма выполнения включает получение сульфированного поли(ариленсульфона) следующими стадиями:
a) получение сульфированного арильного мономера F1-AS-F2, характеризующегося функциональными группами F1 и F2, которые могут быть одинаковыми или разными и могут вступать в реакцию конденсации с сульфидными группировками, или нескольких таких различных арильных мономеров, как определено выше;
b) поликонденсация сульфированного арильного мономера или сульфированных арильных мономеров из стадии a) с арилдисульфидом или сульфидом щелочного металла с образованием сульфированного поли(ариленсульфидсульфона);
c) окисление сульфированного поли(ариленсульфидсульфона) со стадии b) до сульфированного поли(ариленсульфона).
Предпочтительно функциональные группы F1 и F2 арильного мономера, одинаковые или разные, опять выбраны из группы, включающей фтор, хлор, бром или иод.
В форме выполнения способа согласно изобретению сульфированные арильные мономеры характеризуются структурной формулой F1-Ar1-SO2-Ar2-F2, т.е. AS = Ar1-SO2-Ar2-, причем Ar1 и Ar2 могут быть одинаковыми или разными и соответственно представляют собой ароматичекую или гетероароматическую циклическую систему с 5-18 атомами в кольце, с оговоркой, что у, по меньшей мере, одного используемого арильного мономера Ar1 и/или Ar2 замещен (или замещены), по меньшей мере, одной группой SO3M, причем M определен, как описано выше.
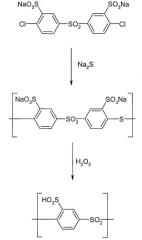
На следующей схеме реакции I показаны принципиальные стадии способа согласно изобретению на конкретном, не ограничивающем примере получения гомополимера поли(сульфокислота-1,4-фениленсульфона) (детальное описание в примерах 1 и 2).
Схема реакции I
Как уже указывалось выше, в этом способе может быть использован только один арильный мономер, так что образуется гомополимер поли(ариленсульфон), или могут быть получены два или более различных арильных сомономера и подвергнуты сополиконденсации и последующему окислению. Вследствие этого специальная форма выполнения способа предполагает, что, по меньшей мере, у одного арильного сомономера остатки Ar1 и/или Ar2 замещены группой SO3M, причем M определен, как описано выше, и, по меньшей мере, у одного другого арильного мономера остатки Ar1 и/или Ar2 не замещены группой SO3M.
Предпочтительно функциональные группы F1 и F2 арильного мономера, одинаковые или разные, опять выбраны из группы, включающей фтор, хлор, бром или иод.
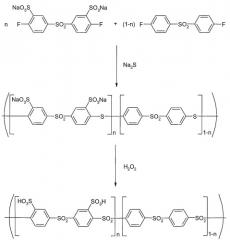
На следующей схеме реакции II показаны принципиальные стадии получения сополимера сульфированного поли(ариленсульфона) при использовании исходных мономеров: динатрий-3,3'-дисульфонат-4,4'-дифтордифенилсульфона и 4,4'-дифтордифенилсульфона (пример 3). С помощью запланированного соотношения обоих исходных мономеров может регулироваться состав конечного полимера. В указанной схеме реакции II и в схемах примеров 3-10 продукт реакции поликонденсации для обзорности представлен в качестве блок-сополимера обоих различных исходных мономеров. Однако данное изобретение включает равным образом или даже предпочтительнее также соответствующие статистические сополимеры, которые могут быть получены способом, описанным в примере 3. Другие статистические или блок-сополимеры достаточно легко могут быть получены аналогичным образом (смотри примеры 4-10).
Предпочтительными растворителями для реакций полимеризации или сополимеризации являются апротонные, полярные, высококипящие растворители, как 1-метил-2-пирролидон (NMP) (НМП), диметилсульфоксид (DMSO)(ДМСО), диметилформамид (DMF) (ДМФ), диметилацетамид (DMAc) (ДМАц), сульфолан, дифенилсульфон, 1,3-диметил-2-имидазолидинон.
Типичным образом температура реакции составляет 100-250°С, предпочтительно 140-200°С.
Реакция с сульфидами щелочных металлов (например, сульфидом натрия), как правило, происходит в присутствии добавок карбоксилатов щелочных металлов (например, ацетата натрия, ацетата лития), карбонатов щелочных металлов (например, карбоната лития), сульфонатов щелочных металлов, бората лития, хлорида лития.
Сульфид щелочного металла (например, сульфид натрия) также может быть использован в качестве гидрата (например, Na2S·9H2O).
Схема реакции II
Такого рода сополимеры различного состава также характеризуются различной ионообменной емкостью. Вышеописанный способ дает возможность посредством пригодного проведения реакции при использовании определенных исходных мономеров и определенных соотношений мономеров целенаправленно получать сополимеры с регулируемой разнообразной ионообменной емкостью (ИОЕ) (IES = ion exchange capacity [мэкв/г], (ЕВ = эквивалентный вес; EW = equivalent weight [г/экв]).
Для образцов сополимеров, получаемых согласно или аналогично вышеуказанной схеме, в соответствующих примерах приведены расчетные формулы. Для других сополимеров согласно изобретению соответствующие формулы без труда могут быть определены эмпирически.
При использовании новых мембранных материалов в каждом случае можно ожидать значительно более высокой гидролитической, а также термоокислительной устойчивости.
Характеристика сульфированных поли(ариленсульфонов) согласно изобретению может осуществляться различными способами, например, посредством элементного анализа, ЯМР, растворимости, ГПХ, MALDI-TOF (хромато-масс-спектрометрия с лазерным детектором), ДСК, рентгена, ИОЕ с помощью титрования, плотности, ИК, набухания в воде и метаноле, водно-абсорбционной изотермии, исследований водной диффузии и электроосмоса, измерений проводимости в особенности при повышенных температурах при увлажнении, исследований водопоглощения и гидролитической устойчивости (ТГА при 1 атм водяного пара) и термоокислительной устойчивости (ТГА в атмосфере кислорода, например 80% N2 и 20% O2). Некоторые результаты последних исследований приведены на фиг. 1-4. Следующие результаты исследований, при которых подробно изучали свойства полимеров согласно изобретению и с которыми сравнивали известные из литературы сульфированные поли(ариленэфирсульфоны) и сульфированные поли(ариленсульфидсульфоны), приведены на фиг. 5-11.
Краткое описание фигур
Фиг.1 изображает протонную проводимость свыше 100°С поли(сульфокислота-1,4-фениленсульфон)а по сравнению с Nafion 117, измеренную в атмосфере водяного пара (p(H2O)=105 Па).
Фиг.2А изображает водопоглощение Nafion 117 в атмосфере водяного пара (p(H2O)=105 Па).
Фиг.2B изображает водопоглощение поли(сульфокислота-1,4-фениленсульфон)а в атмосфере водяного пара (p(H2O)=105 Па).
Фиг.3А изображает водопоглощение сульфированного поли(1,4-фениленсульфон-1,4-фениленсульфид-1,3-фениленсульфид)а в атмосфере водяного пара (p(H2O)=105 Па).
Фиг.3B изображает водопоглощение сульфированного поли(1,4-фениленсульфон-1,4-фениленсульфид)а в атмосфере водяного пара (p(H2O)=105 Па).
Фиг.4 показывает более высокую термоокислительную устойчивость сульфированного поли(ариленсульфона) (S-PS 220) в сравнении с соответствующим сульфированным поли(ариленсульфидсульфоном) посредством термогравиметрических измерений в кислородсодержащей атмосфере (20% O2 и 80% N2).
Фиг.5A показывает более высокую термоокислительную устойчивость сульфированного поли(ариленсульфона) (sPS-430, n=0,8, пример 4) в сравнении с сульфированным поли(ариленсульфидсульфоном) (sPSS-312, n=1,0, пример 4) посредством термогравиметрических измерений в кислородсодержащей атмосфере (20% O2 и 80% N2, скорость нагрева 2 К/мин). Также представлена чисто термическая устойчивость sPS-430 а атмосфере азота.
Фиг.5B показывает, что в кислородсодержащей атмосфере у сульфированного поли(ариленсульфидсульфона) спонтанное превращение (окисление) сульфидных групп -S- до сульфогрупп -SO2- при образовании сульфированного поли(ариленсульфона) не имеет места.
Фиг.6A показывает температурную зависимость водопоглощения и десорбции воды Nafion® 117 в атмосфере водяного пара (p(H2O)=105 Па, скорость нагрева и охлаждения 12°С/час).
Фиг.6B показывает температурную зависимость водопоглощения и десорбции воды сульфированного поли(ариленсульфона) (sPS-220, n=1,0, пример 2) в атмосфере водяного пара (p(H2O)=105 Па, скорость нагрева и охлаждения 12°С/час). Обратимое изменение веса вследствие десорбции воды и водопоглощения во время фаз нагревания и охлаждения доказывает высокую гидролитическую устойчивость сульфокислотных групп.
Фиг.6C показывает температурную зависимость водопоглощения и десорбции воды сульфированного поли(ариленсульфона) (sPS-360, n=1,0, пример 4) в атмосфере водяного пара (p(H2O)=105 Па, скорость нагрева и охлаждения 12°С/час). Обратимое изменение веса вследствие десорбции воды и водопоглощения во время фаз нагревания и охлаждения доказывает высокую гидролитическую устойчивость сульфокислотных групп.
Фиг.6D показывает температурную зависимость водопоглощения и десорбции воды сульфированного поли(ариленсульфона) (sPS-430, n=0,8, пример 4) в атмосфере водяного пара (p(H2O)=105 Па, скорость нагрева и охлаждения 12°С/час). Обратимое изменение веса вследствие десорбции воды и водопоглощения во время фаз нагревания и охлаждения доказывает высокую гидролитическую устойчивость сульфокислотных групп.
Фиг.6E показывает температурную зависимость водопоглощения и десорбции воды сульфированного поли(ариленсульфона) (sPS-336, n=1,0, пример 6) в атмосфере водяного пара (p(H2O)=105 Па, скорость нагрева и охлаждения 12°С/час). Обратимое изменение веса вследствие десорбции воды и водопоглощения во время фаз нагревания и охлаждения доказывает высокую гидролитическую устойчивость сульфокислотных групп.
Фиг.6F показывает температурную зависимость водопоглощения и десорбции воды сульфированного поли(ариленэфир-эфир-кетона) (sPEEK-500, ИОЕ (IEC)=2,0 ммоль/г) в атмосфере водяного пара (p(H2O)=105 Па, скорость нагрева и охлаждения 12°С/час). Необратимое изменение веса доказывает гидролитическое разложение сульфокислоты в ароматическом соединении.
Фиг.6G показывает температурную зависимость водопоглощения и десорбции воды сульфированного поли(ариленсульфидсульфона) (sPSS-204, n=1,0, пример 2) в атмосфере водяного пара (p(H2O)=105 Па, скорость нагрева и охлаждения 12°С/час). Необратимое изменение веса доказывает гидролитическое разложение сульфокислоты в ароматическом соединении.
Фиг.6H показывает температурную зависимость водопоглощения и десорбции воды сульфированного поли(ариленсульфидсульфона) (sPSS-312, n=1,0, пример 4) в атмосфере водяного пара (p(H2O)=105 Па, скорость нагрева и охлаждения 12°С/час). Необратимое изменение веса доказывает гидролитическое разложение сульфокислоты в ароматическом соединении.
Фиг.6I показывает температурную зависимость водопоглощения и десорбции воды сульфированного поли(ариленсульфидсульфона) (sPSS-258, n=1,0, пример 5) в атмосфере водяного пара (p(H2O)=105 Па, скорость нагрева и охлаждения 12°С/час). Необратимое изменение веса доказывает гидролитическое разложение сульфокислоты в ароматическом соединении.
Фиг.6J показывает температурную зависимость водопоглощения и десорбции воды сульфированного поли(ариленсульфидсульфона) (sPSS-304, n=1,0, пример 6) в атмосфере водяного пара (p(H2O)=105 Па, скорость нагрева и охлаждения 12°С/час). Необратимое изменение веса доказывает гидролитическое разложение сульфокислоты в ароматическом соединении.
Фиг.7 показывает 13С-ЯМР-спектр образца сульфированного поли(ариленсульфидсульфона) (sPSS-304, n=1,0, пример 6) перед и после ТГА в атмосфере водяного пара (p(H2O)=105 Па). Спектры доказывают количественное отщепление сульфокислотных групп от ароматического соединения.
Фиг.8 показывает температурную зависимость водопоглощения в жидкой воде сульфированного поли(ариленсульфона) (sPS-430, n=0,8, пример 4) по сравнению с Nafion® 117, сульфированного поли(ариленэфир-эфир-кетона) (sPEEK, ИОЕ=1,35 ммоль/г) и известного из литературы сульфированного поли(ариленсульфидсульфона) (sPSS-661, n=0,4, ИОЕ=1,51 ммоль/г).
Фиг.9 показывает зависимость от температуры и набухания протонной проводимости сульфированного поли(ариленсульфона) (sPS-430, n=0,8, пример 4), измеренную с помощью импеданс-спектроскопии.
Фиг.10 показывает температурную зависимость протонной проводимости двух сульфированных поли(ариленсульфонов) (sPS-220, n=1,0, пример 2 и sPS-430, n=0,8, пример 4) по сравнению с Nafion® 117 и сульфированным поли(ариленэфир-эфир-кетоном) sPEEK, измеренную в атмосфере водяного пара (p(H2O)=105 Па) с помощью импеданс-спектроскопии.
Фиг.11 показывает зависимость от температуры и мольной доли набухания сульфированного поли(ариленсульфона) (sPS-430, n=0,8, пример 4) в смеси вода/метанол по сравнению с Nafion® 117.
В исследованиях характеристик, результаты которых представлены на фиг. 1-4, определяли проводимость в атмосфере водяного пара (p(H2O)=105 Па) с помощью импеданс-спектроскопии, водопоглощение полимеров в атмосфере водяного пара (p(H2O)=105 Па) посредством ТГА (термогравиметрического анализа) и термоокислительную устойчивость посредством ТГА в кислородсодержащей атмосфере.
Путем циклических измерений между Т=105 и 180°С в атмосфере водяного пара (p(H2O)=105 Па, скорость нагрева и охлаждения 12°С/час) можно оценить гидролитическую устойчивость сульфокислотных групп в ароматическом соединении. Обратимое изменение веса вследствие десорбции и поглощения воды во время фаз нагревания и охлаждения указывает на высокую устойчивость сульфокислотных групп в исследованной области температур, в то время как необратимое изменение веса указывает на гидролитическое разложение ароматической сульфокислоты. Так как при гидролизе в качестве продукта реакции образуется серная кислота, и она является более гигроскопичной, чем соответствующая сульфокислота, во время разложения наблюдают возрастание водопоглощения. Сульфированные поли(ариленсульфоны) (фиг.2А) и Nafion (фиг.2B) в этих условиях являются стабильными, в то время как соответствующие сульфированные поли(ариленсульфидсульфоны) характеризуются реакциями разложения (фиг. 3А и 3B).
Чтобы показать отчетливое различие между сульфированными поли(ариленсульфонами) sPS, описанными в этом изобретении, от известных из литературы сульфированных поли(ариленэфирсульфонов) и сульфированных поли(ариленсульфидсульфонов) sPSS [реф.: 1-6], получали несколько этих указанных полимеров, подробно исследовали их свойства и сравнивали со свойствами полимеров согласно изобретению.
Структурное звено сульфированного поли(ариленсульфона) sPS согласно изобретению:
Структурное звено сульфированного поли(ариленэфирсульфона) или поли(ариленсульфидсульфона) sPSS:
Другим общеупотребительным обозначением для поли(ариленсульфидсульфона) является поли(арилентиоэфирсульфон).
Кроме различного молекулярного строения между сульфированными поли(ариленэфирсульфонами) или сульфированными поли(ариленсульфидсульфонами) и чистыми сульфированными поли(ариленсульфонами) наблюдают отчетливые различия в термической, термоокислительной и гидролитической устойчивости, а также в растворимости, набухаемости и проводимости этих полимеров, причем возможно явное разграничение.
Для термического или термоокислительного сравнения устойчивости сульфированных поли(ариленсульфонов) и сравнительных полимеров был проведен термогравиметрический анализ (ТГА при 2 К/мин) в атмосфере азота или кислородсодержащей атмосфере (20% O2 и 80% N2 или чистая атмосфера O2). Эти измерения показали отчетливо более высокую область стабильности для сульфированных поли(ариленсульфонов) sPS по сравнению с сульфированными поли(ариленсульфидсульфонами) sPSS. Как представлено на изображении фиг.5А, реакция разложения (вероятно, отщепление сульфокислотной группы от ароматического кольца) у сульфированных поли(ариленсульфидсульфонов) sPSS начинается уже ниже 250°С, в то время как эта реакция у сульфированных поли(ариленсульфонов) sPS со сравнимой обменной емкостью начинается только выше 300°С. На фиг.5А приведены примеры ТГА сульфированного поли(ариленсульфона) sPS-430 (пример 4, n=0,8) и сульфированного поли(ариленсульфидсульфона) sPSS-312, (пример 4, n=0,8) в кислородсодержащей атмосфере. Чисто термическая устойчивость sPS-430 (пример 4, n=0,8) в атмосфере азота сравнима с термоокислительной устойчивостью или незначительно выше, как и представлено на фиг.5А.
В особенности сравнение измерений в инертной атмосфере (азот) и в кислородсодержащей атмосфере сульфированного поли(ариленсульфидсульфона) sPSS (смотри фиг.5B) показывает, что превращение (окисление) сульфидной группы до сульфоновой группы -SO2- с образованием чисто сульфированного поли(ариле