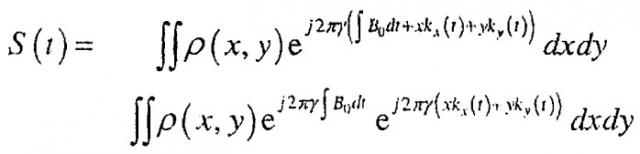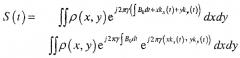Оценивание структуры с использованием пространственно-частотного анализа
Иллюстрации
Показать всеИзобретение относится к способу получения пространственно-частотных спектров для конкретных мест в 3D образце с использованием модификаций современных техник МРТ для локализованной спектроскопии ЯМР. Новым является дополнительное применение градиента считывания к последовательностям импульсов, используемым в современной спектроскопии ЯМР, и регистрация результирующего отраженного сигнала, что позволяет формировать спектры из выбранной области или формировать изображение результатов в области образца. Способы можно применять для анализа структуры трабекулярной кости, а также для анализа или диагностики заболевания в случаях наличия различий в пространственно-частотном спектре мощности вследствие физиологических или болезненных процессов. Раскрыты различные варианты осуществления. Технический результат - оценивание одномерного распределения пространственных частот внутри образца, не требуя получения всех данных, необходимых для создания изображения. 2 н. и 17 з.п. ф-лы, 19 ил.
Реферат
Перекрестная ссылка на родственную заявку
Данная заявка испрашивает приоритет по предварительной патентной заявке США №60/597349, поданной 27 ноября 2005 г., а также приоритет по предварительной патентной заявке США №60/743779, поданной 25 марта 2006 г.
Область техники, к которой относится изобретение
Настоящее изобретение относится к области диагностической оценки сложных биологических и физических структур, в том числе прочности кости у пациентов с подозрением на остеопороз и находящихся в других условиях, которые ухудшают трабекулярную структуру губчатого вещества костей. Дополнительные структуры включают в себя оценивание кровеносной сети в опухолях и распределение пористых углеводородных коллекторов в толще пластов.
Уровень техники
Трабекулярная архитектура наиболее чувствительна к метаболическим изменениям в кости (относительно более плотной внешней оболочки кортикального слоя кости) и является основным фактором общей прочности кости. Поэтому она является подходящим заменяющим показателем для наблюдения заболевания и лечения.
Влияние костных заболеваний. Заболевания скелетной системы, включая остеопороз и другие менее распространенные условия, являются главной угрозой здоровью пожилых людей, особенно женщин. Значимость костных заболеваний явствует из доклада на «2004 Surgeon General» под названием "Состояние здоровья кости и остеопороз" и из объявления 2002-2011 годов десятилетием костей и суставов. Более 10 миллионов американцев старше 50 лет страдают остеопорозом (ослаблением скелетной системы вследствие потери костной массы), и еще 34 миллиона находятся под угрозой. Более 1,5 миллиона переломов происходит ежегодно в результате остеопороза с прямыми затратами на уход примерно 15 миллиардов долларов, и дополнительно затрачиваются еще миллиарды долларов в связи с потерей трудоспособности и трехкратным повышением риска смертности, связанным с переломами. Продолжающееся старение населения приводит к тому, что количество переломов и связанный с этим удар по экономике и социальной сфере более чем удвоится к 2020 г., причем, по меньшей мере, 50% населения в возрасте свыше 50 лет будет страдать остеопорозом или находиться под угрозой.
Диагностика и лечение остеопороза. Цикл образования кости имеет ряд стадий, причем наиболее быстрый рост костей происходит в первые двадцать лет жизни, после чего постепенно замедляется. В среднем возрасте и, в особенности, у женщин постклимактерического возраста выработка ячеистой костной ткани может становиться отрицательной, и трабекулярная кость, структура стержней и пластин, которая поддерживает внешнюю оболочку трубчатой кости, становится тоньше и слабее. Эта деградация проиллюстрирована путем сравнения фиг.1 и 2, где показаны вырезанные участки соответственно здоровой кости и остеопорозной кости. Обызвествленная кость выглядит яркой на этих изображениях, и области, которые были бы заполнены костным мозгом в живой ткани выглядят темными. Потеря прочности кости, обусловленная утончением и увеличением пористости костной структуры в остеопорозной кости, повышает опасность перелома в уязвимых местах, например тазе и позвоночнике. Хотя большинство переломов происходит в тазе и позвоночнике, их изображение получать труднее, чем для пяточной кости и дистального отдела лучевой кости. Поскольку остеопороз является системным метаболическим заболеванием, и кости, несущие весовую нагрузку, являются хорошими индикаторами состояния заболевания, изображения любой из этих костей указывает развитие заболевания в скелетной системе пациента в целом. Пяточная кость особенно полезна для оценивания трабекулярной архитектуры, поскольку она является костью, несущей весовую нагрузку, и сравнительно доступна для формирования изображений с использованием МРТ (магнитно-резонансного томографа или магнитно-резонансной томографии).
Остеопороз не является неизбежным следствием старения. Здоровый образ жизни, подразумевающий отказ от курения, умеренную физическую нагрузку и прием адекватных доз кальция и витамина D, может снизить потерю кости и риск перелома. Также существует несколько лекарств для лечения остеопороза. Бисфосфонаты, в том числе Fosamax™ и Actonel™, являются оральными агентами, которые снижают рассасывание кости. Терипаратид, продаваемый под названием Forteo™, представляет собой экстракт анаболического гормона, который стимулирует рост кости, но подлежит приему с ежедневным наблюдением. Другие формы гормональной терапии также стимулируют развитие кости, но сопряжены со значительным риском побочных эффектов, о чем свидетельствуют клинические испытания.
Для правильного лечения требуется своевременный и точный диагноз. Современный стандарт диагностики остеопороза предусматривает измерение плотности костного минерала (BMD) путем абсорбциометрии рентгеновскими лучами двух уровней энергии (DEXA). Последние исследования в США показали, что DEXA используется недостаточно эффективно, поскольку менее 25% населения, относящегося к группе риска, проходит тестирование на BMD, отчасти ввиду стоимости DEXA, но, в основном, из-за неосведомленности. Гораздо большее значение имеет тот факт, что врачи начали сомневаться в клинической значимости DEXA исходя из практических наблюдений, говорящих о том, что измерения DEXA не позволяют правильно прогнозировать угрозу перелома, и особенно не адекватны при оценивании эффективности лечения.
В итоге, в качестве альтернатив DEXA, исследуется ряд других способов построения изображений, в том числе количественная компьютерная томография, ультразвуковые исследования и магнитно-резонансная томография. Устойчивость кости к перелому зависит, как и для большинства материалов, не просто от плотности, но также от структуры кости, включающей в себя относительное содержание, толщину, ориентацию трабекулярных стержней и пластин. МРТ, которая, по природе своей, является трехмерной техникой, весьма пригодна для определения структурных деталей, определяющих устойчивость к перелому.
Техники МРТ, применяемые в настоящее время для диагностики остеопороза, требуют получения изображений чрезвычайно высокого разрешения, а также требуют ряда операций по обработке изображений. На фиг.3 показано МР-изображение, полученное от иссеченного образца кости с использованием устройства МРТ с напряженностью поля в 7 тесла. На фиг.3, как и в живой ткани, МР-изображения имеют высокий сигнал в костном мозге и низкий сигнал от плотной обызвествленной кости. Изображения живой кости можно получить в системе МРТ сильного поля с использованием особых катушек и продолжительного времени исследования. Требуется также тщательное позиционирование и стабилизация пациента. Эти системы сильного поля стоят около 2 миллионов долларов и должны размещаться в строго контролируемых условиях и обслуживаться специалистами по радиологии. Заявленное здесь изобретение предусматривает устройства, которые можно устанавливать в кабинете обычного врача и которые стоят менее 200000 долларов.
Магнитный резонанс (МР) в ряде случаев особенно пригоден для измерения живой кости, поскольку твердая кость (т.е. обызвествленная структура трабекул и трубчатая кость) дает очень слабый сигнал, тогда как костный мозг (который заполняет пустоты в трабекулярной решетке) дает сильные сигналы, тем самым обеспечивая высокую контрастность и высокое отношение сигнал-шум. Однако высокая стоимость систем сильного поля и необходимость в длительном времени съемки для разрешения тонких структур в сочетании с требованием, чтобы пациент (обследуемая часть тела) не двигался(ась) при съемке, затрудняют практическую реализацию стандартной МРТ для этой цели.
МРТ основана на применении математического аппарата разложения в ряд Фурье, согласно которому одномерную повторяющуюся форму сигнала (например, амплитуду сигнала как функцию времени или интенсивность как функцию линейной позиции) можно представить в виде ряда синусоидальных сигналов уменьшающегося периода (повышающейся частоты) с соответствующими коэффициентами (значениями k).
В МРТ, предмет (часть тела), изображение которого нужно построить, является трехмерным объектом. Основную концепцию значений k в одном измерении можно распространить на два или три измерения. При этом, вместо последовательности значений k, рассматривается двух- или трехмерная матрица значений k, причем каждое значение k представляет конкретную пространственную частоту и направление в образце.
В Фурье-анализе преобразование значений k в нужную форму сигнала (зависимость амплитуды от времени для сигнала, изменяющегося со временем или зависимость интенсивности изображения от позиции для случая МРТ) осуществляется с использованием преобразования Фурье. Преобразование Фурье, в общих чертах, является хорошо известным средством преобразования между частотным измерением и временным измерением (для сигналов, изменяющихся со временем). Для изображений, как в случае МРТ, преобразование Фурье используется для преобразования между пространственно-частотым измерением (рядом синусоидальных сигналов и их коэффициентов, именуемым k-пространством) и пространственным распределением интенсивности сигнала для каждой ячейки формируемого изображения (для каждого вокселя). Аналогично случаю сигналов, изменяющихся со временем, где значения k являются коэффициентами для синусоидальных сигналов с заданными периодами, значения k в случае МРТ являются коэффициентами для синусоидальных сигналов с заданными длинами волны (где длины волны обратно пропорциональны пространственным частотам, т.е. большая длина волны соответствует малой пространственной частоте).
Современная технология МРТ использует ряд способов получения изображений. В принципе, все они основаны на сборе коэффициентов k-пространства, которые подвергаются преобразованию Фурье с получением изображения (или набора изображений, как в 3D-съемке). В простейшей абстракции это осуществляется путем помещения изображаемой части в сильное магнитное поле и возбуждения ядер водорода в образце путем передачи на образец импульсного электромагнитного сигнала радиочастоты, настроенной на резонансную частоту ядер водорода. Этот импульс заставляет ядра резонировать на их резонансной частоте. Затем, для получения информации о том, из какого места в образце исходит сигнал, спины возбужденных атомов водорода кодируются комбинацией фазовых и частотных кодов, соответствующих полезным данным в k-пространстве, получаемым при этом возбуждении. (Здесь под фазой и частотой подразумевается резонансная частота и фаза ядер водорода.) Это осуществляется путем модуляции магнитного поля в пространстве и времени для соответствующего пространственного изменения резонансной частоты ядер и модуляции их фазы. Затем сигнал возвращается от возбужденных ядер водорода образца, и значения k извлекаются из сигнала. Этот процесс возбуждения, кодирования и получения сигнала повторяется, пока не будет получена полная матрица значений в k-пространстве (надлежащим образом выбранных для построения ряда Фурье) с достаточно высокой пространственной частотой для разрешения нужных особенностей в образце. Наконец, матрица значений k подвергается преобразованию Фурье для создания изображения или изображений. Современные системы МРТ допускают разнообразные вариации и расширения этой темы. Один подход предусматривает использование частотного кодирования для локализации сигналов в тонких слоях и фазовое кодирование для формирования значений k для каждого из этих 2D-слоев.
В опубликованной патентной заявке США №US-2006-0155186-A1 раскрыто оценивание состояния здоровья кости с использованием пространственно-частотного анализа для оценивания состояния здоровья трабекулярной кости путем получения данных в k-пространстве для соответствующих пространственных частот и векторов направления, указывающих состояние здоровья кости. Для этого не требуется собирать данные в k-пространстве, когда кость остается неподвижной во время анализа. Предпочтительный способ получения этих данных предусматривает использование магнитно-резонансного устройства с возможностью измерять значения в k-пространстве для соответствующих пространственных частот и векторов направления, требование, которое значительно снижает необходимую сложность и стоимость устройства по сравнению с традиционным оборудованием МРТ. Магнитный резонанс особенно хорошо подходит для этого, поскольку кость дает очень слабый сигнал, а костный мозг (который заполняет пустоты в решетке трабекулярной кости) дает сильные сигналы, тем самым обеспечивая высокую контрастность. Раскрыты различные иллюстративные техники получения и анализа данных. Однако в этой заявке не раскрыта необходимость в обработке методом окна или в использовании градиента считывания для получения линии в k пространстве за один период.
Краткое описание чертежей
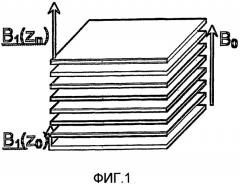
Фиг.1 иллюстрирует Iso-B0 слои c линейной поверхностью.
Фиг.2 иллюстрирует Iso-B0 слои с нелинейной поверхностью.
Фиг.3 - гипотетический график энергии, наблюдаемой на слое n, для всех слоев, для которых получают данные.
Фиг.4 представляет графики, аналогичные графику на фиг.3, но с большими изменениями между слоями, свидетельствующими о том, что количество костного мозга в каждом слое изменяется.
Фиг.5 представляет графики, демонстрирующие, насколько быстро энергия изменяется от слоя к слою, причем медленно изменяющийся уровень энергии свидетельствует о наличии нижележащей структуры, которая отличается от более быстро изменяющейся структуры.
Фиг.6 представляет графики величины дискретного преобразования Фурье для графиков энергии, показанных на фиг.5.
Фиг.7 представляет графики процентного содержания энергии на частотах ≤ частоты fn.
Фиг.8 иллюстрирует эффект размера образца относительно преобладающих (или характерных) размеров фазы порождающего сигнала, оказываемый на среднее значение и изменяемость отраженного сигнала как функцию от z в одномерном анализе.
Фиг.9 - схематическое изображение варианта осуществления очерчивания объема образца, показывающего ствол скважины, проходящий через толщу пластов, содержащую каверны с нефтью.
Фиг.10 иллюстрирует концепцию, аналогичную показанной на фиг.9, но, на этот раз, для оценивания трабекулярной структуры в губчатом веществе кости.
Фиг.11 иллюстрирует позиционирование объема образца внутри кортикального слоя кости предполагаемого анатомического места.
Фиг.12 - кубический образец, демонстрирующий применение считывания градиента в нужном направлении.
Фиг.13 - пластинчатый образец, демонстрирующий применение считывания градиента в нужном направлении и тот факт, что образец разделен в виде матрицы 6x6 с использованием одного из описанных способов.
Фиг.14 иллюстрирует выбор пластины в дистальном отделе большой берцовой кости и матрицу 6x6, очерченную путем фазового кодирования.
Фиг.15 - последовательность импульсов, используемая в спектроскопическом методе PRESS.
Фиг.16 - последовательность импульсов, используемая в пространственно-спектральном спектроскопическом методе.
Фиг.17 показывает сверху 2D изображение, полученное методом КТ (компьютерная томография), и 2D преобразование Фурье, в котором указано два направления, показывающие анизотропию в изображении и 2D ПФ.
Фиг.18 показывает два пространственно-частотных спектра, соответствующие двум стрелкам, показанным в 2D ПФ на фиг.17, демонстрирующие значительные различия на пространственных частотах менее 5 мм-1.
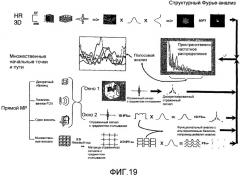
Фиг.19 - иллюстрация различных иллюстративных техник для получения и анализа данных согласно настоящему изобретению.
Осуществление изобретения
Как отмечено выше, данная заявка испрашивает приоритет по двум предварительным заявкам. Первая предварительная заявка описывает способ и устройство для получения характеристик распределений размера диспергированной фазы ЯМР, порождающей сигнал, смешанной с одной или несколькими дополнительными фазами со значительно отличающимися свойствами сигнала. Примерами являются костный мозг в губчатом веществе кости и нефть, рассеянная в толще пластов.
Подход предусматривает следующие компоненты. Во-первых, обеспечение магнитного поля (B0), охватывающего интересующую область (ROI) в образце, которую нужно охарактеризовать. Во-вторых, обеспечение градиента B0 по ROI. В-третьих, обеспечение передающих (возбуждающих) и приемных антенн/систем, имеющих высокую чистую чувствительность к сигналам, возбуждаемым в ROI и исходящим из нее.
С использованием этого устройства осуществляется эксперимент ЯМР путем передачи импульса заданной ширины полосы для возбуждения сигнала ЯМР в нужном диапазоне B0, а затем одного или нескольких изменений фокусировки передаваемых импульсов и дискретизации принятого отраженного сигнала. Альтернативно, это можно делать способом градиентного отраженного сигнала. Образцы этого отраженного сигнала обеспечивают линию в k-пространстве, представляющую преобразование Фурье интенсивности сигнала ЯМР, исходящего из ROI в направлении градиента B0.
Вышеописанный эксперимент ЯМР можно осуществлять в одном или нескольких направлениях или местах (ROI) в образце для оценивания пространственно-частотного контента и его однородности и анизотропии в образце.
В абзацах ниже будет описано и выведено соотношение между сигналом и пространственно-частотным распределением в ROI в конфигурации одного градиента.
В этом подходе предполагается, что существует одно измерение, в котором можно добиться некоторого особого распознавания с использованием частотного градиента. Остальные два измерения образуют поверхность, которая, при добавлении к «толщине», связанной с частотным градиентом, создает слой в пространстве, который не обязан быть линейным в евклидовом пространстве. Это показано на фиг.1 (Iso-B0 линейные слои [поверхности] с добавленным линейным градиентом) и на фиг.2 (Iso-B0 нелинейные слои [поверхности]).
На геометрию слоя влияет не только однородность (или ее отсутствие) основного магнитного поля (B0), но также однородность (или ее отсутствие) градиента, и конкретная(ые) апертура(ы) передающих и приемных катушек. Апертуры передающих и приемных катушек служат для задания поперечной протяженности отдельных Iso-B0 слоев, но не контура поверхности.
Независимо от геометрической конфигурации слоя (так называемой Iso-B0 поверхности), именно направление градиента - будь то вследствие сознательного применения или же в результате нелинейности поля B - позволяет отличить друг от друга различные слои в гиромагнитно-частотном измерении.
Образцы можно получать по-разному. Ниже приведено несколько примеров:
2D стимуляция
В системе однородного магнитного поля применяется градиент GSS выбора слоя, задаваемый как
Избирательные слои, имеющие положение z0 и ширину ΔZ, стимулируются посредством аподизированного сигнала надлежащей формы в виде
Толщина слоя ΔZ выбирается для данного градиента Gss выбора слоя путем выбора fΔ, которая задается в виде
,
и конкретный центр слоя Z0 выбирается путем выбора fL, которая задается в виде
В этом случае fL соответствует гиромагнитной частоте в центре слоя Z0. γ соответствует гиромагнитному отношению, которое приблизительно равно 4.258 кГц/Гс для 1H. Это проясняется через проверку соответствующего преобразования Фурье в виде
где
В приложениях 2D МРТ спинового отраженного сигнала (SE) остальные две оси, которые мы обозначаем ′X′ и ′Y′, обычно кодируются частотным градиентом со значением единица и последовательностью фазовых градиентов, назначаемых друг для друга, чтобы формировать достаточную информацию для локализации конкретного вокселя в 3D пространстве. Без потери общности полагаем, что ось ′X′ соответствует оси частотного градиента, и ось ′Y′ соответствует оси, закодированной фазой.
В обычной МР-томографии наклон фазы задается для каждого значения ′Y′, частотный градиент применяется к оси ′X′ и результирующее эхо дискретизируется и сохраняется в строке матрицы k-пространства. Таким образом, вся матрица k-пространства заполняется для данного слоя. Затем 2D преобразование Фурье применяется к этим образцам, и полученная величина создает изображение.
Чтобы соблюсти математическую строгость, полный принятый сигнал после стимуляции РЧ-импульсом выбора слоя можно выразить в виде:
где
представляет фазовый компонент сигнала по x, y и t (время), и Gx и Gy представляет сигналы градиента магнитного поля
и соответственно
Явная зависимость от времени Gx и Gy от t состоит в учете того факта, что сигналы градиента регулируются для выбора нужного опережения/отставания по фазе. Первый член в выражении ϕ(x, y, t) является лишь интегралом от гиромагнитной частоты.
Если мы сделаем несколько подстановок, уравнение для S(t) немного упростится.
Пусть
;
Подстановка их в выражение для S(t) дает
Далее его можно преобразовать следующим образом:
Левая часть этого уравнения представляет стандартный сигнал "k-пространства" как функцию времени, модулированную соответствующей гиромагнитной частотой. Правая часть уравнения показывает, что она просто связана с ρ(x,y) посредством 2D преобразования Фурье по kx и ky так же, как функция времени, и также модулируется гиромагнитной частотой.
В одном из вариантов осуществления нам, в конечном итоге, не интересны изменения в плоскостях ′X′ или ′Y′, но интересен полный сигнал в каждой плоскости, проходящей через Z0. Проще говоря, нам нужен результирующий сигнал при kx=ky=0. Это дает
Но это просто сигнал, измеренный при kx,ky=0,0 в k-пространстве. Для его получения из стандартной машины МР-томографии нам нужно иметь доступ к "сырым" данным в k-пространстве, и просто извлечь значение в (0,0).
Теперь, весьма возможно, что результирующее значение будет комплексным. Раз так, было бы разумно проверить модуль результирующего сигнала в виде
,
где верхний индекс в виде звездочки обозначает комплексное сопряжение.
Заметим, что хотя данное рассмотрение сосредоточено на изменении этих значений как функции z, тот же подход можно применять, проверяя значения по оси x (т.е. в направлении частотного градиента) и затем объединяя одинаковые положения по диапазону значений z.
Хотя предыдущее рассмотрение посвящено традиционной технике МРТ с получением 2D слоев, техники 3D МРТ также можно использовать для получения слоя посредством сигналов слоя от образца.
Независимо от того, как получаются данные, со значением для каждого слоя будет связана интенсивность, которая пропорциональна содержанию вещества, порождающего ЯМР (например, костного мозга), в этом слое. Чем слабее сигнал, тем меньше костного мозга (и, предположительно, больше вещества с более слабым сигналом [например, кости]) находится в этом слое.
Энергия является другим параметром, позволяющим описывать и анализировать сигналы, поступающие из материалов, порождающих ЯМР в образце. Энергия является скалярным значением в отличие от сигнала, который может быть комплексным (т.е. иметь разные фазовые соотношения).
Построив графики E(n) энергии, наблюдаемой на слое n, для всех полученных слоев, можно получить график, показанный на фиг.3.
Заметим, что нижеследующее рассмотрение относится к костному мозгу в кости в порядке примера - анализ также применим к другим многофазным смесям с существенно отличающимися уровнями сигнала ЯМР. Интерес представляет изменение этого уровня сигнала при исследовании различных слоев. Если энергия для каждого слоя, в основном, такая же, как в следующем, это говорит о том, что уровень энергии в каждом слое, в основном, одинаков (т.е. в каждом слое существует одинаковое полное количество костного мозга). С другой стороны, если существуют большие изменения между слоями, как на фиг.4, это говорит о том, что количество костного мозга изменяется от слоя к слою.
Однако другой важный аспект состоит в том, насколько быстро энергия изменяется от слоя к слою. Медленное изменение уровня энергии свидетельствует о наличии нижележащей структуры, которая отличается от более быстро изменяющейся структуры (см. фиг.5).
Можно определить толщину слоя, а также зазор между слоями (с использованием наклона градиента, ширины полосы принятого сигнала и частоты передаваемого сигнала), что позволяет связать ′скорость′ изменения уровня энергии с размером между слоями.
Это говорит о том, что нужно обратить внимание на график зависимости результирующей энергии от слоя в частотном измерении (т.е. осуществить преобразование Фурье для E(n). Заметим, что это частотное измерение отличается от гиромагнитно-частотного измерения, используемого для различения слоев, но, как мы увидим ниже, соотношение между ними представляет интерес и практическую пользу). Для предыдущих графиков E(n) соответствующий график преобразования Фурье (фактически, это будет модуль дискретного преобразования Фурье) может выглядеть, как на фиг.6.
Путем проверки можно убедиться, что график справа отличается большей концентрацией энергии на более низких частотах, а график слева отличается сдвигом распределения энергии в сторону более высоких частот. При условии, что изменение в сторону более низких частот является возможным индикатором увеличенных "карманов" костного мозга (и, таким образом, более широко разнесенной трабекулярной структуры или увеличенных или более удлиненных каверн с сырой нефтью в породе), было бы интересно выявить это отличие в сравнительных образцах.
Вернувшись на мгновение на шаг назад, обратим внимание, что сначала нужно рассмотреть значения Sn(0,0) для каждого слоя n, лежащей в основе непрерывной функции Sz(0,0), затем рассмотреть соответствующую периодическую структуру, выполнив преобразование Фурье следующим образом:
Теперь надо помнить, что значение точки сигнала Sz(0,0) соответствует сигналу, соответствующему положению z. Если вместо поочередного извлечения этих значений, соответствующих отдельным срезам, в направлении z применяется градиент, и весь объем стимулируется, результирующий сигнал, зависящий от времени, будет иметь вид:
Таким образом, можно видеть, что соответствующее преобразование Фурье спектра выборок слоев вдоль z (т.е. пространственно-частотные спектры) можно получить непосредственно из сигнала, зависящего от времени, путем стимуляции в присутствии градиента, умножения на комплексную экспоненту, частота которой связана с величиной B0 напряженности поля и z-градиентом "выбора слоя" напряженности поля. Это можно делать независимо от использования преобразования Фурье на полученных данных - дискретизированный отраженный сигнал уже является искомой пространственной частотой (преобразованием Фурье сигнала «слой за срезом» в зависимости от Z).
Теперь, когда показано, что спектр преобразования Фурье распределения сигнала (например, количества материала, генерирующего сигнал ЯМР) в направлении z получается непосредственно из вышеописанного эксперимента ЯМР, рассмотрим подробно, как выбирать данные и подходы для количественного описания этих спектров.
Техника анализа
Теперь рассмотрим построение графика, который отображает процентное содержание энергии на частотах □ частоты fn. Если это сделано для предыдущих графиков, можно получить графики, показанные на фиг.7.
В этом случае левый график отчетливо показывает влияние ненулевых энергий в более высокочастотных компонентах по сравнению с правым. Если задан порог, например 80%, и проверена соответствующая частота, мы получаем указание частоты, на которой или ниже нее сосредоточено 80% полной энергии. Мы предполагаем, что чем ниже эта величина (т.е. энергия, в основном, сосредоточена на более низких частотах), тем выше вероятность заболевания костей.
Влияние размера образца на полученные данные
Размер образца относительно преобладающих (или характерных) размеров фазы, порождающей сигнал, оказывает влияние на среднее значение и изменчивость сигнала как функция z в одномерном анализе. Это показано на фиг.8, где в случае a объем образца приближается к характерному размеру и присутствует значительное изменение значения сигнала (пропорциональное величине фазы, порождающей сигнал как функция Z) в зависимости от Z. Случай c, напротив, имеет, в среднем, значительно более высокий уровень сигнала, но меньшее изменение уровня сигнала как функцию Z.
Выбирая объем образца, достаточно большой для выбора характерных размеров, но недостаточно большой для усреднения большого количества характерных размеров, можно получить оптимальную чувствительность (а следовательно, объем образца) к нужному размеру структуры. Это особенно пригодно для системы с использованием одного градиента, как в случае недорогого устройства для оценивания структуры кости у пациентов или для оценивания размера и распределения пор в нефтеносной толще пластов с помощью устройства ЯМР, вставленного в ствол скважины. Эти два устройства, более подробно описанные ниже, обычно используют фиксированный градиент, генерируемый главным магнитом, который также используется для кодирования в направлении Z.
В обоих этих случаях дополнительную информацию об анизотропии образца можно получить, изменяя направление градиента в образце. Этого можно добиться физически, перемещая образец или магнит относительно друг друга, или электрически, модулируя магнитное поле. Информацию об однородности образца можно получить, перемещая (параллельно) чувствительный объем по образцу.
Оконтуривание объема образца
В случае вышеописанной системы одного градиента оконтуривание объема образца осуществляется посредством комбинации
ширины полосы приемника
функции чувствительности приемной антенны (катушки)
передаваемого поля B
распределения поля магнита
На фиг.9 показана схема осуществления оконтуривания объема образца, где показан ствол скважины 1, проходящий через пласт, содержащий каверны с нефтью 5. Устройство размещено в корпусе 2 с магнитом 3 для формирования ряда Iso-B0 поверхностей 6 и 7 в пласте. Передающая/приемная антенна 4 (здесь показана как единая антенна - также может быть реализована в виде отдельных передающей и приемной антенн) с функцией чувствительности, указанной пунктирными линиями 8. Объем образца 9 оконтуривается шириной полосы приемника (альтернативно или дополнительно, шириной полосы передатчика) между Iso-B0 поверхностями 6 и 7 и комбинированной границей 8 минимальной чувствительности передачи/приема.
Эту конфигурацию можно использовать для оценивания анизотропии в плоскости, ортогональной стволу скважины, путем вращения зонда относительно оси ствола скважины, и в плоскостях, параллельных стволу скважины, путем придания Iso-B0 поверхностям наклона к стволу скважины, тогда как обычно они параллельны ему, как показано на фиг.9. Придание наклона можно осуществлять, поворачивая магнит 3 или модулируя поле с помощью дополнительных электромагнитов.
На фиг.10 представлена концепция, аналогичная показанной на фиг.9, но, на этот раз, для оценивания трабекулярной структуры губчатого вещества кости. Затем чувствительный объем (объем образца) 9 размещается в интересующей области соответствующей кости для оценивания трабекулярной структуры. Предполагаемые положения образца включают в себя проксимальный и дистальный отделы большой берцовой кости, дистальный отдел лучевой кости, пяточную кость, таз, подвздошный гребень и позвонки.
На фиг.11 показано позиционирование объема образца 9 внутри трубчатой кости 16 предполагаемого анатомического места.
Особенности конструкции устройства для осуществления этой техники оценивания трабекулярной кости у пациентов-людей включают в себя:
1. магнит, предназначенный для создания номинально постоянного градиента в области съемки для обеспечения чувствительности как функции пространственной частоты.
2. возможность выбирать множественные ориентации в целевой кости путем механического перемещения магнита относительно кости или электрического модулирования картины поля для изменения ориентации Iso-B0 поверхностей.
3. устройство для повторяемого и удобного позиционирования анатомии.
4. механическое или электронное сканирование в 3D пространстве для оценивания анизотропии и/или определения граничного направления.
5. контроллер для формирования и возбуждения передающей антенны.
6. приемная система для приема сигнала от объема образца и его анализа.
Эта система оценивает свойства, включающие в себя:
7. порядок короткого диапазона.
8. анизотропию.
9. однородность.
10. характерное разнесение/наличие структур с низкими пространственными частотами.
Вторая предварительная заявка относится к пространственно-частотной спектроскопии с разрешаемой позицией и описывает способ получения измерений пространственно-частотных спектров (ПЧС) в локализованных областях 3-мерного образца. Этот подход является расширением спектроскопических техник МРТ ("NMR chemical shift imaging in three dimensions", T.R.Brown et al., Proc. Natl. Acad. Sci. USA, 79:3523, 1982) Hornak обеспечивает описание этих различных способов в "The Basics of NMR" (Joseph P. Hornak, Ph.D., Copyright 1996-2006), которая включена сюда посредством ссылки. Также описаны в P.A.Bottomley "Spatial localization in NMR spectroscopy in vivo." Ann. NY Acad. Sci. 508:333 (1987). Обе вышеприведенные ссылки, таким образом, включены в данную заявку посредством ссылки.
Пространственно-частотные спектры (ПЧС) содержат (представляют) спектр мощности для распределения измерений в образце. В этом раскрытии дополнительно описано использование пространственно-частотной спектроскопии для оценивания и диагностики нормальных и аномальных медицинских условий. Применение к остеопорозу описано в находящейся в рассмотрении заявке на изобретение №11/064381, поданной 23 февраля 2005 года и включенной сюда посредством ссылки. Использование пространственно-частотной спектроскопии для оценивания заболевания (состояния здоровья) зависит от источника ПЧС. ПЧС можно получать из магнитного резонанса, а также посредством Фурье-анализа 3D и 2D изображений анатомических структур, подлежащих анализу. На фиг.17 и 18 показаны генерация и анализ ПЧС из 2D изображения высокого разрешения, полученного методом компьютерной томографии, для трабекулярной кости из позвонка. Анизотропия, отчетливо наблюдаемая в изображении, также отчетливо проявляется в 2D ПФ и отдельных спектрах на фиг.18.
В некоторой степени аналогичная техника проиллюстрирована в верхней строке фиг.19 (обозначенная HR 3D, или 3D высокого разрешения). Там берутся двумерные данные для ряда слоев образца, например данные, полученные с помощью устройства компьютерной томографии (КТ). Стопка изображений образует 3D модель структуры. Вместо того чтобы анализировать 3D данные с использованием традиционных способов оценивания томографии, в этом альтернативном подходе область трехмерных данных сжимается (проецируется) в двумерные данные путем суммирования данных в одн