Полиморфная форма гидрохлорида лерканидипина и способ ее получения
Иллюстрации
Показать всеИзобретение описывает способы очистки гидрохлорида лерканидипина, которые используют бинарные системы спиртосодержащего растворителя такого, как метанол и алифатического эфирсодержащего растворителя, такого как изопропилацетат. А кроме того, описывается гидрохлорид лерканидипина в полиморфной форме V, способы ее получения, а также фармацевтическая композиция для лечения гипертензии, содержащая гидрохлорид лерканидипина в полиморфной форме V. Технический результат: изобретение обеспечивает улучшенную эффективность, поскольку использует экономичные реагенты, уменьшает количество отходов, а также приводит к чистому гидрохлориду лерканидипина. 11 н. и 9 з.п.ф-лы, 1 табл., 3 ил.
Реферат
ДАННЫЕ О ПРИОРИТЕТЕ
Настоящая заявка испрашивает преимущество в соответствии с §119 35 U.S.C. на основании индийской предварительной заявки, поданной 24 Марта 2006 и имеющей название «ПО СУЩЕСТВУ ЧИСТЫЙ ГИДРОХЛОРИД ЛЕРКАНИДИПИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ», и на основании индийской предварительной заявки No. 75/MUM/2006, поданной 17 января 2006 и имеющей название «ПОЛИМОРФНАЯ ФОРМА V ГИДРОХЛОРИДА ЛЕРКАНИДИПИНА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ», и на основании американской предварительной заявки No. 60/751834, поданной 20 декабря 2005 и имеющей название «ПОЛИМОРФНАЯ ФОРМА V ГИДРОХЛОРИДА ЛЕРКАНИДИПИНА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ», и на основании индийской предварительной заявки No. 1125/MUM/2005, поданной 16 сентября 2005 и имеющей название «НОВЫЕ ПОЛИМОРФНЫЕ ФОРМЫ ГИДРОХЛОРИДА ЛЕРКАНИДИПИНА И СПОСОБ ИХ ПОЛУЧЕНИЯ», содержание каждой из которых включено в описание настоящей заявки посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
1. Область техники, к которой относится изобретение
Настоящее изобретение в целом относится к новому полиморфу гидрохлорида лерканидипина и способам его получения. Настоящее изобретение также в целом относится к способу получения гидрохлорида аморфной формы лерканидипина и способу очистки гидрохлорида лерканидипина.
2. Описание предшествующего уровня техники
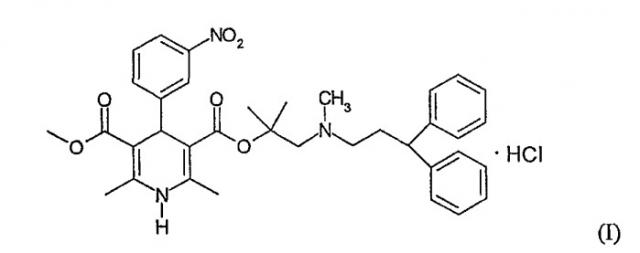
Гидрохлорид лерканидипина, также известный, как гидрохлорид 2-[(3,3-дифенилпропил)метиламино]-1,1-диметилэтилметилового эфира 1,4-дигидро-2,6-диметил-4-(3-нитрофенил)-3,5-пиридинкарбоновой кислоты, представлен структурой Формулы I.
Гидрохлорид лерканидипина представляет собой синтетический антигипертензивный блокатор кальциевых каналов, продаваемый под торговыми марками Леркадип, Лердип, Лерзам, Занедип и Занидип®. Гидрохлорид лерканидипина представляет собой дигидропиридиновый блокатор кальциевых каналов, используемый для лечения гипертензии. Он может уменьшать системное артериальное кровяное давление в течение длительного периода действия и, как полагают, уменьшает развитие атеросклероза. См., например, The Merck Index, Thirteenth Edition, 2001, p. 973, monograph 5465.
Европейский патент № 0153016 ("патент '016") и патент США № 4968832 ("патент '832"), введенные здесь посредством ссылки, раскрывают гидрохлорид лерканидипина. Патенты '016 и '832 далее раскрывают способы получения гидрохлорида лерканидипина и гидрохлорида аморфной формы лерканидипина. Недостатки, связанные с этими способами, включают, например, получение примесей. Следовательно, предпочтительно уменьшить уровень примесей при получении гидрохлорида лерканидипина.
Патент США № 5912351 раскрывает простой способ получения гидрохлорида лерканидипина. Он включает реакцию 1,4-дигидро-2,6-диметил-5-метоксикарбонил-4-(3-нитрофенил)пиридин-3-карбоновой кислоты с тионилхлоридом в дихлорметане и диметилформамиде при температуре между -4 и +1°C и последующую этерификацию полученного хлорида кислоты 2, N-диметил-N-(3,3-дифенилпропил)-1-амино-2-пропиловым спиртом при температуре между -10 и 0°C. Способ дает выход гидрохлорида лерканидипина в безводной негигроскопичной кристаллической форме и позволяет избежать образования нежелательных побочных продуктов и последующую очистку на хроматографических колонках.
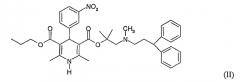
Одна примесь, как полагают, присутствует при получении гидрохлорида лерканидипина и представляет собой 2-[N-(3,3-дифенилпропил)-N-метиламино]-1,1-диметилэтилпропиловый диэфир 1,4-дигидро-2,6-диметил-4-(3-нитрофенил)пиридин-3,5-дикарбоновой кислоты, как определено при помощи ВЭЖХ анализа различных партий гидрохлорида лерканидипина, полученного реакцией бутановой кислоты, гидрохлорида 2-[(3-нитрофенил)метилен]-3-оксо-2-[(3,3-дифенилпропил)метиламино]-1,1-диметилэтилового эфира и метил-3-аминокротоната в присутствии триэтиламина и н-пропанола, применяя набор методов далее в Примере 16 EP 0153016. Структура 2-[N-(3,3-дифенилпропил)-N-метиламино]-1,1-диметилэтилпропилового диэфира 1,4-дигидро-2,6-диметил-4-(3-нитрофенил)пиридин-3,5-дикарбоновой кислоты представлена структурой Формулы II.
Примесь, образованная из-за переэтерификации гидрохлорида лерканидипина в положении 5 н-пропанолом в присутствии HCl в н-пропаноле. Кроме того, эту примесь очень трудно удалить из неочищенного гидрохлорида лерканидипина.
Патент США № 6852737 ("патент '737") раскрывает кристаллические Формы I и II и неочищенные Формы A и B гидрохлорида лерканидипина и способ их получения. Неочищенная Форма А гидрохлорида лерканидипина описана в Примере 2 как имеющая пик в дифференциальной сканирующей калориметрии (ДСК) при 150-152°C. Неочищенная Форма В гидрохлорида лерканидипина описана в Примере 3 как имеющая пик в дифференциальной сканирующей калориметрии (ДСК) при 131-135°C. Патент '737, кроме того, раскрывает, что патент США № 5912351 ("патент '351 ") получает третью неочищенную форму гидрохлорида лерканидипина, называемую неочищенной Формой C. Неочищенная Форма C, как сообщается, имеет ДСК пик при 186-192°C. Кроме того, патент '737 раскрывает, что термогравиметрические изучения показывают, что неочищенная Форма А содержит 3-4% остаточного этилацетата, неочищенная Форма В содержит 0,3-0,7% остаточного этилацетата и неочищенная Форма C содержит 0-0,1% остаточных растворителей. Кристаллические Формы I и II гидрохлорида лерканидипина являются хорошо охарактеризованными при помощи дифракционного рентгеновского анализа в патенте '737. Пример 12 патента '737 раскрывает, что кристаллическая Форма I имеет температуру плавления (T пик) 198,7°C и начальную температуру 179,8°C и кристаллическая Форма II имеет температуру плавления (T пик) 209,3°C и начальную температуру 169,0°C.
WO 2006/089787 раскрывает гидрохлорид аморфного лерканидипина, имеющий чистоту, по меньшей мере, 95%, и способ его получения. Способ включает растворение кристаллического гидрохлорида лерканидипина в органическом растворителе, чтобы обеспечить раствор и выделение гидрохлорида аморфного лерканидипина при помощи или (a) добавления воды к раствору, чтобы образовать осадок и собрать осадок, или (b) выпаривания органического растворителя.
Полиморфизм представляет собой явление различных кристаллических форм взятого отдельно соединения и представляет собой свойство некоторых соединений и комплексов. Таким образом, полиморфы представляют собой определенные твердые фазы, совместно использующие одинаковую молекулярную формулу, еще каждый полиморф может иметь определенные физические свойства. Следовательно, отдельно взятое соединение может давать разнообразие полиморфных форм, где каждая форма имеет различные и определенные физические свойства, такие как различные кривые растворимости, различные точки температур плавления и/или различные пики дифракции рентгеновских лучей. Так как растворимость каждого полиморфа может варьироваться, идентификация существования фармацевтических полиморфов является существенной для обеспечения фармацевтических препаратов с приписываемыми кривыми растворимости. Желательно исследовать все формы твердых состояний лекарственного средства, включая все полиморфные формы и определить стабильность, растворение и свойства текучести каждой полиморфной формы. Полиморфные формы соединения могут различаться в лаборатории при помощи рентгеновской спектроскопии и при помощи других методов таких, как ИК-спектрометрия. Кроме того, полиморфные формы одинакового лекарственного вещества или активного фармацевтического ингредиента могут быть введены сами по себе или в составе готовой лекарственной формы (также известной, как окончательная или готовая лекарственная форма) и являются хорошо известными специалисту в области фармацевтики, чтобы воздействовать, например растворимость, стабильность, текучесть, податливость и сжимаемость лекарственных веществ и эффективность готовых лекарственных форм.
Открытие новых полиморфных форм фармацевтически пригодного соединения обеспечивает новую возможность улучшить характеристики применения фармацевтического препарата. Также добавляется к материалу, что технолог имеет возможность для разработки, например, формы фармацевтического препарата лекарственного средства с целевым профилем высвобождения или другими желаемыми характеристиками. Новую полиморфную форму гидрохлорида лерканидипина сейчас раскрывают.
Попытки также были сделаны, чтобы приготовить фармацевтические препараты с высокой степенью чистоты и минимальным количеством присутствия примесей. Контроль примесей требует изучения различных средств, чтобы остановиться на условиях реакции и протоколах испытаний, необходимых для гарантии, что лекарственные средства, которые вводятся пациентам, по существу чистые. Следовательно, остается необходимость в улучшенном способе получения гидрохлорида лерканидипина, в котором устраняются или уменьшаются примеси удобным и экономичным методом, чтобы обеспечить по существу чистые формы гидрохлорида лерканидипина.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В соответствии с одним вариантом осуществления настоящего изобретения способ получения по существу чистого гидрохлорида лерканидипина обеспечивается, включая (a) растворение гидрохлорида лерканидипина в спиртосодержащем растворителе для образования раствора,
(b) добавление алифатического эфирсодержащего растворителя к раствору и (c) выделение гидрохлорида лерканидипина из раствора.
В соответствии со вторым вариантом осуществления настоящего изобретения гидрохлорид лерканидипина обеспечивается по существу в полиморфной форме V.
В соответствии с третьим вариантом осуществления настоящего изобретения по существу чистый гидрохлорид лерканидипина обеспечивается в полиморфной форме V.
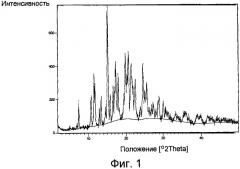
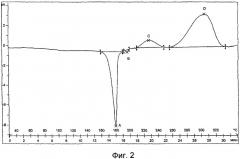
В соответствии с четвертым вариантом осуществления настоящего изобретения обеспечивается гидрохлорид лерканидипина по существу в полиморфной форме V и имеющий, по меньшей мере, одну из следующих характеристик (a) модель дифракции рентгеновских лучей (XRD) по существу в соответствии с Фиг.1 и/или термограмма дифференциальной сканирующей калориметрии (ДСК) по существу в соответствии с Фиг.2.
В соответствии с пятым вариантом осуществления настоящего изобретения гидрохлорид лерканидипина обеспечивается по существу в полиморфной форме V и показывающий характерные пики (выраженные в градусах 2θ±0,2°θ) приблизительно при одном или большем количестве положений около 17,2752 и около 19,8836.
В соответствии с шестым вариантом осуществления настоящего изобретения способ получения гидрохлорида лерканидипина обеспечивается по существу в полиморфной форме V, способ, включающий:
(a) растворение гидрохлорида лерканидипина в спиртосодержащем растворителе для получения раствора;
(b) добавление алифатического эфирсодержащего растворителя к раствору и
(c) выделение гидрохлорида лерканидипина по существу в полиморфной форме V из раствора.
Преимущества способа вышеупомянутых вариантов осуществления включают, по меньшей мере, следующие:
1. Способ представляет собой простой способ, который целесообразен и эффективен в промышленном масштабе и приводит по существу к чистому гидрохлориду лерканидипина.
2. Способ обеспечивает улучшенную эффективность, поскольку он использует экономичные реагенты и производит меньше отходов и меньше примесей.
В соответствии с другим вариантом осуществления настоящего изобретения способ получения гидрохлорида аморфной формы лерканидипина обеспечивается способом, включающим (a) растворение гидрохлорида лерканидипина по существу в полиморфной форме V в органическом растворителе; и (b) выделение гидрохлорида аморфной формы лерканидипина.
В соответствии с еще другим вариантом осуществления настоящего изобретения способ получения гидрохлорида аморфной формы лерканидипина обеспечивается, способ, включающий (a) растворение по существу чистого гидрохлорида лерканидипина в органическом растворителе; (b) обработка раствора осветляющим веществом для образования осветленного раствора и (c) выделение гидрохлорида аморфной формы лерканидипина.
Преимущества способа этого варианта осуществления включают, по меньшей мере, следующие:
1. Способ представляет собой простой способ, который целесообразен и эффективен в промышленном масштабе и приводит по существу к чистому гидрохлориду лерканидипина.
2. Способ обеспечивает улучшенную эффективность, поскольку он использует экономичные реагенты и производит меньше отходов и меньше примесей.
ОПРЕДЕЛЕНИЯ
Термины «обработка» или «лечение» состояния, нарушения или заболевания, используемые в описании, обозначают: (1) предотвращение или задержку возникновения клинических симптомов состояния, нарушения или заболевания, возникающих у млекопитающих, которые могут страдать от или быть предрасположенными к состоянию, нарушению или заболеванию, но все еще не иметь опыта или показывать клинические или субклинические симптомы состояния, нарушения или заболевания, (2) ингибирование состояния, нарушения или заболевания, т.е. прекращение или уменьшение развития заболевания или, по меньшей мере, одного их клинического или субклинического симптома или (3) смягчение заболевания, т.е. вызывая ослабление симптомов состояния, нарушения или заболевания или, по меньшей мере, одного из их клинических или субклинических симптомов. Преимущество для объекта, который проходит лечение, представляет собой или статистически значимое, или, по меньшей мере, ощущаемое для пациента или для врача.
Термин «терапевтически эффективное количество», используемый в описании, обозначает количество соединения, которое при введении млекопитающему для лечения состояния, нарушения или заболевания, является достаточным для проведения такого лечения. «Терапевтически эффективное количество» может варьироваться в зависимости от соединения, заболевания и его тяжести и возраста, веса, физического состояния и восприимчивости млекопитающего, который подвергается лечению.
Термин «доставка», используемый в описании, обозначает терапевтически эффективное количество активного ингредиента к определенному месту в пределах организма «хозяина», обозначает, вызывая терапевтически эффективную концентрацию активного ингредиента в крови в определенном месте. Это может быть выполнено, например, топическим, очаговым или систематическим введением активного ингредиента в организм «хозяина».
Термин «буферное вещество», используемый в описании, как предполагается, обозначает соединение, используемое для устойчивости изменений pH при разбавлении или добавлении кислот или щелочей. Такие соединения включают путем примера и без ограничений метафосфат калия, фосфат калия, одноосновный ацетат натрия и безводный и дегидратированный цитрат натрия и другие такие вещества, известные специалисту в данной области.
Термин «подслащивающее вещество», используемый в описании, как предполагается, обозначает соединение, используемое для придания сладкого вкуса при получении. Такие соединения включают путем примера и без ограничений аспартам, декстрозу, глицерин, маннитол, сахариновый натрий, сорбит, сахарозу, фруктозу и другие такие вещества, известные специалисту в данной области.
Термин «связывающее вещество» используемый в описании, как предполагается, обозначает вещества, используемые, чтобы вызвать адгезию частиц порошка в гранулах таблеток. Такие соединения включают путем примера и без ограничений акациевую альгиновую кислоту, трагант, карбоксиметилцеллюлозу натрия, поливинилпирролидон, сжимающийся сахар (например, NuTab), этилцеллюлозу, желатин, жидкую глюкозу, метилцеллюлозу, повидон и пептизированный крахмал, их комбинации и другие вещества, известные специалисту в данной области.
При необходимости другие связывающие вещества можно включить в настоящее изобретение. Типовые связывающие вещества включают крахмал, поли(этиленгликоль), гуаровую камедь, полисахарид, бентониты, сахара, инвертированные сахара, полоксамеры (PLURONICTM F68, PLURONICTM F127), коллаген, альбумин, целлюлозы в безводных растворителях, их комбинации и т.п. Другие связывающие вещества включают, например, поли(пропиленгликоль), полиоксиэтилен-полипропилен сополимер, полиэтиленовый эфир, полиэтиленовый сорбитановый эфир, поли(этиленоксид), микрокристаллическую целлюлозу, поли(винилпирролидон), их комбинации и другие такие вещества, известные специалисту в данной области.
Термин «разбавитель» или «наполнитель», используемые в описании, как предполагается, обозначают инертные вещества, используемые в качестве наполнителей для создания желаемого объема, скользящих свойств и характеристик компрессии при получении таблеток и капсул. Такие соединения включают путем примера и без ограничений двухосновный фосфат кальция, каолин, сахарозу, маннит, микрокристаллическую целлюлозу, порошковую целлюлозу, осажденный карбонат кальция, сорбит, крахмал, их комбинации и другие такие вещества, известные специалисту в данной области.
Термин «вещество, способствующее скольжению», используемый в описании, как предполагается, обозначает вещества, используемые в рецептуре таблеток и капсул для улучшения скользящих свойств в течение сжатия таблетки и получения эффекта, предотвращающего слипание. Такие соединения включают путем примера и без ограничений коллоидную окись кремния, силикат кальция, силикат магния, кремниевый гидрогель, кукурузный крахмал, тальк, их комбинации и другие такие вещества, известные специалисту в данной области.
Термин «смазывающее вещество», используемый в описании, как предполагается, обозначает вещества, используемые в рецептуре таблеток, для уменьшения трения в течение сжатия таблеток. Такие соединения включают путем примера и без ограничений стеарат кальция, стеарат магния, минеральное масло, стеариновую кислоту, стеарат цинка, их комбинации и другие такие вещества, известные специалисту в данной области.
Термин «вещество, вызывающее дезинтеграцию», используемый в описании, как предполагается, обозначает соединение, используемое в твердых лекарственных формах для поддержания разрушения твердой массы на маленькие частицы, которые являются более легко диспергированными или растворенными. Типовые вещества, вызывающие дезинтеграцию, включают путем примера и без ограничений крахмалы, такие как кукурузный крахмал, картофельный крахмал, пептизированный и модифицированный крахмал, подслащивающие вещества, глины, такие как бентонит, микрокристаллическая целлюлоза (например, AvicelTM), карзиум (например, AmberliteTM), альгинаты, натриевый гликолят крахмала, камедь, такую как агар, гуар, плод рожкового дерева, карайя, пектин, трагант, их комбинации и другие такие вещества, известные специалисту в данной области.
Термин «смачивающее вещество», используемый в описании, как предполагается, обозначает соединение, используемое для поддержания достигнутого внутреннего контакта между твердыми частицами и жидкостями. Типовые смачивающие вещества включают путем примера и без ограничений желатин, казеин, лецитин (фосфатиды), аравийскую камедь, холестерин, трагант, стеариновую кислоту, бензалконий хлорид, стеарат кальция, глицерин моностеарат, цетостеариловый спирт, цетомакрогольный эмульгирующий парафин, сорбитановые эфиры, полиоксиэтиленалкиловые эфиры (например, макрогольные эфиры такие, как цетомакрогол 1000), производные полиоксиэтиленового касторового масла, полиоксиэтиленовые сорбитановые эфиры жирных кислот (например, TWEENTMs), полиэтиленгликоли, полиоксиэтиленовый стеариновый коллоидальный диоксид кремния, фосфаты, додецилсульфат натрия, карбоксиметилцеллюлозу кальция, карбоксиметилцеллюлозу натрия, метилцеллюлозу, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозы фталат, некристаллическую целлюлозу, магнийалюмосиликат, триэтаноламин, поливиниловый спирт, поливинилпирролидон (ПВП), тилоксапол (неионный жидкий полимер алкиларилполиэфирного спиртового типа, также известный как суперинон или тритон), их комбинации и другие такие вещества, известные специалисту в данной области.
Большинство из этих вспомогательных веществ описаны детально, например, в Howard C. Ansel et al., Pharmaceutical Dosage Forms and Drug Delivery Systems, (7th Ed. 1999); Alfonso R. Gennaro et al., Remington: The Science and Practice of Pharmacy, (20th Ed. 2000); и A. Kibbe, Handbook of Pharmaceutical Excipients, (3rd Ed. 2000), которые включены в настоящее описание посредством ссылки.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1 представляет собой характерный дифракционный рентгеновский анализ образца порошка полиморфной формы V гидрохлорида лерканидипина.
Фиг.2 представляет собой характерную термограмму дифференциальной сканирующей калориметрии полиморфной формы V гидрохлорида лерканидипина.
Фиг.3 представляет собой характерный дифракционный рентгеновский анализ образца порошка гидрохлорида лерканидипина в аморфной форме.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНОГО ВАРИАНТА ОСУЩЕСТВЛЕНИЯ
Один вариант осуществления настоящего изобретения направлен на новую полиморфную форму гидрохлорида лерканидипина, обозначаемую полиморфная форма V. Новая полиморфная форма V гидрохлорида лерканидипина может быть охарактеризована, например, дифракционным рентгеновским анализом образца порошка и/или точкой плавления. Спектр XRD порошка полиморфной формы V представлен на Фиг.1 и изложен в табличной форме в Таблице 1 ниже. Рентгеновская дифракция порошка была измерена порошковым рентгеновским дифрактометром, оборудованным Cu-анодом (λ =1,54 Ангстрема), источник рентгеновских лучей работает при 45 кВ, 40 мА и Ni фильтр используют, чтобы отделить K-бета радиацию. Калибровка 2 тета выполняется, используя NIST SRM 640c Si стандарт. Образец был проанализирован, используя следующие измеряемые параметры: диапазон измерения=2-50° 2θ.; ширина шага=0,017 °; и время измерения за шаг=5 сек.
| ТАБЛИЦА 1 | |
| 2θ | Относительная интенсивность |
| 7,5567 | 24,60 |
| 10,8095 | 25,08 |
| 11,5702 | 44,58 |
| 11,7830 | 33,49 |
| 12,9422 | 12,58 |
| 13,4256 | 23,29 |
| 14,5405 | 12,60 |
| 15,1595 | 100,00 |
| 15,8627 | 20,42 |
| 16,5901 | 28,77 |
| 16,9949 | 26,39 |
| 17,2752 | 49,84 |
| 17,9432 | 35,18 |
| 19,4545 | 20,72 |
| 19,8836 | 55,07 |
| 20,7967 | 50,73 |
| 21,4870 | 43,92 |
| 22,5097 | 29,56 |
| 23,9261 | 8,41 |
| 24,6309 | 43,50 |
| 25,6598 | 27,78 |
| 27,4245 | 11,03 |
| 29,0007 | 16,64 |
| 30,1320 | 15,10 |
| 30,7263 | 8,19 |
| 33,4079 | 5,76 |
| 36,0060 | 8,13 |
| 38,9590 | 6,69 |
| 39,8607 | 6,22 |
| 41,6170 | 6,11 |
Как показано на Фиг.2, полиморфная форма V гидрохлорида лерканидипина показывает преобладающий эндотермальный пик при около 179,5°C, как измерено дифференциальным сканирующим калориметром (DSC 822, Mettler Toledo) при скорости сканирования 10°C в минуту со стандартом индия. В этом отношении, должно пониматься, что эндотерм, измеренный определенным дифференциальным сканирующим калориметром, зависит от множества факторов, включая скорость нагрева (т.е. скорость сканирования), используемый калибровочный стандарт, градуировку средства измерений, относительную влажность и химическую чистоту тестируемого образца.
Таким образом, эндотерм, как измерено ДСК на приборе, идентифицированном выше, может измениться до ±1°C или даже ±11/2°C. Следовательно, термин «около 179,5°C», как предполагается, охватывает такие колебания прибора.
В одном варианте осуществления полиморфная форма V гидрохлорида лерканидипина может быть получена, по меньшей мере:
(a) растворением гидрохлорида лерканидипина в спиртосодержащем растворителе для получения раствора;
(b) добавлением алифатического, эфирсодержащего растворителя к раствору стадии (a); и
(c) выделением гидрохлорида лерканидипина по существу в полиморфной форме V из раствора.
На стадии (a) способа настоящего изобретения гидрохлорид лерканидипина растворяют в спиртосодержащем растворителе. Гидрохлорид лерканидипина может быть получен, используя методы, хорошо известные в данной области техники или из коммерческих источников и не составляют часть настоящего изобретения.
Пригодные спиртосодержащие растворители включают ароматические и алифатические C1-C12 спирты и т.п. и их смеси. Пригодные алифатические спирты включают C1-C8 спирты, такие как, например, метанол, этанол, н-пропанол, изопропанол, н-бутанол, изобутанол, трет-бутанол и т.п., и их смеси. Пригодные ароматические спирты включают C3-C12 спирты, такие как, например, бензиловый спирт, бензилоксиэтанол, феноксиэтанол и т.п., и их смеси. Обычно спиртосодержащий растворитель может присутствовать в отношении около 1:1 объем/вес по отношению к гидрохлориду лерканидипина. Гидрохлорид лерканидипина и спиртосодержащий растворитель(и) может быть нагрет до температуры в пределах от около 40°C до около 60°C, предпочтительно от около 45°C до около 55°C и наиболее предпочтительно от около 50°C до около 55°C в течение периода времени в пределах от около 30 минут до около 40 минут. Раствор предпочтительно охлаждают до комнатной температуры, температура в пределах от около 25°C до около 30°C.
На стадии (b) способа настоящего изобретения алифатический эфирсодержащий растворитель добавляют к раствору. Пригодные алифатические эфирсодержащие растворители включают эфирные группы, имеющие от около 2 до около 12 углеродных атомов, например, этилацетат, изопропилацетат и т.п., и их смеси. Алифатический эфирсодержащий растворитель может присутствовать в отношении около 10:1 объем/вес по отношению к гидрохлориду лерканидипина.
Алифатический эфирсодержащий растворитель предпочтительно добавляют при комнатной температуре, температура в диапазоне от около 25°C до около 30°C.
На стадии (c) способа настоящего изобретения гидрохлорид лерканидипина по существу в полиморфной форме V выделяют из раствора. Полиморфная форма V гидрохлорида лерканидипина может быть выделена, например, кристаллизацией раствора стадии (b)для получения по существу чистых кристаллов гидрохлорида лерканидипина; и выделением кристаллов методами, известными в данной области техники, например фильтрацией для получения полиморфной формы V гидрохлорида лерканидипина. Выделенные кристаллы могут тогда быть далее высушены. Кристаллизация может быть выполнена перемешиванием раствора при от около 60 до около 100 оборотов в минуту (об/мин) в течение периода времени в пределах от около 1 часа до около 16 часов. Температура в течение перемешивания может располагаться от около 25°C до около 30°C. Полученное твердое вещество может тогда быть отфильтровано и промыто эфирсодержащим растворителем, например, изопропилацетатом (около 1:1 объем/вес, растворитель:гидрохлорид лерканидипина), чтобы обеспечить кристаллы гидрохлорида лерканидипина. Кристаллы могут затем быть высушены. Кристаллы могут быть высушены при температуре в пределах от около 50°C до около 55°C, пока потеря в массе при высушивании ("LOD") меньше чем около 10% не достигнута. Период времени для высушивания может располагаться от около 6 часов до около 12 часов и предпочтительно около 8 часов.
Определенные эксплуатационные стадии хорошо известны в данной области техники и, если не обозначено иначе, любой известный метод для того, чтобы выполнять эти функции, может использоваться в способах этого изобретения. Например, растворители могут быть удалены дистилляцией при атмосферном давлении или под вакуумом. Высушивание может быть достигнуто выпариванием, сушкой распылением, сушкой под вакуумом и сушкой сублимацией. Перемешивание обозначает любой метод для смешивания или перемешивания реакционной смеси.
В другом варианте осуществления высокоочищенный гидрохлорид лерканидипина может быть получен
(a) реагированием раствора, включающего бутановую кислоту, 2-[(3-нитрофенил) метилен]-3-оксо-2-[(3,3-дифенилпропил)метиламино]-1,1-диметилэтиловый эфира гидрохлорид и метилен дихлорид, с метил 3 аминокротонатом и н-пропанолом и устанавливая pH раствора около 8 до около 9 основанием;
(b) охлаждением реакционной массы до температуры от около 50°C до около 55°C, отгоняя н-пропанол для получения остатка, растворяя осадок в н-пропаноле, устанавливая pH реакционной массы, используя н-пропанол/HCl и отгоняя н-пропанол для получения осадка;
(c) растворением осадка в изопропилацетате, промывая водой, обрабатывая раствор углем и отгоняя изопропилацетат для получения осадка;
(d) растворением осадка в метаноле и изопропилацетате, отбирая раствор с полиморфной формой V гидрохлорида лерканидипина и фильтрованием и промыванием твердого вещества; и
(e) высушиванием твердого вещества, полученного на стадии (d)для получения по существу чистого гидрохлорида лерканидипина.
На стадии (a) способа настоящего изобретения бутановая кислота, 2-[(3-нитрофенил) метилен]-3-оксо-2-[(3, 3-дифенилпропил)метиламино]-1,1-деметилэтилового эфира гидрохлорида раствор (около 77% вес/объем) в галогенизированном углеводородном растворителе, например метилендихлориде, реагирует с метил 3-аминокротонатом и н-пропанолом. Раствор гидрохлорида реагирует с метил 3-аминокротонатом при молярном отношении около 1:1. Реакция может иметь место при температуре в пределах от около 70°C до около 90°C и предпочтительно от около 75°C до около 80°C. Период времени для реакции может располагаться от около 8 часов до около 12 часов и предпочтительно в течение около 10 часов. После реакции pH реакционной массы может быть установлен от около 8 до около 9, используя подходящее основание, например триалкиламин, такое как триэтиламин.
На стадии (b) способа настоящего изобретения реакционную массу охлаждают до подходящей температуры, и затем н-пропанол удаляют, например, дистилляцией. Подходящая температура будет обычно располагаться от около 40°C до около 70°C и предпочтительно от около 50°C до около 55°C. Осадок, таким образом полученный, может тогда быть перерастворен в н-пропаноле. Это растворение может иметь место при комнатной температуре, температура в пределах от около 25°C до около 30°C. рH реакционной массы может тогда быть установлен от около 3 до около 4, используя раствор н-пропанол/HCl (20%) и н-пропанол отгоняют. Эта дистилляция может иметь место при температуре ниже около 35°C.
На стадии (c) способа настоящего изобретения осадок растворяют в изопропилацетате и промывают водой. Раствор затем обрабатывают с углем с подходящим угольным веществом, таким как активированный уголь. Изопропилацетат затем отгоняют.
Эта дистилляция может иметь место при температуре ниже около 35°C и может располагаться от около 25 до около 35°C.
На стадии (d) способа настоящего изобретения, осадок растворяют в растворе метанола и изопропилацетата. Это разбавление может иметь место при комнатной температуре. При желании раствор может быть отобран с полиморфной формой V гидрохлорида лерканидипина. Полиморфная форма V гидрохлорида лерканидипина может быть получена способом, обсужденным выше. В течение отбора раствор может перемешиваться при около 15 до около 18 оборотов в минуту (об/мин). Кристаллизация может иметь место при комнатной температуре в течение от около 20 часов до около 28 часов и предпочтительно в течение около 24 часов. Твердые частицы тогда отфильтровывают и необязательно промывают изопропилацетатом.
На стадии (e) способа настоящего изобретения твердые частицы высушивают для получения по существу чистого гидрохлорида лерканидипина. Твердые частицы могут быть высушены при температуре в пределах от около 50°C до около 55°C.
Другой вариант осуществления настоящего изобретения обеспечивает способ для очистки гидрохлорида лерканидипина. Было обнаружено, что использование спиртосодержащего растворителя, например, метанола и эфирсодержащего растворителя, например изопропилацетата может быть очень эффективным по существу в удалении примесей, обнаруженных в гидрохлориде лерканидипина, особенно примеси 2-[N-(3,3-дифенилпропил)-N-метиламино]-1,1-диметилэтилпропилового диэфира l,4-дигидро-2,6-диметил-4-(3-нитрофенил)пиридин-3,5-дикарбоновой кислоты, обсужденной выше. Способ включает, по меньшей мере, растворение неочищенного гидрохлорида лерканидипина в спиртосодержащем растворителе, таком как метанол, добавление алифатического эфирсодержащего растворителя, такого как изопропилацетата и затем выделение по существу чистого гидрохлорида лерканидипина, например, кристаллизацией, как обсуждено выше.
В еще другом варианте осуществления настоящего изобретения способ очистки гидрохлорида лерканидипина включает, по меньшей мере, стадии (a) первое растворение, (b) второе растворение, (c) кристаллизация и (d) высушивание. На стадии (a) способа очистки этого варианта осуществления настоящего изобретения гидрохлорид лерканидипина по существу растворяют в спиртосодержащем растворителе, таком как C1-C8 спирт, например метанол, этанол, изопропанол, бутанол и т.п., и их смеси. Обычно спиртосодержащий растворитель присутствует в отношении около 1:1 объем/вес по отношению к гидрохлориду лерканидипина. Гидрохлорид лерканидипина и спиртосодержащий растворитель может быть нагрет до температуры в пределах от около 40°C до около 65°C в течение периода времени в пределах от около 20 минут до около 1 часа. Раствор может затем быть охлажден до комнатной температуры, температура в пределах от около 25°C до около 30°C.
На стадии (b) способа очистки этого варианта осуществления настоящего изобретения разбавление далее включает добавление к раствору алифатического эфирсодержащего растворителя такого, как эфирная группа, имеющая от около 2 до около 12 углеродных атомов, например изопропилацетата. Алифатический эфирсодержащий растворитель может присутствовать в отношении около 10:1 объем/вес по отношению к гидрохлориду лерканидипина. Алифатический эфир может быть добавлен при комнатной температуре, температура в диапазоне от около 25°C до около 30°C.
На стадии (с) способа очистки этого варианта осуществления настоящего изобретения раствор может перемешиваться при температуре в пределах от около 25°C до около 30°C. Раствор может перемешиваться от около 60 оборотов в минуту до около 100 оборотов в минуту в течение периода времени в пределах от около 12 часов до около 20 часов. Полученное твердое вещество может тогда быть выделено стандартными методами, например фильтрацией, и необязательно промыто подходящим растворителем, таким как изопропилацетат (около 1:1 объем/вес, изопропилацетат: гидрохлорид лерканидипина) для получения кристаллов гидрохлорида лерканидипина.
На стадии (d) способа очистки этого варианта осуществления настоящего изобретения кристаллы могут быть высушены при температуре в пределах от около 50°C до около 55°C, до тех пор пока LOD будет не меньше, чем около 10% за период времени от около 6 до около 12 часов и предпочтительно через около 8 часов.
Выполняя способы очистки настоящего изобретения, по существу чистый гидрохлорид лерканидипина может быть получен со степенью чистоты, большей чем или равной около 98,5%, предпочтительно больше чем или равной около 99,5% и более предпочтительно больше чем или равной около 99,7%. Чистота гидрохлорида лерканидипина настоящего изобретения может быть определена любым методом, известным в данной области техники, например анализ с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ).
Другой вариант осуществления настоящего изобретения обеспечивает способ получения гидрохлорида аморфной формы лерканидипина. Было обнаружено, что очищенный гидрохлорид лерканидипина в подходящем органическом растворителе, таком как спиртосодержащий растворитель, например, метанол, который объединен с осветляющим веществом, таким как активированный уголь и затем смешан с водой, является предпочтительно эффективным при получении гидрохлорида аморфного лерканидипина с никаким значительным изменением в профиле распределения примесей. Обычно способ включает, по меньшей мере, (a) растворение очищенного гидрохлорида лерканидипина, как получено выше, в органическом растворителе, (b) обработка раствора осветляющим веществом для получения осветленного раствора и (c) выделение гидрохлорида аморфной формы лерканидипина. В одном варианте осуществления очищенный гидрохлорид лерканид