4-гетеро-16 , 17 -циклогексанопрегнаны
Иллюстрации
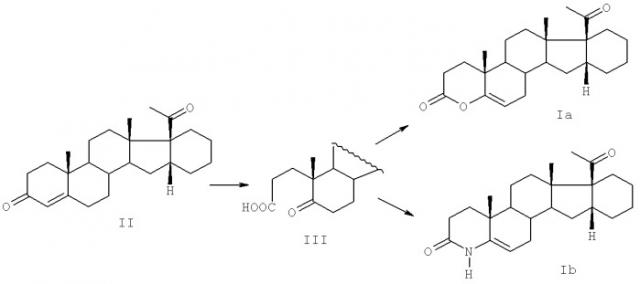
Показать всеИзобретение относится к новым 4-окса- и 4-аза-16α,17α-циклогексанопрегнанам (4-окса- и 4-аза-прегна-D′-пентаранам), которые могут найти применение в медицине для лечения злокачественных опухолей, общей формулы I
где Х=0 или NR, R=R1=R2=R4=H, при этом R1+R3 образуют связь. Указанные соединения получают путем окисления кольца А 16α,17α-циклогексанопрогестерона перманганатом калия и периодатом натрия в присутствии карбоната натрия в 5-оксо-А-нор-3,5-секокислоту с последующим замыканием кольца А в последней в 4-окса-16α,17α-циклогексанопрегн-5-ен-20-он при обработке дегидратирующим агентом ацетатом натрия в Ac2O и в 4-аза-16α,17α-циклогексанопрегн-5-ен-20-он действием ацетата аммония в уксусной кислоте. Полученные соединения являются эффективными ингибиторами эстроген-стимулированной пролиферации клеток HeLa. 1 з.п. ф-лы, 1 табл.
Реферат
Изобретение относится к области химии природных и физиологически активных веществ, а именно к области стероидных гормонов, содержащих гетероатом в стероидном ядре, конкретно к новым 4-окса- и 4-аза-16α,17α-циклогексанопрегнанам (4-окса- и 4-аза-прегна-D′-пентаранам), которые могут найти применение в медицине для лечения злокачественных опухолей.
Известно, что стероиды, содержащие гетероатом(ы) в стероидном скелете, могут обладать различными видами биологической (гормональной и негормональной) активности в зависимости от особенностей структуры и типа стероида [М. Ibrahim-Quali. Recent advances in oxasteroid chemistry. Steroids, 2007, 72, 475; Recent advances in azasteroid chemistry. Steroids, 2008, 73, 375]. Современной терапии гормонозависимых опухолей нужны препараты, останавливающие неконтролируемую пролиферацию (рост) раковых клеток. Наряду с различными цитостатическими препаратами для этой цели широко используются прогестины и антипрогестины - модуляторы рецептора прогестерона (РП). Среди них перспективную группу представляют прегна-D′-пентараны - производные прогестерона с дополнительным карбоциклом D′ в 16α,17α-положениях стероидного скелета, обладающие прогестагенной и антипрогестагенной активностями in vivo и пригодные для перорального применения.
Наиболее близким по структуре и свойствам является 16α,17α-циклогексанопрогестерон II, который является активным прогестином, но его антипролиферативное действие невелико [А.В. Камерницкий, И.С. Левина. Прегна-D′-пентараны. Прогестины и антипрогестины. Биоорган. химия, 2005, т.31, c.115 и 227]. Но среди этих описанных стероидов неизвестны пентараны, содержащие гетероатом в кольце А.
Задачей настоящего изобретения является создание новых стероидов, содержащих гетероатом в положении 4 кольца А и шестичленное кольцо D′ в 16α,17α-положениях стероидного скелета, обладающих сродством к рецептору прогестерона и проявляющих антипролиферативную (ингибирующую рост раковых клеток) активность.
Поставленная задача достигается новыми 4-окса- и 4-аза-16α,17α-циклогексанопрегнанами общей формулы I
где X=O или NR, R=H, низший алкил, R1=R2=H или R1+R2 образуют связь, R1=R3=R4=H или R1+R3 образуют связь, и при этом R4=Н.
Предлагаемые соединения получают путем окисления кольца А 16α,17α-циклогексанопрогестерона II перманганатом калия и периодатом натрия в присутствии карбоната натрия в 5-оксо-А-нор-3,5-секокислоту III с последующим замыканием кольца А в последней в 4-оксастероид Iа при обработке дегидратирующим агентом ацетатом натрия в Ac2O и в 4-азастероид Ib действием ацетата аммония в уксусной кислоте по следующей схеме:
Строение полученных соединений подтверждено данными элементного анализа, масс- и ЯМР 1Н и 13С спектрами.
Эффект замещения атома углерода в положение 4 на гетероатом в молекуле пентарана на связывание был апробирован по способности полученных соединений Ia и Ib взаимодействовать с РП цитозоля матки крысы. Для оценки сродства применили конкурентный анализ (вытеснение из комплексов с белками [3H]прогестерона II. Средние величины относительной конкурентной активности (ОКА) с применением в качестве стандарта высокоэффективного прогестина ряда пентаранов 16α,17α-циклогексанопрогестерона II, который можно рассматривать как базовую структуру для заявленных соединений, представлены в таблице.
| №№ | Соединение | ОКА, % |
| П | Прогестерон | 93±8 (8)* |
| II | 16α,17α-Циклогексанопрогестерон | 100 |
| Iba | 16α,17α-Циклогексано-4-оксапрегн-5-ен-3,20-дион | 0.72±0.21 (8) |
| Ib | 16α,17α-Циклогексано-4-азапрегн-5-ен-3,20-дион | 0.84±0.26 (8) |
| * Среднее ± стандартное отклонение. В скобках - количество измерений. |
Влияние пентаранов Ia и Ib на жизнеспособность опухолевых клеток изучено на клеточной линии рака шейки матки HeLa. Для проведения эксперимента суспензию клеток помещали в 96-луночный планшет. Исследуемые вещества растворяли в диметилсульфоксиде до концентрации 10-2 М, затем на среде инкубации до конечных концентраций в культуре 10-6 и 10-5 М. Во все лунки (кроме «чистого» контроля) также вносили эстрадиол до конечной концентрации 10-8 М и инкубировали в течение 6 суток. Жизнеспособность клеток оценивали по цветной реакции живых клеток с тетразолиевым красителем МТТ. Оптическую плотность контрольных образцов принимали за 100%-ную выживаемость клеток. Величина эстроген-стимулированной пролиферации рассчитывалась как разница между жизнеспособностью клеток контроля с эстрогеном (10-8 М эстрадиол) и в его отсутствие. Оба соединения Ia и Ib в исследованных дозах оказались эффективными ингибиторами эстроген-стимулированной пролиферации клеток HeLa: они на 90-100% ингибируют жизнеспособность клеток.
Пример 1
К раствору 1.105 г (3 ммоля) 16α,17α-циклогексанопрегн-4-ен-3,20-диона II в смеси 40 мл третбутанола и 3 мл 40% водного Na2CO3 прибавляют при 60°С раствор 5.6 г (26.18 ммоллей) NaJO4 и 0.18 г (1.13 ммолей) KMnO4 в 25 мл воды и выдерживают при этой температуре 3 ч. Затем реакционную смесь охлаждают до 30°С и через 15 мин твердый осадок отфильтровывают, промывают на фильтре водой и объединенные фильтраты упаривают. Водный остаток подкисляют (рН 2) 6 М HCl, экстрагируют CH2Cl2, органический экстракт промывают водой и сушат Na2SO4. После удаления растворителя получают 1.04 г (90%) секокислоты в виде бесцветной пены, которую используют в следующей стадии без дополнительной очистки. Часть кислоты очищают хроматографически на колонке. Элюирование смесью петр.эфир-ацетон - CH2Cl2 (85:10:5) дает кристаллическую секокислоту III с т.пл. 179-182°С (из смеси эфир-гексан). ИК-спектр (CHCl3), √см-1: 3600-3000, 1692. Спектр ЯМР 1H (δ, м.д., J/Гц): 0.75 (с, 3Н, Ме (18)); 1.15 (с, 3Н, Ме (19)); 2.15 (с, 3Н, Ме (21)); 3.0 (с, 1Н, 16Н).
Смесь 0.39 г (1 ммоль) кетокислоты III и 0.82 г (10 ммолей) высушенного при 180°С AcONa в 10 мл Ас2О кипятят 4 ч. К остатку после удаления Ac2O добавляют EtOAc и Н2О, органический слой промывают насыщенным раствором NaCl, сушат Na2SO4 и растворитель удаляют в вакууме. Остаток очищают хроматографически. При элюировании смесью петр.эфир-ацетон (93:7) получают 0.198 г (53%) кристаллического 4-оксастероида Ia с т.пл. 158-160°С (из смеси ацетон-гексан). Найдено (%): С, 77.94; Н, 8.99. С24Н34О3. Вычислено (%): С, 77.80; Н, 9.25. Спектр ЯМР 1Н (δ, м.д., J/Гц): 0.72 (с, 3Н, Ме (18)); 1.12 (с, 3Н, Ме (19)); 2.14 (с, 3Н, Ме (21)); 2.97 (с, 1Н, 16Н); 5.25 (д, 1Н, Н (6)).
Пример 2
Полученную аналогично примеру 1 кетокислоту III (0.34 г, 0.87 ммоля) и 0.40 г (5.2 ммоля) AcONH4 в 10 мл лед.АсОН кипятят 6 ч. К остатку после удаления АсОН добавляют воду, выпавший коричневый порошок отфильтровывают, промывают водой и сушат на воздухе. После хроматографической очистки на колонке (элюирование смесью петр.эфир-ацетон 90:10→88:12) выделяют 0.21 г (65%) кристаллического 4-азастероида Ib с т.пл. 305-308°С (из смеси ацетон-гексан). Спектр ЯМР 1Н (δ, м.д., J/Гц): 0.72 (с, 3Н, Ме (18)); 1.10 (с, 3Н, Ме (19)); 2.14 (с, 3Н, Ме (21)); 2.97 (с, 1Н, 16Н); 4.85 (м, 1Н, Н (6)); 7.85 (шир. с, 1Н, NH).
Пример 3. Метод определения связывания соединений Ia и Ib с РП цитозоля матки крысы
В работе используют половозрелых девственных самок крыс смешанной популяции массой 200-250 г. Животным вводят внутримышечно эстрадиол по 10 мкг в 200 мкл пропиленгликоля ежедневно на протяжении 4-х дней и их забивают декапитацией на 5-й день. Матки измельчают и гомогенизируют в стеклянном гомогенизаторе при 0-4°С в течение 5 мин в буферном растворе, содержащем 10 мМ Трис-HCl (рН 7.5), 10 мМ KCl, 1 мМ EDTA, 0.5 мМ фенилметилсульфонилфторид (PMSF), 1 мМ дитиотреит, 10% глицерин, при весовом соотношении ткань/буфер 1:6. Гомогенат центрифугируют при 4°С в течение 1 ч при 50000g. Надосадочную фракцию (цитозоль) с концентрацией белка 4-6 мг/мл используют немедленно. Используют [1,2,6,7-3H]прогестерон с удельной радиоактивностью 86 Ки/ммоль (Санкт-Петербург).
Измерение относительной конкурентной активности (ОКА) стероидов для РП проводят с применением [3H]прогестерона в присутствии 3 мкМ гидрокортизона. Цитозоль матки (100 мкл) инкубируют при 0-4°С в течение 20 ч со 100 мкл смеси стероидов в буфере, включающей (60-80)·103 имп./мин (конечная концентрация 3-6 нМ) [3H]лиганда и немеченый конкурент (конечные концентрации от 0 до 10 мкМ). Связанный белком и свободный лиганд разделяют инкубацией со 100 мкл 2% суспензии активированного угля Norit A (Serva, Германия), покрытого декстраном-70 (Fluka, Швейцария) в течение 5 мин при 0-4°С. После центрифугирования в течение 5 мин при 3000g отбирают аликвоты (250 мкл) надосадочной фракции для измерения радиоактивности. Инкубацию проводят в кварцевых пробирках, покрытых BSA. Радиоактивность измеряют с использованием диоксанового сцинтиллятора при эффективности счета 20%. Содержание белка определяют с помощью красителя Кумасси синего. Все измерения проводят в двух параллельных образцах. Каждый эксперимент воспроизводят 3-4 раза. Безразмерные величины ОКА рассчитывают по соотношению Kd для прогестерона и сравниваемого лиганда, полученных в отдельных экспериментах, и рассчитанные величины ОКА усредняют.
Пример 4. Оценка влияния заявляемых соединений на жизнеспособность клеточной линии рака шейки матки HeLa
Культивирование клеток HeLa осуществляют в стерильных условиях с использованием ламинарбокса ЛБ-В (Россия). Клетки инкубируют при 37°С в условиях 5% CO2. При культивировании клеток используют стандартную среду DMEM с добавлением 10% эмбриональной телячей сыворотки, L-глутамина в концентрации 100 мкг/мл и антибиотика гентамицина сульфата в концентрации 40 мкг/мл. Клетки выращивают при 37°С в присутствии 10-8 М эстрадиола на среде DMEM, содержащей 10% эмбриональной телячьей сыворотки. Для проведения эксперимента суспензию клеток помещают в 96-луночный плоскодонный планшет. Исследуемые вещества растворяют в диметилсульфоксиде до концентрации 10-2 М, затем в среде инкубации до конечных концентраций в культуре 10-6-10-5 М. Концентрация диметилсульфоксида в культуре клеток составляет 10-3-10-6 М. Во все лунки также вносят эстрадиол до конечной концентрации 10-8 М, кроме чистого контроля. Инкубируют в течение 6 суток, после чего результаты учитывают методом МТТ. Оптическую плотность образцов регистрируют при длине волны 530 нм на анализаторе "УНИПЛАН" АИФР-01 (Россия). Оптическую плотность контрольных образцов в присутствии только эстрадиола принимают за 100%-ную выживаемость клеток.
Таким образом, как видно из вышеописанных примеров, получены новые 4-окса- и 4-аза-16α,17α-циклогексанопрегнаны Ia и Ib, которые связываются с рецептором прогестерона матки крысы и являются высокоэффективными ингибиторами роста раковых клеток, т.е. проявляют высокую антипролиферативную активность. Заявленные соединения могут представить интерес в медицине в качестве противоопухолевых средств, например, при лечении гормонозависимых раковых заболеваний.
1. 4-Гетеро-16α,17α-циклогексанопрегнаны общей формулы I где Х-О или NR, R=R1=R2=R4=Н, при этом R1+R3 образуют связь.
2. Соединения по п.1, 16α,17α-циклогексано-4-оксапрегн-5-ен-3,20-дион и 16α,17α-циклогексано-4-азапрегн-5-ен-3,20-дион, обладающие сродством к рецептору прогестерона и антипролиферативной активностью.