Стерилизующая среда, способ получения стерилизующей среды, способ стерилизации упаковочного материала для упаковки пищи и применение композиции распределяющего агента в стерилизующей среде
Иллюстрации
Показать всеСтерилизующая среда состоит из водного раствора пероксида водорода и добавочной композиции распределяющего агента, содержащего лецитиновое соединение и неионогенный эмульгатор. Изобретение также относится к способу получения стерилизующей среды, способу стерилизации слоистого упаковочного материала или контейнера для упаковывания пищи и применению лецитинового соединения вместе с неионогенным эмульгатором в качестве добавочной композиции распределяющего агента в водном растворе пероксида водорода для стерилизации упаковочного материала или контейнеров для упаковывания пищи. В способе получения стерилизующей среды в водный раствор пероксида водорода добавляют эмульсию добавочного лецитинового распределяющего агента и неионогенного эмульгатора, затем компоненты перемешивают. Способ стерилизации упаковочного материла или контейнера состоит в использовании стерилизующей среды, содержащей водный раствор пероксида водорода и добавочную композицию распределяющего агента. Изобретение обеспечивает повышение эффективности и надежности стерилизации и повышение производительности. 4 н. и 15 з.п. ф-лы, 18 ил., 1 табл.
Реферат
ОБЛАСТЬ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к стерилизующей среде для стерилизации упаковочного материала для упаковки пищи, содержащей водный раствор пероксида водорода и добавочную композицию распределяющего агента. Изобретение также относится к способу получения стерилизующей среды, способу стерилизации слоистого упаковочного материала или контейнера из него для упаковки пищи и к применению композиции распределяющего агента в стерилизующей среде, содержащей пероксид водорода, для стерилизации упаковочного материала или контейнеров для упаковки продуктов.
ПРЕДШЕСТВУЮЩИЙ УРОВНЕНЬ ТЕХНИКИ И ПРОБЛЕМЫ
При производстве асептически упакованной пищи взаимодействует несколько факторов с целью получения пищевого продукта, который может храниться на складе в течение длительного времени без ухудшения вкуса и питательных качеств. Важно, чтобы пищевой продукт как таковой являлся стерильным до такой степени, чтобы микроорганизмы не размножались в течение длительного хранения, чтобы заполнение продуктом упаковки выполнялось в асептических условиях в чистых машинах в чистой производственной среде и чтобы сама упаковка была способна сохранять продукт от действия окружающей влажности, света, кислорода и бактерий в течение длительного времени. Большое значение имеет, конечно, то, что упаковочный материал или упаковка являются стерильными, т.е. не содержащими микроорганизмов, в момент заполнения их пищевым продуктом. Стерилизация упаковочных машин, упаковочного материала или упаковок для заполнения продуктом может достигаться различными способами, например, посредством применения химической стерилизующей жидкости или газофазными средами на поверхностях, требующих стерилизации, посредством ультрафиолетового облучения или облучения электронным пучком, или сочетанием таких способов. Разумеется, тщательная промывка в первую очередь и ополаскивание стерильной водой также значительно влияют на полученную асептическую среду в упаковочной машине.
Одноразовые упаковочные контейнеры для жидких продуктов и текучих продуктов с высокой вязкостью часто производят из упаковочного слоистого материала, содержащего внутренний слой бумаги или картона и внешние, непроницаемые для жидкости, термосклеивающиеся слои полиолефина. Часто встречающиеся такие упаковочные контейнеры являются маркироваными, например, под товарными знаками Tetra Brik Aseptic® или Tetra Classic Aseptic®, и используются главным образом для жидких продуктов, таких как молоко, фруктовые соки и т.д. Упаковочным материалом в этих известных упаковочных контейнерах обычно является слоистый материал, содержащий основной внутренний слой из бумаги или картона и внешние непроницаемые для жидкости слои из термопластиков. С целью придания упаковочному контейнеру свето- и газонепроницаемости, в частности, непроницаемости для кислорода, например, с целью асептической упаковки и упаковки фруктовых соков, слоистый материал для таких упаковочных контейнеров содержит, как правило, по меньшей мере, один добавочный слой, наиболее часто алюминиевой фольги, который, кроме того, делает упаковочный материал термосклеивающимся посредством индуктивного термосклеивания, которое является быстрым и эффективным методом получения механически прочных, непроницаемых для жидкости и газа уплотнительных соединений или швов в процессе производства контейнеров. С внутренней стороны слоистого материала, т.е. стороны, предназначенной быть обращенной к содержимому контейнера, полученного из слоистого материала, имеется самый крайний слой, прилегающий к алюминиевой фольге, который может состоять из нескольких отдельных слоев, содержащих адгезивные полимеры и/или полиолефины.
Такие упаковочные контейнеры получают, как правило, при помощи современных упаковочных машин, которые формируют, заполняют и заклеивают упаковки из рулона или из стандартных заготовок упаковочного материала. Из рулона, например, упаковочные контейнеры получают таким образом: рулон преобразуется в трубку посредством соединения внахлест одного с другим обоих продольных краев рулона. Трубку заполняют внутри жидким пищевым продуктом и разделяют на индивидуальные упаковки посредством повторяющихся поперечных склеиваний трубки с расстоянием от одного до другого ниже уровня содержимого трубки. Упаковки отделяют от трубки посредством разрезания поперечных соединений и придают требуемую геометрическую конфигурацию, обычно в форме параллелепипеда или тетраэдра, посредством складывания вдоль заранее готовых линий сгиба упаковочного материала.
Перед формированием трубки и заполнением трубки продуктом, рулон обычно проходит через ванну с жидким стерилизующим агентом. Так называемые отжимные резиновые валики удаляют излишек стерилизующей жидкости посредством отжимания ее из рулона перед тем, как трубка высушивается горячим стерильным воздухом. Другими способами стерилизации такой трубки из упаковочного материала, кроме простого погружения рулона посредством проведения его через глубокую ванну стерилизующей среды, являются распыление, конденсация газовой фазы или, наиболее часто, покрытие рулона упаковочного материала при помощи ролика для равномерного нанесения жидкости на поверхность рулона упаковочного материала.
Одним из наиболее часто используемых стерилизующих агентов, который является пригодным и для жидких, и для газофазных стерилизующих сред, является пероксид водорода H2O2. Обычно для применения в пищевой промышленности пероксид водорода используется в форме водного раствора с концентрацией приблизительно 35 масс.%, но также возможны более высокие концентрации, например, вплоть до 50 масс.%. Также часто применяют другие стерилизующие агенты, такие как перуксусная кислота.
Эффект стерилизации в большой степени зависит от способности стерилизующей среды равномерно распространяться по стерилизуемой поверхности и свойства смачивания конкретной поверхности. Когда поверхностное натяжение слишком высокое, стерилизующая среда образует более крупные капли и не распределяется равномерно по поверхности. Имеются две главных проблемы, возникающие вследствие этого. Первой проблемой является то, что стерилизация будет менее эффективной, поскольку стерилизующий агент не действует на всю поверхность и поскольку слишком много стерилизующей среды применяется в участках с большими каплями и слишком мало в участках между ними. Второй проблемой является то, что остатки стерилизующей среды будут оставаться на поверхности после стерилизации, поскольку капли большего размера сложно удовлетворительно удалить при высокой скорости производства в упаковочной машине.
Две проблемы связаны друг с другом, поскольку лучшее распределение пероксида водорода по рулону будет способствовать испарению капель при высушивании и, следовательно, приводить к уменьшению количества остатков пероксида в упаковках.
Эти две проблемы еще более выражены при высокой скорости производства, поскольку стерилизующий агент тогда имеет только минимум времени для воздействия на стерилизуемую поверхность и должен быть очень быстро удален перед наполнением упаковки пищевым продуктом. Проблема также особенно выражена, когда стерилизуемая поверхность является слишком ровной и гладкой, как в случае наличия определенных свойств у пленки, используемой в качестве крайнего слоя упаковочного слоистого материала. Например, для продуктов с высокой вязкостью требуется крайняя поверхность материала, обращенная внутрь упаковочного контейнера, к которой не будут прилипать вязкие пищевые продукты, с целью облегчить опорожнение упаковки. Естественно, стерилизующий агент также не распределяется и не остается равномерно нанесенным на такую «нелипкую» поверхность. Также, пленка с определенными свойствами, применяемая для внутренней полоски, прикрепленной к самому внутреннему слою, для покрытия продольного шва внутри упаковки, имеет такие характеристики несмачивания. Хотя возможно держать процесс стерилизации под строгим контролем для достижения достаточной и адекватной стерилизации с применяемой в настоящее время стерилизующей средой с пероксидом водорода, желательно иметь более широкий интервал действия для учитываемых параметров, таких как скорость производства и время контакта, температура и концентрация стерилизующего агента.
Долгое время было известно, что для устранения до некоторой степени этих проблем можно применять смешивание водного раствора пероксида водорода с неионогенным смачивающим агентом, называемым "Tween™ 20" полиэтиленгликоль 20 сорбитана монолаурат. Некоторый эффект распространения по поверхности был получен, но сохранялась возможность для улучшения, особенно для производства с высокой скоростью и в тех случаях, когда сложно контролировать вариации в условиях производства.
Из EP 1384670 известно применение смачивающих агентов, т.е. или сложных эфиров жирных кислот, или лецитина, в водном стерилизующем растворе стерилизующего агента на основе хлорина, содержащего гипохлористую кислоту. Однако достаточный стерилизационный эффект при коротком времени контакта будет возможен только в том случае, если способ стерилизации также включает термическую стерилизацию.
Из US 5858933 известно, что применение химически модифицированного лецитина в комбинации со сложным эфиром жирной кислоты в качестве смазочной добавки для покрытия бумажного рулона клеевым покрытием во время производства бумаги, приводя к улучшению свойств покрытия вследствие улучшенного контроля вязкости, улучшенной способности поддаваться обработке и меньшим проблемам покрытия, таким как кальцификация, образование царапин или отделение волокон и т.д. Эти свойства зависят от того, насколько хорошо частицы и пигменты распределены в покрывающей композиции.
Из US 4200551 дополнительно известно об улучшении способности диспергировать немодифицированного исходного лецитина в воде посредством добавления неионогенного эмульгатора.
Однако до настоящего времени не рассматривалась возможность применения этих свойств лецитиновых соединений при создании пригодной добавочной композиции распределяющего агента для водных стерилизующих сред на основе пероксида водорода.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Следовательно, целью настоящего изобретения является преодоление или уменьшение вышеописанных проблем.
Основной целью изобретения является получение стерилизующей среды на основе пероксида водорода, которая имеет улучшенные свойства распределения по стерилизуемой поверхности.
Следовательно, целью является получение стерилизующей среды на основе пероксида водорода, которая является более эффективной и может повышать надежность процесса стерилизации, т.е. является менее чувствительной к изменениям режима процесса, и, таким образом, также хорошо функционирует при более высоких скоростях производства в упаковочной машине. Более конкретно, целью является получение стерилизующей среды на основе пероксида водорода, которая имеет улучшенный стерилизующий эффект. Конкретной целью предпочтительного варианта осуществления изобретения является получение стерилизующей среды на основе пероксида водорода, которая имеет стерилизующий эффект, оптимизированный в отношении смачивания и расхода стерилизующей среды.
Дополнительной конкретной целью изобретения является получение стерилизующей среды на основе пероксида водорода, которая оставляет сниженное количество остатков на поверхности после стерилизации.
Еще одной дополнительной целью изобретения является получение стерилизующей среды на основе пероксида водорода, которая хорошо функционирует на ровных и гладких поверхностях с низкой смачиваемостью.
Эти цели достигаются в соответствии с настоящим изобретением при помощи стерилизующей среды на основе пероксида водорода, как определено в п.1. Предпочтительные варианты осуществления стерилизующей среды по настоящему изобретению определены в пп.2-11.
Эти цели достигаются, таким образом, в соответствии с настоящим изобретением с применением стерилизующей среды, содержащей водный раствор пероксида водорода и добавочную композицию распределяющего агента, содержащую соединение, выбранное из группы, состоящей из лецитина и химически модифицированного лецитина, и дополнительно содержащую неионогенный эмульгатор.
Наиболее часто используемым стерилизующим агентом является пероксид водорода вследствие его превосходного бактерицидного действия и его сравнительно низкой стоимости и хороших санитарных характеристик и характеристик безопасности, в связи с применением в пищевой промышленности. Водные растворы пероксида водорода с концентрацией до 50 масс.% являются допустимыми для этого изобретения, а растворы с концентрацией до приблизительно 35 масс.% являются коммерчески доступными для применения в пищевой промышленности. Предпочтительно в стерилизующей среде в соответствии с изобретением применяется концентрация от 30 до 40 масс.%, более предпочтительно 35 масс.%.
Лецитин считается хорошо переносимым и нетоксичным поверхностно-активным веществом. Он одобрен Управлением по контролю качества пищевых продуктов и лекарственных средств Соединенных штатов для употребления человеком со статусом «Признанный полностью безвредным» (GRAS) и также одобрен ЕС в качестве пищевой добавки. В биохимии лецитин, как правило, применяется в качестве синонима фосфатидилхолина, фосфолипида, который является главным компонентом фосфатидной фракции, который может быть выделен из яичного желтка или соевых бобов. Промышленный лецитин представляет собой смесь фосфолипидов в масле. Основными фосфолипидами в лецитине из соевого или подсолнечного масла являются фосфатидилхолин, фосфатидилинозитол, фосфатидилэтаноламин и фосфатидная кислота. Для улучшения характеристик лецитинов они должны быть химически модифицированы.
Пригодные химически модифицированные лецитины для настоящего изобретения в норме способны более быстро диспергироваться в воде, чем исходный лецитин, и обычно имеют йодное число (I.V.) менее 50. Йодное число представляет собой количество этиленовых непредельных связей в молекуле рассматриваемого вещества. Химические модификации, как правило, вводят гидрофильные замещающие группы в сложноэфирные группы жирной кислоты, которые, в свою очередь, делают лецитин более гидрофильным. Предпочтительно такие химически модифицированные лецитины являются гидроксилированными или ацетилированными лецитинами, омыленными гидроксилированными лецитинами или их смесью. Другие химически модифицированные лецитины могут быть получены посредством реакций с ферментами, такими как липаза. Более предпочтительно химически модифицированный лецитин в соответствии с изобретением является гидроксилированным лецитином.
Было, однако, неожиданно обнаружено, что также немодифицированный, исходный лецитин очень хорошо диспергируется и действует в водных растворах пероксида водорода. Вероятно, это происходит вследствие химического реагирования или взаимодействия между немодифицированным лецитином и водным раствором пероксида водорода таким образом, что первоначально немодифицированный лецитин фактически в результате становится химически модифицированным, наиболее вероятно, гидроксильными группами, как гидроксилированный лецитин.
Хотя лецитиновое соединение может до некоторой степени использоваться как единственный распределяющий агент для стерилизующей среды, содержащей водный раствор пероксида водорода, неожиданно было обнаружено, что при комбинации композиции распределяющего агента и неионогенного эмульгатора, способность к растеканию стерилизующей среды на основе пероксида водорода значительно возрастает. Предпочтительно неионогенный эмульгатор представляет собой полиоксиалкиленовое производное глицерида жирной кислоты или полиоксиалкиленовое производное частичного сложного эфира жирной кислоты или смесь таких эмульгаторов. Типичными примерами полиоксиалкиленовых производных частичных сложных эфиров жирных кислот и гекситных ангидридов являются РОЕ (полиоксиэтилен) 20 сорбитан моностеарат, РОР (полиоксипропилен) 20 сорбитан моностеарат, РОЕ 20 сорбитан тристеарат, РОЕ 10 сорбитан дистеарат, РОЕ 15 маннитан монопальмитат, РОЕ 10 маннитан димиристат, РОЕ 20 сорбитан диолеат, РОЕ 20 сорбитан моноолеат, РОЕ 20 сорбитан триолеат, РОЕ 20 галактитан моностеарат, РОЕ 20 галактитан диолеат, РОЕ 30 сорбитан моностеарат, РОЕ 20 монолаурат, РОЕ 20 сорбитан монопальмитат, РОЕ 5 сорбитан моноолеат и тому подобное. Полиоксиалкиленовые производные моно- и диглицеридов жирных кислот соответствуют следующей формуле
(I) CH2(R2)CH(R3)CH2(R4)
в которой по меньшей мере два из членов (R2), (R3) и (R4) выбраны из группы, состоящей из сложных эфиров жирных кислот, имеющих по меньшей мере 12 атомов углерода, и молекул полиоксиэтилена, представленных формулой
-(-OCH2CH(Y)-)n-OY,
в которой n представляет среднее число повторяющихся оксиалкиленовых единиц, Y представляет собой или водород, или метильную группу и оставшийся член композиции R1, R2 или R3 формулы (I) является или гидроксильной, или полиоксиалкиленовой группой, или сложным эфиром жирной кислоты.
Более предпочтительно неионогенный эмульгатор представляет собой алкоксилированный сложный эфир жирной кислоты и сорбитана, наиболее предпочтительно полиэтиленгликоль 20 сложный эфир жирной кислоты и сорбитана. Предпочтительным хорошо функционирующим примером является полиэтиленгликоль 20 сорбитана монолаурат, также называемый «Tween™ 20». Было обнаружено, что стерилизующая среда должна предпочтительно содержать от 0,1 до 0,4 масс.% немодифицированного или химически модифицированного лецитина. При концентрации свыше 0,4 масс.% стерилизующая среда становится маслянистой и более трудно удаляется со стерилизуемой поверхности при высушивании. При концентрации лецитина менее 0,1 масс.% расход или потребление стерилизующего агента, т.е. пероксида водорода, снижается, т.е. слишком малое количество пероксида водорода переносится на стерилизуемую поверхность, и стерилизующий эффект слишком низкий для того, чтобы являться надежным.
Лецитиновое соединение смешивают с неионогенным эмульгатором, дополнительно улучшая таким образом распределение, и предпочтительно концентрация неионогенного эмульгатора в стерилизующей среде должна составлять от 0,1 до 0,3 масс.%. Оптимально, если стерилизующая среда содержит от 0,2 до 0,3 масс.% химически модифицированного лецитина и от 0,1 до 0,2 масс.% неионогенного эмульгатора. Абсолютно наилучшая и оптимально предпочтительная стерилизующая среда содержит приблизительно 0,3 масс.% химически модифицированного лецитина и от 0,1 до 0,2 масс.% неионогенного эмульгатора. Иначе говоря, добавочная композиция распределяющего агента должна наиболее предпочтительно содержать от 60 до 75 масс.% химически модифицированного лецитина и от 25 до 40 масс.% неионогенного эмульгатора при расчете на общую массу композиции распределяющего агента.
В соответствии с другим аспектом изобретения стерилизующую среду на основе пероксида водорода в соответствии с изобретением получают посредством добавления вначале добавочного соединения распределяющего агента, выбранного из группы, состоящей из лецитина и химически модифицированного лецитина в водном растворе пероксида водорода или деионизированной воды при массовом отношении от 1:5 до 1:20, предпочтительно приблизительно 1:10, взбалтывая смесь для получения стабильной эмульсии, добавляя полученную таким образом водную эмульсию лецитина и распределяющего агента к водному раствору стерилизующей среды с пероксидом водорода, добавляя на некоторых этапах неионогенный эмульгатор и в заключение взбалтывая для получения стабильной стерилизующей среды на основе пероксида водорода. Для конечного результата не является особенно важным, на какой стадии был добавлен неионогенный эмульгатор, но предпочтительно неионогенный эмульгатор сначала добавляют в добавочную лецитиновую эмульсию распределяющего агента для получения добавочной композиции распределяющего агента. В качестве альтернативы, неионогенный эмульгатор может быть добавлен непосредственно в водную стерилизующую среду на основе пероксида водорода в форме самостоятельной стабильной водной эмульсии. В соответствии с третьим аспектом изобретения описан способ стерилизации упаковочного материала или контейнера для упаковки пищи посредством применения стерилизующей среды по настоящему изобретению на стерилизуемой поверхности. В соответствии с одним из предпочтительных вариантов осуществления способа по настоящему изобретению, стерилизующая среда применяется посредством погружения упаковочного материала в ванну со стерилизующей жидкостью. В соответствии с другим предпочтительным вариантом осуществления способа по настоящему изобретению, стерилизующая среда применяется посредством покрытия упаковочного материала при помощи передаточного ролика, переносящего жидкую стерилизующую среду из ванны со стерилизующей жидкостью на поверхность упаковочного материала. В соответствии с еще одним дополнительным вариантом осуществления способа по настоящему изобретению, стерилизующая среда применяется посредством распыления жидкой стерилизующей среды на поверхности стерилизуемого упаковочного материала.
В соответствии с дополнительным аспектом изобретения композиция распределяющего агента, содержащая соединение, выбранное из группы, состоящей из немодифицированного лецитина и химически модифицированного лецитина, и дополнительно содержащая неионогенный эмульгатор, применяется в водной стерилизующей среде на основе пероксида водорода для стерилизации упаковочного материала или контейнеров для упаковки пищи.
ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Ниже будут описаны предпочтительные варианты осуществления изобретения со ссылкой на чертежи:
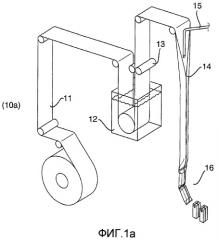
фиг.1а является схематическим изображением того, как рулон упаковочного слоистого материала проводится через глубокую ванну жидкой стерилизующей среды в асептической упаковочной машине такого типа, который обычно применяется для получения упаковок Tetra Brik Aseptic®, а фиг.1b представляет собой схематическое изображение такой упаковочной машины для производства заполненных упаковочных контейнеров из упаковочного слоистого материала в непрерывном процессе формирования, заполнения и заклеивания;
фиг.2 является схематическим изображением того, как рулон упаковочного слоистого материала проводится через мелкую ванну жидкой стерилизующей среды в альтернативном процессе стерилизации;
фиг.3 представляет собой схематическое изображение того, как рулон упаковочного слоистого материала может быть покрыт стерилизующей средой при помощи стерилизующей жидкости из мелкой ванны посредством передаточного ролика с одной стороны рулона, в дополнительном альтернативном процессе стерилизации;
фиг.4 представляет собой схематическое изображение того, как рулон упаковочного слоистого материала может быть покрыт стерилизующей средой посредством распыления стерилизующей жидкости на одной стороне рулона и, при необходимости, облучения впоследствии стерилизуемой поверхности УФ излучением, в упаковочной машине такого типа, который обычно применяется для производства упаковок, предназначенных для хранения ESL (увеличенного срока годности) в условиях охлаждения;
фиг.5а-5j представляют собой УФ фотографии распространения или распределения жидкой стерилизующей среды, применяемой на упаковочном материале, имеющем стерилизуемую поверхность из очень гладкой выдувной пленки, посредством ролика стандартного применения в соответствии со способом фиг.2, описанной выше. УФ изображения получают включением флуоресцирующего агента, а именно Tinopal®, в стерилизующую среду;
фиг.6а, 6b и 6с показывают влияние стерилизующей среды на остаточное содержание стерилизующей жидкости при использовании стерилизующего процесса, описанного в связи с фиг.2 выше.
Фиг.1а, таким образом, показывает принцип процесса упаковки и стерилизации 10, в котором рулон упаковочного слоистого материала протягивается через глубокую ванну 12 с жидкой стерилизующей средой в асептической упаковочной машине такого типа, который обычно используют для получения упаковок Tetra Brik Aseptic®. Обычно время задержки, в течение которого происходит стерилизация на поверхности упаковочного материала, представляет собой общее время, в течение которого рулон упаковочного материала вымачивается в ванне со стерилизующей жидкостью. Более или менее сразу после того, как рулон выходит из ванны, он отжимается при помощи так называемых резиновых отжимных роликов 13, которые отжимают жидкость из рулона, и затем он высушивается горячим стерильным воздухом. При стерилизации посредством этого процесса фактическая проблема смачивания отсутствует, поскольку стерилизуемая поверхность погружена и напрямую контактирует с жидкостью всей поверхностью в течение достаточного времени. Однако может сохраняться проблема, насколько большие капли останутся на поверхности после прохождения рулона через отжимные ролики и, следовательно, насколько легко они могут быть удалены при высушивании и, таким образом, также, каким будет остаточное содержание стерилизующей жидкости на стерилизуемой поверхности. После процедуры стерилизации рулон сворачивают в трубку 14, заполняют жидким продуктом 15, запаивают и разделяют на отдельные упаковки 16.
На фиг.1b показан пример упаковочной машины 10b для непрерывного высокоскоростного процесса упаковывания в упаковки типа Tetra Brik® Aseptic. Рулон слоистого упаковочного материала раскручивают с катушки 11 на задней стороне машины и пропускают через ванну стерилизующей жидкости 12 сразу после присоединения продольной покрывающей полосы термопластического полимера 11'. После высушивания и испарения стерилизующей жидкости рулон сворачивают в трубку 14, которая продольно запаивается и практически одновременно заполняется пищевым продуктом 15 через канал 15', входящий в верхнюю часть трубки, заклеивается в поперечном направлении трубки ниже уровня заполнения пищевым продуктом и нарезается на отдельные упаковки и окончательно сворачивается и формируется в виде упаковок в их конечном виде 17.
На фиг.2 используют процесс стерилизации 20а, в соответствии с которым поверхность упаковочного материала не контактирует непосредственно с жидкостью дольше, чем в течение части всего «времени задержки», т.е. времени, в течение которого стерилизующая среда действует на поверхности, в котором рулон упаковочного материала погружают в ванну на ограниченное время, так называемая мелкая ванна. Эксперименты, выполненные как описано далее, проводились в машине с применением этой системы стерилизации, посредством погружения рулона упаковочного материала 21 в мелкую ванну 22. Отжимные ролики 23 удаляют избыток стерилизующей жидкости из рулона, и затем рулон протягивают через нагревательную камеру 25. Для повышения эффективности этого процесса стерилизации и уменьшения остаточного содержания стерилизующей среды система оснащается специальным так называемым блистерным роликом 24 с неровной поверхностью, которая разбивает капли жидкости на поверхности упаковочного материала на более мелкие, в нагревательной камере 25. Для дополнительного повышения эффективности с нагревательной камерой 25 может быть соединена единица 26 для дополнительного нагревания и высушивания с обеспечением дополнительным нагреванием и током воздуха.
На фиг.3 используют процесс стерилизации, в соответствии с которым поверхность упаковочного материала покрывается стерилизующей средой посредством нанесения роликом, т.е. переносящий ролик 33 переносит жидкую стерилизующую среду из мелкой ванны 32 на поверхность упаковочного материала 31. Покрытая поверхность затем высушивается посредством нагревательного элемента (не показан). При нанесении стерилизующей среды в соответствии с этим процессом при помощи специально изготовленного переносящего ролика, достижимо более равномерное покрытие поверхности, по сравнению с простым погружением рулона в жидкость. Замечено, что лучшее распределение стерилизующей среды вдоль поверхности упаковочного материала достигается в тех случаях, когда только лецитин применяется в качестве добавки распределяющего агента, по сравнению с применением только традиционной добавки Tween™ 20; во втором случае хорошего распределения не достигается.
Способ стерилизации, представленный на фиг.4, может использоваться для получения упаковочного контейнера со сниженными требованиями по условиям хранения, такими как упаковки для ESL хранения в охлажденном состоянии. Также выполнимыми, однако, являются способы асептической стерилизации, включающие распыление стерилизующей жидкости на стерилизуемой поверхности упаковочного материала. Рулон упаковочного материала 41 протягивается через камеру 44, в которой стерилизующая жидкость распыляется на всю поверхность рулона посредством спреевого наконечника 42 и вслед за этим проводится через УФ лампу 43 для облучения этой поверхности стерилизующим УФ-светом, перед тем, как рулон высушивают и затем сформировывают в трубку, заполняют и в конце запаивают в отдельные упаковки.
ПРИМЕРЫ
Химически модифицированный лецитин, который применяется в примерах, представляет собой ALCOLEC® Aquasperse A, произведенный Американской лецитиновой компанией. Этот продукт представляет собой гидроксилированный лецитин, который обладает свойствами диспергироваться в воде. После химической модификации лецитин сохраняет свойство растворяться в масле, но также начинает диспергироваться в воде и становится способным к образованию эмульсий «масло-в-воде». Модифицированный лецитин смешивается с водным раствором пероксида водорода или деионизированной водой при помощи миксера или посредством встряхивания контейнера с плотно закрытой крышкой с целью получения стабильной эмульсии. Затем растворенная лецитиновая смесь с легкостью диспергируется в растворе пероксида водорода. Оптический контроль смачивающей способности лецитинсодержащих стерилизующих сред осуществляется посредством включения флуоресцирующего агента под названием Tinopal® в стерилизующую среду и УФ-фотографирования покрытой поверхности.
Различные количества модифицированного лецитина и/или неионогенного эмульгатора полиэтиленгликоля 20 сорбитана монолаурата (Tween™ 20) смешивают с 35%-ным (по массе) водным раствором пероксида водорода в соответствии с таблицей. Концентрация Tinopal составляла 2 масс.% во всех примерах. УФ-фотографии на фиг.5а-5j соотнесены с соответствующими примерами в таком же порядке, как представлено в таблице. Первые три примера представляют собой справочные примеры, или совсем не содержащие распределяющего агента, или содержащие только Tween 20.
| Лецитин, масс.% | Tween 20, масс.% | Tinopal, масс.% | Смачивание | Расход | |
| Справочный пример 1 | - | - | 2 | - | |
| Справочный пример 2 | - | 0,3 | 2 | - | |
| Справочный пример 3 | - | 0,1 | 2 | - | |
| Пример 1 | 0,1 | - | 2 | ОК | Низкий |
| Пример 2 | 0,1 | 0,1 | 2 | ОК | ОК на нижней границе |
| Пример 3 | 0,3 | 0,1 | 2 | ОК | ОК |
| Пример 4 | 0,3 | 0,2 | 2 | ОК | ОК |
| Пример 5 | 0,1 | 0,3 | 2 | ОК на нижней границе | ОК |
| Пример 6 | 0,3 | 0,3 | 2 | ОК на нижней границе | ОК |
| Пример 7 | 0,4 | 0,3 | 2 | ОК, но до некоторой степени маслянистый | ОК |
Примеры 1-7 показывают, что приемлемое смачивание получают при применении модифицированного лецитина в отдельности в различных концентрациях и в смесях с Tween™ 20, но что оптимизированные свойства, также и в отношении расхода, т.е. поглощение раствора пероксида водорода, получают при условиях в соответствии с примерами 2-4. «Расход» обозначает количество стерилизующего агента, которое переносится рулоном и проходит через отжимные ролики и поступает в нагревательную камеру. Если расход является слишком низким, очевидно, что стерилизующий эффект будет недостаточным и ненадежным. Исследовалось влияние стерилизующей среды на остаточное содержание на стерилизуемой поверхности, и результаты представлены на фиг.6а-6с. Применялся признанный способ с применением Chemets® тиоцианата железа. В соответствии с этим способом ампулу с реагентом, т.е. ионами железа и тиоцианатом аммония в кислом растворе, погружают в упаковку, наполненную деионизированной водой. Если остатки пероксида водорода остаются в упаковке при заполнении деионизированной водой, он будет окислять ионы железа в ампуле до состояния железа и образовывать тиоцианатный комплекс красного цвета. Красный цвет будет иметь различные градации в зависимости от концентрации. Для положительной оценки остаточное содержание должно составлять менее 0,4 промилле. На диаграммах остаточное содержание в промилле показано по оси Y, тогда как время после начала показано по оси Х. Измерения остаточного содержания осуществляются на упаковках в различные моменты времени после начала работы упаковочной машины (с применением системы стерилизации в соответствии с вышеупомянутой фиг.2), т.е. на 1, 30, 60, 90, 102 и 105 секундах после начала работы и 1, 2 (3 упаковки), 3, 6, 9, 12, 15, 18, 20 (2+5 упаковок), 23, 26 и 29 минутах после начала работы. Можно увидеть, что по мере нагревания машины и достижения процессом установившегося режима работы, уровни остаточного содержания стабилизируются на низких значениях. Тестовые испытания осуществляются в трех различных наборах условий, т.е. в отношении фиг.6а с нормальными установками машины и с применением химически модифицированного лецитина (гидроксилированного лецитина) в качестве агента, улучшающего смачивание, на фиг.6b без всех устройств, сделанных с целью снизить остаточное содержание, таких как, например, дополнительные поток воздуха и нагревание после нагревательной камеры и действие блистерного ролика на рулон внутри нагревательной камеры, с гидроксилированным лецитином в качестве агента, улучшающего смачивание. В отношении фиг.6с машина работает при тех установках, как на фиг.6b, но с Tween™ 20 в качестве единственного агента, улучшающего смачивание, вместо гидроксилированного лецитина. Концентрация пероксида водорода в трех тестах приблизительно одинаковая и, следовательно, не влияет на результат тестов. На фиг.6с можно увидеть, что при происходящей стерилизации без каких-либо устройств для снижения остаточного количества стерилизующей жидкости к водному раствору пероксида водорода с добавлением только Tween™ 20, остаточное содержание пероксида водорода находится на неприемлемом уровне. Посредством приспособлений, описанных выше, остаточное содержание будет снижено до уровня ниже 0,4 промилле, но не настолько, как в случае, когда вместо Tween™ 20 в качестве агента, улучшающего смачивание, применяется гидроксилировнный лецитин. На фиг.6а и 6b остаточное содержание будет очень низким, и с применением, и без применения дополнительных устройств в системе стерилизации, но лучше, естественно, в первом случае.
Примеры со ссылками на фиг.5 и 6 повторяют с применением немодифицированного лецитина вместо гидроксилированного лецитина, т.е. Leciprime™ 1400, производимого Cargill. Такие же результаты были получены относительно смачивания, поглощения/расхода, так же как и остаточного содержания пероксида водорода в упаковках. Это возможно, в соответствии с действующей теорией, вследствие перехода немодифицированного лецитина в химически модифицированный при смешивании с пероксидом водорода. В полученной стерилизующей среде, при смешивании с химически модифицированным или с нормальным немодифицированным лецитином, приходят к таким же ингредиентам и всей композиции. Этот эффект, полученный при применении также немодифицированного лецитина, был необъ