Применение неомыляемого экстракта растительной пульпы для лечения старения кожи
Иллюстрации
Показать всеИзобретение относится к косметологической и фармацевтической промышленности и предназначено для лечения и/или профилактики кожных нарушений, связанных со старением. Средство, представляющее собой неомыляемый экстракт пульпы растений, выбранный из семейства растений Sapotaceae, содержащий тритерпеновую фракцию, включающую определенное количество эритродиола, α-амирина, β-амирина и лупеола, для получения косметического, фармацевтического или пищевого продукта, предназначенного для профилактики и/или лечения нарушений кожи, связанных со старением кожи. Вышеописанное средство обладает выраженным омолаживающим действием. 11 з.п. ф-лы., 3 ил. 5 табл.
Реферат
Настоящее изобретение относится к применению неомыляемого экстракта растительной пульпы для получения косметического, фармацевтического или пищевого продукта, предназначенного для лечения и/или профилактики кожных нарушений, связанных со старением.
Старение - это явление неизбежное, медленно развивающееся и необратимое, вызывающее анатомические и гистологические изменения, являющиеся причиной функциональных аномалий органов. Первые видимые признаки проявляются на уровне кожных тканей в виде изменения текстуры, цвета, прозрачности и появления морщин. Этим проявлениям могут способствовать внешние факторы, такие как солнце, табак.
Одной из основных теорий является значение свободных радикалов кислорода (СРК) в процессе старения.
На уровне кожи СРК описаны как ранние медиаторы воспалительных патологий и старения (Kress M. et al., Pain 1995; 62:87-94).
В процессе старения все структуры кожи изменяются. Но фундаментальные изменения преобладают в дерме, и основными мишенями и основными активными участниками являются фибробласты и внеклеточный матрикс. Фибробласты способны стареть. Следовательно, их количество уменьшается, их функция замедляется и их фенотип меняется. И тогда они активно участвуют в деградации внеклеточного матрикса дермы. К тому же во время старения фибробласты теряют свою реактивность и их регуляция модулируется. Действительно, считается, что старение свзано с уменьшением, даже отсутствием ответа на внешние стрессы и, следовательно, с появлением инфекционных, аутоиммунных заболеваний и рака (Gardner I.D. Rev.Infect.Dis. 1980; 2:801-10).
Появление морщин является одним из наиболее ранних признаков старения. Для некоторых людей оно является настоящей проблемой в их отношениях с внешним миром. Поэтому в настоящее время многие косметические продукты, предназначенные для лечения старения кожи, являются общедоступными. Эти специальные продукты созданы главным образом на основе растительных экстрактов.
Aргания, известная в международной ботанической номенклатуре под названием Аrgania spinosa (L.) Skells, особенно ценится в косметической промышленности, более конкретно ядро зерна.
Аргания - это невысокое дерево, высотой от 6 до 10 метров, по внешнему виду напоминающее оливковое дерево.
Внешний вид кроны может варьировать, она может быть вертикальной или плакучей.
На очень колючих ветвях находятся совсем мелкие листья, копьевидные, очереднорасположенные, узкие, короткие (примерно 2 см), часто сгруппированные в пучки.
Листва Aргании обычно неопадающая, но иногда в период сильной засухи она опадает.
Цветы желто-зеленой окраски, двуполые (тычинки и пестики на одном цветке) и пентамерные (5 лепестков и 5 чашелистиков…) образуют соцветия типа клубочка. Период цветения с мая по июнь.
Аргания начинает плодоносить в возрасте 5 лет. Плод представляет собой желтую бесчерешковую овальную ягоду длиной 4-5 см. Она имеет мясистый околоплодник (который также называют пульпой), в котором находится нечто вроде «ложной косточки», очень твердой, коричневого цвета. Этот элемент на самом деле состоит из 2-3 плоских сросшихся между собой зерен, внутри каждого из которых находится маслянистое ядро. Наибольшую ценность в применении представляет ядро зерна. Из него получают масло, затем жмых.
Масло, полученное из зерен, явилось объектом нескольких патентов на изобретение: получение масла при помощи растворителя (FR 2553788), масло аргании, обогащенное неомыляемым веществом (FR 2724663).
Кроме масла были также запатентованы другие вещества. Например, пептиды, происходящие из жмыха зерен, полученного в результате экстракции масла: сочетание масла и пептидов жмыха для лечения нарушений, связанных со старением кожи (FR 2756183). Лист аргании, белки и сапонины, происходящие из жмыха, также являются объектами патентов на изобретение: ЕР 1213025 относится к экстрактам листьев, ЕР 1213024 касается белков, полученных из жмыха и ЕР 1430900 - сапонинов, полученных из жмыха.
Пульпа плодов аргании является объектом более поздней заявки на патент WO2005/039610.
Плод аргании представляет собой плод с ложной косточкой. Он состоит из мясистого околоплодника, называемого пульпой (55-75% плода), и косточки, имеющей очень твердую оболочку, в которой находятся от одного до трех ядер. Из последних получают масло.
Пульпу плода подвергли химическому анализу. Она состоит из углеводов, в том чиле целлюлозы, глюкозы, фруктозы и сахарозы (Charrouf Z. Guillaume D., Ethnoeconomical, enthnomedical and phytochemical study of Argania spinosa (L.), Skeels., Journal of Ethnopharmacology, 1999, 67, 1, 7-14 - Sandret F.G., Etudes préliminaires des glucides et du latex de la pulpe du fruit d'Argan (Argania spinosa): variation au cours de la maturation, Bulletin de la Société de Chimie Biologique, 1957, 39, 5-6, 619-631).
Заявка на патент WO2005/039610 относится главным образом к применению композиции на основе пульпы плодов аргании для получения косметических продуктов. Экстракт пульпы плодов был более или менее очищен. Действительно авторы изобретения тестировали экстракт на разных стадиях способа. Предпочтительно описано применение экстакта пульпы плодов, полученного в результате экстракции гексаном (стр.15). Затем после традиционной стадии омыления, известной специалисту, авторы тестировали неомыляемую фракцию, полученную таким образом. Наконец, авторы также предусмотрели стадию фракционирования неомыляемого вещества путем хроматографии, удалив тритерпеновое соединение эритродиола.
Такой подход вероятно основывался на полученных результатах, в частности, на том факте, что эритродиол как таковой обладает токсичностью (пример 1) в меньшей дозе, чем тритерпеновое соединение, такое как определено в документе: фракция А без эритродиола (стр.38). К тому же сам по себе эритродиол имеет слабое преимущество в отношении UVA и UVB (примеры 3 и 4) по сравнению с указанной тритерпеновой фракцией. Таким образом, этот документ в целом касается применения тритерпеновой фракции экстракта пульпы плодов аргании для получения косметических продуктов и предпочтительно для лечения кожи после воздействия UVA и UVB путем стимуляции метаболизма фибробластов. Более конкретно в этом документе указано, что эта тритерпеновая фракция, такая как раскрыта в WO2005/039610, обладает тем большей активностью, чем меньше содержание эритродиола.
Неожиданно авторы настоящего изобретения выявили эффект ингибирования физиологического старения фибробластов зрелой кожи неомыляемым экстрактом пульпы плодов аргании, богатым эритродиолом; причем указанный экстракт можно получить путем экстракции ацетоном с последующим проведением традиционной стадии омыления. Однако можно обоснованно считать, что преимущества настоящего изобретения можно распространить на любой неомыляемый экстракт растительной пульпы, содержащей тритерпеновую фракцию, состав которой по своим основным компонентам близок к составу, полученному из пульпы плодов аргании.
Настоящее изобретение относится к применению неомыляемого экстракта растительной пульпы, содержащего тритерпеновую фракцию, отличающегося тем, что указанная тритерпеновая фракция содержит эритродиол, α-амирин, β-амирин и лупеол, для получения косметического, фармацевтического или пищевого продукта, предназначенного для профилактики и/или лечения нарушений кожи, связанных со старением кожи. Предпочтительно указанный экстракт получают путем экстракции ацетоном с осуществлением последующей традиционной стадии омыления.
Этот неомыляемый экстракт, который также называют первичным омыляемым веществом, можно растворить в эксципиенте для того, чтобы облегчить приготовление лекарственной формы.
Предпочтительно указанный экстракт получают из растения, выбранного из семейства Sapotaceae; и более предпочтительно укзанный экстркт получают из пульпы плодов аргании.
Преимущество экстракции ацетоном заключается в том, что можно не использовать латекс, который образует большую часть липидной фракции, и таким образом получать высокую концентрацию неомыляемых веществ в липидной фракции.
Композиция неомыляемого вещества по настоящему изобретению отличается как в качественном, так и в количественном отношении от предпочтительной композиции, описанной в заявке на патент WO2005/039610.
Экстракты по настоящему изобретению отличаются своим содержанием тритерпеновых веществ. Анализ последних можно проводить хроматографией в газообразной фазе соответствующим традиционным методом, который позволяет идентифицировать β-амирин, эритродиол. Напротив, α-амирин и лупеол этим методом не выделяются, количественный анализ этих молекул можно проводить традиционным методом.
Преимущественно тритерпеновая фракция указанного экстракта состоит из эритродиола, массовая фракция которого составляет примерно от 7% до 40% первоначального неомыляемого вещества, β-амирина, массовая фракция которого составляет примерно от 5% до 30% первоначального неомыляемого вещества, α-амирина и лупеола, сумма массовых фракций которых составляет примерно от 10% до 50% первоначального неомыляемого вещества.
Преимущественно указанная массовая фракция эритродиола составляет примерно от 10% до 20% первоначального неомыляемого вещества; и более предпочтительно равна примерно 15% первоначального неомыляемого вещества.
Преимущественно указанная массовая фракция β-амирина составляет примерно от 7% до 20% первоначального неомыляемого вещества; и более предпочтительно равна примерно 10% первоначального неомыляемого вещества.
Преимущественно сумма массовых фракций α-амирина и лупеола составляет примерно от 15% до 30% первоначального неомыляемого вещества; и более предпочтительно равна примерно 20% первоначального неомыляемого вещества.
Содержание этих разных молекул зависит от условий проведения экстракции. Эти значения будут меньше в косметическом, фармацевтическом или пищевом продукте в зависимости от одного или нескольких эксципиентов, которые будут введены в первоначальное неомыляемое вещество.
Преимуществом настоящего изобретения является существенный вклад эритродиола в свойства неомыляемого экстракта по настоящему изобретению против старения. Поскольку СРК играют важную роль в процессе старения кожи, антирадикальный эффект (анти-СРК) эритродиола оценивали путем сравнения с неомыляемым веществом пульпы плодов аргании по настоящему изобретению.
Вред, наносимый СРК клеткам, проявляется в изменении липидных компонентов плазматической мембраны (липоперокисление), белков (денатурация и разложение) и генетического материала ДНК (мутации). Цель экспериментов, проведенных in vitro, заключалась в определении:
эффективности защиты посредством эритродиола и неомыляемого экстракта от окисления мембранных липидов (пример 3);
и защитной способности эритродиола и других тритерпеновых молекул (лупеол, α- и β-амирин) в отношении изменения ДНК генома (пример 4).
Эти эксперименты позволили показать, что эритродиол - это молекула, которая обладает значительным антиоксидантным потенциалом.
В частном способе осуществления настоящего изобретения экстракцию можно осуществить следующим образом: высушенную пульпу плодов аргании измельчают, затем экстрагируют ацетоном. Можно также применять смесь ацетон-вода. Экстракцию проводят при перемешивании или статически при соотношении растение/растворитель, которое может изменяться от Ѕ до 1/20 при температуре от комнатной до температуры кипения растворителя и в течение времени от 30 минут до 24 часов.
После экстракции твердый остаток растения отделяют от экстрагирующего раствора фильтрованием или центрифугированием. Раствор может быть более или менее концентрирован до получения сухого экстракта. В последнем случае сухое вещество можно растворять в спирте для проведения омыления.
В раствор вводят гидроксид металла, в частности гидроксид натрия или калия в концентрациях, изменяющихся от 0,1 до 10 N. Омыление проводят при температуре от комнатной температуры до температуры кипения при перемешивании и в течение времени от 15 минут до 48 часов в зависимости от температуры.
Очистку проводят путем экстракции жидкость/жидкость. В среду гидролиза добавляют несмешивающийся растворитель, которым может быть вода, насыщенная или ненасыщенная солями [NaCl, (NH4)2SO4], со значениями рН от 3 до 9. Эту фазу промывки можно повторить несколько раз.
После очистки органические фазы обрабатывают так, чтобы устранить растворитель. Эту обработку можно провести путем выпаривания под контролем давления. На стадии выпаривания можно получить продукт, имеющий более или менее воскообразную липидную консистенцию, первоначальное неомыляемое вещество.
Можно добавить эксципиент, в качестве которого можно использовать воск животного происхождения (например, пчелиный) или растительного происхождения (карнаубский воск, канделильский воск или воск жожоба), растительное масло (кукурузное, сафлоровое, кунжутное, аргановое), глицерин, продукты синтетического происхождения, такие как вазелиновое масло, многоатомные спирты (такие как пропиленгликоль, бутиленгликоль, глицерин), этерифицированные триглицериды (такие как miglyol 812, myritol 318, neobee MJ), оксипропилированные полимеры формулы Н(ОСН2-СНСН3)nОН или оксиэтилированные полимеры формулы Н(ОСН2-СН2)nОН, сложные диэфиры жирного спирта разной длины от С1 до С40. Пропорции первоначального неомыляемого вещества пульпы плодов аргании и эксципиента могут варьировать от 1/99 до 99/1.
Преимущество настоящего изобретения заключается в умеренной себестоимости использования пульпы плодов для лечения, направленного против старения. Неомыляемый экстракт используют без дополнительной стадии очистки, которая является очень дорогостоящей. Таким образом, композицию по настоящему изобретению можно получить способом, в котором используют традиционные стадии экстракции и омыления, известные специалисту.
Применение неомыляемого экстракта растительной пульпы по настоящему изобретению позволяет предупреждать и/или лечить кожные нарушения, которые проявляются в виде изменения текстуры, цвета, прозрачности кожи и появления морщин.
В частном способе осуществления изобретения кожные нарушения являются следствием снижения или отсутствия ответа на внешние стрессы, в частности, вызванные солнцем или табаком.
В другом способе осуществления изобретения кожные нарушения являются следствием снижения или потери индуцирования белков HSР72. Белки HSР от “Heat Shock Protein” конститутивно экспрессируются в многочисленных клетках и обладают функциями, необходимыми для поддержания белков, откуда их название «шаперонные» белки. Действительно, они ингибируют агререгацию денатурированных белков, препятствуя образованию нежелательных ассоциаций белков, и они участвуют во внутриклеточном транспорте и поддержании некоторых белков в неактивной форме(Morris S.D. Clin. Exp. Dermatol. 2002; 27: 220-224). Белки HSР также играют главную роль в ответе на стресс и, в частности, в процессах клеточной защиты, запуская адаптативный ответ (Maytin E.V. J.Invest.Dermatol. 1995; 104: 448-55).
Неожиданным образом применение экстракта по настоящему изобретению позволяет восстановить индуцирование белков HSР72 в состаренных фибробластах.
В рамках настоящего изобретения косметический, фармацевтический или пищевой продукт, содержащий экстракт по изобретению, вводят пероральным или топическим путем, предпочтительно топическим.
Галеновую форму для топического нанесения выбирают из группы, содержащей кремы, гели, мази и спреи.
Преимущественно форму для перорального введения выбирают из группы, включающей таблетки, желатиновые капсулы и порошки для питьевых суспензий.
Преимущественно количество указанного экстракта в конечном косметическом продукте составляет примерно от 0,001% до 50%, предпочтительно примерно от 0,01% до 10% и более предпочтительно примерно от 0,1% до 2 вес.% от общего веса препарата.
Препарат может дополнительно содержать другие действующие вещества, хорошо известные специалисту, для лечения и/или предупреждения кожных нарушений, связанных со старением кожи. Преимущественно указанный препарат содержит другие вещества, полученные из аргании, известные своей «антивозрастной» активностью, такие как, например, масло, полученное из ядра зерна, и пептиды жмыха.
Нижеследующий пример композиции по изобретению приведен для сведения и не ограничивает изобретение. Процентное содержание выражено весовыми процентами по отношению к общему весу композиции.
ПРИМЕР 1: Уход против дряблости лица
| Неомыляемый экстракт пульпы плодов аргании | 0,1-2% |
| Обогащенное масло аргании | 1-5% |
| Пептиды аргании | 0,1-1% |
| Производное витамина Е | 0,1-0,5% |
| Сложный глицериновый эфир витамина F | 0,1-0,5% |
| Пальмитат витамина А | 0,1-1% |
| Метилстеарат глюкозы | 1-5% |
| Триглицериды каприновой и каприловой кислот | 2-8% |
| Жидкий парафин | 5-12% |
| Отдушка | достаточное количество |
| Очищенная вода | количество, достаточное до 100 гр |
Следующие примеры иллюстрируют изобретение, не ограничивая его объем.
ПРИМЕР 2: способ получения неомыляемого экстракта пульпы плодов аргании.
1 тонну сухой пульпы плодов аргании измельчают, затем экстрагируют в реакторе при помощи 5 тонн ацетона. Экстракцию проводят при перемешивании в течение одного часа при кипячении с обратным холодильником. После охлаждения раствор фильтруют, затем концентрируют в вакууме до получения маслянистого десольватированного экстракта. Этот остаток обрабатывают 500 литрами этанола 95 об.%. Добавляют в него 100 л 10 н. раствора едкого натра и доводят до кипения с обратным холодильником при перемешивании в течение часа.
После охлаждения гидролизованный раствор помещают в декантатор, вводят в него 500 л гептана и 300 л воды. Экстрагирование жидкость/жидкость проводят осторожно. После декантации извлекают органическую фазу. Проводят две повторные экстракции при помощи 500 л гептана. 3 гептановые фазы группируют и трижды промывают, используя каждый раз 500 л воды. Промытые органические фазы десольватируют. Получают в результате воскообразную массу. В этом экстракте, который соответствует первоначальному неомыляемому веществу, проводят количественное определение содержания тритерпеновых веществ. Он содержит 10% β-амирина, 15% эритродиола и 20% смеси лупеол-α-амирин.
ПРИМЕР 3: анализ антирадикального действия эритродиола - анализ липидного пероксидирования
1) Введение
Плазматическая мембрана является первой и основной мишенью СРК и, будучи богатой липидами, она является местом усиленного пероксидирования (Girotti A.W., J. Free Radic. Biol. Med. 1995; 1: 87-95). Пероксиды, образовавшиеся в процессе этого липидного окисления, также явлются очень реактивными и могут разрушать протеиновый и геномный материал.
Для оценки изменения мембраны авторы изобретения измерили пероксидирование липидов путем количественного определения in vitro комплексов, образованных продуктами липидного окисления и тиобарбитуровой кислотой. Эти комплексы называют TBARS (Thiobarbituric Acid Reactive Substances) и тест называется: Тест TBARS.
С тем, чтобы свести к минимуму химический оксидативный стресс, линию фибробластов L929 обработали комплексом, состоящим из соединения пероксида водорода (Н2О2) и железа (Fe2+/Fe3+), воспроизводя таким образом реакцию Фентона, являющуюся источником СРК и более конкретно гидроксильного радикала (ОНо) (Vessey D.A. et al. J. Invest.Dermatol. 1992; 99: 859-63): Н2О2+Fe2+→ОНо+ОН-+Fe3+.
2) Методология
Тестируемые продукты:
Продукты испытывали на линии состаренных фибробластов L929. Клетки предварительно обработали продуктами в разной концентрации (таблица 1) в течение 16 часов и затем стимулировали комплексом Н2О2-Fe2+/Fe3+ в течение 1 часа. LK0304 неомыляемого экстракта пульпы плодов аргании получали в соответствии с примером 2.
| Таблица 1Тестируемые растворы | ||
| Продукт | Маточный раствор | Тестируемые растворы |
| Неомыляемое вещество пульпы плодов арганииКомплект:LK0304 | 10 мг/мл(DMEM/TWEEN20)-20°C | 0,3 мкг/мл1 мкг/мл3 мкг/мл |
| Эритродиол/EXTRASYNTHESEКомплект:05040605 | 10 мг/мл DMSO-20°C | 0,3 мкг/мл-0,68 мкМ1 мкг/мл-2,26 мкМ3 мкг/мл-6,78 мкМ |
| Витамин Е* SIGMA T-1539 | 400 мг/мл-20°C | 400 мкг/мл-928,7 мкМ |
| (*Молекула, называемая антирадикальной) |
Пероксидирование мембранных липидов анализировали путем измерения показателей TBARS (по Morliére P. et al Biochem. Biophys. Acta. 1991; 1084: 261-268).
Принцип проведения теста:
В кислой среде при 95°С образуются комплексы, обозначенные TBARS, аббревиатура от Thio Вarbituric Acid Reactive Substances, между продуктами липидного окисления (малондиальдегидом или МДА) и тиобарбитуровой кислотой (ТБА), количественный анализ которых можно провести по флуоресценции по сравнению с эталоном гамма при помощи МДА. Количественный анализ TBARS выражают в пмоль/мкг белков. Количественный анализ белков и TBARS проводят во внутриклеточной среде.
Вычисление процента защиты клеточных мембран:
На основании результатов вычисления TBARS в пмоль/мкг белков защитную эффективность разных продуктов против окисления мембранных липидов вычисляли следующим образом:
3) Результаты-обсуждение
После обработки в течение 16 часов с использованием различных тестируемых продуктов модель радикального стресса, используемая в этом эксперименте (реакция Фентона), индуцирует существенное пероксидирование липидов в фибробластах L929. Этот мощный разряд гидроксильного радикала ОНо генерирует оксидативный стресс на клеточном уровне и, в частности, на уровне мембран. Тем не менее в этом типе окислительной реакции продукты, полученные пероксидированием липидов, помещаются в клетки, и количественный анализ TBARS происходит во внутриклеточной среде.
Полученные результаты приведены ниже в таблице II.
| Таблица IIАнализ пероксидирования липидов | |||
| Тестируемые активные вещества | Защита мембранных липидов в % | ||
| Средняя | Типовое отклонение | N:число экспериментов | |
| Vit E 400мкг/мл-928,7мкМ | 56,62 | 8,74 | 3 |
| Эритродиол | |||
| 0,3 мкг/мл-0,68 мкМ | 33,75 | 15,39 | 3 |
| 1 мкг/мл-2,26 мкМ | 38,43 | 7,68 | 3 |
| 3 мкг/мл-6,78 мкМ | 53,22 | 17,30 | 3 |
| Неомыляемое вещество пульпы плодов аргании | |||
| 0,3 мкг/мл | 21,38 | 37,53 | 3 |
| 1 мкг/мл | 30,53 | 17,80 | 3 |
| 3 мкг/мл | 37,39 | 9,45 | 2 |
Витамин Е, образующий молекулу, называемую антирадикальной, уменьшает пероксидирование липидов, индуцированное комплексом Н2О2-Fe2+/Fe3+, и очень эффективно защищает клеточные мембраны (примерно 56%).
Неомыляемый экстракт пульпы плодов аргании, полученный по примеру 2, обладает антирадикальной активностью в концентрациях 1 и 3 мкг/мл (30 и 37% защиты липидных мембран соответственно).
Эритродиол, молекула, содержащаяся в тритерпеновой фракции неомыляемого экстракта, обладает хорошей антиоксидантной активностью, при этом эффективность зависит от дозы. Эритродиол обладает активностью, начиная с 0,3 мкг/мл (33% защиты). Антирадикальное действие эритродиола в концентрации 3 мкг/мл очень значительно и сравнимо с витамином Е.
4) Выводы
Модель in vitro, представленная в этом исследовании, отражает последствия существенного оксидативного стресса, направленного на основную клеточную мишень, которой является плазменная мембрана. Таким образом, количественный анализ пероксидирования липидов является хорошим показателем оксидативного стресса и позволяет оценить антиоксидантное действие действующих веществ в отношении гидроксильного радикала на уровне клеточной мебраны.
Витамин Е, антиоксидантная молекула, позволяет оценить эту модель.
В этих экспериментальных условиях было отмечено, что экстракт по настоящему изобретению, содержащий эритродиол, а также эритродиол как таковой, обладают значительным антиоксидантным потенциалом.
ПРИМЕР 4: анализ антиоксидантного действия эритродиола - анализ геномного удара
1) Введение
ДНК является мишенью СРК, которые вызывают модификацию оснований (окисление, нитрование, деаминирование: Guetens G. et al Clin. Lab. Sci.2002; 39: 331-475), образование разрывов в цепи (безосновные сайты или β-элиминирование) и мостиковой связи ДНК-белки и ДНК-гидроксипероксиды. Изменение геномного материала вызывает каскад клеточных реакций (вилочная блокировка репликации, активация ключевых белков, остановка клеточного цикла), которые приводят к индуцированию механизмов репарации. Таким образом система репарации оснований или BER (Base Excision Repair)(Freidberg E.C. et al DNA repair and mutagenesis, ASMpress; Washington DC 1995) берет на себя восстановление оснований, модифицированных оксидативным стрессом. Эта система действует быстро и эффективно по трем ключевым стадиям:
1 - обнаружение поврежденного основания;
2 - рассечение и иссечение поражения;
3 - повторный синтез в месте разрыва.
СРК могут продуцироваться в таком количестве, что системы клеточной защиты и репарации могут не справляться. Если активируются исполнители апоптоза, поврежденная клетка умирает. Но в случае, если повреждения ДНК плохо репарируются, может возникнуть генерация делетирующих мутаций, которые будут принимать участие в инициации онкогенеза. Поэтому биологические последствия оксидативного стресса (гибель или мутагенез) обусловливают более долгосрочные события, такие как старение или рак.
Многочисленные исследования показали сильную корреляцию между старением и прогрессирующей и необратимой аккумуляцией оксидативных повреждений на уровне клеточных макромолекул. Несколько исследовательских групп показали на грызунах, что содержание 8-оксигуанина, измеренное в различных тканях, таких как кожа, с возрастом увеличивается (Tahara S. et al. Merch. Ageing Dev. 2001; 122: 415-426). Работы Mecocci P. et al. (Free Radic.Biol.Med. 1999; 26: 303-8), касающиеся скелетной мышцы человека, показывают, что оксидантные повреждения ДНК или липидов аккумулируются с возрастом. Та же команда также показала, что у лиц, страдающих болезнью Альцгеймера, содержание окисленных оснований в ДНК лимфоцитов и содержание антиоксидантов в плазме существенно выше и ниже соответственно, чем у здоровых (Mecocci P. et al. Arch. Neurol.2002; 59: 794-8).
2) Цель
После осуществления примера 3 и с тем, чтобы проконтролировать антирадикальную активность эритродиола на другой моделе, авторы изобретения анализировали его защитную способность в отношении изменения геномной ДНК, вызванного оксидативным стрессом, по сравнению с неомыляемым экстрактом пульпы плодов аргании и других тритерпеновых молекул, также содержащихся в этом экстракте.
Они генерировали поражения ДНК стрессом Н2О2 и опосредованно анализировали образовавшиеся в результате повреждения, анализируя реакцию восстановления. Для этого использовали набор, называемый тест 3D (DNA Damage Detection). Этот биохимический опыт имитирует in vitro реакцию восстановления путем иссечения (Salles B. еt al. Anal. Biochem. 1995; 232: 37-42 и Salles B. еt al. Biochimie 1999; 81: 53-58). Тест 3D основан на репарации повреждений ДНК при помощи очищенных человеческих клеточных экстрактов. На стадии репарации маркер встраивали в ДНК и это включение, являющееся количественным отражением репарированных повреждений, затем обнаруживали при помощи хемилюминесценции.
3) Методология
Тестируемые продукты:
Продукты оценивали по линии состаренных фибробластов L929. Клетки предварительно обработали продуктами (таблица III) в течение 16 часов и затем стимулировали при помощи Н2О2 (пероксид водорода 3% - GIFRER- Лаборатория Gifrer Barbezat) в концентрации 100 мкМ в течение 30 минут.
| Таблица IIIТестируемые растворы | ||
| Продукт | Маточный раствор | Тестируемые растворы |
| Неомыляемое вещество пульпы плодов арганииКомплект:LK0304 | 10 мг/мл(DMEM/TWEEN20)-20°C | 3 мкг/мл |
| Эритродиол/EXTRASYNTHESEКомплект:05040605 | 10 мг/мл DSMO-20°C | 3 мкг/мл-6,78 мкМ |
| Лупеол (тритерпен) | 50 мМ DSMO-20°C | 3 мкг/мл-7 мкМ |
| α-амирин (тритерпен) | 50 мМ DSMO-20°C | 3 мкг/мл-7 мкМ |
| β-амирин (тритерпен) | 50 мМ DSMO-20°C | 3 мкг/мл-7 мкМ |
Тест 3D
Принцип проведения был следующим: после повреждения геномной ДНК (оксидативная обработка) клетки лизировали. Лизат накладывали на микропланшет, покрытый полилизином:
1. Адсорбция ДНК
2. Инкубирование ДНК с белковым экстрактом (обогащенным репарирующими ферментами) и нуклеотидным пулом, один из нуклеотидов которого мечен биотином (dUTP-Biotin)-Репарация повреждений и инкорпорирование в ДНК нуклеотидов, меченных «dUTP-Biotin».
3. Инкубирование с ферментативным комплексом «Avidine-Peroxydase”-обнаружение при помощи авидина инкорпорированных dUTP-Biotin.
4. Введение люминесцентного субстрата пероксидазы и количественный анализ сигнала, подаваемого пропорционально числу восстановленных повреждений.
Протокол проведения теста вели в соответствии с инструкциями поставщика комплекта (Test 3D Solyscel-Réf: SFRIDN013-AES Laboratoire). По окончании реакции планшет считывали в люминометре (MITHRAS LB940-BERTHOLD).
Вычисление процента защиты ДНК:
Приведенное ниже отношение позволяет вычислить для каждой концентрации тестируемого продукта % защиты от повреждений ДНК, индуцированных оксидативным стрессом
(интенсивность люминесценции - или IL - выражает количество повреждений ДНК)
4) Результаты и выводы
Результаты, полученные в примере 3, показали, что эритродиол обладает наибольшей антирадикальной активностью при 3 мг/мл (6,78 мкМ). Поэтому авторы тестировали все тритерпены (лупеол, α-амирин, β-амирин и эритродиол) и неомыляемый экстракт пульпы плодов аргании в концентрации 3 мг/мл в тесте 3D “DNA Damage Detection”. Указанный неомыляемый экстракт получали способом по примеру 2. Полученные результаты представлены ниже в таблице IV. Значения, указанные в этой таблице, - это проценты ингибирования (или % защиты) повреждений ДНК в результате экзогенного оксидативного стресса по отношению к клеткам «базального контрольного образца» (100%) и к клеткам, «подвергшимся стрессу Н2О2» (0%).
| Таблица IVЗащита ДНК эритродиолом | |||
| Интенсивность люминесценции | % повреждений ДНК | % защиты ДНК | |
| Контрольный образец | 5460 | 0 | |
| Н2О2 100 мкМ-30 мин | 11576,7 | 100 | 0 |
| Эритродиол3 мкг/мл-6,78 мкм | 5520 | 1 | 99 |
| Неомыляемое вещество пульпы плодов аргании3 мкг/мл | 6193,3 | 12 | 88 |
| Лупеол3 мкг/мл-7 мкМ | 9020 | 58,2 | 41,8 |
| α-амирин3 мкг/мл-7 мкМ | 8663,3 | 52,4 | 47,6 |
| β-амирин3 мкг/мл-7 мкМ | 13133,3 | 125,4 | -25,4 |
Обработка посредством Н2О2 индуцирут высокий процент окисления на уровне гуанина с образованием, в частности, 8-оксо-7,8-дигидро-2'-дезоксигуанозина (8-оксогуанин)(Dizdaroglu M. et al Arch. Biochem. Biophys. 1991; 285: 388-390). Тест 3D показывает сильное увеличение люминесцентности после обработки при помощи Н2О2, которое отражает высокую восстановительную активность и, следовательно, значительное содержание поврежденных оснований в ДНК.
Неомыляемый экстракт пульпы плодов аргании эффективно защищает ДНК от оксидативного стресса.
Эритродиол, молекула, содержащаяся в неомыляемом экстракте в концентрации 3 мкг/мл, обладает очень высокой антиоксидантной активностью, обеспечивая 99% защиты ДНК от образования оксидативных повреждений.
Сравнение тритерпеновых молекул с одинаковой молярной концентрацией (примерно 7 мкМ) показывает, что наиболее активным является эритродиол.
ПРИМЕР 5: Модель исследования in vitro действия неомыляемого экстракта по изобретению на индуцирование белков HSP72
1) Библиография
В разных работах показана потеря индуктивности белков HSP72 в процессе старения. У пациентов пожилого возраста индуцирование белка HSP72 при тепловом воздействии существенно снижена на уровне кожи (Muramatsu T. et al. Br.J.Dermatol.1996; 134: 1035-1038). С другой тороны Gustmann-Conrad A. et al.(Exp.Cell.Res. 1998; 241: 404-413) показали, что индуцирование белка HSP72 под действием теплового стресса существенно снижается в фибробластах кожи у пожилых людей по сравнению с молодыми людьми. В том же исследовании было показано, что уровень индукцирования HSP72 также снижается в фибробластах (молодой кожи) или в линиях фибробластов (IMR-90), состарившихся в процессе клеточных делений.
Первый умеренный стресс является достаточным для того, чтобы индуцировать in vitro белки HSP с тем, чтобы они защищали клетку от новых стрессов (Morris S.D. et al. J. Clin. Invest.1996; 97: 706-12). HSP72 является основным белком семейства HSP70, экспрессированным в кератиноцитах и фибробластах кожи и индуцируемым многочисленными агентами стресса (тепло, УФ и т.д.) (Trautinger F. et al. J. Invest. Dermatol. 1993; 101: 334-38; Charveron M. et al. Cell. Biol. Toxicol. 1995; 11: 161-65).
2) Порядок проведения эксперимента
Авторы настоящего изобретения выбрали анализ уровня индуцирования под воздействием теплового стресса белков HSP72 в фибробластах IMR-90 (линии фибробластов) в процессе старения для оценки «антивозрастных» свойств экстракта пульпы плодов аргании, полученного по примеру 2, т.е. содержащего 10% β-амирина, 15% эритродиола и 20% смеси лупеол-α-амирин.
На первом этапе авторы создали и утвердили модель клеточного старения путем индуцирования старения фибробластов под действием оксидативного стресса.
Модель индуцированного старения:
Фибробласты делятся до критической стадии, которую называют репликативным старением и которая ассимилируется с клеточным старением. Но старение может также быть вызвано, в частности, оксидативным стрессом, речь идет о “Stress-Induced Premature Senescence или SIPS” (Dumont et al. Free Radic. Biol. Med.2000; 28: 361-373).
Используемая модель: индуцирование старения в линии молодых фибробластов IMR-90 было выявлено в результате обработки клеток с использованием Н2О2 в течение 2 часов. Через 72 часа после этого стресса клетки IMR-90 состарились.
На втором этапе они показали снижение уровня индукции HSP72 в результате теплового стресса в состаренных фиброблатах по сравнению с молодыми фибробластами. Наконец, они провели оценку свойств экстракта пульпы плодов аргании, полученного в примере 2, т.е. содержащего 10% β-амирина, 15% эритродиола и 20% смеси лупеол-α-амирин на этой модели старения.
3) Результаты
Для лучшего понимания изобретения и его целей, преимуществ и свойств ниже приведено описание прилагаемых чертежей, на которых:
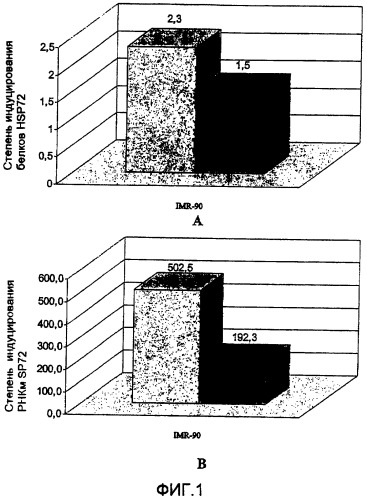
На фигуре 1 представлен анализ степени индуцирования HSP72 в фибробластах IMR-90 на уровне транскрипции и трансляции.
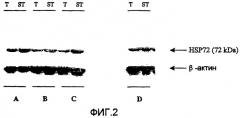
На фигуре 2 представлен анализ, проведенный методом Western Blot, содержания белков HSP72 в клетках IMR-90, обработанных разными концентрациями экстракта пульпы плодов аргании по изобретению.
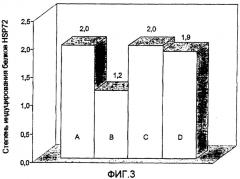
На фигуре 3 представлен полуколичественный анализ степени индуцирования белков HSP72 (нормализованного уровнем экспрессии β-актинина) в состаренных фибробластах IMR-90, предварительно обработанных разными концентрациями экстракта пульпы плодов аргании по изобретению.
Анализ индуцирования HSP72 под действием теплового стресса в процессе старения фибробластов IMR-90:
Клетки, культивируемые при 37°С, инкубировали в течение 1 часа при 45°С и затем инкубировали при 37°С в течение 2 часов (анализ РНКм) или в течение 4 часов (анализ белков):
Экспрессия белка (Western Blot)
Внутриклеточные белки, экстрагированные из фибробластов, анализировали при помощи технологии Western Blot, используя анти-HSP72 антитело (моноклональное антитело, CHEMICON) и систему непрямого обнаружения люминесценции. Мембрану анализировали и количественный анализ интенсивности полос проводили при помощи денситометрии (программа ImageMaster TotalLab AMERSHAM). Уровень экспрессии HSP72 нормализовали уровнем белка, экспрессированного конститутивным образом, β-актинина.
На фигуре 1А представлен полуколичественный анализ методом Western Blot степени индуцирования белков HSP72 в молодых фибробластах IMR-90 (□) и в состаренных фибробластах IMR-90 (■) (старение вызвано Н2О2). Таким образом, на фигуре 1 отчетливо показано, что ур