Новые производные нитрокатехола, обладающие активностью в качестве лигандов селектина
Иллюстрации
Показать всеИзобретение относится к области фармацевтики и косметологии, более конкретно касается соединений, имеющих общую структуру формулы (С2) или (С5) или (С6) или (D2) или (D5) или (D6)
а также раскрывает косметические и фармацевтические композиции, их содержащие.
Композиции, содержащие описанные соединения, могут быть применены для модулирования in vitro и in vivo процессов связывания с посредничеством связывания Е-, Р- или L-селектина. 7 н. и 1 з.п. ф-лы, 2 табл.
Реферат
Настоящее изобретение относится к соединениям, композициям и способам модулирования in vitro и in vivo процессов, опосредованных молекул клеточной адгезии. Описываемые малые молекулы являются ароматическими нитросоединениями, которые эффективно моделируют функции, опосредованные молекулами клеточной адгезии.
Функции, опосредованные молекулами клеточной адгезии являются частью сложного каскада, приводящего к миграции циркулирующих белых кровяных телец (лейкоцитов) из тока крови в окружающую ткань (трансмиграция). С точки зрения физиологии, трансмиграция лейкоцитов является исключительно важной для гомеостаза и иммунного надзора живых существ, включая людей. Лимфоциты, например, по своей природе покидают ток крови и переходят в лимфатические ткани для «патрулирования» в поисках вредных антигенов. Однако в обстоятельствах патологии, например, при местном или общем воспалении и/или повреждении сосудистой системы, этот основной процесс разупорядочивается, по меньшей мере, частично, в силу повышенной экспрессии E- и P-селектинов на поверхности. В результате избыточная трансмиграция лейкоцитов приводит к патологическим клеточным инфильтратам, с последующим повреждением ткани в некоторых клинически важных случаях. Такие болезненные состояния, как острое повреждение легких (ОПЛ), острый респираторный дистресс-синдром (ОРДС), бронхиальная астма (астма), хроническое обструктивное заболевание легких (ХОЗЛ), псориаз, ревматоидный артрит и сепсис, все связаны с воспалением тканей, вызванным и постоянно сохраняемым патологически активированной инфильтрацией лейкоцитов в соответствующие ткани. К тому же, чрезмерно увеличенная инфильтрация лейкоцитов способствует патогенезу ишемического/реперфузионного повреждений, связанных с трансплантацией органов, искусственным кровообращением или чрескожной транслюминальной ангиопластикой.
Для трансмиграции лейкоциты должны связаться со стенкой сосудистого эндотелия, чтобы продиффундировать через клеточную стенку в окружающую ткань. Таким образом, лейкоциты должны свернуться на стенке эндотелиальной клетки и затем связаться с ней (начальное сворачивание, или «привязывание»). Это первичное событие в трансмиграции протекает с участием молекул клеточной адгезии семейства селектинов. В дополнение к прямому связыванию с эндотелием, лейкоциты могут связываться с другими лейкоцитами, лейкоцитными частицами, тромбоцитами или образованными из тромбоцитов частицами, которые уже прикреплены к эндотелию.
Семейство селектинов молекул клеточной адгезии состоит из трех структурно родственных кальций-зависимых белков, связывающихся с поверхностью клетки посредством углеводных остатков, E-, P- и L-селектинов. E-селектин экспрессируется только на воспаленном эндотелии, P-селектин экспрессируется как на воспаленном эндотелии, так и на тромбоцитах, L-селектин экспрессируется на лейкоцитах. Селектины состоят из амино-терминированого лектинного домена, подобного эпидермальному фактору роста (ЭФР) домена, различного числа соотносящихся с комплементарным рецептором повторов, гидрофобного трансмембранного домена и углерод-терминированного цитоплазмического домена. Предполагается, что связывающие взаимодействия, приводящие к адгезии лейкоцитов, реализуются посредством контакта лектинного домена селектинов и различных углеводных лигандов на поверхности лейкоцитов.
Все три селектина могут связываться с углеводом сиалил Льюисx (sLex), присутствующим на поверхности большинства лейкоцитов глигозидным фрагментом, с низким сродством. Структурно родственный гликозидный фрагмент, сиалил Льюисa (sLea), преимущественно обнаружен на поверхности раковых клеток [K. Okazaki et al., J. Surg. Res., 1998, 78(1), 78-84; R. P. McEver et al., Glycoconjugate Journal, 1997, 14(5), 585-591]. В случае P-селектинов был описан гликопротеиновый лиганд с явно выраженным высоким сродством [R.P. McEver, R.D. Cummings, J.Clin.Invest., 1997, 100, 485-492], так называемый P-селектина гликопротеиновый лиганд-1 (PSGL-1), в котором высокое сродство связывания с селектином обеспечивается как его sLex-фрагментом, так и частью его пептидных компонентов, в частности сульфатированными тирозиновыми остатками [R.P.McEver, Ernst Schering Res. Found. Workshop, 2004, 44, 137-147]. PSGL-1 является одним из наиболее важных селектиновых лигандов, связываясь с высоким сродством с P-селектином, но он также связывается с E- и L-селектином [G. Constantin; Drug News Perspect; 2004; 17(9); 579-586]. Он является гомодимерным сиаломуцином, преимущественно экспрессированным на лейкоцитах.
При воспалительных заболеваниях разупорядоченная трансмиграция обеспечивается, по меньшей мере отчасти, посредством повышенной экспрессии E- и P- селектинов на поверхности клеток. В отличие от их низкой базальной экспрессии, экспрессия E- и P-селектинов повышается во время воспаления, приводя к существенному привлечению лейкоцитов в воспаленную ткань. Хотя клеточная адгезия, опосредованная селектинами, требуется для борьбы с инфекцией, существуют различные ситуации, в которых такая клеточная адгезия является нежелательной или избыточной, приводя к тяжелым повреждениям ткани вместо восстановления. В случае многих как острых, так и хронических нарушений (т.к. астма, хроническое обструктивное заболевание легких (ХОЗЛ), псориаз и т.д.) была показана связь инфильтрации активированных лейкоцитов в ткани с одновременным явным усилением экспрессии соответствующих молекул адгезии, в частности, E- и P-селектина, в тканях. [Muller et al., J. Pathol., 2002, 198(2), 270-275; Di Stefano et al., Am. J. Respir. Crit. Care. Med., 1994, 149(3), 803-810; Terajima et al., Arch. Dermatol. Res., 1998, 290, 246-252].
Инфильтрация лейкоцитов может также играть роль в воспалительных симптомах при отторжении трансплантата и пересаженных тканей. Также процесс свертывания крови дополнительно промотируется лейкоцит-лейкоцит и лейкоцит-тромбоцит связываниями, которые реализуются потому, что лейкоциты имеют как L-селектин, так и его соответствующий лиганд PSGL-1, и таким образом могут взаимодействовать с другими лейкоцитами через PSGL-1 и могут также связываться с тромбоцитами, которые несут P-селектин.
Следовательно, модулирование клеточной адгезии с участием селектина и других функций с их участием, например, активации лейкоцитов, предлагает многообещающую возможность вмешиваться в воспалительный каскад и останавливать его на очень ранней стадии. Для предотвращения возможного избыточного наличия селектинов низкомолекулярные антагонисты селектина должны модулировать все три селектина одновременно как пан-селектиновые антагонисты [M. Sperandio et al., Vascular Disease Prevention, 2004, 1, 185-195].
Помимо sLex/sLea природный лиганд высокого сродства PSGL-1 является еще одной структурой-шаблоном для разработки низкомолекулярных антагонистов селектина. По сравнению с sLex/sLea, PSGL-1 проявляет высокое сродство ко всем трем селектинам. Нахождение и обнаружение новых низкомолекулярных лекарственных средств, которые конкурируют с PSGL-1 и PSGL-1-подобными лигандами за связывание с селектином, является, таким образом, многообещающей стратегией разработки нового класса эффективных пан-селектиновых антагонистов для лечения воспалительных заболеваний.
Селектиновые антагонисты могут быть разработаны с использованием в качестве структуры-шаблона как селектинов, так и лигандов типа PSGL-1, т.к. они предназначены для модулирования связывания между селектинами и PSGL-1 или другими лигандами с похожими связывающими фрагментами.
Новые низкомолекулярные антагонисты селектина могут столкнуться с определенными требованиями для того, чтобы соответствовать понятию лекарственного средства и обладать потенциальной биодоступностью при пероральном введении. Термин соответствия лекарственному средству описан в литературе [Lipinski; Adv. Drug Dev. Rev., 1997, 23, 3-25]. Помимо иных молекулярных свойств для соответствия лекарству подразумевается, что пассивно транспортируемые молекулы в среднем имеют относительную молекулярную массу менее 500. Согласно этим правилам, общепринято определять соединения с относительной молекулярной массой менее 500 или несколько выше как малые молекулы (низкомолекулярные вещества). Соединения с относительной молекулярной массой выше 500 скорее всего не являются биодоступными при пероральном введении. Также с концепцией соответствия лекарственному средству не согласуется наличие высокополярных углеводных фрагментов или пептидных компонентов. [H. Ulbrich et al., Trends Pharmacol. Sci., 2003, 24(12), 640-647; D. Slee et al., J. Med. Chem., 2001, 44, 2094-2107]. То же самое имеет значение при разработке медикаментов на основе антител, поскольку они являются полипептидами и в силу этого пероральное введение является проблематичным. Более того, желаемые соединения должны оставаться стабильными при прохождении через желудочно-кишечный тракт, т.к. они должны быть поглощены/впитаны после клетками тонкого кишечника. Такая ситуация не имеет места в случае большинства гликозидных молекул и пептидных структур.
Некоторые нитрокатехолы, выступая как специфические ингибиторы катехол-О-метилтрансферазы (COMT), были предложены для лечения болезни Паркинсона [J. Axelrod et al., J. Biol. Chem., 1958, 233(3), 702-705; P. T. Mānnisto et al., Pharmacological Reviews, 1999, 51, 593-628], например толкапон, нитекапон и энтакапон [EP00426468]. Также нитрокатехолы описаны как обладающие кардиозащитным действием, вызванным хелатированием железа [N. Haramaki et al., Biochemical Pharmacology, 1995, 50, 839-843] или снижением уровня гомоцистеина в плазме [E. Nissinen et al., J. Neural Transm., 2005, 112, 1213-1221]. Нитекапон также заявлялся как перехватчик свободных радикалов [Y. J. Suzuki et al., Free Radical Biology & Medicine, 1992, 13, 517-525; L. Marcocci et al., Biochemistry and Molecular Biology International, 1994, 34, 531-541]. Некоторые наблюдения показывают, что энтакапон может защищать от вызываемого ангиотензином II повреждения почек [T. Helkamaa et al., J. Hypertens., 2003, 21, 2353-2363].
Однако вплоть до настоящего времени нитрокатехолы не были описаны в качестве модулирующих селектин соединений. Для разработки низкомолекулярных соединений с модулирующим процессы, опосредованные селектином действием были предприняты разнообразные исследования. Такие соединения включают дисалицилаты и С-глигозиды на основе дисалицилатов [WO 99/29706], бинзиламиносульфоновые кислоты [WO 03/097658], дигликозилированные 1,2-диолы [WO 97/01569], замещенные пятичленные гетероциклы [WO 00/33836], маннопиранозилоксифенилбензойные кислоты [EP0758243 B1], соединения на основе пиперазина [US6432957B1], производные галловой кислоты и пептидов [WO 2004/018502], галловую кислоту [C. C. M. Appeldoorn et al., Circulation, 2005, 111, 106-112; EP 1481669A1] и производные хинной кислоты [N. Kaila et al., J. Med. Chem., 2005, 48, 4346-4357].
Однако ни одно из этих селектин-антагонизирующих соединений не прошло успешно клинические испытания к настоящему времени. [S. J. Romano, Treat. Respir. Med., 2005, 4(2), 85-94; M. P. Schōn, Therapeutics and Clinical Risk Management, 2005, 1(3), 201-208]. Это является следствием того факта, что многие из этих структур были разработаны на основе слабосвязывающего шаблона sLex. Следовательно, sLex-миметические структуры, скорее всего, проявляют слабое действие. Другие соединения демонстрируют специфичность по отношению к различным членам семейства селектинов, однако антагонизация одного отдельного селектина может быть обойдено другими селектинами [M. P. Schōn, Therapeutics and Clinical Risk Management, 2005, 1(3), 201-208].
К тому же большинство соединений, разработанных к настоящему времени, обладают высокой молекулярной массой и зачастую содержат углеводы и/или пептиды, что делает их подверженными деградации и модификации пептидазами и/или гликозидазами. Углеводсодержащие структуры обладают и другими недостатками, такими как высокая степень хиральности, наличие аномерных центров и связанные с этим явления, низкая вероятность транспорта через липидный двойной слой. Подобные недостатки известны и для пептидсодержащих соединений. Некоторые другие соединения, разработанные для антагонизации процессов с участием селектина, содержат пирогаллольные субструктуры. Эти фрагменты склонны подвергаться окислительным процессам [Kumamoto M. et al., Biosci. Biotechnol. Biochem., 2001, 65(1), 126-132], что делает фармацевтическую разработку этих соединений затруднительной. К тому же известно, что соединения с пирогаллольными субструктурами, такие как галловая кислота, могут быть цитотоксичными [E. Sergediene et al., FEBS Letters, 1999, 462, 392-396] и вызывать апоптоз [K. Satoh et al., Anticancer Research, 1997, 17, 2487-2490; N. Sakaguchi et al., Biochemical Pharmacology, 1998, 55, 1973-1981].
Ведущим соединением среди антагонистов селектина является бимосиамоза (bimosiamose) [S. J. Romano, Treat. Respir. Med., 2005, 4(2), 85-94]. В настоящий момент бимосиамоза [D. Bock et al., New Drugs, 2003, D04, 28, p.28; EP 0 840 606 B1] является наиболее отлаженным соединением в клинических исследованиях. Недавние исследования подтвердили гипотезу, что бимосиамоза может рассматриваться как PSGL-1-миметик [E. Aydt, G. Wolff; Pathobiology; 2002-2003; 70; 297-301]. Это отличает бимосиамозу от других антагонистов селектина. Она, однако, имеет большую молекулярную массу и имеет углеводные структуры. Представляется, что пан-селектиновому антагонисту бимосиамозе недостает биодоступности при пероральном введении. Некоторые наблюдения свидетельствуют, что бимосиамоза демонстрирует хорошее сродство к P-селектину и умеренное сродство к E- и L-селектинам.
Имеется явно выраженная медицинская потребность в новых высокоэффективных пан-селектиновых антагонистах, которые модулируют функции, опосредованные селектинами, например селектин-зависимую клеточную адгезию, и в развитии способов вовлечения таких соединений для модулирования обстоятельств, связанных с взаимодействием лиганд-селектин. Большинство доступных противовоспалительных фармацевтических лечебных средств, доступных на рынке, включают, в основном, кортикостероиды или НСПВС (нестероидные противовоспалительные средства), имеющие несколько серьезных недостатков/побочных эффектов и направленные на различные стадии воспалительного каскада. В отличие от этого модулирование селектиновых функций является концепцией терапии, вмешивающейся в воспалительный каскад на очень ранней стадии. Почти все перспективные антагонисты селектина до настоящего времени не становились лекарственными средствами на рынке, в основном по причине низкой эффективности и/или большого молекулярного веса, что вызывает проблемы в их поведении в рамках абсорбции/распределения/метаболизма/выведения (АРМВ) и тем самым в биодоступности посредством перорального введения, требующейся для лечения большинства воспалительных заболеваний таких, как ревматоидный артрит, септический шок, атеросклероз, реперфузия и многие другие.
EP-A 1 577289 описывает ароматические соединения, гидроксилированные в фенильном кольце молекулы и которые могут быть использованы для лечения воспалительных заболеваний.
В WO 1997/01335 описаны ароматические соединения, связанные с углеводным остатком. Соединения, описанные в этом патенте, являются ингибиторами селектина и могут быть использованы как терапевтические средства, однако они структурно отличны от нитрозамещенных ароматических соединений по настоящему изобретению.
В EP-A 1 481669 описаны полигидроксифенолы, которые обладают P-селектин модулирующим действием.
Одной целью настоящего изобретения является предложение новых низкомолекулярных соединений, особенно негликозилированных/негликозидных и непептидных соединений, которые способны эффективно антагонизировать процессы, опосредованные селектинами и которые имеют меньшие отрицательные побочные эффекты в ходе их применения, чем соединения, известные из предшествующего уровня техники.
В отличие от большинства sLex-миметиков, разработанных в данной области, соединения по изобретению не подвержены действию гликозидаз или пептидаз. Большинство антагонистов селектина, разработанных к настоящему времени, основаны структурно и биологически на свойствах sLex или sLea. Получающиеся соединения показывают поэтому низкую биологическую активность, как и соединения-матрицы. Настоящее изобретение, однако, относится к новым мощным низкомолекулярным и соответствующим лекарственному средству пан-селектиновым антагонистам, которые были созданы на основе биологических in vitro исследований, имитируя PSGL-1 и PSGL-1-подобные лиганды или любые лиганды, несущие sLex или sLea и тирозинсульфатный фрагменты. [N. V. Bovin; Biochem. Soc. Symp.; 2002; (69): 143-60. N. V. Bovin; Glycoconj. J.; 1998; 15(5); 431-46. T. V. Pochechueva et al.; Bioorg. Med. Chem. Lett.; 2003 ; 13(10); 1709-12. G. Weitz-Schmidt et al.; Anal. Biochem.; 1996; 238; 184-190].
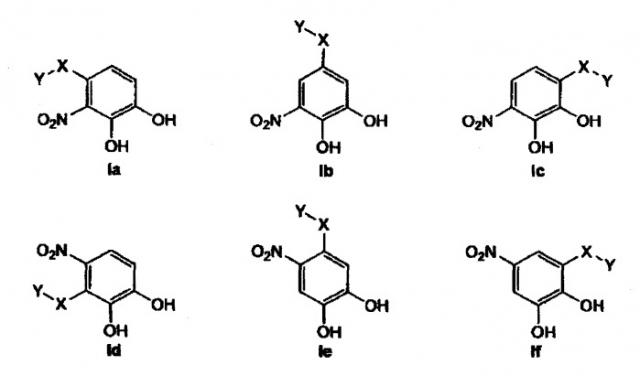
Настоящее изобретение относится к фармацевтическим композициям, содержащим по меньшей мере одно соединение, описываемое формулой (Ia) или (Ib) или (Ic) или (Id) или (Ie) или (If), и фармацевтически приемлемый носитель, используемый в медицине,
где символы и заместители имеют следующее значение:
-X- представляет собой
(a)
m равно 0, 1; n равно целому числу от 1 до 3
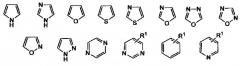
(b)
где “ring” является
и R1 представляет собой H, NO2, CF3, F, Cl, Br, I, CN, CH3, NH2, NHалкил, NHарил, NHацил и k равно 0, 1,
(c)
T представляет собой O, S или [H,H]; p равно 0, 1, 2,
(d)
двойная связь имеет E- или Z- конфигурацию
(e)
(f)
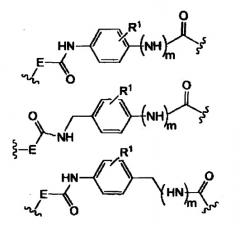
-E- представляет собой -(CH2-)qNH- и q равно 0, 1, 2, 3
-Y представляет собой
(a)
s равно 0 или 1,
R2 представляет собой CO2H, CO2алкил, CO2арил, CO2NH2, CO2аралкил, SO3H, SO2NH2, PO(OH)2, 1-H-тетразолил-, CHO, COCH3, CH2OH, NH2, NHалкил, N(алкил)алкил', OCH3, CH2OCH3, SH, F, Cl, Br, I, CH3, CH2CH3, CN, CF3,
R3, независимо от R2, представляет собой H, CH3, CH2CH3, CF3, F, Cl, Br, I, CN, NO2,
R4, независимо от R2 и R3, представляет собой H, CH3, CH2CH3, CF3, F, Cl, Br, I, CN, NO2, R2,
R5 представляет собой H, NO2, CF3, F, Cl, Br, I, CN, CH3, OCH3, SH, NH2 и
-W- представляет собой -(CH2-)V, цис-CH=CH- или транс-CH=CH-, и v равно 0, 1, 2;
в случае, если -W- является цис-CH=CH- или транс-CH=CH-, R2 не должен быть NH2 или SH;
(b)
R6, независимо от R2, представляет собой H, F, Cl, Me, трет-Bu, CN, NH2,
(c)
(d)
(e)
t равно 0, 1, 2
(f)
(g)
-Z представляет собой
(i)
R7, независимо от R2, представляет собой H, NO2, CF3, F, Cl, Br, I, CN, CH3, OCH3, SH, NH2,
(ii)
R8, независимо от R2, представляет собой H, F, Cl, Me, трет-Bu, CN, NH2,
(iii)
(iv)
K представляет собой NH, NMe, O, S,
(v)
(vi)
(vii)
-W-R2
или фармацевтически приемлемые соли, сложные эфиры или амиды и пролекарства определенных выше соединений формулы (Ia) или (Ib) или (Ic) или (Id) или (Ie) или (If).
В предпочтительном варианте осуществления изобретения композиция включает по меньшей мере одно соединение формулы (Ib) или (Ic) или (Ie) или (If) и фармацевтически приемлемый носитель
где символы и заместители имеют следующее значение
-X- представляет собой
(a)
m равно 0, 1; n равно целому числу от 1 до 3
(b)
где «ring» является
и R1, представляет собой H, NO2, CF3, F, Cl, Br, I, CN, CH3, NH2, NHалкил, NHарил, NHацил и k равно 0, 1.
(e)
- Y представляет собой
(a)
s равно 0 или 1,
R2 представляет собой CO2H, CO2алкил, CO2арил, CO2NH2, CO2аралкил, SO3H, SO2NH2, PO(OH)2, 1-H-тетразолил-, CHO, COCH3, CH2OH, NH2, NHалкил, N(алкил)алкил', OCH3, CH2OCH3, SH, F, Cl, Br, I, CH3, CH2CH3, CN, CF3,
R3, независимо от R2, представляет собой H, CH3, CH2CH3, CF3, F, Cl, Br, I, CN, NO2 и
R4, независимо от R2 и R3, представляет собой H, CH3, CH2CH3, CF3, F, Cl, Br, I, CN, NO2, R2,
R5 представляет собой H, NO2, CF3, F, Cl, Br, I, CN, CH3, OCH3, SH, NH2,
и -W- представляет собой -(CH2-)V, цис-CH=CH- или транс-CH=CH-, и v равно 0, 1, 2;
в случае, если -W- представляет собой цис-CH=CH- или транс-CH=CH-, R2 не должен быть NH2 или SH;
(e)
t равно 0, 1, 2
(f)
(g)
-Z представляет собой
(i)
R7, независимо от R2, представляет собой H, NO2, CF3, F, Cl, Br, I, CN, CH3, OCH3, SH, NH2,
(iv)
K представляет собой NH, NMe, O, S,
(v)
или фармацевтически приемлемые соли, сложные эфиры или амиды и пролекарства определенных выше соединений формулы (Ib) или (Ic) или (Ie) или (If).
Предпочтительные фармацевтические композиции включают соединения формул (IIa) или (IIb) или (IIc) или (IId) или (IIe) или (IIf)
где -Y является таким, как определено выше и в которых -X'- является X(a), X(b), X(c) и X(d) как определено выше.
В еще одном варианте осуществления изобретение относится к композициям, содержащим соединения структур:
где -Y и -X'- как X(a), X(b) являются такими, как определено выше.
Другие предпочтительные фармацевтические композиции включают соединения формул (A1) или (A2) или (A3) или (A4) или (A5) или (A6) или (B1) или (B2) или (B3) или (B4) или (B5) или (B6)
где -Y и -X'- являются такими, как определено выше и в которых -X”- является
и где Y' является
где все индексы, символы и заместители являются такими, как определено выше.
В еще одном варианте осуществления изобретение относится к фармацевтическим композициям, содержащим соединения формулы:
где -X'- и -Y являются такими, как определено выше и в которых -X”- является
и где Y' является
где все индексы, символы и заместители являются такими, как определено выше.
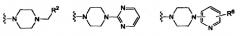
Особенно предпочтительные фармацевтические композиции содержат соединения формул (C1) или (C2) или (C3) или (C4) или (C5) или (C6)
где -X”- и -Y' являются такими, как определено выше.
Другая предпочтительная группа соединений соответствующей композиции имеет следующие структуры
где -X”- и -Y' являются такими, как определено выше.
Наиболее предпочтительные фармацевтические композиции содержат соединения формул (D1) или (D2) или (D3) или (D4) или (D5) или (D6)
где -X”- является таким, как определено выше, и -Y” является
R9 представляет собой CO2H, CO2алкил, CO2арил, CO2NH2, CO2аралкил, CH2SO3H, CH2SO2NH2, CH2PO(OH)2, 1-H-тетразолил, CHO, COCH3, CH2OH, CH2NH2, CH2NHалкил, CH2N(алкил)алкил', CH2OCH3, CH2SH.
Также предпочтительными являются фармацевтические композиции, в которых соединения определены формулами (D2) или (D3) или (D5) или (D6).
где -X”- является таким, как определено выше, и -Y” является
R9 представляет собой CO2H, CO2алкил, CO2арил, CO2NH2, CO2аралкил, CH2SO3H, CH2SO2NH2, CH2PO(OH)2, 1-H-тетразолил, CHO, COCH3, CH2OH, CH2NH2, CH2NHалкил, CH2N(алкил)алкил', CH2OCH3, CH2SH,
в которых все индексы, символы и заместители являются такими, как определено выше.
Эти химические соединения (C1), (C2), (C3), (C4), (C5), (C6), (D1), (D2), (D3), (D4), (D5) и (D6) являются также новыми соединениями сами по себе. Химические соединения, имеющие общую структуру формулы (C2) или (C3) или (C5) или (C6) или (D2) или (D3) или (D5) или (D6) являются предпочтительными.
Все описанные выше соединения проявляют способность модулированию клеточной адгезии и модулируют связывание, опосредованное селектином, а также аналога PSGL-1. Соединения имеют способность модулировать взаимодействие селектинов с sLex/sLea, а также взаимодействия между селектинами и тирозинсульфатными остатками. По сравнению с бимосиамозой, ведущим пан-селектиновым антагонистом, описанные здесь соединения показывают увеличенную биологическую активность. Поэтому они являются полезными для лечения острых и хронических воспалительных заболеваний, равно как и других медицинских состояний, в которых процессы, опосредованные селектином играют роль.
Термин «фармацевтический» включает также диагностические применения.
Термин «фармацевтический» включает также профилактические применения для предотвращения медицинских состояний, в которых играют роль процессы, опосредованные селектином.
Термин «фармацевтический» включает также применения, в которых соединения по настоящему изобретению могут быть использованы как носитель для введения лекарственного средства при диагностике или терапии.
Изобретение относится к фармацевтическим композициям, содержащим соединения в соответствии с формулами (Ia) или (Ib) или (Ic) или (Id) или (Ie) или (If) и в предпочтительном варианте в соответствии с формулами (IIa) или (IIb) или (IIc) или (IId) или (IIe) или (IIf).
В еще одном предпочтительном варианте изобретение относится к фармацевтическим композициям, содержащим по меньшей мере одно соединение, соответствующее формуле (A1) или (A2) или (A3) или (A4) или (A5) или (A6) или (B1) или (B2) или (B3) или (B4) или (B5) или (B6).
В особенно предпочтительном варианте изобретение относится к фармацевтическим композициям, содержащим по меньшей мере одно соединение, соответствующее формуле (C1) или (C2) или (C3) или (C4) или (C5) или (C6).
В предпочтительном варианте изобретение относится к фармацевтическим композициям, содержащим по меньшей мере одно соединение, соответствующее формуле (D1) или (D2) или (D3) или (D4) или (D5) или (D6).
В еще одном варианте осуществления изобретения соединения, соответствующие формулам A2, A3, A5, A6, B2, B3, B5, B6, C2, C3, C5, C6, D2, D3, D5 или D6, используются в композиции.
Настоящее изобретение далее относится к способу модулирования связывания P-селектина, L-селектина или E-селектина c sLex или sLea и тирозинсульфатных остатков, включающий стадию введения пациенту эффективного количества по меньшей мере одного соединения, имеющего формулу (Ia) или (Ib) или (Ic) или (Id) или (Ie) или (If) для модулирования связывания P-, L- или E-селектина c sLex или sLea и тирозинсульфатным остатком. Было обнаружено, что соединения, имеющие формулу (Ia) или (Ib) или (Ic) или (Id) или (Ie) или (If), показанные выше, выступают в качестве модуляторов связывания P-, L- или E-селектина.
Используемый здесь термин «алкил» следует понимать как одновалентную, с неразветвленной или разветвленной цепочкой, группу из 1 или 2 или 3 или 4 или 5 или 6 или 7 или 8 или 9 или 10 или 11 или 12 углеродными атомами, включая, но не ограничиваясь перечисленным, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил и т.п. «Алкил» является независимым один от другого и может отличаться или совпадать.
Термин «арил» следует понимать как карбоциклические или гетероциклические ароматические группы, включая, но не ограничиваясь, фенил, 1-нафтил, 2-нафтил, флуоренил, 1,2-дигидронафтил, инденил, инданил, тиенил, бензотиенил, тиенопиридил и т.п.
Термин «аралкил», также называемый «арилалкил» следует понимать как арильную группу, прикрепленную к алкильной группе, включая, но не ограничиваясь, бензил, 1-нафтилметил, 2-нафтилметил, фторбензил, хлорбензил, бромбензил, иодбензил, алкоксибензил (где «алкокси» означает метокси, этокси, изопропокси, н-бутокси, втор-бутокси, трет-бутокси и т.п.), гидроксибензил, аминобензил, нитробензил, гуанидинобензил, флуоренилметил, фенилметил (бензил), 1-фенилэтил, 2-фенилэтил, 1-нафтилэтил и т.п.
Термин «ацил» следует понимать как -(CHO) или -(С=O)-арил или -(С=O)-алкил или -(С=О)-аралкил, включая, но не ограничиваясь, формил, ацетил, н-пропионил, изопропионил, н-бутирил, изобутирил, пивалоил, бензоил, 4-нитробензоил и т.п.
Используемый здесь термин «фармацевтически приемлемые соли, сложные эфиры, амиды и пролекарства» относится к тем солям карбоновых кислот, солям присоединения аминокислот, сложным эфирам, амидам и пролекарствам соединений по настоящему изобретению, которые, в рамках действующих медицинских представлений, подходят для использования при контакте с тканями пациента без чрезмерной токсичности, раздражающего действия, аллергического отклика и т.п., обладают соответствующим разумным отношением польза/риск, эффективны в назначаемом использовании, равно как и цвиттерионные формы, где они возможны, соединений по настоящему изобретению. Термин «соли» относится к солям присоединения относительно нетоксичных неорганических и органических кислот соединений по настоящему изобретению. Эти соли могут быть получены in situ во время конечного выделения и очистки соединений или же отдельным вовлечением очищенных соединений в их свободной форме в реакцию с соответствующей неорганической или органической кислотой или основанием и выделения таким образом полученной соли. Типичные соли соединений по изобретению включают гидробромид, гидрохлорид, сульфат, бисульфат, нитрат, ацетат, оксалат, валерат, пальмитат, стеарат, лаурат, борат, бензоат, лактат, фосфат, тозилат, цитрат, малеат, фумарат, сукцинат, тартрат, нафтилат, мезилат, глюкогептонат, лактиобионат, лаурилсульфонат и т.п. Они могут включать катионы щелочных и щелочноземельных металлов, таких как натрий, литий, калий, кальций, магний и т.п., также как нетоксичные катионы аммония, четвертичного аммония и аминов включая, но не ограничиваясь, аммоний, тетраметиламмоний, тетраэтиламмоний, метиламин, диметиламин, триметиламин, триэтиламин, этиламин и т.п.
Примеры фармацевтически приемлемых нетоксичных сложных эфиров соединений по настоящему изобретению включают C1, C2, C3, C4, C5 и C6 алкиловые сложные эфиры, в которых алкильная группа имеет прямую или разветвленную цепь. Приемлемые сложные эфиры также включают C5, C6 и C7 циклоалкиловые сложные эфиры, равно как и арилалкиловые эфиры, такие как, но не ограничиваясь, бензиловый. C1, C2, C3, C4, C5 и C6 алкиловые сложные эфиры являются предпочтительными. Сложные эфиры соединений по настоящему изобретению могут быть получены общепринятыми способами.
Примеры фармацевтически приемлемых нетоксичных амидов соединений по этому изобретению включают амиды-производные аммиака, первичных C1, C2, C3, C4, C5 и C6 алкиламинов и вторичных C1, C2, C3, C4, C5 и C6 диалкиламинов, в которых алкильная группа имеет прямую или разветвленную цепь. В случае вторичных аминов амин может быть в виде пяти- или шестичленного гетероцикла, содержащего один атом азота. Амиды - производные аммиака, C1, C2 и C3 первичные алкиламины и C1, C2 вторичные диалкиламины являются предпочтительными. Амиды соединений по настоящему изобретению могут быть получены с использованием общепринятых способов.
Термин «пролекарство» относится к одному или более соединений, которые легко трансформируются in vitro и из неактивного в активное состояние in vivo с образованием соединения, родственного вышеупомянутым формулам (Ia) или (Ib) или (Ic) или (Id) или (Ie) или (If), например, посредством гидролиза в крови или метаболизма in vivo.
Также предполагается, что фармацевтически активная композиция может содержать соединения по настоящему изобретению или другие соединения, которые модулируют или составляют конкуренцию в связывании E-селектина или P-селектина или L-селектина.
Фармацевтически активные композиции по настоящему изобретению включают фармацевтически приемлемый носитель и соединение по формуле (Ia) или (Ib) или (Ic) или (Id) или (Ie) или (If), в каком случае фармацевтически приемлемый носитель может также быть медицински подходящей наночастицей, дендримером, липосомой, микропузырьком или полиэтиленгликолем (ПЭГ). Фармацевтические композиции по настоящему изобретению могут включать одно или более соединений, имеющих вышеприведенные структуры (Ia) или (Ib) или (Ic) или (Id) или (Ie) или (If), составленные вместе с одним или более физиологически приемлемым носителем, адъювантом или наполнителем, которые все вместе описываются здесь как носители, для парентерального введения, для перорального введения в жидкой или твердой форме, для ректального или местного введения и т.п.
Композиции могут быть введены человеку или животным перорально, ректально, парентерально (внутривенно, внутримышечно, внутрикожно или подкожно), интрацистернально, вагинально, внутрибрюшно, местно (порошки, мази или капли) или буккально или ингаляционно (распыленным или в виде назальных спреев).
Композиции, подходящие для парентерального введения, могут включать физиологически приемлемые стерильные водные или неводные растворы, стабилизаторы, антиоксиданты, консерванты (например, аскорбиновую кислоту, сульфит натрия, гидросульфит натрия, бензиловый спирт, ЭДТА), дисперсии, суспензии или эмульсии и стерильные порошки для воссоздания в стерильный вводимый раствор или дисперсию. Примеры подходящих водных или неводных носителей, разбавителей, растворителей или носителей включают воду, этанол, полиол (пропиленгликоль, полиэтиленгликоль, глицерин и т.п.), подходящие смеси таковых, растительные масла (такие как оливковое или масло канола) и вводимые органические сложные эфиры, такие как этилолеат. Подобающая текучесть может поддерживаться, например, использованием покрытий, таких как лецитин, поддерживанием требуемого размера частиц в случае дисперсий и использованием сурфактантов.
Эти композиции могут также содержать такие вспомогательные вещества, как консервирующие, увлажняющие, эмульгирующие и диспергирующие вещества. Предохранение от действия микроорганизмов может быть обеспечено различными противомикробными и противогрибковыми веществами, например парабенами, хлорбутанолом, фенолом, (Е,Е)-Гекса-2,4-диеновая кислотой и т.п. Также может быть желательным включение изотонических веществ, например сахаров, хлорида натрия и т.п. Пролонгированное впитывание для закапываемых фармацевтических форм может быть осуществлено использованием веществ, замедляющих всасывание, например, моностеаратом алюминия и желатином.
Если желательно для более эффективного распределения, со