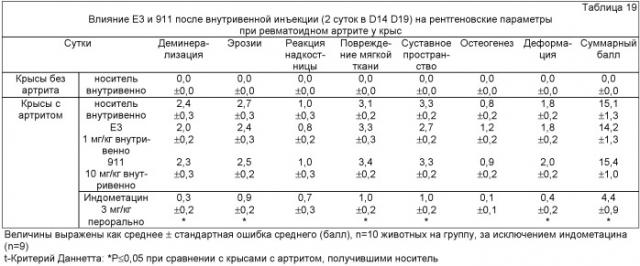
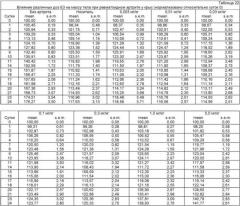
Способы лечения боли, вызванной остеоартритом, путем введения антагониста фактора роста нервов и содержащих его композиций
Иллюстрации
Показать всеГруппа изобретений относится к применению антител против фактора роста нервов (NGF) (анти-NGF антитела) для лечения боли, улучшения физической функции и уменьшения ригидности у индивида, имеющего остеоартрит. Представлены: способ лечения боли, улучшения физической функции и уменьшения ригидности у индивида, имеющего остеоартрит, включает введение указанному индивиду эффективного количества анти-NGF антитела, а также набор и фармацевтическая композиция для осуществления такого способа лечения. Показано, что разовое введение анти-NGF антитела не только снижает боль, но также улучшает физическую функцию и уменьшает ригидность у пациентов, имеющих остеоартрит. 3 н. 21 з.п. ф-лы, 23 табл., 27 ил.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
В данной заявке испрашивается приоритет заявки на патент США №11/104248, поданной 11 апреля 2005, которая включена в данное описание ссылкой во всей полноте.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к антителам против фактора роста нервов (NGF), таким как антагонистические антитела против NGF. Это изобретение дополнительно относится к применению антагонистов, таких как антитела, в лечении и/или предотвращении боли, включая послеоперационную боль, боль, вызванную ревматоидным артритом, и боль, вызванную остеоартритом.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Фактор роста нервов (NGF) был первым идентифицированным нейротрофином, и его роль в развитии и выживании как периферических, так и центральных нейронов хорошо охарактеризована. Показано, что при развитии NGF является критическим фактором выживания и поддержания периферических симпатических и эмбриональных сенсорных нейронов и холинергических нейронов базального переднего мозга. Smeyne et al., Nature 368:246-249 (1994), и Crowley et al., Cell 76:1001-1011 (1994). NGF повышает экспрессию нейропептидов в сенсорных нейронах (Lindsay and Harmer, Nature 337:362-364 (1989)), причем его активность опосредована двумя разными связанными с мембраной рецепторами, тирозинкиназным рецептором TrkA и общим рецептором нейротрофинов р75 (иногда называемых рецепторами NGF "высокой аффинности" и "низкой аффинности" соответственно). Chao et al., Science 232:518-521 (1986). р75-Рецептор по структуре родственен другим членам семейства рецепторов фактора некроза опухолей (Chao, et al., Science 232:518-521 (1986)). Обзор по NGF см. в Huang et al., Annu. Rev. Neurosci. 24:677-736 (2001); Bibel et al., Genes Dev. 14:2919-2937 (2000). Определена кристаллическая структура NGF и NGF в комплексе с TrkA-рецептором. См. Nature 254:411 (1991); Nature 401:184-188 (1996).
В дополнение к его эффектам в нервной системе, NGF все больше считают вовлеченным в процессы вне нервной системы. Например, показано, что NGF усиливает сосудистую проницаемость (Otten et al., Eur J Pharmacol. 106:199-201 (1984)), усиливает Т- и В-клеточные иммунные ответы (Otten, et al., Proc. Natl. Acad. Sci. USA 86:10059-10063 (1989)), индуцирует дифференцировку лимфоцитов и пролиферацию тучных клеток и вызывает высвобождение растворимых биологических сигналов из тучных клеток (Matsuda, et al., Proc. Natl. Acad. Sci. USA 85:6508-6512 (1988); Pearce, et al., J. Physiol. 372:379-393 (1986); Bischoff, et al., Blood 79:2662-2669 (1992); Horigome, et al., J. Biol. Chem. 268:14881-14887 (1993)). Хотя показано, что экзогенно добавленный NGF способен ко всем этим эффектам, важно отметить, что только в редких случаях показано, что эндогенный NGF является важным в каком-либо из этих процессов in vivo (Torcia, et al., Cell. 85(3):345-56 (1996)). Поэтому неясно, каким может быть эффект, если он вообще есть, ингибирования биологической активности эндогенного NGF.
NGF продуцируют многие типы клеток, в том числе тучные клетки (Leon, et al., Proc. Natl. Acad. Sci. USA 91:3739-3743 (1994)), В-лимфоциты (Torcia, et al., Cell 85:345-356 (1996), кератиноциты (Di Marco, et al., J. Biol. Chem. 268:22838-22846)), гладкомышечные клетки (Ueyama, et al., J. Hypertens. 11:1061-1065 (1993)), фибробласты (Lindholm, et al., Eur. J. Neurosci. 2:795-801 (1990)), бронхиальные эпителиальные клетки (Kassel, et al., Clin, Exp. Allergy. 31:1432-40 (2001)), почечные мезангиальные клетки (Steiner, et al., Am. J. Physiol. 261:F792-798 (1991)) и мышечные трубочки скелетных мышц (Schwartz, et al., J Photochem. PhotoBiol. B66:195-200 (2002)). Рецепторы NGF обнаружены на множестве разных типов клеток вне нервной системы. Например, Trka обнаружен на человеческих моноцитах, Т- и В-лимфоцитах и тучных клетках.
Взаимосвязь между повышенными уровнями NGF и множеством различнных воспалительных состояний наблюдали у больных людей, а также в некоторых животных моделях. Они включают системную красную волчанку (Bracci-Laudiero, et al., Neuroreport 4:563-565 (1993)), рассеянный склероз (Bracci-Laudiero, et al., Neurosci. Lett. 147:9-12 (1992)), псориаз (Raychaudhuri, et al., Acta Derm. l'enereol. 78:84-86 (1998)), артрит (Falcim, et al., Ann. Rheum. Dis. 55:745-748 (1996)), интерстициальный цистит (Okragly, et al., J. Urology 161:438-441 (1999)) и астму (Braun, et al., Eur. J Immunol. 28:3240-3251 (1998)).
Соответственно повышенный уровень NGF в периферических тканях связан с гипералгезией и воспалением, и его наблюдали при многих формах артрита. Синовиальная мембрана пациентов, пораженных ревматоидным артритом, экспрессирует высокие уровни NGF, в то время как сообщалось, что в невоспаленной синовиальной мембране NGF не выявлен (Aloe, et al., Arch. Rheum. 35:351-355 (1992)). Такие же результаты наблюдали у крыс с экспериментально индуцированным ревматоидным артритом (Aloe, et al., Clin. Exp.Rheumatol. 10:203-204 (1992)). Сообщалось о повышенных уровнях NGF наряду с увеличенным числом тучных клеток у трансгенных артритных мышей (Aloe, el al., Int. J. Tissue Reactions-Exp.Clin. Aspects. 15:139-143 (1993)). В публикации РСТ WO № 02/096458 раскрыто применение антител против NGF с определенными свойствами в лечении различных расстройств, связанных с NGF, таких как воспалительное состояние (например, ревматоидный артрит). Сообщалось, что очищенное антитело против NGF, инъецированное артритным трансгенным мышам, несущим ген человеческого фактора-α некроза опухолей (tumor necrosis factor, TNF-α), вызывает снижение числа тучных клеток, а также снижение уровней гистамина и вещества Р в синовиальной мембране артритных мышей (Aloe et al., Rheumatol. Int. 14: 249-252 (1995)). Показано, что экзогенное введение антитела против NGF снижает повышенные уровни TNF-α, имеющие место у артритных мышей (Manni et al., Rheumatol. Int. 18: 97-102 (1998)).
Кроме того, повышенную экспрессию NGF и высокоаффинного рецептора NGF (TrkA) наблюдали в человеческих остеоартритных хондроцитах (Iannone et al., Rheumatology. 41:1413-1418 (2002)).
Сообщалось об антагонистических антителах грызунов против NGF. См., например, Hongo et al, Hybridoma (2000), 19(3):215-227; Ruberti et al. (1993) Cell. Molec. Neurobiol. 13(5): 559-568. Однако когда антитела грызунов используют в терапевтических целях у людей, у значительного числа леченых индивидуумов развивается ответ в виде продуцирования антител человека против мыши. В дополнение, эффекторные функции мышиных антител оказались менее эффективными в контексте человека. Таким образом, имеется насущная необходимость в антагонистических антителах против NGF, в том числе в гуманизированных антагонистических антителах против NGF.
Все ссылки, публикации и заявки на патент, раскрытые здесь, включены в данное описание ссылкой во всей полноте.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Раскрытое здесь изобретение относится к антителам к фактору роста нервов.
В другом аспекте это изобретение представляет собой гуманизированное и имеющее развитую аффинность антитело, Е3, которое специфично связывается с фактором роста нервов ("NGF") человека и грызунов. Аминокислотные последовательности вариабельных областей тяжелой цепи и легкой цепи Е3 показаны на Фиг.1А (SEQ ID NO:1) и 1Б (SEQ ID NO:2) соответственно. Гипервариабельные участки (complementarity determining region, CDR) антитела Е3 (включая CDR по Chothia и по Kabat) представлены в виде диаграмм на Фиг.1А и 1Б. Аминокислотные последовательности тяжелых и легких цепей Е3 и индивидуальных расширенных CDR также показаны ниже (см. ниже "последовательности антител").
В другом аспекте это изобретение представляет собой антитело, содержащее фрагмент или область антитела Е3 (взаимозаменяемым образом обозначаемого здесь как "Е3"). В одном из воплощений этот фрагмент представляет собой легкую цепь антитела Е3, как показано на Фиг.1Б. В еще одном воплощении этот фрагмент представляет собой тяжелую цепь антитела Е3, как показано на Фиг.1А. В еще одном воплощении этот фрагмент содержит одну или более чем одну вариабельную область легкой цепи и/или тяжелой цепи антитела Е3. В еще одном воплощении этот фрагмент содержит один или более чем один гипервариабельный участок (CDR) легкой цепи и/или тяжелой цепи антитела Е3, как показано на Фиг.1А и 1Б.
В другом аспекте это изобретение представляет собой антитело, содержащее легкую цепь, которую кодирует полинуклеотид, продуцируемый клеткой-хозяином, с номером депонирования АТСС № РТА-4893 или АТСС №РТА-4894. В другом аспекте это изобретение представляет собой антитело, содержащее тяжелую цепь, которую кодирует полинуклеотид, продуцируемый клеткой-хозяином, с номером депонирования АТСС № РТА-4895. В другом аспекте это изобретение представляет собой антитело, содержащее: (а) легкую цепь, которую кодирует полинуклеотид, продуцируемый клеткой-хозяином, с номером депонирования АТСС № РТА-4894 или АТСС № РТА-4893, и (б) тяжелую цепь, которую кодирует полинуклеотид, продуцируемый клеткой-хозяином, с номером депонирования АТСС № РТА-4895 (для удобства, полинуклеотид(ы), продуцируемые депонированной клеткой-хозяином, обозначены здесь как имеющие номера депонирования АТСС РТА-4894, РТА-4893 и РТА-4895). В другом аспекте это изобретение представляет собой антитело, содержащее вариабельную область легкой цепи из легкой цепи, которую кодирует полинуклеотид, продуцируемый клеткой-хозяином, с номером депонирования АТСС № РТА-4894 или АТСС № РТА-4893. В другом аспекте это изобретение представляет собой антитело, содержащее вариабельную область тяжелой цепи из тяжелой цепи, которую кодирует полинуклеотид, продуцируемый клеткой-хозяином, с номером депонирования АТСС № РТА-4895. В другом аспекте это изобретение представляет собой антитело, содержащее: (а) вариабельную область легкой цепи из легкой цепи, которую кодирует полинуклеотид, продуцируемый клеткой-хозяином, с номером депонирования АТСС № РТА-4894 или АТСС № РТА-4893, и (б) вариабельную область тяжелой цепи из тяжелой цепи, которую кодирует полинуклеотид, продуцируемый клеткой-хозяином, с номером депонирования АТСС № РТА-4895. В еще одном аспекте это изобретение представляет собой антитело, содержащее один или более чем один CDR, кодируемый: (а) полинуклеотидом, продуцируемым клеткой-хозяином, с номером депонирования АТСС № РТА-4894, и/или (б) тяжелую цепь, которую кодирует полинуклеотид, продуцируемый клеткой-хозяином, с номером депонирования АТСС № РТА-4895.
В некоторых воплощениях антитело содержит константную область тяжелой цепи lgG2a человека. В некоторых воплощениях антитело содержит константную область человеческой легкой каппа-цепи. В некоторых воплощениях антитело содержит модифицированную константную область, такую как константная область, которая является иммунологически инертной, например не вызывает опосредованный комплементом лизис или не стимулирует антителозависимую клеточно-опосредованную цитотоксичность (ADCC). В других воплощениях константная область модифицирована, как описано в Eur. J. Immunol. (1999) 29:2613-2624; заявка РСТ № PCT/G 899/01441; и/или заявка на патент UK №9809951.8. В еще других воплощениях антитело содержит константную область тяжелой цепи lgG2a человека, содержащую следующие мутации: А330Р331 в S330S331 (нумерация аминокислот по последовательности lgG2a дикого типа). Eur. J. Immunol. (1999) 29:2613-2624.
В другом аспекте в этом изобретении предложены полипептиды (которые могут быть или могут не быть антителом), содержащие любое одно или более чем одно из следующего: а) один или более чем один CDR антитела Е3, показанный на Фиг.1А и 1Б; б) CDR-H3 из тяжелой цепи антитела Е3, показанный на Фиг.1А; в) CDR-L3 из легкой цепи антитела Е3, показанный на Фиг.1Б; г) три CDR из легкой цепи антитела Е3, показанные на Фиг.1Б; д) три CDR из тяжелой цепи антитела Е3, показанные на Фиг.1А; и е) три CDR из легкой цепи и три CDR из тяжелой цепи антитела Е3, показанные на Фиг.1А и 1Б. В этом изобретении дополнительно предложены полипептиды (которые могут быть или не быть антителом), содержащие любое одно или более чем одно из следующего: а) один или более чем один (один, два, три, четыре, пять или шесть) CDR, происходящий(е) из антитела Е3, показанный(е) на Фиг.1А и 1Б; б) CDR, происходящий из CDR-H3 из тяжелой цепи антитела Е3, показанный на Фиг.1А; и/или в) CDR, происходящий из CDR-L3 из легкой цепи антитела Е3, показанный на Фиг.1Б. В некоторых воплощениях CDR может представлять собой CDR по Kabat, CDR no Chothia или комбинацию CDR по Kabat и no Chothia (называемую здесь "расширенным" или "объединенным" CDR). В некоторых воплощениях полипептиды (такие как антитело) связываются с NGF (такими как человеческий NGF). В некоторых воплощениях полипептиды содержат любую конфигурацию CDR (включая комбинации, варианты и так далее), описанную здесь.
В одном из аспектов в этом изобретении предложены полипептиды (такие как антитело), которые содержат вариабельную область тяжелой цепи, содержащую SEQ ID NO:9, где I34 представляет собой S, L, V А или I и N35 заменена на N, Т или S. "Заменена на" или "представляет собой" в этом контексте или как ссылка на аминокислоту для удобства относится здесь к вариантам выбора аминокислот(ы) для данного положения. Понятно, что замена или выбор может представлять собой аминокислоту, указанную в SEQ ID или на Фигуре.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые включают вариабельную область тяжелой цепи, содержащую SEQ ID NO:10, где М50 представляет собой М, I, G, Q, S или L; А62 представляет собой А или S и L63 представляет собой L или V.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые включают вариабельную область тяжелой цепи, содержащую SEQ ID NO:11, где Y100 представляет собой Y, L или R; где Y101 представляет собой Y или W; где G103 представляет собой G, А или S; где Т104 представляет собой Т или S; где S105 представляет собой S, А или Т; где Y106 представляет собой Y, R, Т или М; где Y107 представляет собой Y или F; где F108 представляет собой F или W; где D109 представляет собой D, N или G и где Y110 представляет собой Y, K, S, R или Т.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат вариабельную область тяжелой цепи, содержащую SEQ ID NO:11, где Y100 представляет собой Y, L или R; где Y101 представляет собой Y или W; где G103 представляет собой G, А или S; где Т104 представляет собой Т или S; где S105 представляет собой S, А или Т; где Y106 представляет собой Y, R, Т или М; где Y107 представляет собой Y или F; где F108 представляет собой F или W; где D109 представляет собой S, А, С, G, D, N, Т или G и где Y110 представляет собой любую аминокислоту.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат вариабельную область тяжелой цепи, содержащую SEQ ID NO:11, где G98 представляет собой G, S, А, С, V, N, D или Т; где G99 представляет собой G, S, А, С, V, N, D или Т; где Y100 представляет собой Y, L или R; где Y101 представляет собой Y или W; где G103 представляет собой G, А или S; где Т104 представляет собой Т или S; где S105 представляет собой S, А или Т; где Y106 представляет собой Y, R, Т или М; где Y107 представляет собой Y или F; где F108 представляет собой F или W; где D109 представляет собой S, А, С, G, D, N, Т или G и где Y110 представляет собой любую аминокислоту.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат вариабельную область легкой цепи, содержащую SEQ ID NO:12, где S26 представляет собой S или F; D28 представляет собой D, S, А или Y и Н32 представляет собой Н, N или Q.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат вариабельную область легкой цепи, содержащую SEQ ID NO:13, где 151 представляет собой I, Т, V или А и S56 представляет собой S или Т.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат вариабельную область легкой цепи, содержащую SEQ ID NO:14, где S91 представляет собой S или Е; K92 представляет собой K, Н, R или S и где Y96 представляет собой Y или R.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат вариабельную область легкой цепи, содержащую SEQ ID NO:14, где S91 представляет собой S или Е; K92 представляет собой любую аминокислоту; Т93 представляет собой любую аминокислоту и где Y96 представляет собой Y или R.
В одном из аспектов в этом изобретении предложены полипептиды (такие как антитело), которые содержат аминокислотную последовательность, показанную в SEQ ID NO:9, где I34 представляет собой S, L, V А или I и N35 представляет собой N, Т или S.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат аминокислотную последовательность, показанную в SEQ ID NO:10, где М50 представляет собой М, I, G, Q, S или L; А62 представляет собой А или S и L63 представляет собой L или V.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат аминокислотную последовательность, показанную в SEQ ID NO:11, где Y100 представляет собой Y, L или R; где Y101 представляет собой Y или W; где G103 представляет собой G, А или S; где Т104 представляет собой Т или S; где S105 представляет собой S, А или Т; где Y106 представляет собой Y, R, Т или М; где Y107 представляет собой Y или F; где F108 представляет собой F или W; где D109 представляет собой D, N или G и где Y110 представляет собой Y, K, S, R или Т.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат аминокислотную последовательность, показанную в SEQ ID NO:11, где Y100 представляет собой Y, L или R; где Y101 представляет собой Y или W; где G103 представляет собой G, А или S; где Т104 представляет собой Т или S; где 8105 представляет собой S, А или Т; где Y106 представляет собой Y, R, Т или М; где Y107 представляет собой Y или F; где F108 представляет собой F или W; где D109 представляет собой S, А, С, G, D, N, Т или G и где Y110 представляет собой любую аминокислоту.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат аминокислотную последовательность, показанную в SEQ ID NO:11, где G98 представляет собой G, S, А, С, V, N, D или Т; где G99 представляет собой G, S, А, С, V, N, D или Т; где Y100 представляет собой Y, L или R; где Y101 представляет собой Y или W; где G103 представляет собой G, А или S; где Т104 представляет собой Т или S; где S105 представляет собой S, А или Т; где Y106 представляет собой Y, R, Т или М; где Y107 представляет собой Y или F; где F108 представляет собой F или W; где D109 представляет собой S, А, С, G, D, N, Т или G и где Y110 представляет собой любую аминокислоту.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат аминокислотную последовательность, показанную в SEQ ID NO:12, где S26 представляет собой S или F; D28 представляет собой D, S, А или Y и Н32 представляет собой Н, N или Q.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат аминокислотную последовательность, показанную в SEQ ID NO:13, где 151 представляет собой I, Т, V или А и S56 представляет собой S или Т.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат аминокислотную последовательность, показанную в SEQ ID NO:14, где S91 представляет собой S или Е; K92 представляет собой K, Н, R или S и где Y96 представляет собой Y или R.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат аминокислотную последовательность, показанную в SEQ ID NO:14, где S91 представляет собой S или Е; K92 представляет собой любую аминокислоту; Т93 представляет собой любую аминокислоту и где Y96 представляет собой Y или R.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитела, в том числе гуманизированные антитела), которые содержат вариабельную область тяжелой цепи, содержащую CDR1-область из SEQ ID NO:9, где I34 представляет собой S, L, V A или I и N35 представляет собой N, Т или S; CDR2-область из SEQ ID NO:10, где М50 представляет собой М, I, G, Q, S или L; A62 представляет собой А или S и L63 представляет собой L или V; и CDR3-область из SEQ ID NO:11, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой D, N или G, где Y110 представляет собой Y, K, S, R или Т. В некоторых воплощениях вариабельная область тяжелой цепи содержит CDR3-область из SEQ ID NO:11, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой S, А, С, G, D, N, Т или G, где Y110 представляет собой любую аминокислоту. В других воплощениях вариабельная область тяжелой цепи содержит CDR3-область из SEQ ID NO:11, где G98 представляет собой G, S, А, С, V, N, D или Т, где G99 представляет собой G, S, А, С, V, N, D или Т, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой S, А, С, G, D, N, Т или G и где Y110 представляет собой любую аминокислоту. В некоторых воплощениях полипептид (такой как антитело) дополнительно содержит вариабельную область легкой цепи антитела.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат вариабельную область легкой цепи, содержащую CDR1-область из SEQ ID NO:12, где S26 представляет собой S или F, D28 представляет собой D, S, А или Y и Н32 представляет собой Н, N или Q; CDR2-область из SEQ ID NO:13, где I51 представляет собой I, Т, V или А и S56 представляет собой S или Т; и CDRS-область из SEQ ID NO:14, где S91 представляет собой S или Е; K92 представляет собой K, Н, R или S и где Y96 представляет собой Y или R. В некоторых воплощениях вариабельная область легкой цепи содержит CDR3-область из SEQ ID NO:14, где S91 представляет собой S или Е, K92 представляет собой любую аминокислоту, Т93 представляет собой любую аминокислоту и где Y96 представляет собой Y или R. В некоторых воплощениях полипептид (такой как антитело) дополнительно содержит тяжелую цепь антитела.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат (а) вариабельную область тяжелой цепи, содержащую CDR1-область из SEQ ID NO:9, где I34 представляет собой S, L, V А или I и N35 представляет собой N, Т или S; CDR2-область из SEQ ID NO:10, где М50 представляет собой М, I, G, Q, S или L; A62 представляет собой А или S и L63 представляет собой L или V; и CDR3-область из SEQ ID NO:11, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой D, N или G; где Y110 представляет собой Y, K, S, R или Т; и (б) вариабельную область легкой цепи, содержащую CDR1-область из SEQ ID NO:12, где S26 представляет собой S или F, D28 представляет собой D, S, А или Y и Н32 представляет собой Н, N или Q; CDR2-область из SEQ ID NO:13, где 151 представляет собой I, Т, V или А и S56 представляет собой S или Т; и CDR3-область из SEQ ID NO:14, где S91 представляет собой S или Е, K92 представляет собой K, Н, R или S и где Y96 представляет собой Y или R. В некоторых воплощениях вариабельная область легкой цепи содержит CDR3-область из SEQ ID NO:14, где S91 представляет собой S или Е, K92 представляет собой любую аминокислоту, Т93 представляет собой любую аминокислоту и где Y96 представляет собой Y или R. В некоторых воплощениях вариабельная область тяжелой цепи содержит CDR3-область из SEQ ID NO:11, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где 8105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой S, А, С, G, D, N, Т или G, где Y110 представляет собой любую аминокислоту. В других воплощениях вариабельная область тяжелой цепи содержит CDRS-область из SEQ ID NO:11, где G98 представляет собой G, S, А, С, V, N, D или Т, где G99 представляет собой G, S, А, С, V, N, D или Т, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F; где F108 представляет собой F или W; где D109 представляет собой S, А, С, G, D, N, Т или G и где Y110 представляет собой любую аминокислоту. В некоторых воплощениях полипептид дополнительно содержит легкую цепь антитела.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело, включая гуманизированное антитело), которые содержат аминокислотную последовательность, показанную в SEQ ID NO:9, где I34 представляет собой S, L, V А или I и N35 представляет собой N, Т или S; аминокислотную последовательность, показанную в SEQ ID NO:10, где М50 представляет собой М, I, G, Q, S или L, A62 представляет собой А или S и L63 представляет собой L или V; и аминокислотную последовательность, показанную в SEQ ID NO:11, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой D, N или G, где Y110 представляет собой Y, K, S, R или Т. В некоторых воплощениях полипептид содержит аминокислотную последовательность, показанную в SEQ ID NO:11, где Y100 представляет собой Y, L или R и где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой S, А, С, G, D, N, Т или G и где Y110 представляет собой любую аминокислоту. В других воплощениях полипептид содержит аминокислотную последовательность, показанную в SEQ ID NO:11, где G98 представляет собой G, S, А, С, V, N, D или Т, где G99 представляет собой G, S, А, С, V, N, D или Т, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой S, А, С, G, D, N, Т или G и где Y110 представляет собой любую аминокислоту. В некоторых воплощениях полипептид (такой как антитело) дополнительно содержит вариабельную область легкой цепи антитела.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат аминокислотную последовательность, показанную в SEQ ID NO:12, где S26 представляет собой S или F, D28 представляет собой D, S, А или Y и Н32 представляет собой Н, N или Q; аминокислотную последовательность, показанную в SEQ ID NO:13, где I51 представляет собой I, Т, V или А и S56 представляет собой S или Т; и аминокислотную последовательность, показанную в SEQ ID NO:14, где S91 представляет собой S или Е, K92 представляет собой K, Н, R или S и где Y96 представляет собой Y или R. В некоторых воплощениях полипептид содержит аминокислотную последовательность, показанную в SEQ ID NO:14, где S91 представляет собой S или Е, K92 представляет собой любую аминокислоту, Т93 представляет собой любую аминокислоту и где Y96 представляет собой Y или R. В некоторых воплощениях полипептид (такой как антитело) дополнительно содержит вариабельную область тяжелой цепи антитела.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитело), которые содержат (а) аминокислотную последовательность, показанную в SEQ ID NO:9, где I34 представляет собой S, L, V, А или I и N35 представляет собой N, Т или S; аминокислотную последовательность, показанную в SEQ ID NO:10, где М50 представляет собой М, I, G, Q, S или L, А62 представляет собой А или S и L63 представляет собой L или V; и аминокислотную последовательность, показанную в SEQ ID NO:11, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой D, N или G и где Y110 представляет собой Y, K, S, R или Т; и (б) аминокислотную последовательность, показанную в SEQ ID NO:12, где S26 представляет собой S или F, D28 представляет собой D, S, А или Y и Н32 представляет собой Н, N или Q; аминокислотную последовательность, показанную в SEQ ID NO:13, где I51 представляет собой I, Т, V или А, и S56 представляет собой S или Т; и аминокислотную последовательность, показанную в SEQ ID NO:14, где S91 представляет собой S или Е, K92 представляет собой K, Н, R или S и где Y96 представляет собой Y или R. В некоторых воплощениях полипептид содержит аминокислотную последовательность, показанную в SEQ ID NO:14, где S91 представляет собой S или Е, K92 представляет собой любую аминокислоту, Т93 представляет собой любую аминокислоту и где Y96 представляет собой Y или R. В некоторых воплощениях полипептид содержит аминокислотную последовательность, показанную в SEQ ID NO:11, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой S, А, С, G, D, N, Т или G, где Y110 представляет собой любую аминокислоту. В других воплощениях полипептид содержит аминокислотную последовательность, показанную в SEQ ID NO:11, где G98 представляет собой G, S, А, С, V, N, D или Т, где G99 представляет собой G, S, А, С, V, N, D или Т, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой S, А, С, G, D, N, Т или G и где Y110 представляет собой любую аминокислоту. В некоторых воплощениях полипептид дополнительно содержит вариабельную область легкой цепи антитела.
В другом аспекте в этом изобретении предложен полипептид (такой как антитело), содержащий вариабельную область тяжелой цепи, содержащую: (а) CDR1-область из SEQ ID NO:9, где I34 представляет собой S, L, V А или I и N35 заменена на N, Т или S; (б) CDR2-область из SEQ ID NO:10, где М50 представляет собой I, G, Q, S или L, A62 представляет собой А или S и L63 представляет собой L или V; и (в) CDR3-область из SEQ ID NO:11, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой D, N или G и где Y110 представляет собой Y, K, S, R или Т; причем антитело связывается с NGF.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитела), содержащие вариабельную область легкой цепи, содержащую: (а) CDR1-область из SEQ ID NO:12, где S26 представляет собой S или F, D28 представляет собой D, S, А или Y и Н32 представляет собой Н, N или Q; (б) CDR2-область из SEQ ID NO:13, где I51 представляет собой I, Т, V или А и S56 представляет собой S или Т; и (в) CDR3-область из SEQ ID NO:14, где K92 представляет собой K, Н, R или S и где Y96 представляет собой Y или R; причем антитело связывается с NGF.
В другом аспекте в этом изобретении предложены полипептиды (такие как антитела), содержащие (а) вариабельную область тяжелой цепи, содержащую: (1) CDR1-область из SEQ ID NO:9, где I34 заменена на S, L, V A или I и N35 заменена на N, Т или S; (2) CDR2-область из SEQ ID NO:10, где М50 представляет собой I, G, Q, S или L, A62 представляет собой А или S и L63 представляет собой L или V; и (3) CDR3-область из SEQ ID NO:11, где Y100 представляет собой Y, L или R, где Y101 представляет собой Y или W, где G103 представляет собой G, А или S, где Т104 представляет собой Т или S, где S105 представляет собой S, А или Т, где Y106 представляет собой Y, R, Т или М, где Y107 представляет собой Y или F, где F108 представляет собой F или W, где D109 представляет собой D, N или G, где Y110 представляет собой Y, K, S, R или Т; и (б) вариабельную область легкой цепи, содержащую: (1) CDR1-область из SEQ ID NO:12, где S26 представляет собой S или F, D28 представляет собой D, S, А или Y и Н32 представляет собой Н, N или Q; (2) CDR2-область из SEQ ID NO:13, где I51 представляет собой I, Т, V или А и S56 представляет собой S или Т; и (3) CDR3-область из SEQ ID NO:14, где S91 представляет собой S или Е, K92 представляет собой K, Н, R или S и где Y96 представляет собой Y или R; причем антитело связывается с NGF.
Если не указано иначе, выбор (например замена) аминокислоты в одном положении не зависит от выбора аминокислоты в любом другом положении.
В некоторых воплощениях полинуклеотиды (такие как антитело) связываются с NGF (таким как человеческий NGF). В некоторых воплощениях полипептиды содержат любую конфигурацию CDR (включая комбинации, вариации и так далее), описанную здесь.
Как это следует из данного описания, нумерация вариабельной области, использованная здесь, представляет собой нумерацию последовательности. Специалист в данной области легко поймет то, что существует множество систем нумерации для антител (таких как нумерации по Kabat и Chothia), и то, как перевести нумерацию последовательности в другую систему нумерации, такую как нумерацию по Kabat или нумерацию по Chothia.
В другом аспекте в этом изобретении предложен полипептид (такой как антитело), содержащий аминокислотную последовательность (такую как CDR3-последовательность), выбранную из SEQ ID NO:46 или 50. В еще других воплощениях полипептид дополнительно содержит одну или более чем одну аминокислотную последовательность, показанную в SEQ ID NOS:3, 4, 5, 6, 7 и 8. В еще других воплощениях полипептид дополнительно содержит одну из дополнительных аминокислотных последовательностей, показанных в SEQ ID NOS:9, 10, 11, 12, 13, 14 и 15.
В другом аспекте в этом изобретении предложен полипептид (такой как антитело), содержащий аминокислотную последовательность (такую как CDR-область, такая как область CDR-H1 и/или CDR-H2), выбранную из (a) SEQ ID NOS:28 и/или 29; (б) SEQ ID NOS:30 и/или 31; (в) SEQ ID NOS:32 и/или 33; (г) SEQ ID NOS:34 и/или 35; (д) SEQ ID NOS:36 и/или 37; (e) SEQ ID NOS:38 и/или 39 и (ж) SEQ ID NOS:40 и 41. В некоторых воплощениях полипептид содержит аминокислотную последовательность (такую как область CDR-H1), выбранную из SEQ ID NOS:28, 30, 32, 34, 36, 38 и 40. В некоторых воплощениях полипептид содержит аминокислотную последовательность (такую как область CDR-H2), выбранную из SEQ ID NOS:29, 31, 33, 35, 37, 39 и 41. В еще других воплощениях полипептид дополнительно содержит одну или более чем одну аминокислотную последовательность, показанную в SEQ ID NOS:3, 4, 5, 6, 7 и 8. В еще других воплощениях полипептид дополнительно содержит одну из дополнительных аминокислотных последовательностей, показанных в SEQ ID NOS:9, 10, 11, 12, 13, 14 и 15.
В другом аспекте в этом изобретении предложен полипептид (такой как антитело), содержащий аминокислотную последовательность (такую как CDR-область, такая как область CDR-L1 и/или CDR-L2), выбранную из (a) SEQ ID NOS:18 и/или 19; (б) SEQ ID NOS:20 и/или 21 и (в) SEQ ID NOS:22 и/или 23. В некоторых воплощениях полипептид содержит аминокислотную последовательность (такую как область CDR-L1), выбранную из SEQ ID NOS: 18, 20 и 22. В некоторых воплощениях полипептид содержит аминокислотную последовательность (такую как область CDR-L2), выбранную из SEQ ID NOS:19, 21 и 23. В еще других воплощениях полипептид дополнительно содержит одну или более чем одну аминокислотную последовательность, показанную в SEQ ID NOS:3, 4, 5, 6, 7, 8. В еще других воплощениях полипептид дополнительно содержит одну из дополнительных аминокислотных последовательностей, показанных в SEQ ID NOS:9, 10, 11, 12, 13, 14, и 15.
В другом аспекте в этом изобретении предложен полипептид (такой как антитело), содержащий аминокислотную последовательность (такую как CDR-область, такая как область CDR-L3 и/или CDR-H3), выбранную из (a) SEQ ID NOS:51 и/или 52; (б) SEQ ID NOS:55 и/или 56; (в) SEQ ID NOS:57 и/или 58; (в) SEQ ID NOS:59 и/или 60; (г) SEQ ID NOS:61 и/или 62; (д) SEQ ID NOS:63 и/или 64. В некоторых воплощениях полипептид содержит аминокислотную последовательность (такую как область CDR-L3), выбранную из SEQ ID NOS:51, 55, 57, 59, 61 и 63. В некоторых воплощениях полипептид содержит аминокислотную последовательность (такую как область CDR-H3), выбранную из SEQ ID NOS:52, 56, 58, 60, 62 и 64. В еще других воплощениях полипептид дополнительно содержит аминокислотную последовательность, показанную в одном или более чем одном из SEQ ID NOS:18, 19, 30 и 31. В еще других воплощениях полипептид дополнительно содержит одну или более чем одну аминокислотную последовательность, показанную в SEQ ID NOS:3, 4, 5, 6, 7 и 8. В еще других воплощениях полипептид дополнительно содержит одну из дополнительных аминокислотных последовательностей, показанных в SEQ ID NOS:9, 10, 11, 12, 13, 14 и 15.
В другом аспекте в этом изобретении предложен полипептид (такой как антитело), содержащий одну или более чем одну аминокислотную последовательность (такую как CDR-область), показанную в SEQ ID NOS:61, 63, 18, 19, 30 и 31.
В одном из аспектов в этом изобретении предложено антитело против NGF (такое как антагонистическое антитело), которое связывается с NGF (таким как человеческий NGF) с высокой аффинностью. В некоторых воплощениях высокая аффинность представляет собой: (а) связывание с NGF при KD менее чем приблизительно 2 нМ (такой как любое из значений о