Способ получения кардиомиоцитарной матрицы
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, а именно к способу получения кардиомиоцитарной матрицы. Способ включает наращивание биомассы эмбриональных стволовых клеток человека безфидерной линии hESKM-05 с использованием основной среды mTeSR во флаконах, покрытых матригелем. После чего осуществляют пассирование с помощью 0,05% раствора деспазы. Затем для образования из эмбриональных стволовых клеток эмбриоидных телец клетки переносят с помощью деспазы в среду коДМЕМ с добавлением 10% заменителя сыворотки SR, 100 мкг/мл канамицина сульфата, 1 мМ раствора L-глутамина и 1 мМ раствора незаменимых аминокислот, а также 2 мкг/мл раствора 5-аза-2-дезоксицитидина или 2 мкМ раствора бутирата натрия и стимулируют в течение 3 суток. Далее проводят повторный перенос на подготовленную коллаген-хитозановую матрицу и культивирование в питательной среде коДМЕМ с добавлением 1 мМ раствора незаменимых аминокислот, 1 мМ раствора L-глутамина, 10% заменителя сыворотки SR, 10-7 М ретиноевой кислоты и 10 нг/мл аскорбиновой кислоты со сменой среды каждые трое суток. Предложенное изобретение позволяет получать кардиомиоцитарную матрицу, пригодную для прямой трансплантации. 1 з.п. ф-лы, 2 ил.
Реферат
Изобретение относится к биологии и медицине, а именно: к кардиологии и кардиохирургии, к клеточной биотехнологии и биоинженерии, трансплантологии, и может быть использовано для культивирования, пролиферации и дифференцировки стволовых клеток в кардиомиоциты с целью трансплантации.
Цель заявляемой клеточной инженерии - дать возможность клеткам, способным к запуску и поддержке процесса регенерации, сформировать пул клеток кардиомиоцитарного направления. Это может быть достигнуто с помощью подложки или матрицы, создающей геометрическую архитектурную структуру миокардиальной ткани. Растущие потребности в клеточных технологиях диктуются возрастающим уровнем различных патологий, в том числе сердечно-сосудистой системы и недостатком материала для трансплантации. Кислородная недостаточность и последующая реперфузия приводят к необратимым клеточным повреждениям, которые могут повлечь за собой потерю функции, гибель клетки и инфаркт миокарда. Идеальной моделью для трансплантации являются кардиомиоциты благодаря их физиологическим и электрохимическим свойствам. Однако получение взрослых кардиомиоцитов в достаточном количестве для эффективной трансплантации невозможно в силу ограниченных количеств этих клеток, а также их низкой возможности к пролиферации на терминальной стадии дифференцировки. Решением этой проблемы может стать трансплантация эмбриональных стволовых клеток (ЭСК). Однако трансплантация недифференцированных ЭСК может приводить к образованию тератом, в этой связи целесообразно использование коммитированных в кардиомиоциты дериватов ЭСК.
Существуют различные способы коммитирования эмбриональных стволовых клеток к образованию кардимиоцитов. Общей чертой всех этих способов является стадия формирования эмбриональных телец. Некоторые исследователи [1, 2, 3, 4] предлагают способ сокультивирования эмбриональных клеток с клетками мыши. Как правило, в качестве сокультуры используют висцерально-энтодермально подобные клетки мыши (END-2), получаемые из Р19 клеток эмбриональной карциномы мышей. Сокультивирование дает возможность получать кардиомиоциты с высоким выходом. При выращивании эмбриональных стволовых клеток на монослое клеток END-2 C.Mummery et al. [5] наблюдали появление спонтанно пульсирующих клеток. Однако Ch. Xu et al [6] указывает, что результатом сокультивирования эмбриональных клеток с клетками животных, в том числе с клетками линии END-2, а также культивирование клеток в среде, содержащей сыворотку, может быть повышение иммуногенности клеток и заражение зоонозными агентами, что, несомненно, ограничивает возможность использования стволовых клеток в клинике. Ch.Xu et al. предложили способ культивирования стволовых клеток в среде, свободной от сыворотки, и включающей в себя следующие компоненты: креатин, карнитин, таурин и инсулин (CCTI-среда) [7].
Однако предложенные способы культивирования кардиомиоцитов, несмотря на высокий выход специализированных клеток, не могут быть эффективно использованы для трансплантации, поскольку выращиваются не на биодеградируемых матрицах с полным микроокружением и требуют снятия выращенных клеток с подложки с помощью ферментов, что существенно снижает их число и жизнеспособность.
Известен способ получения клеточной матрицы для лечения инфаркта миокарда, где в качестве носителя эндотелиальных клеток и клеток костного мозга использовали фибриновый гель, способный стимулировать неоваскуляризацию и служить в качестве подложки для стволовых клеток как возможного источника кардиомиоцитов [8, 9, 10]. Применение фибриновой конструкции ставит целью увеличить адгезию клеток на матрице при будущей трансплантации в зону инфаркта миокарда, необходимую как условие сохранения числа использованной клеточной массы. Для целей создания тканеподобных структур, близких к строению миокарда, используют различные биодеградируемые матрицы, в основном созданные из искусственных полимеров, обладающих биосовместимостью, способных включать в себя разнообразные факторы роста, гормоны и антисептики. К таким разработкам можно отнести способ создания сердечной ткани с целью тканевой инженерии при сердечной недостаточности путем культивирования стволовых клеток на биодеградируемом матриксе из фибрина и протеогликана [11]. При этом в матрицу внедрены различные факторы дифференцировки клеток в кардиомиоциты, такие как васкулярно-эндотелиальный фактор роста, эпидермальный фактор роста, цитокины и биоактивные молекулы. При этом стволовые клетки, используемые для дифференцировки, могут быть различного происхождения. Кроме того, для индукции образования кардиомиоцитов стволовые клетки трансфецируются лентивирусными векторами, несущими кардиально-специфический промотер и ген, отвечающий за дифференцировку. Однако предложенные способы получения кардиомиоцитов не используют подложки с включенными в них компонентами полной и кондиционированной питательных сред, обладающие биосовместимостью, биодеградируемостью, исключающие цито- и генотоксичность, а предусматривают выборочное добавление ряда искусственно полученных различных факторов дифференцировки клеток, указанных выше. В результате такого подхода стволовые клетки не получают полноценного микроокружения из внеклеточного матрикса за счет иммобилизованных факторов роста и дифференцировки с помощью кондиционированной среды, что не создает условий для направленной дифференцировки и пролиферации стволовых клеток. Пассирование клеток или их трансплантацию осуществляют путем снятия их с фибрино-протеогликановой подложки с применением процедуры обработки клеточной массы ферментами, которые повреждают поверхностные рецепторы при переносе и вызывают реакцию запрограммированной клеточной гибели.
Известно использование биодеградируемой желатиновой матрицы, несущей фетальные клетки желудочка крысы. Клеточная конструкция на такой матрице начинала спонтанно сокращаться как в культуре (in vitro), так и после трансплантации клеток [12]. В другом исследовании было выявлено, что трансплантаты из миобластов на полиуретановой подложке препятствуют развитию сердечной недостаточности после инфаркта миокарда у крыс [13]. Однако использование указанных матриц не создает условий для высокой адгезии клеток к матрице и сопровождается их потерей при культивировании на подложке в результате недостаточной биосовместимости с ингредиентами подложки. Кроме того, трансплантация миобластов в зону инфаркта миокарда не означает наличие в клеточной массе кардиомиоцитов. Использование недеградируемой полиуретановой подложки предусматривает снятие клеток с матрицы для трансплантации с помощью ферментов, а это всегда сопровождается потерей числа жизнеспособных клеток в результате развития реакции запрограммированной клеточной гибели. Предлагаемые авторами матрицы не создают условий для высокой пролиферации и дифференцировки стволовых клеток в кардиомиоциты, кроме того, матрицы не обеспечивают построение функциональной ткани из продуктов распада носителя. Известные матрицы из полилактата, коллагена и полиэтиленгликоля [14] не имеют высоких гидрофобных и адгезионных свойств из-за отсутствия заряженных групп на поверхности биополимерной конструкции, что снижает прикрепление клеток к поверхности матрицы и не создает условий для их наращивания в достаточном количестве. Общими недостатками известных способов получения кардиомиоцитов или клеток с близкой функциональной направленностью из стволовой клеточной массы являются низкое их содержание при культивировании, наличие опасности малигнизации стволовых клеток при их трансплантации без предварительной дифференцировки в кардиомиоциты, ожидаемого тератогенного эффекта по причине отсутствия полного микроокружения, формируемого из внеклеточного матрикса. К серьезным недостаткам можно отнести опасность тромбообразования в массе культивируемых стволовых и кардиомиоцитарных клеток, адгезированных на поверхности матрицы. Применение рекомбинантных белков или генетически трансформированных клеток, повышающих стоимость производства таких матриц, сопровождается формированием иммунного ответа на трансплантацию матрицы не только при использовании аллоклеточной массы, но и в случае использования аутоклеток. Кроме того, известные матрицы не обладают антибактериальными свойствами и не индуцируют неоваскуляризацию, так необходимую для формирования миокардиальной ткани при инфаркте миокарда.
Наиболее близкими к предлагаемому по составу являются матрицы, в качестве подложки которых используют коллаген-хитозановую конструкцию, содержащую полную и кондиционированную питательные среды. Подложка обладает антибактериальными свойствами и индуцирует неоваскуляризацию, создает высокую биосовместимость благодаря присутствию хитозана с высокой степенью дезацетилирования, хондроитинсульфата, гиалуроновой кислоты и гепарина. Кроме того, коллаген-хитозановая подложка повышает качество и стабильность культивирования, пролиферативную активность стволовых плюрипотентных клеток различного происхождения, исключает цито-генотоксичность клеточной подложки и обработку клеток ферментами в процессе пассирования при смене питательной среды, повышает прикрепление клеток к поверхности матрицы, обеспечивает получение клеточной матрицы, пригодной для прямой трансплантации, исключает тромбообразованне при культивировании стволовых клеток в присутствии гепарина [15]. Однако матрица, предложенная авторами, относится к способу получения клеточной матрицы кожи, а не клеток сердца, так как микроокружение, создаваемое для стволовых клеток, направлено на дифференцировку их в клетки кожи (фибробласты, эпидермобласты).
Задача изобретения - повысить качество и стабильность культивирования, пролиферативную активность стволовых плюрипотентных клеток с их дифференцировкой в кардиомиоциты, исключить иммуногенность микроокружения клеток и обеспечить получение кардиомиоцитарной матрицы, пригодной для прямой трансплантации.
Задачу достигают за счет того, что биомассу эмбриональных стволовых клеток человека безфидерной линии hESKM-05 наращивают с использованием основной среды mTeSR. во флаконах, покрытых матригелем, и пассируют с помощью 0,05% раствора деспазы, затем для образования из эмбриональных стволовых клеток эмбриоидных телец клетки переносят с помощью деспазы в среду коДМЕМ с добавлением 10% заменителя сыворотки SR, 100 мкг/мл канамицина сульфата, 1 мМ раствора L-глутамина и 1 мМ раствора незаменимых аминокислот, а также 2 мкг/мл раствора 5-аза-2-дезоксицитидина или 2 мкМ раствора бутирата натрия и стимулируют в течение 3 суток, при этом эмбриоидные тельца в дальнейшем переносят на подготовленную коллаген-хитозановую матрицу и культивируют в питательной среде коДМЕМ с добавлением 1 мМ раствора незаменимых аминокислот, 1 мМ раствора L-глутамина, 10% заменителя сыворотки SR, 10-7 М ретиноевой кислоты и 10 нг/мл аскорбиновой кислоты со сменой среды каждые трое суток.
Способ осуществляют следующим образом. На первом этапе культивируют плюрипотентные клетки человека линии hESKM-05. Первоначально для наращивания биомассы используют основную среду mTeSR (StemcellTeq, USA) во флаконах, покрытых матригелем, пассируют ЭСК с помощью 0,05% раствора деспазы. На втором этапе для стимуляции образования эмбриоидных телец ЭСК снимают деспазой, затем переносят в эмбриологическую чашку Петри (low adgesion) со средой коДМЕМ с добавлением 10% заменителя сыворотки SR, 100 мкг/мл раствора канамицина сульфата, 1 мМ раствора L-глутамина и 1 мМ раствора незаменимых аминокислот, добавляют 2 мкг/мл раствора 5-аза-2-дезоксицитидина или 2 мкМ раствора бутирата натрия и культивируют в течение 3-х суток. На третьем этапе проводят подготовку коллаген-хитозановых матриц «Коллахит-бол» [16, 17[, которые предварительно замачивают в течение 20-30 минут в стерильном бикарбонатном буфере для понижения их кислотных свойств, а после фазы нейтрализации матрицу в виде губки, пленки, микросфер или волокон промывают трижды стерильным фосфатным буфером Дульбекко и помещают во флаконы, покрытые 0.1% раствором желатина и содержащие среду коДМЕМ с добавлением 1 мМ раствора незаменимых аминокислот, 1 мМ раствора глутамина, 10% SR, 10-7 М ретиноевой кислоты, 10 нг/мл аскорбиновой кислоты. На четвертом этапе переносят эмбриональные тельца во флаконы, содержащие коллаген-хитозановые матрицы. Смену среды проводят каждые трое суток до момента использования клеточной матрицы по назначению.
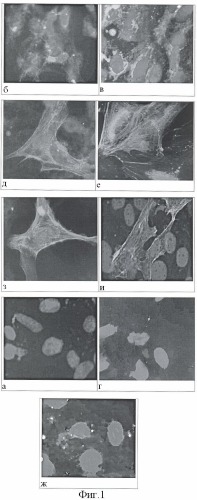
По истечении 14 суток культивирования проводят фиксацию клеток 1% раствором формальдегида в фосфатном буфере и последующую их последовательную обработку с помощью антител против альфа-актинина, десмина и миозина и меченых вторичных антител с детекцией флюоресценции. Выявление маркеров осуществляют методом согласно инструкции производителя антител. Ядра клеток окрашивают DAPI (0,1 мкг/мл) в течение 10 мин. В контроле клетки инкубируют в среде коДМЕМ с добавлением незаменимых аминокислот, глутамина, 10% SR, ретиноевой кислоты 10-7 М. Для получения изображений и анализа клеток используют флюоресцентный микроскоп «Olympus BX-51» и программные продукты «Applied Spectral Imaging» (USA). Для анализа каждого маркера эксперимент повторяют трижды, наращивая по три флакона, в каждом из которых случайным образом выделяют 6 зон для проведения анализа иммуноцитохимической реакции. Микроскопирование проводят по каждой зоне в 30 полях зрения.
Результаты морфологического анализа матрицы показали, что содержание кардиомиоцитов на одной подложке площадью 30 кв.см составляет около 5 миллионов клеток.
На рисунках 1 (б, д, з) показаны результаты иммуноцитохимического анализа ЭСК и их дериватов, культивируемых в среде коДМЕМ с добавлением незаменимых аминокислот, глутамина, 10% SR, ретиноевой кислоты 10-7 М, аскорбиновой кислоты (10 нг/мл) после обработки в течение 3-х суток 5-аза-2-дезоксицитидином (2 мкг/мл) или бутиратом натрия (2 мкМ) (фиг.1, в, е, и). Результаты иммуноцитохимического анализа показали, что при использовании среды mTeSR без животных компонентов и раствора 5-аза-2-дезоксицитидина или раствора бутирата натрия происходит дифференцировка ЭСК в кардиомиоцитарном направлении. На фиг.1 (а, г, ж) в контрольных образцах клеток экспрессия маркеров, характерных для кардиомиоцитов, не регистрируется. Было установлено, что предварительная экспозиция ЭСК с 5-аза-2-дезоксицитидином или бутиратом натрия приводит к появлению экспрессии исследуемых маркеров по сравнению с контролем.
На фиг.2,а показана фазово-контрастная микроскопия культивируемых дериватов ЭСК человека в кардиомиоцитарном направлении после обработки 5-аза-2-дезоксицитидином, через 14 дней культивирования появляются сокращающиеся волокна. На фиг.2,б показано увеличение количества эмбриональных телец при экспозиции в указанных условиях в течение 20-21 дней.
Исследование морфологии клеток показало, что ЭСК после культивирования в вышеописанных условиях приобретают кардиомиоцитарный фенотип. Известно, что регуляция экспрессии генов в ЭСК находится под эпигенетическим контролем. Использование 5-аза-2-дезоксицитидина играет роль ингибитора ДНК-поддерживающей метилазы-2, а использование бутирата натрия - ингибитора гистоновой дезацетилазы [18]. Эти два регулятора участвуют в поддержании эпигенетического статуса клетки в зависимости от ее состояния на уровне ДНК или на уровне конденсации хроматина. Это свидетельствует о наличии эпигенетического контроля дифференцировки при стимуляции ЭСК в кардиомиоцитарном направлении.
Таким образом, предлагаемый способ получения кардиомиоцитарной матрицы повышает качество, стабильность культивирования и пролиферативную активность стволовых плюрипотентных клеток с их дифференцировкой в кардиомиоциты, исключает иммуногенность микроокружения клеток и обеспечивает получение клеточной матрицы, пригодной для прямой трансплантации.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1. Mummery СП., van Oostwaard D.W., Doevendans P., Spijker R., van den Brink S., Hassink R., van der Heyden M., OpthofT., Pera M., de la Riviere А.В., Passier R., Tertoolen L. Differentiation of human embryonic stem cells to cardiomyocytes role ofcoculture with visceral endoderm-like cells.//Circ., 2009,-Vol.107(21).- P. 2733-2740.
2. Mujoo К. Sharin V.G., Bryan N.S., KrumenackerJ.S., Sloan C., Parveen S., NikonoffL.E., Kots A.Y.. Murad F. Role of nitric oxide signaling components in differentiation of embryonic stem cells into myocardial cells.// PNAS, 2008. - Vol.105(48). - P.18924-18929.
3. Bin Z., Sheng L.G., Gang Z.C., Hong J., Jun C.B.Y., HuiBin Z.S. Efficient cardiomyocyte differentiation of embryonic stem cells by bone morphogenetic protein-2 combined with visceral endoderm-like cells. // Cell Biol. Int., 2006.- Vol.30(10).-P.769-76.
4. Passier R., Ward-van Oostwaard D., Snapper J., Kloots J., Hassink R.J., Kuijk E., Roelen В.. de la Riviere A.B-, Mummerya C., Robert P. Increased cardiomyocyte differentiation from human embryonic stem cells in serum-free cultures. // Stem Cells, 2005. -Vol.23. - P.772-780.
5. Mummery Ch., van Oostwaard D.W., Doevendans P., Spijker R., van den Brink S., Hassink R., van der Heyden M., OpthofT., Pera M., de la Riviere A.B., Passier R., Tertoolen L. Differentiation of human embryonic stem cells to cardiomyocytes role ofcoculture with visceral endoderm-like cells. // Circ., 2009.-Vol.107(21).- P. 2733-2740.
6. Xu Ch., Police Sh., Rao N., Carpenter M.K. Characterization and enrichment of cardiomyocytes derived from human embryonic stem cells. // Cellular Biology Circ Res 2002.-Vol.91.-P.501-508.
7. Xu Ch. He J.-Q., Kamp T.J., Police 1 Sh., Hao X., (TSullivan Ch., Carpenter M.K., Lebkowski.1., Gold J.D. Human embryonic stem cell-derived cardiomyocytes can be maintained in defined medium without serum.// Stem Cells and Development "'006 - Vol 15 - P.931-941.
8. Christman К. Fibrin glue alone and skeletal myoblasts in a fibrin scaffold preserve cardiac function after myocardial infarction. / K. Christman. II.I-l. Fok, R.L. Sievers. Q. Рапц, R.I. l.cc. // Tissue Eng.-2004.-Vol.lO.-P.403-409.
9. Ryu J.H. Implantation of bone marrow mononuclear cells using injeclable fibrin matrix enhances neovascuiarization in infarcted myocardium. /J.ll. Rvu, l.K. Kirn, S.W. Cho. // Biomaterials.-2005.-Vol.26 -P.319-326.
10. Huang N.F. Injectable biopolymers enhance angiogenesis after myocardial infarction. / N.F. Huang, J. Yu, R. Sievers. S. Li, R.J. Lee. // Tissue Eng- 2005.-Vol.11.- P 1860-1866
11. Патент ЕР 1730265.
12. Li R.K. Survival and function ofbioengineered cardiac grafts. / R.K. Li, Z.Q. Jia, R. D. Weisel, D. A.G. Mickle, A. Choi T. M. Yau.//Circulation. - 1999. - Vol.100. - P.: 63-69.
13. Siepe M. Myoblast-seeded biodegradable scaffolds to prevent posl-myocardial infarction evolution toward heart failure. / M. Siepe. M.N. Giraud, M. Pavlovic, C. Rccepulo. F. Beyersdorf, P. Menasche, T. Carrel, H. T. Tevaearai. // The Journal ofThoracic and Cardiovascular Surgery. - 2006. - Vol.132 №1. - P.: 124-131.
14. Швед Ю.А., Кухарева Л.В., Зорин И.М., Блинова М.И., Билибин А.Ю., Нинаев Г.Н. Взаимодействие культивированных клеток кожи с разными структурными формами коллагена, нанесенного на полиллактидную матрицу. Цитология, 2007. - Т.49. - №1. - С.32-40.
15. Заявка на изобретение №2008131742/13(03 9611), С 2N 5/00, 2010.02.10.
16. Патент РФ №2 252 787, МПК7 А61L 15/28, А61L 15/32, А61L 27/60, публ. 2005.05.27.
17. Патент РФ №2 254 145, МПК7 А61L 15/28, А61L 15/32, А61L 26/00, публ. 2005.06.20.
18. Gore M.G. Spectrophotometry and spectrofluorimetry. Practical Approach. - New York: Oxford University Press Inc. - 2000. - 368.
1. Способ получения кардиомиоцитарной матрицы, отличающийся тем, что биомассу эмбриональных стволовых клеток человека безфидерной линии hESKM-05 наращивают с использованием основной среды mTeSR во флаконах, покрытых матригелем, и пассируют с помощью 0,05% раствора деспазы, затем для образования из эмбриональных стволовых клеток эмбриоидных телец клетки переносят с помощью деспазы в среду коДМЕМ с добавлением 10% заменителя сыворотки SR, 100 мкг/мл канамицина сульфата, 1 мМ раствора L-глутамина и 1 мМ раствора незаменимых аминокислот, а также 2 мкг/мл раствора 5-аза-2-дезоксицитидина или 2 мкМ раствора бутирата натрия и стимулируют в течение 3 сут, при этом эмбриоидные тельца в дальнейшем переносят на подготовленную коллаген-хитозановую матрицу и культивируют в питательной среде коДМЕМ с добавлением 1 мМ раствора незаменимых аминокислот, 1 мМ раствора L-глутамина, 10% заменителя сыворотки SR, 10-7 М ретиноевой кислоты и 10 нг/мл аскорбиновой кислоты со сменой среды каждые трое суток.
2. Способ по п.1, отличающийся тем, что коллаген-хитозановую матрицу используют в виде губки, пленки, микросфер, геля или волокон.