Способ определения 2,4-динитрофенола и 2-амино-4-нитрофенола при их одновременном присутствии в биологических жидкостях
Иллюстрации
Показать всеИзобретение относится к биологии и токсикологической химии и может быть использовано в практике санэпидстанций, химико-токсикологических, ветеринарных и экологических лабораторий.
Биологическую жидкость, содержащую анализируемые вещества, разбавляют буферным раствором с рН 10-11, обрабатывают хлоридом 2,3,5-трифенилтетразолия, количество которого составляет 0,025% от массы раствора, однократно экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформный экстракт отделяют, фотометрируют, по величине оптической плотности рассчитывают содержание 2,4-динитрофенола, водную фазу дважды экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформные экстракты отбрасывают. Количество хлорида 2,3,5-трифенилтетразолия в водной фазе доводят до 0,6-1,0%, водную фазу однократно экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформный экстракт отделяют, вводят в него этанол в количестве 25% от объема хлороформа, полученный раствор фотометрируют и по величине оптической плотности рассчитывают количественное содержание 2-амино-4-нитрофенола. Достигается повышение селективности и точности анализа. 3 табл.
Реферат
Изобретение относится к биологии и токсикологической химии, а именно к способам определения 2,4-динитрофенола и 2-амино-4-нитрофенола в биологическом материале, и может быть использовано в практике санэпидстанций, химико-токсикологических, ветеринарных и экологических лабораторий. Способ относится к числу массовых.
Известен способ определения 2,4-динитрофенола в биологическом материале, в том числе в биологических жидкостях, заключающийся в том, что биологическую пробу подкисляют концентрированной серной кислотой, встряхивают с диэтиловым эфиром в аппарате для экстракции в течение 6 часов, эфирный экстракт отделяют, упаривают на водяной бане до сухого остатка, остаток растворяют в 0,5 н. растворе гидроксида натрия, раствор разбавляют в 10 раз водой, удаляют из него кислород и проводят определение анализируемого вещества полярографическим методом, принимая во внимание высоту первой полярографической волны, которая располагается в интервале -0,6 - -0,8 вольт относительно насыщенного каломельного электрода (Гадаскина И.Д., Филов В.А. Превращения и определение промышленных органических ядов в организме. - Л.: Медицина, 1971. - С.260).
Способ характеризуется длительностью выполнения, недостаточно высокой чувствительностью, не позволяет проводить определение 2-амино-4-нитрофенола при его одновременном присутствии с 2,4-динитрофенолом в биологических жидкостях.
Известен способ определения 2,4-динитрофенола и 2-амино-4-нитрофенола при их одновременном присутствии в биологическом материале (ткани печени и крови) путем двукратного (каждый раз в течение 30 минут) настаивания биологической пробы с порциями диметилформамида, масса каждой из которых в два раза превышает массу биологического объекта, объединения диметилформамидных извлечений, разбавления части объединенного извлечения буферным раствором с рН 4,0 в три раза, экстракции полученного раствора дважды порциями диэтилового эфира, объем каждой из которых равен объему водно-диметилформамидного слоя, объединения экстрактов, обезвоживания объединенного экстракта безводным сульфатом натрия, испарения растворителя из фильтрата, растворения остатка в диэтиловом эфире, прибавления к полученному раствору равного по объему количества гексана, экстрагирования буферным раствором с рН 12,1-12,4, отделения водного слоя, подкисления хлороводородной кислотой до рН 4,0, экстракции диэтиловым эфиром, обезвоживания органического экстракта безводным сульфатом натрия, испарения растворителя из обезвоженного экстракта, растворения остатка в ацетоне, хроматографирования в тонком слое силикагеля на пластинах «Силуфол» UV-254, обработанных вазелиновым маслом (модель привитой фазы Сu-С15), с использованием подвижной фазы диоксан-вода (4:6), проявления хроматограмм в УФ-свете, элюирования анализируемого вещества из сорбента хлороформом, упаривания элюата до сухого остатка, растворения остатка в смеси растворителей ацетонитрил-ацетатный буфер с рН 5,4 (5:5) с последующим введением части образующегося раствора в хроматограф типа «Милихром» с последующим хроматографированием в колонке с размерами 64×2, заполненной сорбентом «Сепарон С-18», с применением подвижной фазы ацетонитрил-ацетатный буфер с рН 5,4 (5:5).
Способ характеризуется длительностью выполнения, недостаточно высокой точностью и наличием трудоемких операций (Фурсова И.А., Шорманов В.К., Гусев И.В. Определение 2,4-динитрофенола, его основного метаболита 2-амино-4-нитрофенола и 4-оксидифенила в биологическом материале // Судебно-медицинская экспертиза. - 2003. - Т.46, №3. - С.29-33).
Наиболее близким является способ определения нитрофенолов в биологических жидкостях, заключающийся в том, что биологическую пробу разбавляют буферным раствором щелочной реакции (рН 9), образующийся раствор обрабатывают хлоридом 2,3,5-трифенилтетразолия, количество которого составляет 0,025% от массы раствора, однократно экстрагируют хлороформом при объемном соотношении водной и органической фаз 1:1, экстракт отделяют, фотометрируют и по величине оптической плотности определяют содержание нитрофенолов (Шорманов В.К. Экстракционно-фотометрическое определение нитрофенолов в биологических жидкостях // Журнал аналитической химии. - 2002. - Т.57, №2. - С.130-135).
Способ не позволяет селективно определять 2,4-динитрофенол и 2-амино-4-нитрофенол при их одновременном присутствии в биологических жидкостях.
Задачей настоящего изобретения является повышение селективности и точности определения.
Поставленная задача достигается с помощью предлагаемого способа, который заключается в том, что анализируемую пробу разбавляют буферным раствором с рН 10-11, обрабатывают хлоридом 2,3,5-трифенилтетразолия, количество которого составляет 0,025% от массы раствора, однократно экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформный экстракт отделяют, вводят в него этанол в количестве 25% от объема хлороформа, фотометрируют, по величине оптической плотности рассчитывают содержание 2,4-динитрофенола, водную фазу дважды экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформные экстракты отбрасывают, количество хлорида 2,3,5-трифенилтетразолия в водной фазе доводят до 0,6-1,0%, водную фазу однократно экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформный экстракт отделяют, вводят в него этанол в количестве 25% от объема хлороформа, полученный раствор фотометрируют и по величине оптической плотности рассчитывают количественное содержание 2-амино-4-нитрофенола.
Способ осуществляется следующим образом: биологическую жидкость, содержащую анализируемые вещества, разбавляют буферным раствором с рН 10-11, обрабатывают хлоридом 2,3,5-трифенилтетразолия, количество которого составляет 0,025% от массы раствора, однократно экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформный экстракт отделяют, вводят в него этанол в количестве 25% от объема хлороформа, фотометрируют, по величине оптической плотности рассчитывают содержание 2,4-динитрофенола, водную фазу дважды экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформные экстракты отбрасывают. Количество хлорида 2,3,5-трифенилтетразолия в водной фазе доводят до 0,6-1,0%, водную фазу однократно экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформный экстракт отделяют, вводят в него этанол в количестве 25% от объема хлороформа, полученный раствор фотометрируют и по величине оптической плотности рассчитывают количественное содержание 2-амино-4-нитрофенола.
Пример 1
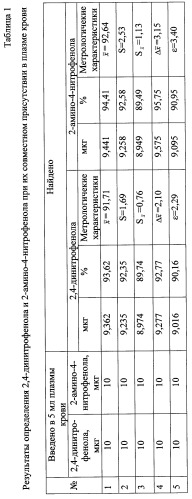
Определение 2,4-динитрофенола и 2-амино-4-нитрофенола при их одновременном присутствии в плазме крови
К 100 мл плазмы крови человека прибавляют по 5 мг 2,4-динитрофенола и 2-амино-4-нитрофенола, тщательно перемешивают биологическую жидкость с веществами и оставляют на 1,5 часа при температуре 18-20°С.
По истечении указанного времени к 5 мл образующегося раствора, содержащего по 10 мкг анализируемых веществ, прибавляют 4 мл буферного раствора с рН 10-11, 1 мл 0,25% раствора трифенилтетразолия и экстрагируют 10 мл хлороформа в течение 4 минут. Хлороформный экстракт отделяют, прибавляют к нему 2,5 мл этанола и измеряют оптическую плотность образующегося раствора на спектрофотометре СФ-46 при длине волны 423 нм в кварцевых кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. По величине оптической плотности определяют количественное содержание 2,4-динитрофенола, используя уравнение калибровочного графика, и пересчитывают на навеску вещества, внесенную в биологический объект. Водную фазу экстрагируют дважды по 4 минуты порциями хлороформа по 10 мл каждая, хлороформные экстракты отбрасывают, в водную фазу вводят 0,08 г хлорида 2,3,5-трифенилтетразолия и экстрагируют 10 мл хлороформа. К полученному экстракту прибавляют 2,5 мл этанола и измеряют оптическую плотность образующегося раствора на спектрофотометре СФ при 431 нм в кварцевых кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. По величине оптической плотности определяют количественное содержание 2-амино-4-нитрофенола, используя уравнение калибровочного графика, и пересчитывают на навеску, внесенную в биологический объект.
Построение калибровочных графиков
А. Построение калибровочного графика для определения 2,4-динитрофенола
В ряд делительных воронок вносят 0,05, 0,1, 0,2, 0,4, 0,8, 1,6, 3,2, 4,8, 5,6 мл 0,005% раствора 2,4-динитрофенола в буферном растворе с рН 10-11, соответственно 8,95, 8,9, 8,8, 8,6, 8,2, 7,4, 5,8, 4,2, 3,4 мл буферного раствора с рН 10-11, по 1 мл 0,25% раствора хлорида 2,3,5-трифенилтетразолия и по 10 мл хлороформа. Содержимое воронок встряхивают в течение 4 минут, хлороформные извлечения отделяют, прибавляют к каждому из них по 2,5 мл этанола и измеряют оптические плотности образующихся растворов на спектрофотометре СФ-46 при длине волны 423 нм в кварцевых кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. По результатам измерений оптической плотности серии растворов с известными концентрациями 2,4-динитрофенола строят график зависимости оптической плотности от концентрации определяемого вещества. График линеен в интервале концентраций 0,25-28,0 мкг/мл. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое в данном случае имеет вид:
А=0,05062·С+0,00072,
где А - оптическая плотность, С - концентрация определяемого вещества в фотометрируемом растворе, мкг/мл.
Б. Построение калибровочного графика для определения 2-амино-4-нитрофенола
В ряд делительных воронок вносят 0,02, 0,04, 0,1, 0,2, 0,4, 1,0 мл 0,025% раствора 2-амино-4-нитрофенола в буферном растворе с рН 10-11, соответственно 9,98, 9,96, 9,9, 9,8, 9,6 и 9,0 мл буферного раствора с рН 10-11, по 0,08 г хлорида 2,3,5-трифенилтетразолия и по 10 мл хлороформа.
Содержимое воронок встряхивают в течение 4 минут, хлороформные извлечения отделяют в ряд пробирок, содержащих по 2,5 мл этанола и измеряют оптическую плотность образующихся растворов на спектрофотометре СФ-46 при длине волны 431 нм в кварцевых кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. По результатам измерений оптической плотности серии растворов с известными концентрациями 2-амино-4-нитрофенола строят график зависимости оптической плотности от концентрации определяемого вещества. График линеен в интервале концентраций 0,5-25,00 мкг/мл. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое в данном случае имеет вид:
А=0,03475·С+0,00145,
где А - оптическая плотность, С - концентрация определяемого вещества в фотометрируемом растворе, мкг/мл.
Результаты количественного определения 2,4-динитрофенола и 2 амино-4-нитрофенола представлены в таблице 1.
Пример 2
Определение 2,4-динитрофенола и 2-амино-4-нитрофенола при их одновременном присутствии в моче
К 100 мл мочи человека прибавляют по 5 мг 2,4-динитрофенола и 2-амино-4-нитрофенола, тщательно перемешивают биологическую жидкость с веществами и оставляют на 1,5 часа при температуре 18-20°С.
По истечении указанного времени к 5 мл образующегося раствора, содержащего по 10 мкг анализируемых веществ, прибавляют 4 мл буферного раствора с рН 10-11, 1 мл 0,25% раствора трифенилтетразолия и экстрагируют 10 мл хлороформа в течение 4 минут. Хлороформный экстракт отделяют, прибавляют к нему 2,5 мл этанола и измеряют оптическую плотность образующегося раствора на спектрофотометре СФ-46 при длине волны 423 нм в кювете с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. По величине оптической плотности определяют количественное содержание 2,4-динитрофенола, используя уравнение калибровочного графика, и пересчитывают на навеску вещества, внесенную в биологический объект. Водную фазу экстрагируют дважды по 4 минуты порциями хлороформа по 10 мл каждая, хлороформные экстракты отбрасывают, в водную фазу вводят 0,08 г хлорида 2,3,5-трифенилтетразолия и экстрагируют 10 мл хлороформа. К полученному экстракту прибавляют 2,5 мл этанола и измеряют оптическую плотность образующегося раствора на спектрофотометре СФ при 431 нм в кювете с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. По величине оптической плотности определяют количественное содержание 2-амино-4-нитрофенола, используя уравнение калибровочного графика, и пересчитывают на навеску, внесенную в биологический объект.
Схемы построения калибровочных графиков для определения 2,4-динитрофенола и 2-амино-4-нитрофенола представлены выше в примере 1.
Результаты количественного определения 2,4-динитрофенола и 2-амино-4-нитрофенола в моче представлены в таблице 2.
Предлагаемый способ по сравнению с прототипом повышает селективность определения, позволяя определять 2,4-динитрофенол и 2-амино-4-нитрофенол при их одновременном присутствии в биологических жидкостях, а также характеризуется более высокой точностью (полуширина доверительного интервала уменьшается в 1,3 раза). Сравнительная характеристика предлагаемого и известного способов представлена в таблице 3.
| Таблица 3 | ||
| Сравнительная характеристика предлагаемого и известного способов | ||
| Показатели | Предлагаемый способ | Известный способ |
| 1. Селективность | Позволяет проводить определение 2,4-динитрофенола и 2-амино-4-нитрофенола в биологических жидкостях при одновременном присутствии данных веществ в анализируемой пробе | Не позволяет проводить определение 2,4-динитрофенола и 2-амино-4-нитрофенола в биологических жидкостях при одновременном присутствии данных веществ в анализируемой пробе |
| 2. Полуширина доверительного интервала (характеристика точности) (на примере 2,4-динитрофенола): | ||
| а) при определении в плазме крови | 2,10% | 3,1% |
| б) при определении в моче | 1,79% | 2,7% |
Способ определения 2,4-динитрофенола и 2-амино-4-нитрофенола при их одновременном присутствии в биологических жидкостях, заключающийся в том, что анализируемую пробу разбавляют буферным раствором щелочной реакции, образующийся раствор обрабатывают хлоридом 2,3,5-трифенилтетразолия, количество которого составляет 0,025% от массы раствора, однократно экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформный экстракт отделяют и фотометрируют, отличающийся тем, что анализируемую пробу разбавляют буферным раствором с рН 10-11, после отделения хлороформного экстракта его фотометрируют, по величине оптической плотности рассчитывают содержание 2,4-динитрофенола, водную фазу дважды экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформные экстракты отбрасывают, количество хлорида 2,3,5-трифенилтетразолия в водной фазе доводят до 0,6-1,0%, водную фазу однократно экстрагируют хлороформом при объемном отношении водной и органической фаз 1:1, хлороформный экстракт отделяют, вводят в него этанол в количестве 25% от объема хлороформа, полученный раствор фотометрируют и определяют по величине оптической плотности количественное содержание 2-амино-4-нитрофенола.