Способ лечения вторичного гиперпаратиреоза
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к хирургии, в том числе экспериментальной, и может найти применение в лечении вторичного гиперпаратиреоза. Способ заключается в тотальной паратиреоидэктомии с одномоментной, гетеротопической, свободной реплантацией жизнеспособных удаленных околощитовидных желез или их фрагментов. При этом околощитовидную железу рассекают на фрагменты. Поочередно каждый фрагмент прошивают и реплантируют на интиму, в просвет притоковой ветви большой подкожной вены нижних конечностей. Затем осуществляют частичную программируемую паратиреоидэктомию при сохранении вторичного гиперпаратиреоза. Использование данного изобретения позволяет повысить эффективность восстановления жизнеспособности и функциональной активности реплантируемой околощитовидной железы, корректировать персистирующий и рецидивный гиперпатиреоз и предупредить развитие послеоперационного гипопаратиреоза. 1 табл., 3 ил.
Реферат
Изобретение относится к области медицины, конкретно к хирургии.
Вторичный гиперпаратиреоз (ВГПТ), характеризующийся гиперплазией околощитовидных желез и гиперсекрецией паратгормона (ПТГ), наблюдается при хронической почечной недостаточности (ХПН). Развитие гиперпаратиреоза в этом случае связано со снижением синтеза витамина D3 в патологически измененной паренхиме почки, что приводит к вторичному высвобождению ПТГ. Проблема диагностики и лечения ВГПТ при тяжелой ХПН возникла после внедрения в клиническую практику хронического почечного диализа, что позволило продлить жизнь ранее обреченным больным. Многолетнее воздействие на организм целого ряда повреждающих факторов, характерных для ХПН, приводит к выраженным морфологическим и функциональным изменениям в околощитовидных железах (ОЩЖ), а также связанным с ними метаболическим расстройствам. При этом на определенном этапе развития болезни проводимая медикаментозная терапия может оказаться неэффективной и хирургическое удаление измененных ОЩЖ становится единственным способом облегчения страданий пациентов, улучшения качества жизни.
Необходимость в хирургическом лечении ВГПТ возникает при безуспешности медикаментозной терапии, причем только в тех случаях, когда удаление гиперфункционирующих ОЩЖ представляется патогенетически оправданным и эффективным.
Показаниями к операции по поводу ВГПТ являются: клинически выраженная прогрессирующая почечная гиперпаратиреоидная остеодистрофия (ГПО), рефрактерная к консервативному лечению, в том числе осложненная патологическими переломами костей; гиперкальциемия, за исключением случаев алюминиевой интоксикации и передозировки препаратами Са и витамина D; выраженный кожный зуд при подтвержденном ВГПТ, кальцифилаксия; прогрессирующая кальцификация мягких тканей, несмотря на попытки контролировать уровень фосфатов в плазме.
Известен способ хирургического лечения ВГПТ - субтотальная резекция ОЩЖ или тотальная паратиреоидэктомия с аутотрансплантацией железистой ткани в предплечье (m. Brahioradialis) с последующим удалением необходимой части аутотрансплантатов для коррекции возвратного или персистирующего ВГПТ [1, 2].
Данный способ является наиболее близким к заявляемому по технической сути и достигаемому результату и выбран в качестве прототипа.
Недостатком данного способа являются развитие рубцовой трансформации аутотрансплантантов, что может затруднять интраоперационный поиск места нахождения пересаженной ткани ОЩЖ при возникновении необходимости ее частичного удаления.
Задачей, решаемой предлагаемым изобретением, является лечение вторичного гиперпаратиреоза и предупреждение послеоперационного гипопаратиреоза.
Поставленная задача решается путем тотальной паратиреоидэктомии с одномоментной, гетеротопической, свободной реплантацией жизнеспособных, неизмененных удаленных околощитовидных желез или их фрагментов, на интиму, в просвет притоковых ветвей большой подкожной вены нижних конечностей, с последующим программированным удалением части трансплантатов до ликвидации вторичного гиперпаратиреоза.
Новым в предлагаемом изобретении является то, что жизнеспособные удаленные околощитовидные железы или их фрагменты реплантируют на интиму в просвет притоковой ветви большой подкожной вены нижней конечности с последующей программируемой частичной паратиреоидэктомией.
Эффективность предложенного способа объясняется функциональной активностью эндотелия венозной стенки - интимой и другими отличительными функциями сосуда: реплантация фрагментов околощитовидной железы к интиме венозной стенки вызывает выработку вазоактивных факторов, в частности эндотелина, ангиотензина I, ангиотензина II и тромбоксана, осуществляющих гемостаз и формирование тромба. В ответ на это, по принципу обратной связи, в восстановленном после реплантации венозном сосуде происходит выработка веществ, препятствующих коагуляции и способствующих фибринолизу, а именно - простациклина и NO - естественных дезагрегантов, образование тканевого активатора плазменогена, экспрессия на поверхности клеток эндотелия тромбомодулина-белка, способного связывать тромбин и гепариноподобный гликозаминогликан, все это приводит к восстановлению кровотока в сосуде. Существенное значение в формировании кровотока в трансплантате имеет система Vasa vasorum. За счет транспортной функции сосуда к трансплантатам осуществляется доставка кислорода, гормонов, питательных и других биологически активных веществ, в том числе и полипотентных мезенхимальных стромальных клеток (стволовых клеток).
Существенные отличия в предложенном способе позволяют получить новый положительный эффект. За счет лучшей трофики повышается эффективность восстановления жизнеспособности и функциональной активности трансплантата, исключаются послеоперационные осложнения - развитие сером, гематом, отторжение трансплантата, рубцовая его трансформация и лизис. Существенным отличием также является то, что местом трансплантации является венозный сосуд, что значительно облегчает интраоперационный поиск места нахождения аутотрансплантата при выполнении последующей программируемой, частичной паратиреоидэктомии.
Отличительные признаки проявили в заявленной совокупности новые свойства, которые не являются очевидными для специалиста и не вытекающие явным образом из уровня техники. Предлагаемое изобретение может быть использовано в здравоохранении для лечения вторичного гиперпаратиреоза и ренальной остеодистрофии у пациентов с хроническими болезнями почек, находящихся на программном гемодиализе.
Идентичной совокупности существенных признаков не обнаружено при исследовании научно-медицинской и патентной литературы.
Предлагаемый способ может быть использован в практическом здравоохранении для повышения эффективности лечения.
Таким образом, данное техническое решение соответствует критериям изобретения: «Новизна», «Изобретательский уровень» и «Промышленная применимость».
Изобретение будет понятно из следующего описания и приложенных к нему чертежей.
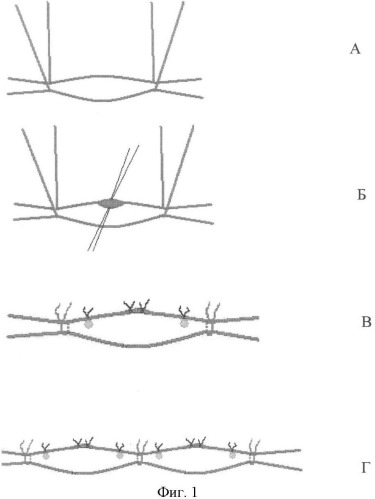
На фиг.1 изображена схема проведения операции.
1А - выделенный сосуд, взятый на держалки,
1Б - разрез в стенке притоковой вены,
1В - фиксация фрагментов ОЩЖ,
1Г - законченный вариант трансплантации.
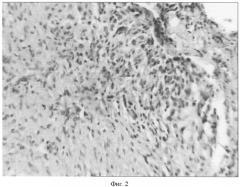
На фиг.2 изображены данные гистологического исследования (срок 1 месяц).
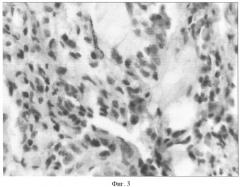
На фиг.3 изображены данные гистологического исследования (срок 1 месяц).
Способ осуществляют следующим образом.
I этап заключается в тотальной паратиреоидэктомии с одномоментной, гетеротопической, свободной аутотрансплантацией ОЩЖ в просвет притоковой ветви большой подкожной вены нижней конечности.
Выполняют оперативное удаление 4 ОЩЖ. После интраоперационной визуализации удаленные ОЩЖ помещают в 0,9%-ный раствор хлорида натрия, охлажденный до 4°С. Выполняют экспресс-цитологию ОЩЖ с целью исключения наличия опухоли и аденомы. Ткань, прошедшую цитологический контроль, используют для трансплантации. После завершения операции на шее приступают к выполнению аутотрансплантации. На бедре выполняют продольный разрез кожи до 5 см длиной в проекции расположения большой подкожной вены. В подкожной жировой клетчатке выявляют и выделяют основной ствол и ближайшие притоковые ветви большой подкожной вены. Под притоковую ветвь вены подводят лигатуры-держалки (фиг.1А). При этом просвет притоковой вены уменьшают с помощью узла лигатуры из цветного, нерассасывающегося шовного материала на участке.
Приподнимают дистальную лигатуру-держалку, тем самым прекращают кровоток в притоковой вене. Продольным разрезом до 0,3 см вскрывают просвет притоковой вены (фиг.1Б). Из физиологического раствора (0,9% раствор хлорида натрия) извлекают околощитовидную железу, с помощью скальпеля или бритвы ее рассекают на фрагменты нужного размера (приблизительно 2*3 мм). Поочередно каждый фрагмент околощитовидной железы прошивают атравматичной иглой, заводят через разрез в стенке сосуда в ее просвет и фиксируют к внутренней стенке проксимальнее и дистальнее разреза. Сделанный разрез в вене после фиксации в ней фрагментов околощитовидной железы ушивают. Проксимальной и дистальной лигатурой-держалкой производят уменьшение диаметра устья притоковой вены (фиг.1В). Далее аналогичным образом выполняют аутотрансплантацию всех фрагментов околощитовидных желез (фиг.1Г). Удаленные околощитовидные железы можно реплантировать в притоковые ветви большой подкожной вены одной нижней конечности или аналогичным образом реплантировать околощитовидные железы в притоковые ветви большой подкожной вены обеих нижних конечностей.
О возобновлении кровотока в зоне реплантации указывает временное поступление крови между швами на вене, которое быстро заканчивается за счет местного гемостаза. Рану на коже ушивают.
I этап операции считают законченным.
II этап - программируемая, отдаленная, частичная паратиреоидэктомия.
Данный этап выполняют с целью коррекции возвратного или персистирующего ВГПТ после стабилизации гормонального статуса пациента, тщательной оценки клинических проявлений вторичного гиперпаратиреоза, динамики уровня ПТГ, кальция и фосфора крови, оценки функции аутотрансплантатов с помощью 99m Тc сцинтиграфии.
Выполняют разрез кожи (старый послеоперационный рубец на коже иссекается) в проекции предыдущей зоны аутотрансплантации. В подкожной жировой клетчатке выявляют и выделяют основной ствол и нужные притоковые ветви большой подкожной вены.
Ориентиром для облегчения интраоперационной визуализации фрагмента нужного притока большой подкожной вены, содержащего аутотрансплантаты околощитовидной железы, служат лигатуры из цветного, нерассасывающегося шовного материала наложенные при проведении I этапа. Выполняют перевязку и удаление участка притока вены с расположенными в нем аутотрансплантатироваными фрагментами околощитовидной железы.
До операции выполняют анализ уровня ПТГ и кальция в сыворотке. Контроль на гемостаз. Рану на коже ушивают. Операцию считают законченной.
Таким образом, на II этапе происходит программируемое уменьшение количества паратиреоидной ткани в организме пациента за счет удаления части аутотрансплантатов.
II этап за счет ранее выполненной гетеротопической аутотрансплантации дает возможность легкой коррекции возвратного или персистирующего ВГПТ путем удаления необходимой части аутотрансплантатов.
После выполнения очередной операции II этапа вновь дожидаются стабилизации гормонального статуса пациента, тщательно оценивают клинические проявления вторичного гиперпаратиреоза, динамику уровня ПТГ, кальция и фосфора крови, оценивают функцию аутотрансплантатов с помощью 99m Тc сцинтиграфии. При возникновении возвратного или персистирующего ВГПТ по показаниям II этап операции выполняется повторно.
Пример 1 выполнения способа в эксперименте.
Для эксперимента использовалась безпородная собака, кобель, массой 15 кг, возраст 2,5 года.
Операция (I этап) - 06.09.2009 г. Тотальная паратиреоидэктомия с одномоментной свободной, гетеротопической аутотрансплантацией околощитовидных желез в просвет малой подкожной вены задней конечности
Под внутривенным наркозом раствором ксилазина (0,25-0,5 мл/10 кг) срединным разрезом на шее выделяют правую и левую доли щитовидной железы. Визуализируют наружные и внутренние околощитовидные железы. Из-за особенностей локализации внутренних ОЩЖ у собак (иногда они расположены в ткани ЩЖ) не всегда удается их визуализировать [3]. Поэтому в ряде экспериментов для обнаружения всех ОЩЖ используют мителенову синь (в/в 2-6 мг/кг за 30 мин до паратиреоидэктомии). Далее после визуализации всех 4 околощитовидных желез их удаляют и помещают в 0,9%-ный раствор хлорида натрия, охлажденный до 4°С. Рану на шее ушивают узловыми швами. В проекции расположения малой подкожной вены по латеральной поверхности производят разрез кожи до 5 см длиной. В подкожной жировой клетчатке выделяют основной ствол малой подкожной вены. Под проксимальный и дистальный участки вены подводят лигатуры-держалки. С помощью этих лигатур временно прекращают кровоток в выбранном сегменте малой подкожной вены (фиг.1А).
Продольным разрезом до 0,5 см вскрывают просвет вены (фиг.1Б). Из физиологического раствора извлекают околощитовидную железу, с помощью скальпеля или бритвы ее рассекают на фрагменты. Поочередно каждый фрагмент околощитовидной железы прошивают цветной нерассасывающеся нитью с атравматичной иглой, заводят через разрез в стенке сосуда в ее просвет и фиксируют к внутренней стенке проксимальнее и дистальнее разреза (фиг.1В). Сделанное отверстие в вене после фиксации в ней фрагмента околощитовидных желез ушивают. Данной методикой трансплантируют остальные околощитовидные железы. Пересаженные аутотрансплантанты разделяются между собой путем частичного сдавления узлом лигатуры из цветного шовного материала (фиг.1Г).
На возобновление кровотока в зоне реплантации указывает временное поступление крови между швами на вене, которое быстро заканчивается за счет местного гемостаза. Рану на коже ушивают. Операцию считают законченной.
После операции за животным ведут динамическое наблюдение. Для профилактики титании в/в вводят глюконат кальция в течение 15 дней.
II этап. Через 4 недели выполняют программируемую, частичную паратиреоидэктомию. Для этого под внутривенным наркозом выполняют разрез кожи в проекции зоны аутотрансплантации. Выделяют основной ствол малой подкожной вены. Ориентиром для облегчения интраоперационной визуализации нужного участка малой подкожной вены, содержащего аутотрансплантат околощитовидной железы, служат лигатуры из цветного, нерассасывающегося шовного материала, наложенные при проведении I этапа. Выполняется перевязка и удаление 1 участка малой подкожной вены с расположенным в нем аутотрансплантатом околощитовидной железы. Контроль на гемостаз. Рану на коже ушивают. Операция считается законченной.
Далее по данной методике каждые 7 дней выполняют удаление остальных участков малой подкожной вены с аутотрансплантатами.
Лабораторные исследования
У собаки производят забор крови из вены для контроля уровня паратгормона и кальция сыворотки. Результаты исследования на различных сроках проведения эксперимента будут понятны из таблицы.
| КритерииСроки забора | ПТГ (пг/мл) | Са2+ (ммоль/л) |
| До операции | 8,6±0,2 | 2,7±0,2 |
| 2 недели после аутотрансплантации | 6,5±0,2 | 1,9±0,1 |
| 4 недель после аутотрансплантации | 7,3±0,4 | 2,1±0,1 |
| 1 забор* | 6,8±0,2 | 1,9±0,1 |
| 2 забор* | 5,9±0,2 | 1,8±0,1 |
| 3 забор* | 5,2±0,2 | 1,7±0,2 |
| Примечание: * - забор участка малой подкожной вены с аутотрансплантированными ОЩЖ. |
Из таблицы видно, что уже через 4 недели уровни ПТТ и Ca близки к нижним границам нормы, а после удаления части трансплантатов уровень частично снижается, что доказывает жизнеспособность и функциональную активность аутотрансплантированной ткани ОЩЖ.
Данные гистологического исследования материала (4 недели), (фиг.2, 3)
Фрагменты ткани, в которых преобладает зрелая, преимущественно волокнистая соединительная ткань, с участками умеренно инфильтрированными лимфо-гистиоцитарными клетками с небольшим количеством лейкоцитов. В краевой зоне инфильтратов обнаруживаются структуры щитовидной железы, представленные редкими небольшими по размерам коллоидсодержащими фолликулами с дистрофически-некробиотическими изменениями эпителия. Кроме того, выявлены очаги со структурами околощитовидной железы. Отмечена лимфогистиоцитарная инфильтрация с небольшим количеством лейкоцитов и многочисленными сосудами капиллярного типа. Перифокально наблюдаются преимущественно фиброзные изменения или участки формирующегося склероза.
Предлагаемый способ апробирован в эксперименте на 8 беспородных собаках обоего пола и показал эффективность в восстановлении жизнеспособности и функциональной активности реплантированных околощитовидных желез, а также возможность отдаленного программируемого уменьшения количества функционально активной аутотрансплантированной ткани ОЖЩ, что напрямую сопровождается снижением уровня ПТГ и кальция - основных составляющих в развитии клинических проявлений вторичного гиперпаратиреоза. Проведение программированного удаления трансплантатов ОЩЖ предупредит развитие гипопаратиреоза.
Источники информации
1. Kraus L., Korzets Z., Erez I., Magen H., Bernheim J.Successful parathyroid gland autotransplantation after total parathyroidectomy in dialysis patients // Israel Journal of medical science - 1983. - Vol.19, №2. - 153-157.
2. Rothmund M., Wagner P.K., Schark С.Subtotal parathyroidectomy versus total parathyroidectomy and autotransplantation in secondary hyperparathyroidism: a randomized trial // World J. Surg. - 1991. - Vol.15, №3. - Р.745-750.
3. Анатомия собаки и кошки (колл. авторов) /Пер. с нем. Е.Болдырева, И.Кравец. - M.: АКВАРИУМ БУК, 2003. - 556 с.
Способ лечения вторичного гиперпаратиреоза в эксперименте, заключающийся в тотальной паратиреоидэктомии с одномоментной, гетеротопической, свободной реплантацией жизнеспособных удаленных околощитовидных желез или их фрагментов, отличающийся тем, что околощитовидную железу рассекают на фрагменты, поочередно каждый фрагмент прошивают и реплантируют на интиму, в просвет притоковой ветви большой подкожной вены нижних конечностей, с последующей частичной программируемой паратиреоидэктомией при сохранении вторичного гиперпаратиреоза.