Ферментативное получение сложных эфиров (мет)акриловой кислоты
Иллюстрации
Показать всеИзобретение относится к способу получения сложных эфиров (мет)акриловой кислоты (F) на основе спиртов, имеющих, по меньшей мере, одну углерод-углеродную тройную связь, характеризующемуся тем, что, по меньшей мере, один спирт, имеющий, по меньшей мере, одну углерод-углеродную тройную связь, формулы (1)
где R1 означает водород, алкил, имеющий от 1 до 18 атомов углерода; алкил, имеющий от 2 до 18 атомов углерода, арил, имеющий от 6 до 12 атомов углерода, циклоалкил, имеющий от 5 до 12 атомов углерода, прерванные, при необходимости, одним или несколькими атомами кислорода и/или серы и/или одним или несколькими замещенными или незамещенными иминогруппами, или пятичленный-шестичленный гетероцикл, имеющий атомы кислорода, азота и/или серы, при этом названные остатки могут быть замещены соответственно арилом, алкилом, арилокси, алкилокси, гетероатомами и/или гетероциклами, и R2 означает алкилен, имеющий от 1 до 20 атомов углерода, циклоалкилен, имеющий от 5 до 12 атомов углерода, арилен, имеющий от 6 до 12 атомов углерода, или алкилен, имеющий от 2 до 20 атомов углерода, прерванный одним или несколькими атомами кислорода и/или серы, и/или одной или несколькими замещенными или незамещенными иминогруппами, и/или одной или несколькими группами циклоалкила, -(СО)-, -O(CO)O-,
-(NH)(CO)O-, -O(CO)(NH)-, -O(CO)- или -(CO)О-, при этом названные остатки могут быть замещены соответственно арилом, алкилом, арилокси, алкилокси, гетероатомами и/или гетероциклами, n означает целое число от 0 до 3, предпочтительно от 0 до 2 и особенно предпочтительно от 1 до 2 и Xi для каждого i=0 до n независимо друг от друга можно выбрать из группы -CH2-СН2-O-, -CH2-CH(CH3)-O-,
-CH(CH3)-CH2-O-, -CH2-C(CH3)2-O-, -C(CH3)2-CH2-O-, -CH2-CHVin-O-, -CHVin-CH2-O-,
-CH2-CHPh-O- и -CHPh-CH2-O-, предпочтительно из группы -CH2-CH2-O-,
-CH2-CH(CH3)-O- и -CH(CH3)-CH2-O-, и особенно предпочтительно -CH2-CH2-O-, где Ph означает фенил и Vin означает винил, причем гидроксигруппы спирта являются первичными или вторичными, этерифицируют в присутствии, по меньшей мере, одного фермента (Е) с (мет)акриловой кислотой или переэтерифицируют с, по меньшей мере, одним сложным эфиром (мет)акриловой кислоты (D). Применение настоящего способа позволяет получать сложные эфиры (мет)акриловой кислоты на основе спиртов, которые имеют углерод-углеродные тройные связи, при хорошем выходе и низких индексах окраски. 4 з.п. ф-лы.
Реферат
Предложенное изобретение относится к способу получения сложных эфиров (мет)акриловых кислот на основе спиртов с углеродуглеродными тройными связями, способу их получения и их применению.
Получение сложных эфиров (мет)акриловых кислот происходит преимущественно путем катализирумой кислотами или основаниями этерификации (мет)акриловых кислот или переэтерификации других сложных эфиров (мет)акриловых кислот со спиртами или путем реакции спиртов с (мет)акрилоил-хлоридом в присутствии оснований.
Сложные эфиры (мет)акриловых кислот на основе спиртов с углерод-углеродными тройными связями в принципе известны. При классической этерификации таких спиртов, например кислотами, путем индуцируемых кислотами побочных реакций, в частности изомеризации тройной связи, получают тем не менее в большинстве случаев неоднородные, по меньшей мере, однако сильно окрашенные смеси продукта.
Аналогично как при перемещении углерод-углеродных двойных связей путем перегруппировки аллила можно переместить в алкины углерод-углеродные тройные связи (перегруппировка алкин-аллен). Такие изомеризации часто являются равновесными реакциями. Перегруппировка происходит, например, путем перемещения аниона или катиона и катализируется кислотами или основаниями (Houben-Weyl, Methoden der organischen Chemie том V/2a, издательство Thieme 1977, стр.282 и cл.). Благодаря данной нестабильности тройной связи алкины при кислотных или основных условиях склонны к образованию побочных продуктов (например, аллены и их последовательные продукты), которые необходимо удалять из реакционной смеси с большими затратами или путем экстрагирования.
В европейской заявке на патент ЕР 508491 (Wacker Chemie, 1992) 2-пропиноксиэтанол азеотропно этерифицируют с акриловой кислотой в толуоле в качестве разделяющего агента при катализе серной кислотой. Через 4 ч при температуре 120°С избыточную кислоту нейтрализуют NaHCO3 и промывают водой. Затем толуол отгоняют и 2-пропаргилокс-этилакрилат очищают путем дистилляции. Получают продукт слегка желтоватого цвета с выходом 85%.
При катализируемой основанием переэтерификации или других синтезах, например с комплексами металлов, по подобной причине также возникают комплексные и окрашенные смеси продукта. Для удаления окраски и не превращенных реагентов смеси продукта обрабатывают путем дорогостоящей щелочной промывки.
Также известно получение из акрилоилхлорида в присутствии оснований:
В патенте США 3254115 (Thiokol Chemical Corp., 1966) описывают получение пропаргил-акрилата из пропаргилового спирта и акрилоилхлорида. Катализатором является триэтиламин и в качестве растворителя применяют бензол. Продукт дистиллируют в вакууме при выходе 60%.
Harvey et al. (J. Am. Chem. Soc., 1992, 114, 8424-8434) представляет про-паргил-акрилат также из пропаргилового спирта и акрилоилхлорида. Катализатором является триэтиламин и в качестве растворителя применяют дихлорметан. Продукт последовательно несколько раз экстрагируют HCl, NаНСО3 и водой с выходом 90%.
Получение сложных эфиров (мет)акриловых кислот путем ферментативной этерификации или переэтерификации известно.
Kumar и Gross описывают в J. Am. Chem. Soc. 2002, 124, 1850-1851 катализуемое липазой превращение сахаров, защищенных изопропилиденом, путем превращения с винилметакрилатом. Полное превращение достигают благодаря специальному эдукту винилметакрилату, так как высвобожденный виниловый спирт забирают из реакционного равновесия в виде ацетальдегида. Недостатком данного способа является то, что винилметакрилат в качестве специального мономера дорогой и коммерчески доступен только в небольших количествах.
А.Т.J.W. de Goede et al. Описывают в Biocatalysis, 1994, 9, 145-155 переэтерификацию α-O-октил-глюкозида с этилакрилатом до получения сложного 6-O-акрилового эфира в присутствии липаз. Недостатком данного способа является то, что он ограничен глюкозидами и гликозидными связями и чувствительно реагирует на стерическое влияние глюкозида. Кроме того, вследствие неселективных побочных реакций получают более высоко акрилированные продукты.
В европейской заявке на патент ЕР-А1 999229 описывают ферментативную этерификацию и переэтерификацию полиоксиалкиленов с (мет)акриловыми кислотами и сложными эфирами (мет)акриловых кислот.
Из международной заявки на патент WO 03/042227 известна катализуемая липазами переэтерификация алкилакрилатов с сахарами.
В патенте США 5240835 описывают переэтерификацию алкилакрилатов со спиртами при катализе биокатализатора из Corynebacterium oxydans. Там приводят, например, реакцию 96-кратного молярного избытка этилакрилата с 2,2-диметил-1,3-пропандиолом. Получают выход 21% только через 3 дня при температуре 30°С.
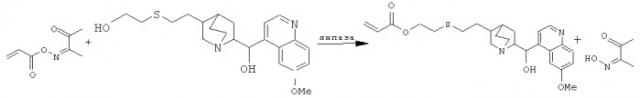
Athawale и Manjrekar (Tetrahedron Lett. 2001, 42 4541-4543) описывают катализуемое липазой акрилирование алкалоидов посредством 2,3-бутандион-монооксимакрилата. Мономер полимеризируют и применяют для индукции энантиоселективного присоединения по Михаэлю.
Athawale и Gaonkar (Makromolecules 1999, 32, 6065-6068) описывают катализуемое липазой акрилирование 2-фенилэтанолов посредством 2,3-бутандион-монооксимакрилата. Мономер в заключение полимеризуют.
Ghogare и Kumar (J. Chem. Soc. 1989, 1533-1535) описывают катализуемое липазой акрилирование различных спиртов, в том числе 2-этилгексан-1,3-диола, активированным 2,3-бутандион-монооксимакрилатом.
Недостатком данных реакций часто является необходимость в применении активированных акрилатов, таких как, например, оксимы или сложные виниловые эфиры, которые дорогие и плохо доступны промышленным способом.
Задачей предложенного изобретения является предоставление способа, с помощью которого из простых эдуктов можно получить сложные эфиры (мет)акриловых кислот на основе спиртов, которые имеют углерод-углеродные тройные связи, при хорошем выходе и низких индексах окраски. Синтез должен протекать при мягких условиях, так что получают продукты с низким индексом цвета и высокой чистотой. Специально нужно отказаться от применения кислотных или основных катализаторов, чтобы предотвратить возникновение побочных продуктов. В результате этого можно отказаться от дорогостоящей дистилляционной иди экстрактивной очистки продукта. Кроме того, нужно отказаться от применения дорогих, активированных производных (мет)акриловых кислот, таких как, например, монооксим или винил(мет)акрилат.
Решением задачи является способ получения сложных эфиров (мет)акриловых кислот (F) на основе спиртов, имеющих, по меньшей мере, одну углерод-углеродную тройную связь, при котором, по меньшей мере, один спирт, имеющий, по меньшей мере, одну углерод-углеродную тройную связь, этерифицируют в присутствии, по меньшей мере, одного фермента (Е) и (мет)акриловых кислот или переэтерифицируют, по меньшей мере, одним сложным эфиром (мет)акриловых кислот (D).
С помощью предложенного согласно изобретению способа возможно получение таких сложных эфиров (мет)акриловых кислот (F) при высоком химическом выходе и при выходе пространство-время и при мягких условиях с хорошими индексами цвета при отказе от работы защитных групп и при применении простых исходных веществ.
В данном документе (мет)акриловые кислоты означают метакриловую кислоту и акриловую кислоту, предпочтительно акриловую кислоту.
Согласно изобретению пригодными спиртами (С) являются такие спирты, которые содержат, по меньшей мере, одну углерод-углеродную тройную связь и, по меньшей мере, одну гидроксигруппу.
Такие спирты могут содержать, например, от 1 до 3, предпочтительно от 1 до 2 и особенно предпочтительно точно одну углерод-углеродную тройную связь.
Спирты (С) могут содержать от одной до шести, предпочтительно от одной до четырех, особенно предпочтительно от одной до трех, в высшей степени предпочтительно от одной до двух и в частности точно одну гидроксигруппу.
Согласно изобретению применяемые спирты (С) могут содержать еще другие гетероатомы, например атомы азота и/или серы, предпочтительно они состоят из атомов углерода, водорода и кислорода.
Согласно изобретению применяемые спирты (С) могут содержать еще другие функциональные группы, например углерод-углеродные двойные связи, аминогруппы, карбоксигруппы, группы простых эфиров или группы сложных эфиров карбоновых кислот. Предпочтительно кроме углерод-углеродной тройной связи и гидроксигруппы они не содержат никаких следующих функциональных групп.
Гидроксигруппы применяемых согласно изобретению спиртов (С) могут быть первичными, вторичными или третичными, предпочтительными являются спирты с первичными или вторичными и особенно предпочтительно с первичными гидроксигруппами. Также в спирте могут одновременно существовать различные гидроксигруппы, например первичные и вторичные.
Первичными гидроксигруппами являются гидроксигруппы, которые связаны точно с одним атомом углерода, который связан точно с одним следующим атомом углерода. Аналогично при вторичных гидроксигруппах связывающий их атом углерода соответственно связан с двумя и при третичных гидроксигруппах с тремя атомами углерода.
Предпочтительными спиртами (С) являются спирты формулы (1)
где
R1 означает водород, алкил, имеющий от 1 до 18 атомов углерода; алкил, имеющий от 2 до 18 атомов углерода, арил, имеющий от 6 до 12 атомов углерода, циклоалкил, имеющий от 5 до 12 атомов углерода, прерванный, при необходимости, одним или несколькими атомами кислорода и/или серы и/или одним или несколькими замещенными или незамещенными иминогруппами, или пятичленный-шестичленный гетероцикл, имеющий атомы кислорода, азота и/или серы, при этом названные остатки могут быть замещены соответственно арилом, алкилом, арилокси, алкилокси, гетероатомами и/или гетероциклами, и
R2 означает алкилен, имеющий от 1 до 20 атомов углерода, циклоалкилен, имеющий от 5 до 12 атомов углерода, арилен, имеющий от 6 до 12 атомов углерода, или алкилен, имеющий от 2 до 20 атомов углерода, прерванный одним или несколькими атомами кислорода и/или серы и/или одним или несколькими замещенными или незамещенными иминогруппами и/или одной или несколькими группами циклоалкилами, -(CO)-, -O(CO)O-, -(NH)(CO)O-, -O(CO)(NH)-, -O(CO)- или -(CO)O-, при этом названные остатки могут быть замещены соответственно арилом, алкилом, арилокси, алкилокси, гетероатомами и/или гетероциклами,
n означает целое число от 0 до 3, предпочтительно от 0 до 2 и особенно предпочтительно от 1 до 2 и
Xi для каждого i=0 до n независимо друг от друга можно выбрать из группы -СН2-СН2-O-, -СН2-СН(СН3)-O-, -СН(СН3)-СН2-O-, -СН2-С(СН3)2-O-, -С(СН3)2-СН2-O-,
-CH2-CHVin-O-, -CHVin-CH2-O-, -CH2-CHPh-O- и -СНРh-СН2-O-, предпочтительно из группы -СН2-СН2-O-, -СН2-СН(СН3)-O- и -СН(СН3)-СН2-O-, и особенно предпочтительно -СН2-СН2-O-,
где Рh означает фенил и Vin означает винил. Особенно предпочтительными спиртами (С) являются спирты формулы (2)
где n, Xi и R1 могут иметь вышеуказанные значения и
R3-R6 независимо друг от друга означают водород, алкил, имеющий от 1 до 18 атомов углерода; алкил, имеющий от 2 до 18 атомов углерода, арил, имеющий от 6 до 12 атомов углерода, циклоалкил, имеющий от 5 до 12 атомов углерода, прерванный, при необходимости, одним или несколькими атомами кислорода и/или серы и/или одним или несколькими замещенными или незамещенными иминогруппами, или пятичленный-шестичленный гетероцикл, имеющий атомы кислорода, азота и/или серы, при этом названные остатки могут быть замещены соответственно арилом, алкилом, арилокси, алкилокси, гетероатомами и/или гетероциклами.
В высшей степени предпочтительными являются спирты (С) формулы (3)
где n, Xi и R1 могут иметь вышеуказанные значения и
R7 и R8 независимо друг от друга означают водород, алкил, имеющий от 1 до 18 атомов углерода; алкил, имеющий от 2 до 18 атомов углерода, арил, имеющий от 6 до 12 атомов углерода, циклоалкил, имеющий от 5 до 12 атомов углерода, прерванный, при необходимости, одним или несколькими атомами кислорода и/или серы и/или одним или несколькими замещенными или незамещенными иминогруппами, или пятичленный-шестичленный гетероцикл, имеющий атомы кислорода, азота и/или серы, при этом названные остатки могут быть замещены соответственно арилом, алкилом, арилокси, алкилокси, гетероатомами и/или гетероциклами,
где R7 и R8 также вместе могут образовать кольцо.
В вышеуказанных определениях означают
алкилен, имеющий от 1 до 20 атомов углерода, замещенный, при необходимости, арилом, алкилом, арилокси, алкилокси, гетероатомами и/или гетероциклами, например метилен, 1,1-этилен, 1,2-этилен, 1,1-пропилен, 1,2-пропилен, 1,3-пропилен, 1,1-бутилен, 1,2-бутилен, 1,3-бутилен, 1,4-бутилен, 1,6-гексилен, 2-метил-1,3-пропилен, 2-этил-1,3-пропилен, 2,2-диметил-1,3-пропилен, 2,2-диметил-1,4-бутилен,
циклоалкилен, имеющий от 5 до 12 атомов углерода, замещенный, при необходимости, арилом, алкилом, арилокси, алкилокси, гетероатомами и/или гетероциклами, например циклопропилен, циклопентилен, циклогексилен, циклооктилен, циклододецилен,
алкилен, имеющий от 2 до 20 атомов углерода, при необходимости, замещенный, арилом, алкилом, арилокси, алкилокси, гетероатомами и/или гетероциклами, прерванный или несколькими атомами кислорода и/или серы, и/или одной или несколькими замещенными или незамещенными иминогруппами, и/или одной или несколькими группами циклоалкила, -(СО)-, -O(СО)O-, -(NН)(СО)O-, -O(СО)(NН)-,
-О(СО)- или -(СО)О-, например 1-окса-1,3-пропилен, 1,4-диокса-1,6-гексилен, 1,4,7-триокса-1,9-нонилен, 1-окса-1,4-бутилен, 1,5-диокса-1,8-октилен, 1-окса-1,5-пентилен, 1-окса-1,7-гептилен, 1,6-диокса-1,10-децилен, 1-окса-3-метил-1,3-пропилен, 1-окса-3-метил-1,4-бутилен, 1-окса-3,3-диметил-1,4-бутилен, 1-окса-3,3-диметил-1,5-пентилен, 1,4-диокса-3,6-диметил-1,6-гексилен, 1-окса-2-метил-1,3-пропилен, 1,4-диокса-2,5-диметил-1,6-гексилен, 1-окса-1,5-пент-3-енилен, 1-окса-1,5-пент-3-инилен, 1,1-циклогексилен, 1,2-циклогексилен, 1,3-циклогексилен или 1,4-циклогексилен, 1,2-циклопентилен или 1,3-циклопентилен, 1,2-фенилен, 1,3-фенилен или 1,4-фенилен, 4,4′-бифенилен, 1,4-диаза-1,4-бутилен, 1-аза-1,3-пропилен, 1,4,7-триаза-1,7-гептилен, 1,4-диаза-1,6-гексилен, 1,4-диаза-7-окса-1,7-гептилен, 4,7-диаза-1-окса-1,7-гептилен, 4-аза-1-окса-1,6-гексилен, 1-аза-4-окса-1,4-бутилен, 1-аза-1,3-пропилен, 4-аза-1-окса-1,4-бутилен, 4-аза-1,7-диокса-1,7-гептилен, 4-аза-1-окса-4-метил-1,6-гексилен, 4-аза-1,7-диокса-4-метил-1,7-гептилен, 4-аза-1,7-диокса-4-(2′-гидроксиэтил)-1,7-гептилен, 4-аза-1 -окса-(2′-гидроксиэтил)-1,6-гексилен или 1,4-пиперазинилен,
арилен, имеющий от 6 до 12 атомов углерода, замещенный, при необходимости, арилом, алкилом, арилокси, алкилокси, гетероатомами и/или гетероциклами, например 1,2-фенилен, 1,3-фенилен или 1,4-фенилен, 4,4′-би-фенилен, толуилен или ксилилен,
алкил, имеющий от 1 до 18 атомов углерода, или алкил, имеющий от 2 до 18 атомов углерода, прерванный, при необходимости, одним или несколькими атомами кислорода и/или серы и/или одной или несколькими замещенными или незамещенными иминогруппами, например, метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, пентил, гексил, гептил, октил, 2-этилгексил, 2,4,4-триметилпентил, децил, додецил, тетрадецил, гетадецил, октадецил, 1,1-диметил-пропил, 1,1-диметилбутил, 1,1,3,3-тетраметилбутил, бензил, 1-фенилэтил, 2-фенилэтил, α,α-диметилбензил, бензгидрил, р-толилметил,1-(р-бутилфенил)-этил, р-хлор-бензил, 2,4-дихлорбензил, р-метоксибензил, м-этоксибензил, 2-цианоэтил, 2-циано-пропил, 2-метоксикарбонэтил, 2-этоксикарбонилэтил, 2-бутоксикарбонилпропил, 1,2-ди-(метоксикарбонил)-этил, 2-метоксиэтил, 2-этоксиэтил, 2-бутоксиэтил, диэтокси-метил, диэтоксиэтил, 1,3-диоксолан-2-ил, 1,3-диоксан-2-ил, 2-метил-1,3-диоксолан-2-ил, 4-метил-1,3-диоксолан-2-ил, 2-изопропоксиэтил, 2-бутоксипропил, 2-октилоксиэтил, хлорметил, 2-хлорэтил, трихлорметил, трифторметил, 1,1-диметил-2-хлорэтил, 2-метоксиизопропил, 2-этоксиэтил, бутилтиометил, 2-додецилтиоэтил, 2-фенилтиоэтил, 2,2,2-трифторэтил, 2-феноксиэтил, 2-феноксипропил, 3-феноксипропил, 4-феноксибутил, 6-феноксигексил, 2-метоксиэтил, 2-метоксипропил, 3-метоксипропил, 4-метоксибутил, 6-метоксигексил, 2-этоксиэтил, 2-этоксипропил, 3-этоксипропил, 4-этоксибутил или 6-этоксигексил, и предпочтительно метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, пентил, гексил, гептил, октил, 2-этилгексил, 2,4,4-триметилпентил, децил, додецил, тетрадецил, гетадецил, октадецил, 1,1-диметилпропил, 1,1-диметилбутил, 1,1,3,3-тетраметилбутил, бензил, 1-фенилэтил, 2-фенилэтил, α,α-диметилбензил, бензгидрил, р-толилметил,1-(р-бутилфенил)-этил, р-хлорбензил, 2,4-дихлорбензил, 2-цианоэтил, 2-цианопропил, хлорметил, 2-хлорэтил, трихлорметил, трифторметил, 1,1-диметил-2-хлорэтил и 2,2,2-трифторэтил,
арил, имеющий от 6 до 12 атомов углерода, прерванный, при необходимости, одним или несколькими атомами кислорода и/или серы и/или одной или несколькими замещенными или незамещенными иминогруппами, например фенил, толил, ксилил, α-нафтил, β-нафтил, 4-дифенилил, хлорфенил, дихлорфенил, трихлорфенил, дифторфенил, метилфенил, диметилфенил, триметилфенил, этилфенил, диэтилфенил, изо-пропилфенил, трет-бутилфенил, додецилфенил, метоксифенил, диметоксифенил, этоксифенил, гексилоксифенил, метилнафтил, изопропилнафтил, хлорнафтил, этоксинафтил, 2,6-диметилфенил, 2,4,6-триметилфенил, 2,6-диметоксифенил, 2,6-дихлорфенил, 4-бромфенил, 2- или 4-нитрофенил, 2,4-динитрофенил или 2,6-динитрофенил, 4-диметиламинофенил, 4-ацетилфенил, метоксиэтилфенил или этоксиметилфенил, и предпочтительно фенил, толил, ксилил, α-нафтил, β-нафтил, 4-дифенилил, хлорфенил, дихлорфенил, трихлорфенил, дифторфенил, метилфенил, диметилфенил, триметилфенил, этилфенил, диэтилфенил, изо-пропилфенил, трет-бутилфенил, додецилфенил, хлорнафтил, 2,6-диметилфенил, 2,4,6-триметилфенил, 2,6-диметоксифенил, 2,6-дихлорфенил, 4-бромфенил, 2- или 4-нитрофенил, 2,4-динитрофенил или 2,6-динитрофенил; циклоалкил, имеющий от 5 до 12 атомов углерода, прерванный,
при необходимости, одним или несколькими атомами кислорода и/или серы и/или одной или несколькими замещенными или незамещенными иминогруппами, например циклопентил, циклогексил, циклооктил, циклододецил, метилциклопентил, диметилциклопентил, метилциклогексил, диметилциклогексил, диэтилциклогексил, бутилциклогексил, метоксициклогексил, диметоксициклогексил, диэтоксициклогексил, бутилтиоциклогексил, хлорциклогексил, дихлорциклогексил, дихлорциклопентил, а также насыщенная или ненасыщенная бициклическая система, такая как, например, норборнил или норборненил, и предпочтительно циклопентил, циклогексил, циклооктил, циклододецил, метилциклопентил, диметилциклопентил, метилциклогексил, диметилциклогексил, диэтилциклогексил, бутилциклогексил, хлорциклогексил, дихлорциклогексил, дихлорциклопентил, а также насыщенная или ненасыщенная бициклическая система, такая как, например, норборнил или норборненил
и
прерванный, при необходимости, одним или несколькими атомами кислорода и/или серы и/или одной или несколькими замещенными или незамещенными иминогруппами, пятичленный-шестичленный гетероцикл, имеющий атомы кислорода, азота и/или серы, например фурил, тиофенил, пиррил, пиридил, индолил, бензоксазолил, диоксолил, диоксил, бензимидазолил, бензтиазолил, диметилпиридил, метилхинолил, диметилпиррил, метоксифурил, диметоксипиридил, дифторпиридил, метилтиофенил, изопропилтиофенил или трет-бутилтиофенил.
Примерами R2 являются метилен, 1,1-этилен, 1,2-этилен, 1,1-пропилен, 2,2-пропилен, 1,2-пропилен, 1,3-пропилен, 1,1-диметил-1,2-этилен, 1,4-бутилен, 1,6-гексилен, 2-метил-1,3-пропилен, 2-этил-1,3-пропилен, 2,2-диметил-1,3-пропилен и 2,2-диметил-1,4-бутилен, 3-метил-1,5-пентилен, 3,5-гептилен, 1,2-циклопентилен, 1,3-циклопентилен, 1,2-циклогексилен, 1,3-циклогексилен и орто-фенилен, предпочтительными являются метилен, 1,1-этилен, 1,2-этилен, 1,1-пропилен и 2,2-пропилен, особенно предпочтительными являются метилен, 1,1-этилен, 1,2-этилен и 2,2-пропилен, и особенно предпочтительным является метилен.
Предпочтительными примерами R1 и R3-R7 независимо друг от друга являются водород, алкил, имеющий от 1 до 4 атомов углерода, н-гексил, н-гептил, н-октил, н-децил, н-додецил, н-тетрадецил, н-гексадецил, н-октадецил, н-эйкозил, 2-этилгексил, циклопентил, циклогексил, циклооктил, циклододецил, фенил, нафтил или бензил. Предпочтительными R1 и R3-R7 являются независимо друг от друга водород и метил, особенно предпочтительно водород.
В рамках данного документа алкил, имеющий от 1 до 4 атомов углерода, означает метил, этил, изо-пропил, н-пропил, н-бутил, изо-бутил, втор-бутил или трет-бутил, предпочтительно метил, этил, н-пропил и н-бутил, особенно предпочтительно метил, этил и н-бутил, в высшей степени предпочтительно метил и этил и в частности метил.
Предпочтительными примерами спиртов (С) являются 3-метил-1-пентин-3-ол, 2-пропин-1-ол (пропаргиловый спирт), 3-бутин-2-ол, 2-метил-3-бутин-2-ол, 4-пентин-1-ол, 1-этинилциклогексанол, 3-бутин-1-ол, 2-бутин-1-ол и 1-октин-3-ол, а также их однократно или двукратно этоксилированные продукты. Особенно предпочтительными являются 2-пропин-1-ол (пропаргиловый спирт), 2-бутин-1-ол, 3-бутин-2-ол и 2-метил-3-бутин-2-ол и их однократно или двукратно этоксилированные продукты и в высшей степени предпочтительным является 2-пропин-1-ол (пропаргиловый спирт) и его однократно или двукратно этоксилированные продукты и особенно предпочтительным является однократно или двухкратно этоксилирован-ный пропаргиловый спирт, а также его смеси.
На реакционной стадии происходит этерификация с (мет)акриловыми кислотами или предпочтительно переэтерификация спирта (С) с, по меньшей мере, одним, предпочтительно одним (мет)акрилатом (D) в присутствии, по меньшей мере, одного, предпочтительно одного фермента в присутствии, по меньшей мере, одного, предпочтительно одного фермента (Е), катализирующего переэтерификацию.
Соединения (D) могут быть (мет)акриловыми кислотами или сложными эфирами (мет)акриловых кислот с насыщенным спиртом, предпочтительно насыщенный сложный алкиловый эфир, имеющий от 1 до 10 атомов углерода, или сложный цикло-алкиловый эфир, имеющий от 3 до 12 атомов углерода, (мет)акриловых кислот, особенно предпочтительно насыщенный сложный алкиловый эфир, имеющий от 1 до 4 атомов углерода, (мет)акриловых кислот.
В рамках данного документа насыщенный означает соединения без углерод-углеродных сложных связей (кроме, разумеется, углерод-углеродных двойных связей в элементах (мет)акрила).
Примерами для соединений (D) являются сложные метиловые, этиловые, н-бутиловые, изо-бутиловые, н-октиловые и 2-этилгексиловые эфиры (мет)акриловых кислот, 1,2-этиленгликольди(мет)-акрилат и 1,2-этиленгликольмоно(мет)-акрилат, 1,4-бутандиолди(мет)-акрилат и 1,4-бутандиолмоно(мет)-акрилат, 1,6-гександиолди(мет)-акрилат и 1,6-гександиолмоно(мет)-акрилат, триметилолпропантри(мет)акрилат и пента-эритриттетра(мет)акрилат.
Особенно предпочтительными являются сложные метиловые, этиловые, н-бутиловые и 2-этил-гексиловые эфиры (мет)акриловых кислот и особенно предпочтительно сложные метиловые, этиловые, н-бутиловые эфиры (мет)акриловых кислот.
Если названные спирты являются оптически активными, то их применяют предпочтительно в виде рацематов или в виде смесей диастереомеров, тем не менее также возможно применять их в виде чистых энантиомеров или диастереомеров или в виде смесей диастереомеров.
Ферментативная этерификация или переэтерификация с (мет)акрилатом происходит в общем при температуре от 0 до 100°С, предпочтительно от 20 до 80°С, особенно предпочтительно от 20 до 70°С, в высшей степени предпочтительно от 20 до 60°С.
Применяемые согласно изобретению ферменты (Е) выбирают из, например, гидролаз (Е.С. 3.-.-.-), и среди них особенно из эстераз (Е.С. 3.1.-.-), липаз (Е.С. 3.1.1.3), гликозилаз (Е.С. 3.2.-.-) и протеаз (Е.С. 3.4.-.-) в свободной форме или в форме, химически или физически иммобилизованной на носителе, предпочтительно липаз, эстераз или протеаз и особенно предпочтительно эстераз (Е.С. 3.1.-.-). Особенно предпочтительными являются Novozyme 435 (липазы из Candida antarctica В) или липазы из Alcaligenes sp., Aspergillus sp., Mucor sp., Penicilium sp., Geotricum sp., Rhizopus sp., Burkholderia sp., Candida sp., Pseudomonas sp., Thermomyces sp. или поджелудочной железы свиней, в частности предпочтительными являются липазы из Candida antarctica В или из Burkholderia sp.
Содержание ферментов в реакционной среде находится, как правило, в области от примерно 0,1 до 10% масс., в расчете на применяемый спирт (С).
Реакционное время зависит в том числе от температуры, применяемого количества и активного ферментативного катализатора и от необходимого превращения, а также от спирта. Предпочтительно реакционное время согласовывают таким образом, что превращение не превращенных, находящихся в спирте (С), то есть более низко замещенных функций гидрокси составляет, по меньшей мере, 70%, предпочтительно, по меньшей мере, 80, особенно предпочтительно, по меньшей мере, 90, в высшей степени предпочтительно, по меньшей мере, 95%, в частности, по меньшей мере, 97% и специально, по меньшей мере, 98%. Как правило, для этого достаточно от 1 до 72 часов, предпочтительно от 3 до 36 и особенно предпочтительно от 3 до 24 часов.
Молярное соотношение соединения (мет)акриловых кислот (D) (в расчете на элементы (мет)-акрила к спирту (С) (в расчете на гидроксигруппы) можно регулировать в широкой области, как, например, в соотношении от 100:1 до 1:1, предпочтительно от 50:1 до 1:1, особенно предпочтительно от 20:1 до 1:1 и в высшей степени предпочтительно от 10:1 до 1:1.
Реакция может протекать в органических растворителях или их смесях или без добавления растворителей. Предпочтительно не добавляют никакого растворителя. Добавления, как правило, являются абсолютно безводными (то есть при 10, предпочтительно при 5, особенно предпочтительно при 1 и в высшей степени предпочтительно при 0,5% масс. добавления воды).
Пригодными органическими растворителями являются растворители, известные для данных целей, например третичные моноолы, такие как спирты, имеющие от 3 до 6 атомов углерода, предпочтительно трет-бутанол, трет-амиловый спирт, пиридин, простой поли-С1-С4-алкиленгликольди-С1-С4-алкиловый эфир, предпочтительно простой полиэтилен-гликольди-С1-С4-алкиловый эфир, такой как, например, 1,2-диметоксиэтан, простой диэтиленгликольдиметиловый эфир, простой полиэтиленгликольдиметиловый эфир 500, простой метил-трет-бутиловый эфир, простой этил-трет-бутиловый эфир, алкиленкарбонаты, имеющие от 1 до 4 атомов углерода, в частности пропиленкарбонат, сложный эфир алкилуксусной кислоты, имеющей от 3 до 6 атомов углерода, в частности сложный эфир трет-бутил-уксусной кислоты, ТГФ, толуол, 1,3-диоксолан, ацетон, озо-бутил-метилкетон, этилметилкетон, 1,4-диоксан, простой трет-бутилметиловый эфир, циклогексан, метилциклогексан, толуол, гексан, диметоксиметан, 1,1-диметоксиэтан, ацетонитрил, а также их однофазные и многофазные смеси. Может быть предпочтительно отделять высвобожденную воду или спирт через бинарный или тройной гетероазеотроп, кипящий по возможности более близко к температурному оптимуму применяемого фермента. Удаленный таким образом спирт можно затем удалять через разделение фаз или мембранное паровое отделение.
Выборочно к органическим растворителям можно добавлять водный растворитель, так что, в зависимости от органического растворителя, возникают однофазные или многофазные реакционные растворы. Водными растворителями являются, например, вода, а также водные, разбавленные (например, 10-100 мМ) буферы, например, с значением pH в области от примерно 6 до 8, как, например, фосфат калия или буфер TRIS-HCl.
Содержание воды в реакционной исходной смеси находится, как правило, при 0-10% масс. Предпочтительно реагенты применяют без предварительной обработки (сушки, введения воды).
Субстраты присутствуют или растворенными, суспендированными как твердое вещество, или в эмульсии в реакционной среде. Предпочтительно первоначальная концентрация реагентов находится в области от примерно 0,1 до 20 моль/л, в частности при от 0,15 до 10 моль/л или от 0,2 до 5 моль/л.
Реакцию можно проводить непрерывно, например в трубном реакторе или в каскаде трубных реакторов, или периодически.
Превращение можно проводить во всех реакторах, подходящих для таких превращений. Такие реакторы известны специалисту в данной области. Предпочтительно превращение происходит в реакторе с мешалкой или в реакторе с неподвижным слоем.
Для перемешивания реакционной исходной смеси можно применять любые способы. Не требуются специальные устройства для перемешивания. Реакционная среда может быть однофазной или многофазной и реагенты в ней растворяют, суспендируют или эмульгируют, при необходимости, представляют вместе с молекулярным ситом и для инициирования реакции, а также при необходимости, однократно или многократно в ходе реакции, смешивают с ферментативным препаратом. Температуру во время реакции устанавливают на желаемом значении и можно, при желании, во время течения реакции повышать или понижать.
Если реакцию проводят в реакторе с неподвижным слоем, то реактор с неподвижным слоем предпочтительно оснащают иммобилизованными ферментами, при этом реакционную смесь можно перекачивать через колонну, заполненную ферментом. Также возможно проводить превращение в реакторе с кипящим слоем, при этом фермент применяют иммобилизованным на носителе. Реакционную смесь можно непрерывно перекачивать через колонну, при этом с помощью скорости течения регулировать время превращения и таким образом желаемое превращение. Также возможно перекачивать реакционную смесь в циркуляции через колонну, при этом также одновременно можно отогнать под вакуумом высвобожденный спирт.
Удаление воды в случае этерификации или спиртов, которые высвобождаются при переэтерификации из алкил(мет)акрилатов, происходит непрерывно или постепенно известным способом, например посредством вакуума, азеотропного удаления, абсорбции, первапорации и диффузии через мембраны.
Для этого подходят предпочтительно молекулярные сита или цеолиты (величина пор, например, в области примерно 3-10 ангстрем), отделение путем дистилляции или с помощью подходящих полупроницаемых мембран.
Однако также возможно добавлять отделенную смесь из алкил(мет)акрилата и лежащего в его основе спирта, который часто образует азеотроп, непосредственно в устройство для получения алкил(мет)акрилата, чтобы снова применять в этерификации с (мет)акриловыми кислотами.
После окончания реакции реакционную смесь, полученную из этерификации или переэтерификации, можно применять далее без дальнейшей очистки или при необходимости очищать на следующей стадии.
Как правило, на стадии очистки из реакционной смеси отделяют только применяемый фермент и реакционный продукт отделяют от, при необходимости, применяемого органического растворителя.
Отделение фермента происходит, как правило, путем фильтрации, абсорбции, центрифугирования или декантирования. Отделенный фермент можно затем применять для следующих реакций.
Отделение от органического растворителя происходит, как правило, путем дистилляции, ректификации или при твердых реакционных продуктах путем фильтрации.
Для следующего очищения реакционного продукта также можно проводить хроматографию.
Однако предпочтительно на стадии очистки отделяют только применяемый фермент и, при необходимости, используемый растворитель или избыток (мет)акриловых кислот или (мет)акрилата.
Реакционные условия при ферментативной этерификации или переэтерификации являются мягкими. На основе низких температур и прочих мягких условий избегают образования побочных продуктов во время реакции, которые могут происходить в противном случае, например от химических катализаторов или вследствие нежелательной радикальной полимеризации используемых (мет)акрилатов, которую иначе можно предотвратить только путем добавления стабилизаторов.
При предложенном согласно изобретению проведении реакции соединение (мет)акрила (D) можно добавлять сверх и так уже содержащегося сухого наливного катализатора дополнительный стабилизатор, например простой гидрохинонмонометиловый эфир, фенотриазин, фенолы, такие как, например, 2-трет-бутил-4-метилфенол, 6-трет-бутил-2,4-диметил-фенол или N-оксилы, такие как 4-гидрокси-2,2,6,6-тетраметил-пиперидин-N-оксил, 4-оксо-2,2,6,6-тетраметил-пиперидин-N-оксил, например, в количествах от 50 до 2000 ppm. Предпочтительно этерификацию или переэтерификацию проводят в присутствии кислородсодержащих газов, предпочтительно воздуха или смесей воздух-азот.
Далее ферментный катализатор можно без проблем удалять из конечного продукта
Реакционную смесь можно, при необходимости, очищать, например путем фильтрации, дистилляции, ректификации, хроматографии, обработки с ионообменниками, адсорбентами, нейтральной, кислой и/или щелочной промывки, отпаривания или кристаллизации.
Следующим предметом предложенного изобретения являются (мет)акрилаты, полученные из спиртов (С) путем ферментативной этерификации или переэтерификации. Благодаря предложенным согласно изобретению условиям (мет)акрилаты имеют индекс окраски ниже 100 АРНА согласно DIN ISO 6271, предпочтительно ниже 80. Кроме того, они содержат, как правило, менее чем 1,0% побочных продуктов из реакций перегруппировки кратной связи из катализуемых кислотами или основаниями побочных реакций.
Преимуществом полученных таким образом предложенным согласно изобретению способом сложных эфиров (мет)акриловых кислот является то, что их на основании своего низкого индекса цвета можно предпочтительно использовать в применениях лаков и там, в частности, в бесцветных лаках, так как они благодаря незначительной собственной окраске вызывают незначительную окраску покрытий по сравнению со спиртом, полученным обычными способами.
Кроме того, покрытия с полученными согласно предложенному изобретению сложными эфирами могут обладать очень высокой стойкостью к царапанью, твердостью, стойкостью к действию химических реагентов, эластичностью и сцепляемостью, как на гидрофильных, так и на гидрофобных субстратах.
Полученные согласно изобретению сложные эфиры (мет)акриловых кислот (F) можно применять предпочтительно в качестве мономеров или сомономеров в поли(мет)акрилатах или в качестве реактивных разбавителей в поли(мет)акрилатах, отверждаемых термически, облучением и/или двухсторонним термоотверждением. Такие поли(мет)акрилаты пригодны, например, в виде связующих веществ в материалах покрытия, отверждаемых термически, облучением и/или двухсторонним термоотверждением, а также в клеях, например акрилатных клеях, а также в герметизирующих составах.
Поэтому следующим предметом данного изобретения является применение сложных эфиров (мет)акриловых кислот, полученных предложенным согласно изобретению способом, в качестве реактивных разбавителей или клеев в составах для покрытий, отверждаемых облучением или двухсторонним термоотверждением, предпочтительно в защитных покрытиях, особенно предпочтительно в прозрачных бесцветных лаках. Разумеется предложенные согласно изобретению сложные эфиры (мет)акриловых кислот можно применять также в качестве мономеров в полимеризациях, при необходимости вместе с другими полимеризуемыми мономерами, такими как, например, (мет)акриловые кислоты, сложные эфиры (мет)акриловых кислот, стирол, бутадиен, акрилнитрил, винилацетат, N-винилпирролидон, простой 4-гидроксибутил-виниловый эфир или М-винилформамид.
Под "двухсторонним термоотверждением" понимают, что составы для покрытия отверждают термически или с помощью актиничного облучения. В рамках предложенного изобретения под актиничным облучением понимают электромагнитное облучение как видимый свет, УФ-облучение или рентгеновское облучение, в частности УФ-облучение, и корпускулярное облучение, такое как электронное облучение.
Отверждаемыми облучением клеями являются такие, которые являются отверждаемыми с помощью актиничного облучения, как определено выше, в частности с помощью УФ-облучения.
Следующим предметом предложенного изобретения являются композиции лаков, содержащие сложные эфиры (мет)акриловых кислот, полученные предложенным согласно изобретению способом. П