Картридж, система и способ автоматизированной медицинской диагностики
Иллюстрации
Показать всеГруппа изобретений относится к детектированию присутствия, отсутствия или количества специфических последовательностей ДНК и РНК. Раскрыт картридж, предназначенный для детектирования присутствия, отсутствия и/или количества целевой последовательности нуклеотидов в образце, содержащем одну или более последовательностей нуклеиновых кислот, причем картридж содержит общую часть, содержащую средство обработки жидкости, множество камер обработки, которые используются независимо от применения картриджа, и резервуар для жидкости, а также отсеки для отходов, предназначенные для разных жидкостей, картридж также содержит, одну или более отдельных специфичных для применения частей, выбранных из группы, содержащей устройство детектирования, контейнер для жидкости и устройства амплификации, и специфичные для применения части выполнены с возможностью соединения с общей частью с использованием соединения с защелкой. Также раскрыты система и способ детектирования присутствия, отсутствия и/или количества целевой последовательности нуклеотидов в образце, содержащем одну или более последовательностей нуклеиновых кислот. Достигается повышение надежности детектирования. 3 н. и 11 з.п. ф-лы, 5 ил.
Реферат
Изобретение относится к картриджу для детектирования присутствия, отсутствия или количества специфических последовательностей ДНК или РНК. Изобретение также относится к использованию системы, в которой, в случае необходимости, применяется картридж для детектирования присутствия, отсутствия или количества специфических последовательностей ДНК или РНК.
С момента открытия ДНК технология, относящаяся к детектированию присутствия, отсутствия или количества специфических последовательностей ДНК или РНК в образце, получила чрезвычайно большое развитие. В частности, ПЦР (PCR), полимеразная цепная реакция, позволила сделать существенный вклад в развитие всех типов анализа детектирования присутствия или отсутствия последовательностей ДНК или РНК. В настоящее время возможно получать образцы, содержащие ДНК, из организма и определять присутствие, отсутствие или количество в них определенных специфических последовательностей ДНК (целевых последовательностей). Существует технология выполнения такого анализа, проводимая одновременно для множества целевых последовательностей, так называемое составное детектирование целевых последовательностей, которое позволяет повысить производительность.
В настоящее время анализы такого типа еще не проводят на рутинной основе так, как, например, измерения содержания глюкозы в крови в случае диабета. Как правило, необходимо использовать хорошо оборудованные лаборатории и тщательное вести протоколы для исключения перекрестного загрязнения и обеспечения надежности полученных результатов, то есть сведения к минимуму ложноположительных или ложноотрицательных данных тестов. Однако в настоящее время для этого требуется большое количество ручного труда хорошо подготовленного и работающего под квалифицированным контролем персонала, и в данной области техники сохраняется потребность преодоления упомянутых выше недостатков используемых в настоящее время способов анализа ДНК или РНК. В частности, анализ РНК, как известно, является очень трудновыполнимым, поскольку очень легко возникают загрязнения в результате присутствия незначительных количеств РНК в атмосфере и на руках квалифицированных лаборантов. Кроме того, используемые в настоящее время способы анализа являются не только трудоемкими, они также требуют значительного времени. Как правило, эффективная процедура для обычного анализа ДНК или РНК занимает приблизительно 6 часов, в частности, помимо прочего, из-за того, что требуется выполнять определенную обработку между различными системами для отбора образцов, изоляцию ДНК или РНК из образца, последующую оценку результатов анализа на присутствие, отсутствие или количество целевой последовательности в образце, обработку каких-либо полученных результатов и соответствующее представление результатов.
Системы, построенные на основе картриджа, предназначенные для детектирования ДНК, были раскрыты ранее.
Например, в US 5,882,903 раскрыта система детектирования ДНК. Эта система содержит первый узел, имеющий одну или больше реакционных камер, и второй узел, содержащий множество камер для жидкости. В каждой камере для жидкости содержится жидкость, используемая во время детектирования ДНК. Такие жидкости содержат промывные жидкости, жидкость для лизиса и раствор для амплификации, содержащий буфер для амплификации и соответствующие праймеры. Реакционные камеры используются для выполнения различных этапов детектирования, таких как промывка, лизис и амплификация.
Другие системы на основе картриджа, известные из предшествующего уровня техники и используемые для детектирования ДНК, раскрыты, например, в US 5,585,069, US 6,168,948 и WO97/27324.
Недостаток известных систем на основе картриджа состоит в том, что картриджи в этих системах разработаны как единая деталь. Известный картридж не обеспечивает гибкость при применении, для которого этот картридж предназначен, например, для специфических бактерий, которые могут детектироваться в системе или для различных видов образцов, которые могут быть введены в картридж.
Цель настоящего изобретения состоит в создании картриджа для детектирования присутствия, отсутствия и/или количества целевой последовательности нуклеотидов в образце, в котором обеспечивалась бы возможность более гибкого использования такого картриджа.
Эта цель достигается с помощью картриджа, заявленного в п. 1 формулы изобретения.
Благодаря созданию общей части, которую можно использовать для широкого разнообразия вариантов применения, и одной или больше специфичных для применения частей, которые специально выполнены с возможностью использования для определенного варианта применения, картридж можно собирать для конкретного варианта применения, для использования в котором он предназначен.
Общая часть типично может включать средство обработки жидкости, такое как насос и клапаны, множество камер обработки, которые используются независимо от применения картриджа, и резервуар для жидкости, а также отсеки для отходов, предназначенные для разных жидкостей, таких как буферы для лизиса и промывки. Эти элементы картриджа будут более подробно описаны ниже.
В варианте выполнения одна или более специфичных частей представляет собой корпус ПЦР, имеющий одну или больше камер термоциклирования и содержащий множество праймеров. При этом возможно использовать картридж для различных панелей бактерий/устойчивостей. Благодаря предоставлению разных корпусов ПЦР, содержащих множество праймеров, корпус ПЦР, специфичный для варианта применения, можно выбрать на основе варианта применения, для которого используется картридж. Например, корпус ПЦР, содержащий праймеры, можно выбрать на основе групп детектируемых бактерий/устойчивостей, причем этот выбор может быть специфичным для конкретного анализа или для конкретного региона, такого как Европа, Азия или Африка. Также возможно выбирать размер или количество камер термоциклирования на основе детектируемых бактерий/устойчивостей. В предпочтительном варианте выполнения камеры термоциклирования используются только для этапа термоциклирования. На камеры обработки, в частности, праймеры, в таком варианте выполнения, не влияют какие-либо другие этапы, выполняемые в картридже.
В варианте выполнения предусмотрены две или больше камеры термоциклирования. В каждой из камер термоциклирования может быть помещено определенное количество обрабатывающей жидкости, что позволяет выполнять эффективную параллельную обработку.
В варианте выполнения праймер помещают в каждую одну из одной или больше камер термоциклирования. Благодаря размещению праймеров в одной или больше камерах термоциклирования, праймеры не требуется переносить перед выполнением этапов термоциклирования. Таким образом, обеспечивается более эффективное использование праймеров. Кроме того, это позволяет создать более простую конструкцию корпуса ПЦР.
В одном варианте выполнения праймер наносят в виде пятна на корпус ПЦР. Такое нанесение пятна может быть выполнено с использованием любой известной технологии нанесения пятен, такой как, например, струйная печать. Предпочтительно, нанесенные в виде пятна праймеры помещают в одну или больше камер термоциклирования, но они также могут быть предоставлены в любом другом соответствующем местоположении, таком как входные каналы для подачи образца в одну или больше камер термоциклирования.
В варианте выполнения одна или больше специфичных для применения частей представляет собой устройство детектирования. Множество разных способов детектирования можно использовать для детектирования ампликонов в образце после амплификации ДНК/РНК. Такие способы детектирования могут включать в себя оптические, электрохимические, магнито-капиллярные и гель-электрофорезные способы детектирования. В зависимости от способа детектирования, используемого для определенного образца, устройство детектирования или, по меньшей мере, его часть можно выбрать и подключить к общей части картриджа.
В одном варианте выполнения устройство детектирования выбирают на основе корпуса ПЦР, который используют для детектирования определенных бактерий/устойчивостей. Некоторые способы детектирования обычно относятся к определенным бактериям/устойчивостям, которые требуется детектировать, и вместе с ними также используются праймеры, которые применяют в способе детектирования. В результате, корпус ПЦР с праймерами и устройством детектирования можно выбирать как пару, то есть при выборе корпуса ПЦР также можно выбирать устройство детектирования.
При этом возможно, чтобы только конкретная часть устройства детектирования, такая как подложка и/или держатель подложки, могла быть специфичной для детектирования определенной ДНК/РНК. В связи с этим рассматривается вариант, в котором специфичное для варианта применения устройство детектирования может представлять собой только часть фактической системы детектирования, используемой в картридже для обеспечения возможности детектирования конкретной ДНК/РНК.
В варианте выполнения изобретения одна из одной или больше частей, специфичных для варианта применения, представляет собой устройство ввода образца. В зависимости от количества требуемого образца, типа образца, состояния, в котором он предоставляется, могут использоваться разные устройства ввода образца для ввода образца в картридж. Использование устройства ввода образца дополнительно обеспечивает простое и надежное соединение с картриджем и, в результате, простой и надежный ввод образца в картридж.
В варианте выполнения устройство ввода образца представляет собой устройство обработки до лизиса, выполненное с возможностью приготовления образца в определенном состоянии. Общая часть картриджа разработана так, чтобы образец можно было обрабатывать в определенном состоянии образца, например жидком. Устройство обработки до лизиса может быть предусмотрено для обработки образца из конкретного состояния, в котором он доступен и в котором его нельзя использовать в картридже, в состояние, в котором картридж конструктивно может его обрабатывать. Такое состояние может представлять собой состояние, для которого требуется высушить жидкость, присутствующую в твердом носителе, и тому подобное. Обработка до лизиса может выполняться до того, как устройство обработки до лизиса будет соединено с общей частью, но также и после такого соединения.
В варианте выполнения, по меньшей мере, одна в одной или более специфичных для варианта применения частей предусмотрено устройство идентификации. Для исключения ошибок при выборе частей, специфичных для варианта применения, полезно обеспечить идентификацию специфичных для применения частей, что позволяет легко проверять, была ли правильная, специфичная для применения часть или множество частей соединена с общей частью.
Такое устройство идентификации может включать в себя наклейки, штрих-коды, цветовые коды, магнитные коды и тому подобное. Предпочтительно, используется система автоматической идентификации, такая как система идентификации радиочастотных меток. Такие более усовершенствованные устройства идентификации также можно использовать для отслеживания истории места расположения общей части и/или специфичных для применения частей. Например, может быть важно охладить определенную, специфичную для применения часть. При использовании системы отслеживания истории местоположения можно проверять, не находилась ли специфичная для применения часть слишком длительное время вне устройства охлаждения. В предпочтительном варианте выполнения модуль управления системы детектирования проверяет, были ли правильные специфичные для применения части соединены с общей частью и выполняют ли все еще общая часть и специфичные для применения части все требования, относящиеся к истории места расположения и тому подобное.
В настоящем изобретении обычно исключается или сводится к минимуму ручная работа, предотвращается взаимное загрязнение, обеспечивается более быстрое получение результатов, которые являются более надежными, устройство является удобным для пользователя, и его можно легко адаптировать для анализа разных целевых последовательностей. Настоящее изобретение обеспечивает высокопроизводительный способ анализа присутствия, отсутствия или количества ДНК или РНК в образце любого типа, предпочтительно, в крови.
Настоящее изобретение направлено на картридж, который пригоден для детектирования присутствия, отсутствия или количества ДНК и/или РНК. Детектирование присутствия, отсутствия или количества ДНК и/или РНК представляет собой показатель, например, присутствия, отсутствия или количества гена, аллели гена, генетического признака или генетического нарушения, полиморфизма, полиморфизма одиночного нуклеотида (ПОН, SNP) или присутствия экзогенных ДНК или РНК в организме, то есть присутствия, отсутствия или количества патогенов или бактерий в организмах.
С помощью настоящего изобретения могут быть разработаны соответствующие лечебные средства для приготовления медикаментов, предназначенных для лечения диагностированного таким образом заболевания. Например, детектирование в образце (например, крови) организма (например, человека) патогенов (например, вирусов), можно, таким образом, привести к диагнозу и к соответствующему лечению (например, антибиотиком).
Картридж может быть картриджем сменного типа, который может быть установлен в устройство многократного использования. Такой картридж может быть однократным, пригодным для переработки или повторного использования, возможно, после очистки. Благодаря предоставлению сменного картриджа, все части, которые могут входить в контакт с образцом, можно после процесса детектирования извлекать из устройства, и картридж можно заменять на другой картридж или очищенный картридж перед следующим использованием. В других вариантах выполнения картридж может составлять единую деталь с устройством многократного использования, которое очищают после каждого использования.
В некоторых вариантах выполнения устройство содержит модуль управления, предназначенный для управления средством изоляции, средством амплификации и/или средством детектирования. Модуль управления делает возможным автоматическое управление изоляцией ДНК, амплификацией ДНК и детектированием амплифицированной ДНК.
Картридж содержит одну или более камер, в которых содержится образец во время процесса детектирования. Такие камеры могут содержать камеру ввода, предназначенную для ввода образца в картридж, камеру лизиса, предназначенную для лизиса клеток в образце, камеру промывки, предназначенную для промывки одной или более камер термоциклирования для амплификации ДНК, и камеру детектирования, которая обеспечивает возможность детектирования. Также можно обеспечить одну камеру для одной или больше функций, описанных в отношении этих камер. В таком варианте выполнения две или больше камеры из камеры ввода, камеры лизиса, камеры промывки, камеры (камер) термоциклирования и камеры детектирования могут быть скомбинированы в одну единственную камеру.
Во время разных этапов процесса детектирования образец размещают в соответствующей камере. С этой целью, образец переносят из одной камеры в другую камеру между двумя этапами обработки. Для обеспечения возможности такого переноса каждая камера, по меньшей мере, соединена с другой камерой с помощью канала для жидкости. По меньшей мере, в одном, но предпочтительно, в каждом из этих каналов для жидкости может быть предусмотрено средство клапана, и это средство клапана, предпочтительно, обычно закрывает канал для жидкости, но открывает канал для жидкости после активации средства клапана, приводя, в результате, две соответствующие камеры в стояние сообщения по жидкости. Средство клапана может быть разработано как односторонний клапан.
В определенных вариантах выполнения средство клапана может быть активировано устройством привода клапана. Такое устройство привода клапана, предпочтительно, установлено в устройстве для многократного использования.
В определенных вариантах выполнения предусмотрено средство насоса, предназначенное для перекачки образца или какой-либо другой жидкости, используемой для процесса детектирования, такой как буфер лизиса, реагенты, буферы промывки и разделения, буферы предварительной амплификации, из одной камеры в другую камеру. Такое средство насоса может быть активировано с помощью средства привода насоса, которое предпочтительно установлено в устройстве, предназначенном для многократного использования.
В определенных вариантах выполнения система содержит средство, предназначенное для сбора данных и/или средство для обработки данных. Это средство предназначено для использования при анализе детектируемой ДНК и/или для интерпретации результатов. В частности, в определенных вариантах выполнения средство обработки данных выполнено с возможностью связывания присутствия, отсутствия или количества целевой нуклеиновой кислоты (или их комбинации) с определенным диагнозом. Такое средство обработки данных может быть выполнено, например, в форме компьютера в комбинации с базой данных.
В определенных вариантах выполнения система также может содержать средство ввода одного или больше образцов. Такое средство ввода образца может содержать любое соответствующее устройство, такое как устройство удержания или стыковочное устройство, предназначенное для ввода образца из шприца или пипетки, или тому подобное, и может, например, содержать односторонний входной клапан, перегородку, фильтры и переток.
В определенных вариантах выполнения система также может содержать устройство лизиса. В устройстве лизиса, которое может находиться под управлением модуля управления, образец обрабатывают для получения каких-либо нуклеиновых кислот, находящихся в образце, в форме, в которой они могут быть изолированы от образца. Этап лизиса обычно включает в себя лизис клеток, в результате которого мембраны клетки и/или ядра клетки разрываются для высвобождения в результате содержащихся в них нуклеиновых кислот. При этом можно использовать средство физической или механической манипуляции для этапа лизиса, но также можно использовать и химическое средство для лизиса клеток в образце, такое как буфер лизиса. Средство смешивания может быть предусмотрено для смешивания образца и буфера лизиса. Способы лизиса клеток хорошо известны в данной области техники из учебников и т.д. В случае необходимости, такие способы могут быть адаптированы для использования в настоящей системе. Любые отходы, формируемые на этапе лизиса, могут быть сброшены, например, в устройство для отходов.
В определенных вариантах выполнения устройство ввода образца и устройство лизиса могут быть скомбинированы.
В определенных вариантах выполнения система также может содержать устройство обогащения, в случае необходимости, работающее под управлением модуля управления. Устройство обогащения позволяет изолировать ДНК из образца, подвергавшегося лизису. С этой целью устройство обогащения может быть оборудовано средством изоляции ДНК, таким как магнитные частицы. В данном варианте выполнения, ДНК или РНК в соответствии с настоящим изобретением абсорбируются на магнитных частицах. Абсорбированный материал нуклеиновой кислоты может подвергаться одному или больше этапам промывки, дренажа и/или очистки для удаления какого-либо нежелательного материала, такого как остатки биологического материала, содержащегося в образце, и других компонентов образца, которые не являются ДНК и/или РНК. Когда будет достигнута требуемая степень чистоты абсорбированной ДНК или РНК, они могут быть десорбированы или элюированы из магнитных частиц. Устройство обогащения также может быть оборудовано средством физической или механической манипуляции с жидкостями для смешения, разделения и изоляции ДНК или РНК.
В определенных вариантах выполнения система также может содержать реагенты, необходимые для этапа обогащения, то есть изоляции ДНК или РНК, такие как буферы, промывочные жидкости, воду, фильтры, магнитные шарики и т.д.
В определенных вариантах выполнения система также может содержать устройство для отходов, предназначенное для размещения в нем каких-либо отходов, образующихся на этапе обогащения, таких как использованные буферы, промывочные жидкости и т.п.
В определенных вариантах выполнения разные устройства для отходов системы могут быть выполнены отдельными для каждого разного назначения или объема. В определенных вариантах выполнения два или больше из описанных здесь устройств для отходов могут быть скомбинированы для размещения в них всех отходов, образующихся в результате применения способа в соответствии с настоящим изобретением.
В определенных вариантах выполнения система дополнительно содержит устройство предварительной амплификации, в случае необходимости находящееся под управлением модуля управления. Устройство предварительной амплификации можно использовать, например, для увеличения общего количества анализируемой ДНК или РНК. Обработка ДНК или РНК, полученных на этапе изоляции, выполняемая на этапе предварительной амплификации, позволяет увеличить общее количество ДНК. Это является предпочтительным, в частности, в случае сложного анализа, в котором выполняют множество тестов с изолированной ДНК, например для детектирования одновременного присутствия, отсутствия или количества множества патогенов в одном образце. Соответствующая технология доступна в данной области техники и предназначена для увеличения количества ДНК и, в общем, известна как амплификация целого генома.
В устройстве предварительной амплификации изолированная и очищенная ДНК или РНК могут быть предварительно обработаны с использованием, помимо прочего, буфера предварительной амплификации и, в случае амплификации целого генома, с ферментами и ДНТФ (DNTP). Устройство предварительной амплификации может быть соединено с устройством для отходов, для отправки материалов в отходы.
В определенных вариантах выполнения устройство предварительной амплификации также можно использовать для выполнения определенных оценок при детектировании специфичных нуклеиновых кислот. Их примеры представляют собой технологии, аналогичные OLA-PCR, такие как предоставляемые Applera (SNPplex), Keygene (SNPWave) и MRC-Holland (MPLA).
В определенных вариантах выполнения система содержит устройство амплификации. Устройство амплификации может находиться под управлением модуля управления. Изолированную ДНК, в случае необходимости, предварительно обработанную, как описано здесь, в других местах, подвергают в устройстве амплификации обработке амплификации, выполняемой в устройстве амплификации. Обработка амплификации содержит ввод изолированной ДНК в контакт с набором праймеров ПЦР, которые являются специфичными для целевой нуклеиновой кислоты, ферментов ПЦР, таких как один или больше полимераз и дНТФ.
В определенных вариантах выполнения устройство амплификации содержит множество камер. Множество камер обеспечивает возможность изолировать предварительно амплифицированную ДНК или РНК, которые будут разделены на части и распределены между камерами. В каждой камере может выполняться этап амплификации с использованием разных наборов праймеров. Таким образом, обеспечивается множественный анализ в этом одном образце, который может выполняться на присутствие, отсутствие или количество разных целевых нуклеиновых кислот. В случае множественного анализа набор праймеров для каждой целевой нуклеиновой кислоты может быть снабжен детектируемыми, отличающимися друг от друга метками, то есть метками с разным флуоресцентным спектром.
В определенных вариантах выполнения система также может содержать реактивы для амплификации изолированной ДНК, такой как ферменты, дНТФ и т.д.
В определенных вариантах выполнения система также может содержать устройство детектирования. Устройство детектирования может находиться под управлением модуля управления. Устройство детектирования выполнено с возможностью детектирования одной из амплифицированных ДНК или РНК и, предпочтительно, для детектирования меток, внедренных в продукты амплификации.
Устройство детектирования может проводить детектирование на основе метки, длины, мобильности, последовательности нуклеотидов, массы или их комбинации. В определенных вариантах выполнения устройство детектирования может детектировать на основе оптических, электрохимических, магнитных свойств или свойств мобильности (гель-электрофорез). В принципе, можно использовать любое соответствующее устройство детектирования, известное из предшествующего уровня техники.
В определенных вариантах выполнения система также содержит устройство сбора данных, предназначенное для сбора данных, полученных из устройства детектирования.
В определенных вариантах выполнения система также содержит устройство обработки данных, предназначенное для обработки данных.
В одном аспекте настоящего изобретения предусмотрен способ детектирования присутствия, отсутствия и/или количества целевой последовательности нуклеотидов в образце, содержащем одну или больше последовательностей нуклеиновой кислоты, в котором способ содержит следующие этапы:
- получают образец из организма;
- выполняют этапы изоляции последовательностей нуклеиновых кислот из образца;
- выполняют этапы амплификации (части) последовательности нуклеиновых кислот, для получения, в результате, ампликонов;
- детектируют присутствие, отсутствие и/или количество ампликонов, соответствующих целевой последовательности нуклеотидов среди последовательностей нуклеиновых кислот в образце.
В определенных вариантах выполнения способ выполняют в картридже, как определено в настоящем варианте применения.
В определенных вариантах выполнения целевая последовательность нуклеотидов может быть выбрана из группы, состоящей из ДНК, геномной ДНК, РНК, мРНК, кДНК, трансгенной ДНК и т.д.
В определенных вариантах выполнения организм представляет собой организм человека, животного, которое не является человеком, микроорганизм или растение.
В определенных вариантах выполнения образец представляет собой ткань, телесные жидкости, такие как слюна, сперма, кровь, моча и/или кал.
В определенных вариантах выполнения целевая нуклеотидная последовательность представляет собой экзогенную последовательность.
В определенных вариантах выполнения целевая нуклеотидная последовательность является патогенной.
В определенных вариантах выполнения образец, содержащий последовательности нуклеиновой кислоты, подвергают лизису для высвобождения содержащихся в нем последовательностей нуклеиновых кислот. В определенных вариантах выполнения образец, подвергавшийся лизису, подвергают последовательности этапов промывки и сбора, как хорошо известно в данной области техники и описано в стандартных учебниках, с целью изоляции нуклеиновых кислот из образца. Эти этапы могут выполняться на одном этапе или в ходе последовательности множества этапов. После изоляции нуклеиновых кислот из образца нуклеиновые кислоты могут подвергаться реакции амплификации, с использованием праймеров, которые можно выбирать для детектирования целевой нуклеиновой кислоты.
В способах амплификации нуклеиновой кислоты обычно используют два праймера, дНТФ и (ДНК) полимеразу. Предпочтительный способ амплификации представляет собой ПЦР. "ПЦР" или "полимеразная цепная реакция" представляет собой быструю процедуру для ферментной амплификации in vitro специфичного сегмента ДНК. ДНК, подвергаемую амплификации, денатурируют путем нагрева образца. В присутствии полимеразы ДНК и при избытке дезоксинуклеотидтрифосфатов, олигонуклеотидов, которые специфично гибридизируются на целевой последовательности, инициируют синтез новой ДНК. В результате одного цикла синтеза получают новые цепи заданной длины, которые аналогично родительским цепям могут гибридизироваться с праймерами после денатурации и отжига. После второго цикла денатурации, отжига и синтеза получают два одноцепочечных продукта, которые вместе составляют отдельный двуцепочечный продукт, имеющий точную длину между концами праймера. Этот отдельный продукт накапливается экспоненциально с каждым последовательным циклом амплификации. После определенного курса, состоящего из приблизительно 20-30 циклов, можно получить многомиллионную амплификацию дискретного фрагмента. Протоколы ПЦР хорошо известны в данной области техники и описаны в стандартных лабораторных учебниках, например, в публикации Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, Inc. (1995). Другие способы многократной и/или изотермальной амплификации могут применяться, которые включают в себя, например, LCR, самоподдерживающуюся репликацию последовательности (3SR), амплификацию РНК посредством Q-P-репликазы, амплификацию по типу катящегося кольца (АКК, RCA) или амплификация со смещением цепи (АСЦ, SDA).
Детектирование меченых ампликонов выполняют с помощью детектора для получения данных детектирования. Детектор, конечно, зависит от общей системы, с которой выполняется дискриминация между ампликонами целевых последовательностей, но также зависит от метки, присутствующей на праймере, такой как флуоресцентная или фосфоресцентная метка. Для различения разных целевых последовательностей в образце, предпочтительно, используют различие в спектре флюоресценции соответствующих ампликонов. В определенных вариантах выполнения, по меньшей мере, один из праймеров содержит метку, предпочтительно, прямой праймер содержит метку. Метку можно выбирать из большой группы, содержащей помимо прочего флуоресцентные и/или фосфоресцентные компоненты, таких как красители, хромофоры или ферменты, антигены, тяжелые металлы, магнитные зонды, фосфоресцентные компоненты, радиоактивные метки, хемилюминесцентные компоненты или компоненты электрохимического детектирования. В определенных вариантах выполнения метка представляет собой флуоресцентный или фосфоресцентный пигмент. Примеры таких пигментов представляют собой FAM, HEX, TET, JOE, NED и (ET-)ROX. Пигменты, такие как FITC, Cy2, Техас Red, TAMRA, Alexa fluor 488TM, BodipyFL, Rhodamine 123, R6G, Bodipy 530, AlexafluorTM532.
В результате использования разных наборов праймеров, каждый из которых содержит разные метки, количество целевых последовательностей, которые можно различать в образце и, следовательно, количестве целевых последовательностей в образце, которые можно детектировать, можно увеличить, используя дополнительные метки. Максимальное количество меток, которое можно использовать в одном образце в множественном способе, определяется, в основном, ограничениями способностей детектирования доступных платформ детектирования.
В определенных вариантах выполнения амплификацию выполняют, используя полимеразную цепную реакцию, по меньшей мере, с одним прямым и, по меньшей мере, одним обратным праймером, которые являются избирательными по отношению к целевой последовательности, а не по отношению к каким-либо другим последовательностям в образце.
В определенных вариантах выполнения, по меньшей мере, один из либо прямого, или обратного праймера метят.
В определенных вариантах выполнения перед этапом амплификации или вместо него используется анализ для детектирования нуклеиновых кислот в образцах.
В определенных вариантах выполнения ампликоны детектируют на основе метки, длины, мобильности, последовательности нуклеотидов, массы или их комбинации.
В определенных вариантах выполнения ампликоны детектируют на основе оптического, электрохимического или магнитного детектирования.
На Фиг. 1 показан вид в перспективе системы в соответствии с вариантом выполнения изобретения;
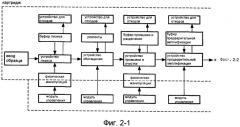
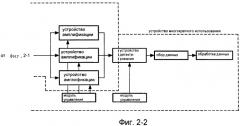
на Фиг. 2 показана блок-схема архитектуры варианта выполнения системы в соответствии с изобретением;
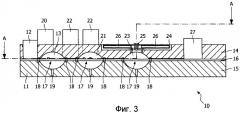
на Фиг. 3 схематично показан вид в разрезе (B-B на Фиг. 4) варианта выполнения картриджа в соответствии с настоящим изобретением; и
на Фиг. 4 схематично показан вид сверху/в разрезе (А-А на Фиг. 3) варианта выполнения по Фиг. 3.
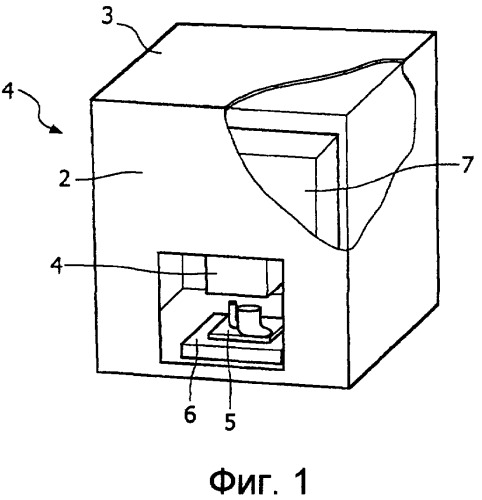
На Фиг. 1 показан вариант выполнения системы, предназначенной для детектирования присутствия, отсутствия и/или количества целевой последовательности нуклеотидов в образце, содержащем одну или больше последовательностей нуклеиновых кислот, в общем, обозначенной ссылочной позицией 1. Система содержит устройство 2 многократного использования с корпусом 3 (частично показан в разрезе).
В устройстве 2 предусмотрена полость 4. Сменный картридж 5 установлен с возможностью его изъятия в этой полости 4. Картридж 5 может быть картриджем, пригодным для повторного использования, переработки, или картриджем однократного использования.
Для обеспечения возможности детектирования картридж 5 содержит средство ввода, предназначенное для ввода образца, средство изоляции, предназначенное для изоляции ДНК, средство амплификации, предназначенное для амплификации ДНК, и средство детектирования, предназначенное для детектирования амплифицированной ДНК. Средство ввода, средство изоляции, средство амплификации и/или средство детектирования могут быть расположены на картридже и/или в устройстве, предназначенном для многократного использования. Обычно предпочтительно располагать в устройстве 2 все части системы 1, которые обычно не входят в контакт с образцом. Образец удерживают в ходе процесса детектирования в картридже, который работает как картридж.
Ниже описан предпочтительный вариант выполнения компоновки средства ввода, средства изоляции, средства амплификации и/или средства детектирования. Однако также возможны другие варианты выполнения.
Устройство 2 содержит модуль 7 управления, предназначенный для автоматического управления различными этапами процесса детектирования, как будет описано ниже.
Кроме того, устройство 2 содержит одно или больше устройств привода, предназначенных для привода различных элементов, расположенных на картридже. Эти устройства привода могут содержать одно или больше устройств привода средств насоса, предназначенных для привода одного или больше средств насоса для перекачки жидкости, одного или больше устройств привода клапана, предназначенных для привода одного или больше клапанов, расположенных в канале для жидкости в картридже, и другие устройства привода, такие как устройства механического привода, предназначенные для обеспечения, например, вращательного или поступательного движения одной или больше частей картриджа.
В устройстве предусмотрено устройство детектирования, которое может детектировать присутствие, отсутствие и/или количество ДНК. С этой целью, ДНК может быть помещена в камеру детектирования, которая размещена на картридже. Устройство детектирования может работать на основе оптического, электрохимического или магнитного принципа, как известно из предшествующего уровня техники. Может применяться любой другой соответствующий способ детектирования.
Устройство может дополнительно содержать устройство сбора данных и устройство обработки данных, предназначенное для сбора данных, полученных из устройства детектирования, и для соответствующей обработки этих данных.
Устройство 2 содержит носитель 6, предназначенный для поддержки картриджа 5. Носитель 6 выполнен с возможностью движения в вертикальном направлении между нижним положением (в котором носитель показан) и верхним положением. В нижнем положении картридж 5 может быть помещен на носитель 6 или может быть удален с него. Верхнее положение представляет собой рабочее положение, в котором картридж 5 устанавливается во время процесса детектирования. В этом верхнем положении картридж зажимается между носителем 6 и множеством устройств, расположенных на картридже, таких как средство насоса, клапаны, механическое средство и камера детектирования, может взаимодействовать с соответствующими устройствами, расположенными в устройст