Способ получения абакавира
Иллюстрации
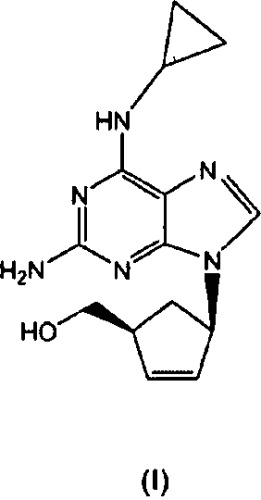
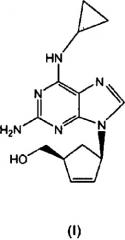
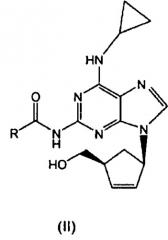
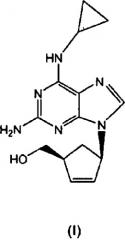
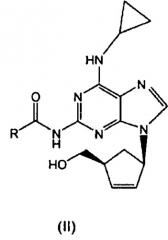
Показать всеИзобретение относится к улучшенному способу получения абакавира формулы (I) или его фармацевтически приемлемой соли, включающему взаимодействие соединения формулы (II),
где R представляет собой Н или (С1-С4)-алкильный радикал с неорганическим основанием, таким как гидроксид щелочного металла в смеси (С1-С6)-спирта и воды; и выделение абакавира формулы (I) в виде свободного основания или в виде фармацевтически приемлемой соли путем обработки указанного свободного основания соответствующей кислотой. Способ позволяет обеспечить высокую степень превращения без рацемизации, минимизировать образование примесей и значительно уменьшить время реакции. 18 з.п. ф-лы.
Реферат
Изобретение относится к способу получения активного фармацевтического ингредиента, известного как абакавир. Способ основан на удалении защитной группы N-2-ацилабакавира с использованием определенных основных условий.
Уровень техники
Абакавир - международное непатентуемое название (INN) {(1S,4R)-4-[2-амино-6-(циклопропиламино)-9H-пурин-9-ил]циклопент-2-енил}метанола, CAS №136470-78-5. Абакавира сульфат представляет собой активный селективный ингибитор ВИЧ-1 и ВИЧ-2 и может быть использован для лечения инфекции вирусом иммунодефицита человека (ВИЧ).
Структура гемисульфатной соли абакавира соответствует формуле (I):
EP 434450-A раскрывает некоторые 9-замещенные 2-аминопурины, включая абакавир и его соли, способы их получения и фармацевтические композиции, использующие данные соединения.
В данной области известны различные способы получения абакавира. В некоторых из них абакавир получают, исходя из подходящего пиримидинового соединения, конденсируя его с сахароподобным остатком с последующей циклизацией с образованием имидазольного кольца и в завершении вводя циклопропиламиногруппу в положение 6 пуринового кольца.
Пиримидиновые соединения, для которых установлено, что они пригодны в качестве интермедиатов указанных способов получения, включают интермедиаты N-2-ацилированного абакавира, такие как N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}ацетамид или N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамид. Удаление аминозащитной группы данных соединений с использованием кислых условий известно в данной области. Согласно примеру 28 EP 434450-A аминозащитную группу N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамида удаляют перемешиванием с 1Н хлороводородной кислотой в течение 2 дней при комнатной температуре. Основание абакавира после доведения pH до 7,0 и выпаривания растворителя, в конечном счете, выделяют тритурацией и хроматографированием. Затем реакцией с кислотой его превращают в соответствующую соль абакавира. Основными недостатками данного способа являются: (i) применение в значительной степени вызывающей коррозию минеральной кислоты для удаления аминозащитной группы; (ii) необходимость сильной степени разведения; (iii) длительное время реагирования, необходимое для завершения реакции; (iv) необходимость выделения свободного абакавира; и (v) сложный способ хроматографической очистки.
Таким образом, несмотря на предложение, изложенное в приведенном документе уровня техники, исследование новых способов удаления защиты N-ацилированного {(1S,4R)-4-[2-амино-6-(циклопропиламино)-9H-пурин-9-ил]циклопент-2-енил}метанола все еще представляет собой важную область, поскольку промышленное применение известного способа затруднительно, на что указано выше. Таким образом, в настоящем изобретении описан новый способ удаления аминозащитной группы N-ацилированного {(1S,4R)-4-[2-амино-6-(циклопропиламино)-9H-пурин-9-ил]циклопент-2-енил}метанола.
Сущность изобретения
Авторы изобретения обнаружили, что удаление аминозащитной группы N-2-ацилированного {(1S,4R)-4-[2-амино-6-(циклопропиламино)-9H-пурин-9-ил]циклопент-2-енил}метанола с использованием основания в смеси воды и спирта протекает очень быстро, и продукт может быть получен с высоким выходом и с высокой чистотой, поскольку не происходит значительного образования побочных продуктов по сравнению со способом, известным в данной области.
Таким образом, настоящее изобретение относится к созданию способа получения абакавира формулы (I) или его фармацевтически приемлемых солей или их сольватов, включающего в себя взаимодействие соединения формулы (II) с неорганическим основанием в смеси (C1-C6)-спирта и воды, где R представляет собой H или (C1-C4)-алкильный радикал.
Среди обеспечивающих наибольшее преимущество признаков способа настоящего изобретения могут быть упомянуты следующие: (i) гидролиз, проводимый в указанных основных условиях, более эффективен; (ii) требуется меньшее время реакции, поскольку условия реакции способа по изобретению позволяют осуществлять гидролиз при более высоких температурах; (iii) меньшее образование примесей; в условиях реакции настоящего изобретения гидролиз имеет место с низким образованием побочных продуктов даже при высоких температурах, напротив, при использовании кислых условий наблюдается быстрое разложение продукта при нагревании; (iv) реакционные объемы оптимизированы с учетом того, что гидролиз может быть проведен при высоких концентрациях; (v) реакция протекает без рацемизации; (vi) абакавир или его соли легко выделять и очищать и (vii) получают высокие выходы.
Подробное описание изобретения
Как описано выше, абакавир может быть получен гидролизом в основных условиях из соединения формулы (II) с использованием неорганического основания. В предпочтительных вариантах осуществления соединения формулы (II) представляют собой соединения, где R представляет собой H, метил или изопропил. В более предпочтительном варианте осуществления соединение формулы (II) представляет собой N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамид (соединение формулы (II), где R=изопропил).
Предпочтительно основание представляет собой гидроксид щелочного металла, такой как гидроксид лития, натрия или калия. Наиболее предпочтительным гидроксидом щелочного металла является гидроксид натрия. Предпочтительно использование количества неорганического основания в диапазоне от 0,1 до 10 моль основания на моль исходного материала формулы (II). Более предпочтительно количество основания в диапазоне от 1 до 5 моль основания на моль исходного материала.
Гидролиз проводят в смеси воды и спирта, такого как этанол, н-пропанол, изопропанол, н-бутанол, изобутанол или трет-бутанол. Предпочтительно система растворителя представляет собой смесь изопропанола и воды. Обычно количество растворителя находится в диапазоне от 1 до 15 мл/г исходного материала. Предпочтительно - от 2 до 10 мл/г. Аналогично, количество воды обычно находится в диапазоне 1-15 мл/г исходного материала. Предпочтительно - от 1 до 10 мл/г.
Реакцию предпочтительно проводят при температуре в диапазоне от комнатной температуры до температуры кипения использованного растворителя. В предпочтительном варианте осуществления реакцию проводят при температуре в диапазоне от 50°C до температуры кипения смеси. Таким образом, это обеспечивает преимущество, поскольку неожиданно время реакции сильно уменьшается при данных температурах и при этом не наблюдается значительного образования побочных продуктов. В более предпочтительном варианте осуществления реакцию проводят при температуре кипения смеси.
Абакавир может быть выделен из реакционной среды в виде фармацевтически приемлемой соли, предпочтительно гемисульфатной соли, отделением водной фазы и осаждением соли абакавира из органической фазы добавлением подходящего количества соответствующей фармацевтически приемлемой соли. Необязательно, второй растворитель может быть добавлен перед отделением водной фазы. Примеры подходящих растворителей включают простые алифатические (C2-C8)-эфиры, такие как этиловый простой эфир, изопропиловый простой эфир, трет-бутилметиловый простой эфир, ди-н-бутиловый простой эфир или тетрагидрофуран, ароматические (C6-C8)-углеводороды, такие как толуол или ксилол, или хлорсодержащие растворители, такие как хлороформ или метиленхлорид. Необязательно, органическая фаза может быть промыта водным гидроксидом натрия или водным раствором другого неорганического основания перед добавлением фармацевтически приемлемой кислоты. Более высокие выходы могут быть получены, когда соль абакавира выделяют из растворителя в безводной среде. Например, вода может быть удалена азеотропной отгонкой или выпариванием досуха и затем добавлением подходящего растворителя, чтобы осадить соль абакавира.
Гемисульфатная соль {(1S,4R)-4-[2-амино-6-(циклопропиламино)-9H-пурин-9-ил]циклопент-2-енил}метанола представляет собой соль, образованную {(1S,4R)-4-[2-амино-6-(циклопропиламино)-9H-пурин-9-ил]циклопент-2-енил}метанолом и серной кислотой в стехиометрическом соотношении 2:1.
Альтернативно, абакавир может быть выделен из реакционной среды в виде свободного основания путем кристаллизации. Для проведения кристаллизации растворитель может быть заменен на другой. Подходящая система растворителя для кристаллизации представляет собой, например, (C2-C6)-спирты, такие как этанол, н-пропанол, изопропанол, н-бутанол, изобутанол или трет-бутанол, (C3-C9)-кетоны, такие как ацетон, метилизобутилкетон или метилэтилкетон, простые алифатические (C2-C8)-эфиры, такие как этиловый простой эфир, изопропиловый простой эфир, трет-бутилметиловый простой эфир, ди-н-бутиловый простой эфир или тетрагидрофуран, сложные (C2-C10)-эфиры, такие как этилацетат, ацетонитрил или смеси названных. Предпочтительные системы растворителей представляют собой ацетон, ацетонитрил, этилацетат, изопропанол или смеси изопропанола/трет-бутилметилового простого эфира. Необязательно, органическая фаза может быть промыта водным гидроксидом натрия или водным раствором другого неорганического основания перед кристаллизацией абакавира в виде свободного основания.
Абакавир также может быть выделен из реакционной среды в виде свободного основания, необязательно, добавлением растворителя, выбранного из простых алифатических (C2-C8)-эфиров и ароматических (C6-C8)-углеводородов, отделением водной фазы, необязательно, удалением оставшейся воды и кристаллизацией абакавира формулы (I) в виде свободного основания в подходящей системе растворителя. Предпочтительно система растворителя для кристаллизации выбрана из систем, упомянутых выше. Необязательно, органическая фаза может быть промыта водным гидроксидом натрия или водным раствором другого неорганического основания перед кристаллизацией абакавира в виде свободного основания.
Когда желательной является фармацевтически приемлемая соль, она может быть также получена из основания абакавира обработкой соответствующей кислотой. Предпочтительной солью является гемисульфатная соль абакавира.
Наиболее подходящие условия осуществления указанного способа изменяются в зависимости от параметров, принимаемых во внимание специалистом в данной области, таких как, например, концентрация реакционной смеси, температура, растворитель, использованный в ходе реакции и выделения продукта, и тому подобное. Они могут быть легко определены указанным специалистом в данной области с помощью идей, показанных в примерах, приведенных в данном описании.
В описании и формуле изобретения слово “включает” и варианты данного слова не подразумевают исключение других технических признаков, добавок, компонентов или стадий. Реферат данной заявки включен в нее посредством ссылки. Дополнительные задачи, преимущества и признаки изобретения будут очевидны специалистам в данной области при прочтении описания или будут очевидны при реализации на практике изобретения. Следующие примеры даны для иллюстрации и не подразумеваются в качестве ограничения настоящего изобретения.
Примеры
Пример 1: Получение абакавира гемисульфата
N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамид (6,56 г, 18,40 ммоль) суспендировали в смеси изопропанола (32,8 мл) и 10% раствора NaOH (36,1 мл, 92,0 ммоль). Смесь кипятили при температуре флегмы в течение 1 ч. Полученный раствор охлаждали до 20-25°C и добавляли трет-бутилметиловый простой эфир (32,8 мл). Слои разделяли и по каплям добавляли 96% H2SO4 (0,61 мл, 11,03 ммоль) к органическому слою. Данную смесь охлаждали до 0-5°C и полученную суспензию фильтровали. Твердый продукт высушивали в вакууме при 40°C. Получали абакавира гемисульфат (5,98 г, 97%) в виде белого порошка.
Пример 2: Получение абакавира гемисульфата
N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамид (6,56 г, 18,40 ммоль) суспендировали в смеси изопропанола (32,8 мл) и 10% раствора NaOH (36,1 мл, 92,0 ммоль). Смесь кипятили при температуре флегмы в течение 1 ч. Полученный раствор охлаждали до 20-25°C и добавляли толуол (32,8 мл). Слои разделяли и по каплям добавляли 96% H2SO4 (0,61 мл, 11,03 ммоль) к органическому слою. Данную смесь охлаждали до 0-5°C и полученную суспензию фильтровали. Твердый продукт высушивали в вакууме при 40°C. Получали абакавира гемисульфат (5,42 г, 88%) в виде белого порошка.
Пример 3: Получение абакавира гемисульфата
К раствору N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамида (1,0 г, 2,80 ммоль) в изопропаноле (10 мл) добавляли 10% раствор NaOH (5,5 мл, 14,03 ммоль). Смесь кипятили при температуре флегмы в течение 1 ч. Полученный раствор охлаждали до 20-25°C и водный слой отделяли. К органическому слою по каплям добавляли 96% H2SO4 (0,07 мл, 1,22 ммоль). Смесь концентрировали до половины объема и соли отфильтровывали. К полученному раствору по каплям добавляли 96% H2SO4 (0,07 мл, 1,22 ммоль) и охлаждали до 0-5°C. Твердый продукт фильтровали и высушивали в вакууме при 40°C. Получали абакавира гемисульфат (0,56 г, 60%) в виде белого порошка.
Пример 4: Получение абакавира гемисульфата
N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамид (5,0 г, 14,03 ммоль) суспендировали в смеси изопропанола (25 мл) и 10% раствора NaOH (27,5 мл, 70,1 ммоль). Смесь кипятили при температуре флегмы в течение 1 ч. Полученный раствор охлаждали до 20-25°C и водный раствор отбрасывали. Органический слой концентрировали досуха. Добавляли изопропанол (10 мл) и дополнительно дважды упаривали (концентрировали) досуха. К данному остатку добавляли изопропанол (25 мл) и соли отфильтровывали. К полученному раствору по каплям добавляли 96% H2SO4 (0,39 мл, 7,0 ммоль). Данную смесь охлаждали до 0-5°C и полученную суспензию фильтровали. Твердый продукт высушивали в вакууме при 40°C. Получали абакавира гемисульфат (3,7 г, 79%) в виде белого порошка.
Пример 5: Получение абакавира гемисульфата
Смесь N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамида (10 г, 28 ммоль), изопропанола (100 мл) и 10% раствора NaOH (16,8 мл, 42 ммоль) кипятили при температуре флегмы в течение 1 ч. Полученный раствор охлаждали до 20-25°C и промывали несколько раз 25% раствором NaOH (10 мл). Влажный органический слой нейтрализовали до pH 7,0-7,5 17% хлороводородной кислотой и концентрировали досуха в вакууме. Остаток растворяли в изопропаноле (100 мл) и соли отфильтровывали. К фильтрату по каплям добавляли 96% H2SO4 (0,78 мл, 14,0 ммоль). Данную смесь охлаждали до 0-5°C и осадок отфильтровывали и высушивали в вакууме при 40°C, получая 15,0 г (80%) абакавира гемисульфата в виде белого порошка.
Пример 6: Получение абакавира
N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамид (1,0 г, 2,80 ммоль) суспендировали в смеси изопропанола (2 мл) и 10% раствора NaOH (1,1 мл, 2,80 ммоль). Смесь кипятили при температуре флегмы в течение 1 ч. Полученный раствор охлаждали до 20-25°C и добавляли трет-бутилметиловый простой эфир (2 мл). Водный слой отбрасывали, органическую фазу охлаждали до 0-5°C и полученную суспензию фильтровали. Твердый продукт высушивали в вакууме при 40°C. Абакавир (0,62 г, 77%) получали в виде белого порошка.
Пример 7: Получение абакавира
N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамид (1,25 г, 3,51 ммоль) суспендировали в смеси изопропанола (2,5 мл) и 10% раствора NaOH (1,37 мл, 3,51 ммоль). Смесь кипятили при температуре флегмы в течение 1 ч и концентрировали досуха. Остаток кристаллизовали из ацетона. Абакавир (0,47 г, 47%) получали в виде белого порошка.
Пример 8: Получение абакавира
N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамид (1,25 г, 3,51 ммоль) суспендировали в смеси изопропанола (2,5 мл) и 10% раствора NaOH (1,37 мл, 3,51 ммоль). Смесь кипятили при температуре флегмы в течение 1 ч и концентрировали досуха. Остаток кристаллизовали из ацетонитрила. Абакавир (0,43 г, 43%) получали в виде белого порошка.
Пример 9: Получение абакавира
Смесь N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамида (10 г, 28 ммоль), изопропанола (100 мл) и 10% раствора NaOH (16,8 мл, 42 ммоль) кипятили при температуре флегмы в течение 1 ч. Полученный раствор охлаждали до 20-25°C и несколько раз промывали 25% раствором NaOH (10 мл). Влажный органический слой нейтрализовали до pH 7,0-7,5 17% хлороводородной кислотой и концентрировали в вакууме досуха. Остаток кристаллизовали из этилацетата (150 мл), получая абакавир (7,2 г, 90%).
Пример 10: Получение абакавира
Смесь N-{6-(циклопропиламино)-9-[(1R,4S)-4-(гидроксиметил)циклопент-2-енил]-9H-пурин-2-ил}изобутирамида (10 г, 28 ммоль), изопропанола (100 мл) и 10% раствора NaOH (16,8 мл, 42 ммоль) кипятили при температуре флегмы в течение 1 ч. Полученный раствор охлаждали до 20-25°C и несколько раз промывали 25% раствором NaOH (10 мл). Влажный органический слой нейтрализовали до pH 7,0-7,5 17% хлороводородной кислотой и концентрировали в вакууме досуха. Остаток кристаллизовали из ацетона (300 мл), получая абакавир (7,0 г, 88%).
1. Способ получения абакавира формулы (I) или его фармацевтически приемлемой соли, включающий (а) взаимодействие соединения формулы (II), где R представляет собой Н или (С1-С4)-алкильный радикал с неорганическим основанием, таким как гидроксид щелочного металла в смеси (С1-С6)-спирта и воды; и (b) выделение абакавира формулы (I) в виде свободного основания или в виде фармацевтически приемлемой соли путем: обработки указанного свободного основания соответствующей кислотой или обработки выделенного в виде свободного основания абакавира соответствующей кислотой.
2. Способ по п.1, где R в соединении формулы (II) представляет собой изопропил.
3. Способ по п.2, где гидроксид щелочного металла представляет собой гидроксид натрия.
4. Способ по п.3, где (С1-С6)спирт представляет собой изопропанол.
5. Способ по п.1, где реакцию проводят при температуре, включенной в диапазон от 50°С до температуры кипения смеси.
6. Способ по п.1, где абакавир (I) выделяют в виде соли, и способ выделения (b) включает в себя: (i) добавление растворителя, выбранного из группы, состоящей из алифатических простых (С2-С8)-эфиров, ароматических (С6-С8)-углеводородов и хлорсодержащих растворителей, таких как хлороформ или метиленхлорид; (ii) отделение водной фазы; (iii) проведение по меньшей мере одной промывки водным раствором неорганического основания, таким как гидроксид щелочного металла; (iv) удаление оставшейся воды; и (v) осаждение фармацевтически приемлемой соли из органической фазы добавлением соответствующей фармацевтически приемлемой кислоты.
7. Способ по п.6, где указанная соль абакавира (I) представляет собой гемисульфатную соль.
8. Способ по п.1, где абакавир формулы (I) выделяют в виде свободного основания, и способ выделения (b) включает в себя кристаллизацию абакавира (I) в виде свободного основания из подходящей системы растворителя, выбранного из группы, включающей (С2-С6)-спирты, (С3-С9)-кетоны, простые алифатические (C2-C8)-эфиры, сложные (С2-С10)-эфиры, ацетонитрил или их смеси; и, если необходимо, обработку полученного соединения фармацевтически приемлемой кислотой с образованием соответствующей соли.
9. Способ по п.8, где абакавир формулы (I) выделяют в виде свободного основания, и способ выделения (b) включает в себя кристаллизацию абакавира (I) в виде свободного основания из подходящей системы растворителя, выбранного из группы, включающей трет-бутилметиловый простой эфир, ацетон, ацетонитрил и этилацетат; и, если необходимо, обработку полученного соединения фармацевтически приемлемой кислотой с образованием соответствующей соли.
10. Способ по п.1, где абакавир (I) выделяют в виде свободного основания, и способ выделения (b) включает: (i) добавление растворителя, выбранного из группы, состоящей из алифатических простых (С2-С8)-эфиров и ароматических (С6-C8)-углеводородов; (ii) отделение водной фазы; (iii) проведение по меньшей мере одной промывки водным раствором неорганического основания; (iv) удаление оставшейся воды; и (v) кристаллизацию абакавира (I) в виде свободного основания из подходящей системы растворителя, выбранного из группы, включающей (С2-С6)-спирты, (С3-С9)-кетоны, простые алифатические (С2-С8)-эфиры, сложные (С2-С10)-эфиры, ацетонитрил или их смеси; и, если необходимо, обработку полученного на стадии (v) соединения фармацевтически приемлемой кислотой с образованием соответствующей соли.
11. Способ по п.8, где система растворителя для кристаллизации свободного основания абакавира выбрана из группы, состоящей из ацетона, ацетонитрила, этилацетата, изопропанола и смесей изопропанола/трет-бутилметилового простого эфира.
12. Способ по п.1, где основание представляет собой гидроксид натрия, a R в соединении формулы (II) представляет собой изопропил.
13. Способ по п.12, где абакавир (I) выделяют в виде соли, и способ (b) выделения включает в себя: (i) добавление растворителя, выбранного из группы, состоящей из алифатических простых (С2-С8)-эфиров, ароматических (С6-С8)-углеводородов и хлорсодержащих растворителей, выбранных из группы, включающей хлороформ и метиленхлорид; (ii) отделение водной фазы; (iii) проведение по меньшей мере одной промывки водным раствором неорганического основания; (iv) удаление оставшейся воды; и (v) осаждение фармацевтически приемлемой соли из органической фазы добавлением соответствующей фармацевтически приемлемой кислоты.
14. Способ по п.12, где абакавир формулы (I) выделяют в виде свободного основания, и способ выделения (b) включает кристаллизацию абакавира (I) в виде свободного основания из подходящей системы растворителя, выбранного из группы, включающей (С2-С6)-спирты, (С3-С9)-кетоны, простые алифатические (С2-С8)-эфиры, сложные (С2-С10)-эфиры, ацетонитрил или их смеси; и, если необходимо, обработку полученного соединения фармацевтически приемлемой кислотой с образованием соответствующей соли.
15. Способ по п.12, где абакавир (I) выделяют в виде свободного основания, и способ выделения (b) включает: (i) добавление растворителя, выбранного из группы, состоящей из алифатических простых (С2-С8)-эфиров, ароматических (С6-С8)-углеводородов; (ii) отделение водной фазы; (iii) проведение по меньшей мере одной промывки водным раствором неорганического основания; (iv) удаление оставшейся воды; и (v) кристаллизацию абакавира (I) в виде свободного основания из подходящей системы растворителя, выбранного из группы, включающей (С2-С6)-спирты, (С3-С9)-кетоны, простые алифатические (С2-С8)-эфиры, сложные (С2-С10)-эфиры, ацетонитрил или их смеси; и, если необходимо, обработку полученного соединения на стадии (v) фармацевтически приемлемой кислотой с образованием соответствующей соли.
16. Способ по п.10, где система растворителя для кристаллизации свободного основания абакавира выбрана из группы, состоящей из ацетона, ацетонитрила, этилацетата, изопропанола и смесей изопропанола/трет-бутилметилового простого эфира.
17. Способ по п.1, где основание представляет собой гидроксид натрия, R в соединении формулы (II) представляет собой изопропил, а (С1-С6)-спирт представляет собой изопропанол.
18. Способ по п.1, где абакавир (I) выделяют в виде соли и способ (b) выделения включает в себя: (i) добавление растворителя, выбранного из группы, состоящей из алифатических простых (С2-С8)-эфиров, ароматических (С6-С8)-углеводородов и хлорсодержащих растворителей, выбранных из группы, включающей хлороформ или метиленхлорид; (ii) отделение водной фазы; и (iii) осаждение фармацевтически приемлемой соли из органической фазы добавлением соответствующей фармацевтически приемлемой кислоты.
19. Способ по п.12, где абакавир (I) выделяют в виде соли, и способ (b) выделения включает в себя: (i) добавление растворителя, выбранного из группы, состоящей из алифатических простых (С2-С8)-эфиров, ароматических (С6-С8)-углеводородов и хлорсодержащих растворителей, выбранных из группы, включающей хлороформ или метиленхлорид; (ii) отделение водной фазы; и (iii) осаждение фармацевтически приемлемой соли из органической фазы добавлением соответствующей фармацевтически приемлемой кислоты.