Адсорбенты-катализаторы, полученные из бытовых и промышленных шламов, компоста и табачных отходов, и способ их получения
Иллюстрации
Показать всеГруппа изобретений относится к области получения и использования адсорбентов. Предложены адсорбенты, полученные из компоста, например, на основе табачных отходов и промышленных или бытовых шламов. Способ получения адсорбентов включает компостирование компостных материалов, термическую сушку обезвоженного шлама сточных вод с образованием гранулированного органического удобрения, смешивание удобрения с компостом и пиролиз смеси. В процессе пиролиза образуются новые минеральные фазы в результате протекания реакций в твердой фазе между компонентами шламов. Полученные адсорбенты могут быть использованы для удаления сероводорода при комнатной температуре в присутствии влаги. Состав используемых исходных веществ и высокая температура пиролиза смеси обеспечивают получение эффективных адсорбентов за счет усиления активации углеродной фазы и химической стабилизации неорганической фазы. 5 н. и 25 з.п. ф-лы, 30 ил., 26 табл.
Реферат
Настоящая заявка испрашивает приоритет согласно предварительной заявке на патент США №60/715788, поданной 8 сентября 2005 г., предварительной заявке на патент США №60/782593, поданной 14 марта 2006 г., и предварительной заявке на патент США №60/801545, поданной 17 мая 2006 г. Описания указанных заявок включены в настоящее изобретение во всей полноте посредством ссылок.
Область техники
Настоящее изобретение относится к получению адсорбентов-катализаторов, образующихся в результате пиролиза различных видов шламов, взятых в отдельности или в сочетании с компостными материалами. Указанные шламы включают бытовые и промышленные шламы, шламы отработанных масел и металлосодержащие шламы. Компостные материалы могут включать табачные отходы.
Уровень техники
Растущая озабоченность состоянием окружающей среды послужила толчком к созданию новых, экологически чистых технологий, новых материалов и новых путей сокращения и сведения к минимуму отходов. Одним из видов отходов, производимых современным обществом в огромном количестве, являются шламы бытовых сточных вод, часто называемые биологическими осадками. Биологические осадки представляют собой смесь отработанной биомассы, образующейся в ходе аэробного и анаэробного разложения органических компонентов бытовых сточных вод, наряду с неорганическими материалами, в частности песком и оксидами металлов. Другие примеры шламов включают промышленные отходы, например, судостроения, сталелитейного и целлюлозно-бумажного производства. По оценке, в Соединенных Штатах Америки образуется примерно 10 миллионов тонн шламов сточных вод в пересчете на сухое вещество. Более того, например, только Швеция производит 220000 тонн сухого шлама из общего количества 8-10 миллионов тонн сухого шлама, производимого странами Европейского Союза.
Для уничтожения или утилизации шламов бытовых сточных вод применяют различные способы, включая сжигание, вывоз на свалку, использование в дорожных покрытиях, переработку в удобрения, прессование с получением строительных блоков и карбонизацию. С 1976 года было выдано несколько патентов на карбонизацию шламов сточных вод и различные применения конечных продуктов. Карбонизация шлама в присутствии химических активирующих агентов, в частности хлорида цинка и серной кислоты, позволяет получать новые сорбенты, для которых запатентован ряд применений в таких процессах, как удаление органических веществ на конечных стадиях очистки воды и удаление хлорорганических соединений. Промышленные шламы после обезвоживания/сушки либо вывозят на свалку, либо в основном захоранивают как опасные отходы.
Как правило, карбонизацию шлама для удаления загрязняющих веществ из газообразной или жидкой фазы проводят с помощью различных видов активированного угля, благодаря тому, что активированный уголь обладает большой площадью поверхности и большим объемом пор. Однако часто эти характеристики активированного угля оказываются недостаточными для удержания некоторых молекул, в особенности небольших молекул, для которых дисперсионные взаимодействия с поверхностью угля являются достаточно слабыми. В таких случаях поверхность угля необходимо модифицировать, чтобы обеспечить возможность специфических взаимодействий. Такие взаимодействия включают водородное связывание, комплексообразование, кислотно-основные взаимодействия или окислительно-восстановительные процессы. К счастью, существуют различные технологии, позволяющие модифицировать поверхность угля, которые могут быть реализованы сравнительно легко. Примерами таких технологий являются окисление различными окислителями, в частности сильными кислотами, озоном или воздухом, импрегнирование каталитически активными металлами или соединениями, выступающими в качестве восстановителей/окислителей, термическая обработка в присутствии источников гетероатомов, в частности соединений хлора или азота, и другие.
Вышеуказанная обработка приводит к образованию на поверхности угля новых функциональных групп/химических группировок. Наличие таких групп обеспечивает специфические и/или химические взаимодействия с веществами, которые необходимо удалить. Важными факторами с точки зрения эффективности процесса удаления являются химическое состояние этих группировок и их распределения по поверхности. Другим важным аспектом является сохранение пористости угля, которая является определяющей для удерживания/накопления загрязняющих веществ. Поэтому модификацию поверхности следует проводить таким образом, чтобы обеспечить минимальное сокращение площади поверхности/пор.
С учетом вышеприведенных требований в некоторых случаях модификация поверхности угля представляет собой непростую задачу и, кроме того, может быть связана с большими затратами, в особенности если модификацию проводят с использованием благородных металлов или каталитически активных металлов. Шламы промышленных сточных вод, производимые, например, судостроительными предприятиями или предприятиями других отраслей промышленности, где используются тяжелые металлы, характеризуются высоким содержанием каталитически активных переходных металлов. При помощи пиролиза таких материалов можно не только сократить объем отходов, но также переработать эти экологически вредные отходы и превратить их в ценные продукты. После использования такие продукты можно вывозить на свалку без угрозы для окружающей среды, поскольку вымывание материалов в почву существенно уменьшается вследствие минерализации указанных металлов в результате протекания высокотемпературных реакций в твердой фазе.
Процесс карбонизации шламов сточных вод подробно изучен и описан в литературе. Площадь поверхности материалов, полученных в результате такой обработки, составляет от 100 до 500 м2/г. Сообщается, что способность таких материалов адсорбировать сероводород, диоксид серы, основные или кислотные красители, фенол или ртуть сопоставима или превышает соответствующие характеристики активированного угля. Во многих процессах превосходная поглощающая способность этих материалов связана с каталитическим действием металлов, присутствующих в различных формах в конечных продуктах. Сообщалось, что химическая форма указанных металлов и их расположение на поверхности являются важными факторами, определяющими способность удалять загрязнения. В некоторых случаях смешение отходов позволяло получить более эффективные адсорбенты за счет синергии компонентов.
Адсорбенты, полученные путем пиролиза шлама, можно рассматривать как псевдокомпозиционные материалы сложного состава. При этом процесс карбонизации твердых веществ биологического происхождения подробно исследован и описан в литературе. Недавно было показано, что простой пиролиз удобрения Terrene®, которое получают из шламов бытовых сточных вод, позволяет получать исключительно хорошие адсорбенты для удаления серосодержащих газов. Способность таких адсорбентов удалять загрязняющие вещества в два раза больше, чем у активированного угля, полученного из скорлупы кокосового ореха. Однако данный эффект объясняли наличием определенной комбинации неорганических оксидов таких металлов, как железо, медь, цинк или кальций. Преобладающее влияние неорганической фазы или комбинации оксидов, которые также достаточно часто используют в качестве катализаторов окисления сероводорода или адсорбции диоксида серы, исключили на основании исследования способности чистой неорганической фазы удалять серосодержащие газы. Указанная способность чистой неорганической фазы, нагретой до 950°С, была незначительной. Полученные данные также свидетельствовали о том, что окисление сероводорода происходит до тех пор, пока все микропоры (размер которых составляет в основном около 6 Å), вероятно, в углеродсодержащем осадке или на границе раздела уголь/оксид, не будут заполнены продуктами реакции. Вид такого углеродсодержащего осадка является важным, и этот осадок может оказывать влияние на поглощающую способность.
Продукты окисления, образующиеся на поверхности, удерживаются на ней. В таблице 1 приведена адсорбционная способность материалов, полученных из шламов сточных вод, по отношению к серосодержащим газам. Способность указанных материалов удалять токсичные газы, содержащие восстановленную серу, намного превышает аналогичную способность активированного угля, несмотря на низкое содержание углерода (примерно 20%) в указанных материалах и гораздо меньший объем пор.
Таблица 1. Емкость до проскока адсорбентов, полученных из шламов (серии SC), и активированного угля (S208) по отношению к H2S и SO2. Число, указанное после обозначения SC, обозначает температуру, при которой проводилась термообработка, в градусах Цельсия.
| Образец | Емкость до проскока H2S [мг/г] | Емкость до проскока SO2 [мг/г] |
| SC-400 | 8.2 | 5.1 |
| SC-600 | 14.9 | 9.5 |
| SC-800 | 23.6 | 22.2 |
| SC-950 | 82.6 | 29.8 |
| S208 | 48.8 | 48.2 |
Поскольку представляется, что фактором, ограничивающим поглощающую способность материалов, полученных из шламов сточных вод, является объем пор, то, по-видимому, дальнейшие исследования должны быть направлены на увеличение содержания углеродсодержащего осадка и объема пор при сохранении заданного содержания каталитически активной фазы. Последние исследования показали, что объем пор, задействованных в удалении таких соединений, как сероводород, может не совпадать с объемом пор, размер которых соответствует размеру молекулы адсорбента. Поскольку каталитическое окисление представляет собой превалирующий механизм протекания адсорбции, было установлено, что предпочтительными являются более крупные поры (мезо- и макропоры), в которых накапливается продукт окисления.
Другим важным фактором является химический состав каталитической фазы, ее дисперсность, расположение на поверхности, совместимость с угольной фазой и влияние обеих фаз на процесс удаления (адсорбция/каталитическое окисление/удерживание). Было установлено, что превосходная эффективность дорогостоящего катализатора десульфурации, US Filter carbon Midas®, связана с присутствием оксидов кальция и магния, диспергированных в микропористом активированном угле. На этом катализаторе происходит окисление сероводорода на основных центрах, образованных оксидами щелочноземельных металлов, с образованием серы. Тот факт, что такой уголь способен удерживать до 60 мас.% серы, связан с ограниченной реакционной способностью MgO и СаО. На поверхности указанных оксидов благодаря pH среды, лежащему в области основных значений, и наличию влаги образуется сера; вследствие непосредственной близости угольной фазы образующаяся сера мигрирует к адсорбционным центрам с высокой энергией, которыми являются мелкие поры. Таким образом, происходит обновление каталитических центров, и адсорбенты работают до тех пор, пока все мелкие поры не будут заполнены серой.
Было также установлено, что материалы на основе шламов сточных вод являются эффективными адсорбентами для удаления ртути и меди из сточных вод. Другими широко распространенными промышленными загрязняющими веществами, которые можно эффективно удалять с использованием указанных материалов, являются основные и кислотные красители. В случае таких адсорбатов высокая поглощающая способность связана с химической природой поверхности (кислотные и основные центры) и относительно большими порами, размер которых сопоставим с размером молекул органических красителей.
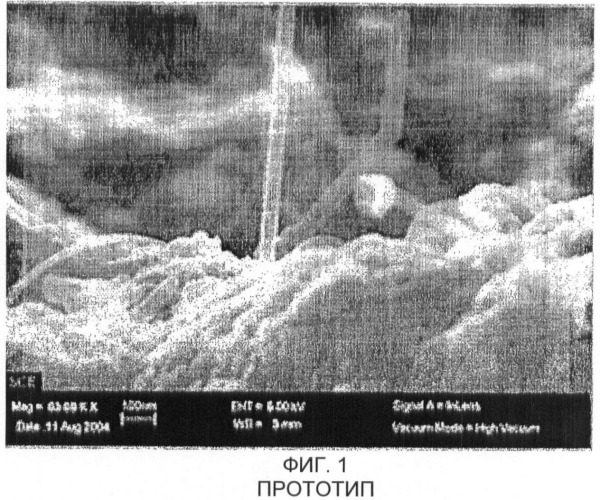
При высокой температуре органические вещества испаряются, происходит дегидрогенизация, и углерод может быть осажден обратно на поверхность неорганической подложки в виде углеродных нанотрубок или волокон. Это оказывается возможным благодаря присутствию высокодисперсных каталитически активных металлов. Поскольку данный процесс напоминает химическое парофазное осаждение (chemical vapor deposition, CVD), его называют самопроизвольным химическим парофазным осаждением (self-imposed chemical vapor deposition, SICVD). Способ выращивания углеродных нанотрубок на катализаторах, содержащих никель или кобальт, хорошо известен и описан в литературе. Нанотрубки и углеродные волокна выращивают на металлических «затравках», и их эффективный размер зависит от размеров затравок. Увеличение содержания углеродсодержащей фазы может приводить к увеличению пористости, что, в свою очередь, приводит к увеличению пространства для удерживания продуктов окисления, а также может приводить к образованию большего числа новых углеродных фрагментов в процессе парофазного осаждения. На фиг.1 представлено полученное методом сканирующей электронной микроскопии изображение углеродной нанотрубки, выращенной на поверхности материалов, полученных из шламов сточных вод.
Содержание в шламе углерода и азота оказывает влияние на формирование и свойства адсорбента. Шламы бытовых сточных вод являются перспективным материалом для применения в качестве основы наряду со шламами других сточных вод; тем не менее также могут использоваться и другие углерод- или азотсодержащие отходы. Кроме получения новых углеродных фрагментов в присутствии металлов-катализаторов с помощью термообработки можно получать новые активные компоненты, подобные шпинели/минералам. В последнее время в некоторых шламах сточных вод, содержащих железо и кальций, были идентифицированы каталитически важные фрагменты, такие как двухкальциевый феррит (Ca2Fe2O5).
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
Термин "адсорбция" относится к явлению, при котором на поверхности твердого тела происходит концентрирование молекул из газообразной или жидкой среды.
Термин "адсорбент" относится к материалу, который при определенных условиях способен адсорбировать газы или пары.
Термин "пиролиз" относится к термообработке (например, при температуре более 400°С) в инертной атмосфере материалов органического происхождения.
Термин "химическая активация" относится к обработке органических исходных материалов определенными химическими веществами в процессе пиролиза.
Термин "активированный уголь" относится к углеродсодержащему материалу, полученному путем пиролиза органических исходных материалов (например, угля, древесины, торфа и т.п.) при повышенной температуре с их последующей активацией с использованием различных физических или химических агентов (например, при температуре примерно от 600°С до 1000°С).
Термин "уголь, импрегнированный щелочью", относится к активированному углю, импрегнированному KOH и NaOH для повышения значения pH указанного угля и его поглощающей способности по отношению к кислотным газам.
Термин "емкость до проскока" относится к количеству вещества, которое адсорбировалось на поверхности сорбента до появления определенной концентрации этого вещества в потоке выходящего воздуха.
Термин "кислотные газы" относится к газам, которые способны превращаться в кислоты или способны взаимодействовать как кислоты (например, являются акцепторами электронов).
Термин "удельная площадь поверхности" относится к площади поверхности адсорбента, которую рассматривают в качестве области, где может происходить адсорбция различных молекул.
Термин "объем пор" относится к объему пор адсорбента, доступному согласно расчету для молекул азота при его температуре кипения.
Термин "окисление" относится к изменению химического состояния вещества, связанному с потерей электронов. При этом заряд частицы становится более положительным.
Термин "время пребывания" относится к среднему времени, которое требуется молекулам реагента для прохождения через реактор.
Термин "компостный материал" относится к отдельным материалам, которые подвергают компостированию.
Термины "компост" и "компостировать" относятся к смеси, состоящей по большей части из разлагающихся органических материалов, и к действию, направленному на превращение компостных материалов в компост соответственно.
Шламы отработанных масел и шламы, содержащие отработанные металлы (оба указанных вида шлама представляют собой отходы судостроения, однако, источником указанных шламов может быть любое предприятие тяжелой промышленности, где используют переходные металлы, в частности железо, цинк, медь, никель, хром), смешивали со шламами бытовых сточных вод в различных соотношениях, а затем подвергали пиролизу в атмосфере азота при 650°С и 950°С в течение двух различных периодов времени (полчаса и один час). Дополнительные образцы подвергали пиролизу в атмосфере азота при низкой температуре, например примерно 600°С, 625°С, 650°С, 675°С, 700°С или ниже, и при высокой температуре, например примерно 900°С, 925°С, 950°С, 975°С, 1000°С, 1100°С или выше. Используемый в настоящем описании термин "промышленный шлам" включает любой шлам, который не является шламом бытовых сточных вод. Указанный термин включает шламы, образующиеся при изготовлении или обработке исходных материалов, полуфабрикатов, готовых изделий или иных видах деятельности, которые содержат загрязняющие вещества из небытовых источников сточных вод. Шламы "городских" или "бытовых" сточных вод могут образовываться на предприятиях, обслуживающих население, и могут соответствовать требованиям "10 State Standards".
Комбинирование компоста/компостных материалов и шламов бытовых/промышленных сточных вод наряду с пиролизом указанных материалов в атмосфере азота могжет приводить к образованию новых адсорбентов. Новые адсорбенты могут содержать неорганическую фазу (от 70 до 95% и от 80 до 98%) и углеродсодержащую фазу (от 5 до 30% и от 10 до 30%). Неорганическая фаза может содержать высокодисперсные металлы-катализаторы, в частности железо, никель, медь, цинк, хром, а также оксиды кальция и магния, оксид алюминия, оксид кремния и т.п. Углеродсодержащая фаза может содержать соединения азота, в частности, содержащие аминогруппу или пиридиновую группу.
Вследствие синергии образуется смешанная керамическая/минералоподобная фаза. Эта фаза реагирует с газообразным азотом при повышенных температурах. Удельная площадь поверхности указанной фазы составляет от примерно 10 м2/г до примерно 200 м2/г. Так, например, удельная площадь поверхности может составлять примерно 10 м2/г, 20 м2/г, 30 м2/г, 40 м2/г, 50 м2/г, 60 м2/г, 70 м2/г, 80 м2/г, 90 м2/г, 100 м2/г, 110 м2/г, 120 м2/г, 130 м2/г, 140 м2/г, 150 м2/г, 160 м2/г, 170 м2/г, 180 м2/г, 190 м2/г, 200 м2/г или более. Удельный объем пор составляет примерно от 0.002 см3/г до примерно 0.074 м3/г. Так, например, удельный объем пор составляет примерно 0.002 см3/г, 0.005 м3/г, 0.015 м3/г, 0.025 м3/г, 0.035 м3/г, 0.045 м3/г, 0.055 м3/г, 0.065 м3/г, 0.074 м3/г или более. Важным аспектом данной текстуры является значительный объем мезопор, достигающий примерно 0.8 см3/г. Значение pH всех материалов находится в основной области, например, pH более 9. Указанные материалы способны адсорбировать примерно до 10, 15, 20, 25 или 30 мас.% сероводорода, главным образом в виде элементарной серы.
Обнаруженные реакции в твердой фазе приводят к образованию керамических/минералоподобных кристаллографических фаз. Было установлено, что при пиролизе шламов бытовых/промышленных сточных вод при 950°С могут образовываться соединения со структурой шпинели, такие как вюрцит (ZnS), ферроан (Са2(Mg, Fe)5(SiAl)8O22(OH)2), халькоцит (Cu1.96S), шпинель (MgAl2O4) и фероксигит (FeO(OH)). В материалах на основе маслосодержащих отходов кроме металлического железа присутствуют борнит (Cu5FeS4), гибонит (CaAl12O19), цинкит (ZnO) и анкерит (Ca(Fe, Мg)(СО3)2). В адсорбентах на основе металлосодержащих шламов содержатся алюминий, металлическое железо, медь, цинк, пироп (Mg3Al2(SiO4)3), пирротин (Fe7S8), халькопирит (CuFeS2), троилит (FeS) и ферсилицит (FeSi). Смешивание промышленных шламов с компостом или компостными материалами может приводить к синергическому усилению каталитических свойств, что может приводить к образованию новых соединений, в частности сапфирина (Mg3.5Al9Si1.5O20), магемита (Fe2O3), когенита (Fe3C), лавсонита (CaAl2Si2O7(OH)2H2O), смитсонита (ZnCO3), сфалерита (ZnS) и гематита (Fe2O3).
В процессе пиролиза могут быть получены новые соединения, которые взаимодействуют с газообразным азотом при повышенных температурах (от 200 до 600°С). Это может приводить к увеличению веса на 0-3%. Некоторые из таких соединений могут представлять собой нитриды. Удельная площадь поверхности и суммарный объем пор этих адсорбентов составляют от 10 до 210 м2/г и от 0.15 до 0.85 см3/г, соответственно. Важным аспектом текстуры указанных соединений является значительный объем мезопор, достигающий 0.8 см3/г (от 0.14 до 0.77 см3/г). pH всех указанных материалов находится в области основных значений и составляет от 7 до 12. Данные материалы способны поглощать до 30 мас.% сероводорода, главным образом в виде элементарной серы. Воздействие сероводорода и осаждение серы приводит к увеличению объема мезопор до 25% в результате образования нового пористого пространства внутри осажденной серы в крупных порах. Важными компонентами кроме щелочноземельных и переходных металлов являются без ограничения оксиды и гидроксиды железа, поскольку они способствуют окислению сероводорода до элементарной серы. Разработанные материалы являются также хорошими адсорбентами катионных или ионных красителей и тяжелых металлов (до 80 мг/г меди и до 130 мг/г красителей). Шпинелеподобная фаза, образующаяся в процессе пиролиза, участвует в реакциях катионного обмена, комплексообразования и осаждения. Во ходе этих реакций лишь небольшое количество кальция и цинка переходит в раствор в результате катионного обмена.
В настоящем изобретении предложено использование компоста и/или компостных материалов в сочетании со шламами бытовых и/или промышленных сточных вод для получения адсорбентов. Получены хорошие результаты при использовании удобрения и шламов бытовых сточных вод для получения адсорбентов, поскольку некоторые из указанных материалов характеризуются высоким содержанием углерода и азота. Существуют и другие отходы, содержащие большое количество углерода и азота, которые можно использовать в качестве исходного материала. Один из видов отходов представляют собой компост и компостные материалы. Компостные материалы можно разделить на две категории: "бурые" - с высоким содержанием углерода и "зеленые" - с высоким содержанием азота.
Бурые компостные материалы могут представлять собой опавшие листья, растительные отходы, солому и сено, хвою, мелкие ветки и щепки, древесные опилки и стружки, обрывки газет, яичную скорлупу, сердцевину кукурузных початков, хлеб и зерно, древесную золу, старую почву для горшечных культур, бумажные полотенца и салфетки, испачканные пищевыми продуктами, сухие цветы, отходы пивоварения, хмель и жмых, картон, загрязненный пищевыми продуктами (чистый направляют на переработку, а грязный подвергают компостированию), испортившуюся муку, крупу, специи, бобы, ореховую скорлупу, мясные и рыбные отходы.
Зеленые компостные материалы могут представлять собой отходы фруктов и овощей, кофейную гущу и кофейные фильтры, чайные пакетики, свежие листья, зеленые растения, отходы, образующиеся при обрезке растений и живых изгородей, скошенную траву, сорняки, букеты цветов, водоросли, птичьи перья, конский навоз, навоз и подстилки мелких домашних животных, в частности хомяков и кроликов, кукурузный крахмал и другие органические наполнители, а также испорченные соки.
Кроме того, при производстве сигарет ежегодно образуется более 70000 тонн табачных отходов. В одной только Индии более 20 лет тому назад получали почти 100000 тонн табачных отходов, и с каждым годом эта цифра растет. В настоящее время табачные отходы используют в качестве компостного материала и удобрения. Табачные отходы образуются на протяжении всего процесса изготовления сигарет от выращивания и сбора табака до получения готовой продукции. Отходы, которые образуются до и после сбора урожая табака, включают отростки, стебли, средние жилки, отходы листа и табачную пыль. Так, например, обрезки зелени образуются при сборе стеблей и/или листьев и отделении листьев от стеблей для сушки. После сушки некоторые сорта табака обмолачивают (путем отделения жилок от листа), при этом также образуются отходы. На этой стадии можно также удалить стебли в зависимости от вида табака. Из высушенного и выдержанного табака удаляют жилки, и листья и жилки измельчают и смешивают. Табачная пыль может образовываться на операциях измельчения и смешивания. Далее пыль может образовываться на стадии формирования из измельченного табака штрангов и обертывания бумагой. Некоторые химические характеристики табачных отходов приведены в таблице 2.
| Таблица 2. Некоторые химические характеристики табака | ||||||||||||
| О.М. % | pH (1/5) | ЕС(1/5) (мкм/см) | Са (мкг/г) | Mg (мкг/г) | N (%) | K (%) | Р (мкг/г) | Na (мкг/г) | Fe (мкг/г) | Cu (мкг/г) | Zn (мкг/г) | Mn (мкг/г) |
| 41 | 5.80 | 10700 | 8050 | 9400 | 2.35 | 1.95 | 973 | 572 | 3150 | 84 | 90 | 279 |
Возможность применения компоста и/или компостного материала была установлена в ходе исследований с использованием комбинации шламов бытовых сточных вод и шламов промышленных сточных вод, а также шламов бытовых сточных вод и бумажных отходов. Бумажные отходы используют вследствие высокого содержания в них углерода. Бумагу подвергают мелкому помолу и добавляют к шламу. Компостные материалы можно подвергнуть помолу, как бумагу, а табачная пыль находится в виде отдельных частиц/порошка. Древесные опилки представляют собой еще один компостный материал, который находится в виде отдельных частиц/порошка. Древесные опилки представляют собой бурый компостный материал с высоким содержанием углерода. Древесный уголь/золу также можно использовать благодаря высокому содержанию углерода.
Настоящее изобретение позволяет комбинировать компост/компостные материалы с промышленными шламами или со смесью бытовых и промышленных шламов. Компост/компостные материалы можно увлажнять при смешивании, если они содержат недостаточное количество естественной влаги для непосредственного смешивания. Соотношение компоста и шлама может составлять от 25% до 75%. Кроме того, в смесь можно добавлять гидроксид кальция для интенсификации разложения сероводорода.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Вышеуказанные и другие задачи, признаки и преимущества настоящего изобретения поясняются далее с помощью подробного описания конкретных вариантов реализации изобретения, иллюстрируемых с помощью прилагаемых чертежей, при этом одинаковые номера ссылок на различных чертежах используются для обозначения одинаковых компонентов.
Фиг.1 представляет собой полученное способом сканирующей электронной микроскопии изображение углеродных нанотрубок на поверхности адсорбента, известного из уровня техники, который получен из шламов сточных вод;
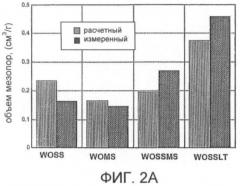
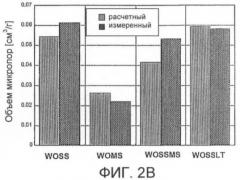
фиг.2А и 2В представляют собой графики, на которых показан рассчитанный и измеренный объем мезо- и микропор, соответственно, для адсорбентов, полученных из смесей промышленных и бытовых шламов;
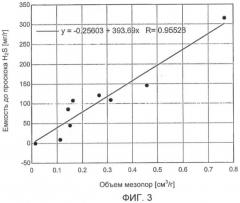
фиг.3 представляет собой график, на котором показана зависимость поглощающей способности по отношению к H2S от объема мезопор адсорбентов, полученных из промышленных и бытовых шламов;
фиг.4 представляет собой график, на котором показаны рассчитанная и измеренная емкости до проскока по отношению к H2S для адсорбентов, полученных из шламов промышленных и бытовых сточных вод;
фиг.5 представляет собой график, на котором показаны кривые дифференциальной термогравиметрии, полученные в атмосфере азота для отдельных адсорбатов (исходные образцы и образцы, выдержанные в атмосфере H2S (Е));
фиг.6 представляет собой график, на котором показаны кривые дифференциальной термогравиметрии в атмосфере азота для отдельных адсорбатов (исходные образцы и образцы, выдержанные в атмосфере H2S (Е));
фиг.7А и 7В представляют собой дифракционные рентгенограммы при 650°С и 950°С соответственно;
на фигуре 8 показаны изменения в распределении пор по размеру после адсорбции H2S;
на фиг.9 представлены кривые дифференциальной термогравиметрии в атмосфере азота для исходных и отработанных образцов;
на фиг.10 представлены дифракционные рентгенограммы для образцов, полученных при 650°С;
на фиг.11 приведено сравнение измеренного и расчетного объема мезопор для образцов WOSS, полученных в различных условиях;
на фиг.12 приведено сравнение измеренной и расчетной емкости до проскока по отношению к H2S для образцов, полученных в различных условиях;
на фиг.13 представлены кривые, характеризующие емкости до проскока по отношению к H2S для адсорбентов, полученных при 650°С;
на фиг.14 представлены кривые, характеризующие емкости до проскока по отношению к H2S для адсорбентов, полученных при 950°С;
на фиг.15 показана зависимость емкости до проскока по отношению к H2S от количества предварительно адсорбированной влаги;
на фиг.16 приведено сравнение измеренной и рассчитанной (для физической смеси компонентов) емкости до проскока по отношению к H2S;
на фиг.17 представлены дифракционные рентгенограммы образцов, полученных из табачных отходов;
на фиг.18 представлены дифракционные рентгенограммы адсорбентов, полученных из шламов сточных вод, содержащих металлы и отработанные масла;
на фиг.19 представлена дифракционная рентгенограмма адсорбентов, полученных из смеси табачных отходов и металлосодержащих шламов;
на фиг.20 приведены изотермы адсорбции азота для образцов, подвергнутых пиролизу при 650°С;
на фиг.21 приведены изотермы адсорбции азота для образцов, подвергнутых пиролизу при 950°С;
фиг.22 иллюстрирует распределение пор по размеру для однокомпонентных образцов;
фиг.23А и 23В иллюстрируют распределение пор по размеру для образцов, подвергнутых пиролизу при 650°С;
фиг.24А и 24В иллюстрируют распределение пор по размеру для образцов, подвергнутых пиролизу при 950°С;
на фиг.25 приведено сравнение объема микропор, измеренного и рассчитанного для физической смеси компонентов;
на фиг.26 приведено сравнение объема мезопор, измеренного и рассчитанного для физической смеси компонентов;
на фиг.27 представлена зависимость емкости до проскока по отношению к H2S от объема пор (микропоры и мезопоры в образцах, подвергнутых пиролизу при двух значениях температуры);
на фиг.28 представлены кривые дифференциальной термогравиметрии в атмосфере азота для однокомпонентных образцов;
на фиг.29А и 29В представлены кривые дифференциальной термогравиметрии в атмосфере азота для образцов, подвергнутых пиролизу при 650°С и
на фиг.30А и 30В представлены кривые дифференциальной термогравиметрии в атмосфере азота для образцов, подвергнутых пиролизу при 950°С.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Промышленные шламы, в частности шламы отработанных масел и металлосодержащие шламы, можно перерабатывать при помощи пиролиза с образованием новых адсорбентов-катализаторов. Важным результатом смешивания является улучшение свойств вышеупомянутых адсорбентов, полученных из шламов сточных вод. Хотя адсорбенты, обладающие исключительной способностью к обессериванию и поглощающей способностью до 30 мас.% могут быть получены только из шламов отработанных масел, добавление шламов сточных вод является экономически целесообразным способом утилизации этого широко распространенного материала.
Смешивание указанных видов шламов и их пиролиз приводит к улучшению свойств конечных продуктов по сравнению со свойствами физической смеси отдельных компонентов, подвергнутых пиролизу. На фиг.2А и 2В показано сравнение объемов пор, измеренных и рассчитанных для физической смеси шлама отработанных масел (waste oil sludge, WO), шлама сточных вод (sewage sludge, SS) и металлосодержащего шлама (metal sludge, MS). Общая наблюдаемая тенденция такова, что смешивание шламов приводит к образованию дополнительного объема пор. Было установлено, что данный объем пор, в особенности мезопор, является одним из факторов, определяющих адсорбционную способность. На фиг.3 показана зависимость адсорбционной способности по отношению к H2S от объема мезопор. Поскольку с помощью определения pH материалов и термодесорбции было установлено, что продуктом окисления является элементарная сера, можно сделать вывод о том, что такое количество серы может накапливаться только в мезопорах (до 30 мас.%, как было установлено при определении емкости до проскока по отношению к H2S).
Наряду с пористостью в процессе пиролиза смеси шламов изменяется также химический состав поверхности по сравнению с отдельными компонентами. На фиг.4 приведено сравнение измеренной адсорбционной способности и адсорбционной способности, рассчитанной для физической смеси компонентов на основании свойств компонентов смеси. Обнаруженное резкое улучшение адсорбционной способности, достигающее 100%, является результатом изменения состава и поверхностного распределения неорганической фазы. Проведенные исследования состава шламов показали, что указанные шламы содержат железо, медь, никель, цинк, кальций, хром и другие металлы в значительных количествах. Взаимодействие этих металлов при высокой температуре в присутствии углеродной фазы может приводить к образованию уникальных шпинеле-/минералоподобных компонентов, проявляющих активность в окислительных реакциях.
На фиг.5 показано увеличение массы образца, полученного с помощью высокотемпературного пиролиза. На фиг.5 представлены кривые дифференциальной термогравиметрии в атмосфере азота, полученные для исходных образцов и образцов, подвергнутых действию H2S (Е), отдельных адсорбантов. Указанное явление не наблюдали для образцов, подвергнутых пиролизу при низкой температуре. В соответствии с неограничивающей гипотезой полагают, что указанное увеличение массы может быть результатом образования нитридов. Было установлено, что некоторые керамические материалы под действием азота в присутствии угля могут образовывать нитриды. Образование этих керамических материалов может быть важным фактором для характеристик катализатора.
Хотя наилучшие адсорбенты получают примерно при 650°С, наиболее сильный синергический эффект возникает примерно при 950°С, когда образуется минералоподобная/керамическая фаза. Более того, увеличение массы образцов в атмосфере азота примерно при 600°С указывает на то, что керамические компоненты адсорбентов образуют нитриды в присутствии углерода. На фиг.6 показаны кривые дифференциальной термогравиметрии в атмосфере азота для исходных образцов и образцов, подвергнутых действию H2S (E), отдельных адсорбантов. Указанные керамические компоненты должны проявлять активность в процессе поглощения H2S, поскольку увеличение массы существенно снижается после воздействия сероводорода и воды. Поверхность адсорбентов, обработанных примерно при 950°С, имеет очень низкое сродство по отношению к воде (гидрофобна). Температура также оказывает влияние на плотность конечных продуктов, которая изменяется примерно от 0.25 при 650°С до примерно 0.50 при 950°С.
Как указано выше, полученные уникальные соединения существуют в виде кристаллографических фаз и содержат металлы, в частности кальций, магний, оксид алюминия, медь, железо, цинк, и неметаллы, в частности кислород, серу, углерод и оксид кремния. Степень минерализации повышается при увеличении температуры и времени пиролиза. Более высокая температура приводит к образованию двухкомпонентных металлических/неметаллических кристаллографических соединений, в которых атомы металла характеризуются низкими степенями окисления. На фиг.7А и 7В показаны различия в дифракционных рентгенограммах образцов, полученных при разных температурах. На фиг.7А представлена дифракционная р