Избирательные андрогенные рецепторные модуляторы
Иллюстрации
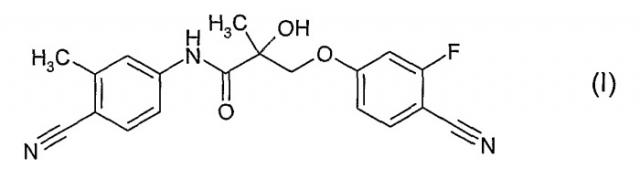
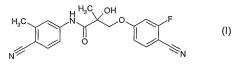
Показать всеИзобретение относится к соединению формулы
представляющему собой (2S)-3-(4-циано-3-фторфенокси)-N-(4-циано-3-метилфенил)-2-гидрокси-2-метилпропионамид, которое обладает действием, модулирующим активность андрогенных рецепторов. Изобретение относится также к фармацевтической композиции и способу лечения или предупреждения состояний, обусловленных андрогенными рецепторами. 3 н.п. ф-лы.
Реферат
Область техники, к которой относится изобретение
Представленное изобретение относится к терапевтически активным соединениям, которые являются полезными при лечении состояний, обусловленных рецепторами андрогенов (АР). В частности, изобретение раскрывает новые соединения, применяемые в качестве ткань-избирательных (селективных) модуляторов андрогенных рецепторов (СМАР). Соединения, представленные в изобретении, которые обладают АР агонистической активностью, полезны при гормональной терапии, особенно при лечении или предупреждении АР зависимых состояний, таких как гипогонадизм, снижение мышечного тонуса, остеопороз, доброкачественная гиперплазия простаты, избыточный вес, связанный с метаболическим синдромом, мужская и женская половая дисфункция и снижение полового влечения, а также снижение содержания андрогена у стареющих мужчин и женщин.
Уровень техники изобретения
Нестероидные пропионанилиды, обладающие АР модулирующей активностью, были описаны, например, в патентных публикациях EP 100172, EP 253503, WO 98/53826 и WO 02/16310. Разработка АР модуляторов пропионанилидной структуры сконцентрирована на соединениях, в которых анилидное кольцо замещено двумя электронно-акцепторными заместителями, такими как трифторметил и нитро заместитель, так как такой заместитель, как сообщалось, повышает сродство лиганда к связыванию с андрогенным рецептором. См., например, ссылку Tucker, H. et al., J. Med. Chem., 1988, 31, 954-959.
Недавно АР модулирующие соединения, имеющие анилидное кольцо, замещенное алкильной группой, были описаны в WO 2005/000794. Однако все еще есть необходимость в АР модулирующих соединениях, которые обладают оптимальным сочетанием свойств, таких как высокое сродство и активность в отношении андрогенных рецепторов, ткань-селективными андрогенными или анаболическими эффектами, высокой пероральной биологической доступностью, низкой возможностью взаимодействия с другими лекарственными препаратами, отсутствием серьезных негативных эффектов и благоприятным метаболическим профилем.
Сущность изобретения
Было найдено, что соединение формулы (I) или изомер, метаболит или фармацевтически приемлемая соль или сложный эфир этого соединения обладают высоким сродством и активностью по отношению к андрогенному рецептору, обеспечивают ткань-избирательные андрогенные или анаболические эффекты, обладают хорошей пероральной биологической доступностью и в то же время обладают низкой возможностью взаимодействия с другими лекарственными препаратами, не имеют серьезных негативных действий и имеют благоприятный метаболический профиль. Более того, соединение в представленном изобретении кристаллизуется достаточно легко и имеет небольшую тенденцию к образованию сольватов. Поэтому соединение представленного изобретения является особенно полезным в качестве ткань-избирательного модулятора (СМАР) андрогенного рецептора. Соединение представленного изобретения является особенно подходящим для использования в гормональной терапии, особенно при лечении или предупреждении АР зависимых состояний, например, но не ограничиваясь только этим, при лечении или предупреждении гипогонадизма, снижения мышечного тонуса, остеопороза, доброкачественной гиперплазии простаты, избыточного веса, связанного с метаболическим синдромом, мужской и женской половой дисфункции и снижения полового влечения, а также снижения уровня андрогена у стареющих мужчин и женщин. Благоприятные андрогенные или анаболические эффекты получают при этом без одновременного вредного стимулирования простаты.
Представленное изобретение обеспечивает соединение формулы (I)
или изомер, метаболит или фармацевтически приемлемую соль или сложный эфир этого соединения.
В особенности предпочтительным соединением формулы (I) является S-энантиомер соединения формулы (I), а именно (2S)-3-(4-циано-3-фторфенокси)-N-(4-циано-3-метилфенил)-2-гидрокси-2-метилпропионамид.
В особенности предпочтительными метаболитами соединения с формулой (I) являются такие соединения, которые полезны при лечении или предупреждении состояний, опосредованных андрогенными рецепторами (АР). Такие предпочтительные метаболиты включают следующие соединения:
2-циано-5-[(S)-3-(4-циано-3-фторфенокси)-2-гидрокси-2-метилпропиониламино] бензойная кислота,
(S)-3-(4-циано-3-фторфенокси)-N-(4-циано-3-гидроксиметилфенил)-2-гидрокси-2-метилпропионамид и
(S)-3-(4-циано-3-фторфенокси)-N-(4-циано-3-формилфенил)-2-гидрокси-2-метилпропионамид.
Фармацевтически приемлемые соли или сложные эфиры вышеуказанных метаболитов также являются полезными при лечении или предупреждении состояний, опосредованных андрогенными рецепторами (АР).
Представленное изобретение обеспечивает, кроме того, способ гормональной терапии, включающий назначение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения формулы (I) или его изомера, метаболита или фармацевтически приемлемой соли или сложного эфира этого соединения.
Представленное изобретение обеспечивает, кроме того, способ лечения или предупреждения состояний, обусловленных андрогенными рецепторами (АР), включающий назначение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения формулы (I) или его изомера, метаболита или фармацевтически приемлемой соли или сложного эфира этого соединения.
Представленное изобретение обеспечивает, кроме того, способ лечения или предупреждения андрогенной недостаточности, включающий назначение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения формулы (I) или его изомера, метаболита или фармацевтически приемлемой соли или сложного эфира этого соединения.
Представленное изобретение также обеспечивает фармацевтическую композицию, включающую соединение формулы (I) или его изомер, метаболит или фармацевтически приемлемую соль или сложный эфир этого соединения, вместе с фармацевтически приемлемым носителем.
Детальное описание изобретения
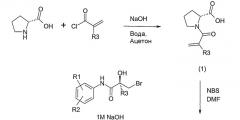
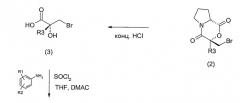
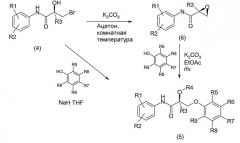
Соединения в изобретении могут быть приготовлены различными синтетическими путями, аналогичными способам, известным в литературе, с использованием подходящих исходных материалов. В частности, соединения в изобретении могут быть приготовлены аналогично общим способам, описанным в WO 2005/000794. Например, соединение формулы (I), включая оптически активные энантиомеры этого соединения, может быть приготовлено согласно следующей схеме реакций, в которой R1 и R3 - метил, R4 - водород, R2 и R7 - циано, R6 - фтор и R5, R8 и R9 - водород:
Метаболиты соединения формулы (I) могут быть подходящим образом получены, например, согласно следующей схеме реакции:
Фармацевтически приемлемые соли, например соли присоединения кислот, как органических, так и неорганических, хорошо известны в фармацевтической области. Неограничивающие примеры этих солей включают хлориды, бромиды, сульфаты, нитраты, фосфаты, сульфонаты, формиаты, тартраты, малеаты, цитраты, бензоаты, салицилаты и аскорбаты. Фармацевтически приемлемые сложные эфиры в случае необходимости могут быть приготовлены с помощью известных способов с использованием фармацевтически приемлемых кислот, которые являются общепринятыми в фармацевтической области и которые сохраняют фармакологические свойства свободной формы. Неограничивающие примеры этих сложных эфиров включают сложные эфиры алифатических или ароматических спиртов, например метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил сложные эфиры. Эфиры орто-фосфорной кислоты и эфиры угольной кислоты также могут быть использованы в рамках данного изобретения.
Определение формулы (I) включает в себя все возможные стерео-изомеры соединений, включая геометрические изомеры, например Z и E изомеры (цис-изомеры и транс-изомеры), и оптические изомеры, например диастереомеры и энантиомеры, и все сложные эфиры, например эфиры орто-фосфорной кислоты и эфиры угольной кислоты. Более того, изобретение включает в свой объем как индивидуальные изомеры, так и любые смеси изомеров, например рацемические смеси.
В первом варианте осуществления термин "изомер" охватывает оптические изомеры соединений изобретения. Квалифицированным специалистам в этой области будет ясно, что соединения в представленном изобретении содержат, по крайней мере, один хиральный центр. Таким образом, соединения в изобретении могут существовать в оптически активной или рацемической формах. Следует понимать, что представленное изобретение включает в себя любую рацемическую или оптически активную форму или смеси этих форм. В первом варианте осуществления соединениями изобретения являются чистые (R)-изомеры. В ином варианте осуществления соединениями изобретения являются чистые (S)-изомеры. В другом варианте осуществления соединениями изобретения являются смеси (R)- и (S)-изомеров. В следующем варианте осуществления соединениями в изобретении являются рацемические смеси, включающие равное количество (R)- и (S)-изомеров. Индивидуальные изомеры могут быть получены с использованием соответствующих изомерных форм из исходного материала, или они могут быть выделены после приготовления конечного соединения с применением общепринятых способов разделения. Для отделения оптических изомеров, например энантиомеров, от смеси этих изомеров могут быть использованы известные способы разделения, например фракционная кристаллизация.
Как определено здесь, термин "метаболит соединения формулы (I)" обозначает биологически активный агент, который образуется в естественных условиях в живом организме из соединения формулы (I).
Согласно представленному изобретению предпочтительными являются метаболиты соединения формулы (I), которые полезны при лечении или предупреждении состояний, опосредованных андрогенными рецепторами (АР). Такие предпочтительные метаболиты включают следующие соединения:
2-циано-5-[(S)-3-(4-циано-3-фторфенокси)-2-гидрокси-2-метилпропиониламино] бензойная кислота,
(S)-3-(4-циано-3-фторфенокси)-N-(4-циано-3-гидроксиметилфенил)-2-гидрокси-2-метилпропионамид и
(S)-3-(4-циано-3-фторфенокси)-N-(4-циано-3-формилфенил)-2-гидрокси-2-метилпропионамид.
Фармацевтически приемлемые соли или сложные эфиры вышеуказанных метаболитов также полезны при лечении или предупреждении состояний, опосредованных андрогенными рецепторами (АР).
Для лечения или предупреждения состояний, опосредованных андрогенными рецепторами (АР), особенно предпочтительно соединение формулы (I), являющееся (S)-изомером соединения формулы (I), а именно (2S)-3-(4-циано-3-фторфенокси)-N-(4-циано-3-метилфенил)-2-гидрокси-2-метилпропионамид.
Соединения изобретения могут быть назначены пациенту в терапевтически эффективных количествах, которые колеблются обычно от примерно 0,1 до примерно 1000 мг в день в зависимости от возраста, веса, этнической принадлежности, состояния пациента, условий, которые должны соблюдаться при лечении, пути введения и используемого андрогенного (АР) модулятора. Соединения изобретения могут быть введены в дозируемых формах с использованием известных принципов в этой области. Соединение может быть введено пациенту как таковое или в сочетании с подходящими фармацевтическими инертными наполнителями в форме таблеток, гранул, капсул, медицинских свечей, эмульсий, суспензий или растворов. Выбор подходящих ингредиентов для композиции осуществляется согласно известным среднему специалисту методикам. Очевидно, что подходящие носители, растворители, гелеобразные ингредиенты, образующие дисперсию ингредиенты, антиоксиданты, красители, подсластители, увлажняющие соединения и другие ингредиенты, как правило, применяемые в этой области, также могут быть использованы. Композиции, содержащие активное соединение, могут быть введены энтерально или парэнтерально, перорально в зависимости от предпочитаемого пути введения. Содержание активного соединения в композиции составляет от примерно 0,5 до 100%, предпочтительно от примерно 0,5 до примерно 20% от общего веса всей композиции.
Данное изобретение более детально объясняется далее с помощью следующих примеров. Примеры приведены только с иллюстративными целями и не ограничивают объем определенного в формуле изобретения.
Примеры
Пример 1
а) (2R)-3-Бром-N-(4-циано-3-метилфенил)-2-гидрокси-2-метилпропионамид
(2R)-3-Бром-2-гидрокси-2-метилпропионовую кислоту (1,52 г, 8,3 ммоль) растворяют в 35 мл чистого тетрагидрофурана (TГФ) и прибавляют 0,5 мл чистого N,N-диметилацетамида (DMA). Раствор охлаждают до 0°С и раствор тионилхлорида (0,8 мл; 10,8 ммоль) добавляют по каплям. Раствор оставляют нагреваться до комнатной температуры и перемешивают в течение 2 часов при комнатной температуре. 4-Циано-3-метиланилин (1,07 г, 8,1 ммоль) прибавляют в 5 мл чистого тетрагидрофурана (ТГФ) и реакционную смесь нагревают с обратным холодильником в течение 2 часов. Выпаривают ТГФ, осадок растворяют в 40 мл CH2Cl2 и промывают 50 мл 1%-ного раствора NaHCO3 и затем водой 4 раза по 25 мл. Органическую фазу выпаривают и осадок сушат при пониженном давлении при 40°С в течение ночи с получением 2,24 г сырого продукта, который кристаллизуют из 5 мл толуола (75°С, затем охлаждают до комнатной температуры и до 0°С), отфильтровывают и промывают 5 мл ледяного толуола. Осадок сушат при пониженном давлении при 40°С в течение ночи; выход продукта составляют 1,54 г.
1H ЯМР (ДМСО-d6): 1,48 (3H, с), 2,45 (3H, с), 3,59 (1H, д, J =10,3 Гц), 3,83 (1H, д, J=10,3 Гц), 6,32 (1H, шир. с), 7,70 (1H, д, J=8,5 Гц), 7,78 (1H, дд, J=8,6 Гц, J=1,9 Гц),7,92 (1H, д, J=1,4 Гц), 9,97 (1H, шир. с).
b) (2R)-2-Метилоксиран-(4-циано-3-метилфенил)амид-2-карбоксиновой кислоты
(2R)-3-Бром-2-гидрокси-2-метил-N-(4-циано-3-метилфенил)пропионамид (1,54 г, 5,2 ммоль) растворяют в 50 мл толуола и перемешивают в течение 5 минут с 15 мл 1М раствора NaOH при комнатной температуре. Органический слой отделяют и промывают дважды 25 мл воды. Толуол отфильтровывают и выпаривают с получением 0,905 г продукта.
1H ЯМР (ДМСО-d6): 1,54 (3H, с), 2,43 (3H, с), 2,99 (1H, д, J=5,1 Гц), 3,04 (1H, д, J=5,1 Гц), 7,65-7,75 (2H, м), 7,82 (1H, д, J=0,6 Гц), 9,77 (1H, шир. с).
с) (2S)-3-(4-Циано-3-фторфенокси)-N-(4-циано-3-метилфенил)-2-гидрокси-2-метилпропионамид
2-Фтор-4-гидроксибензонитрил (0,81 г, 5,9 ммоль) и (2R)-2-метилоксиран-(4-циано-3-метилфенил)амид-2-карбоксиновой кислоты растворяют в 17,6 мл EtOAc. Прибавляют безводный K2CO3 (0,29 г, 2,1 ммоль), смесь нагревают до 50°С и перемешивают в течение 25,5 часов. Смесь охлаждают до комнатной температуры, прибавляют 30 мл EtOAc и промывают сначала дважды по 24 мл 1М раствором Na2CO3 и затем дважды по 24 мл водой. Органический слой сушат над Na2SO4, фильтруют, выпаривают с получением 1,05 г сырого продукта.
1H ЯМР (ДМСО-d6): 1,43 (3H, с), 2,44 (3H, с), 4,10 (1H, д, J=10,0 Гц), 4,36 (1H, д, J=10,0 Гц), 6,29 (1H, bс), 6,96 (1H, дд, J=8,8 Гц, J=2,3 Гц,), 7,18 (1H, дд, J=11,9 Гц, J=2,3 Гц),7,70 (1H, д, J=8,54 Гц), 7,76-7,83 (2H, м), 7,92 (1H, д, J=1,6 Гц), 10,05 (1H, шир. с).
Пример 2
а) Метиловый эфир 5-амино-2-бромбензойной кислоты
Ацетилхлорид (29,2 мл, 32,2 г, 410,7 ммоль) добавляют приливая раствор по каплям в метанол (210 мл) при температуре 0-10°С в атмосфере азота и раствор перемешивают в течение 30 минут при 0°С. После добавления 5-ацетамидо-2-бромбензойной кислоты (21,2 г, 82,1 ммоль) в метанол при 0°С раствор перемешивают в течение 3 часов при 55°С. После выпаривания метанола добавляют этилацетат (160 мл) и перемешивание продолжают в течение 1 часа при комнатной температуре. Осадок отфильтровывают и растворяют в воде. При этом поддерживают pH 8 с помощью NaHCO3. Смесь экстрагируют этилацетатом, промывают водой, сушат над Na2SO4 и концентрируют в вакууме.
1H ЯМР (400 МГц, ДМСО-d6): 3,38 (3H, с), 5,57 (2H, шир. с), 6,64 (1H, дд, 3J=8,6 Гц, 4J=2,9 Гц), 6,95 (1H, д, 4J=2,8 Гц), 7,30 (1H, д, 3J=8,6 Гц).
b) Метиловый эфир 5-амино-2-цианобензойной кислоты
Смесь метилового эфира 5-амино-2-бромбензойной кислоты (14,27 г, 62,0 ммоль) и CuCN (6,11 г, 68,2 ммоль) в N,N-диметилформамиде (DMF) (130 мл) нагревают при 150°С в течение 1 часа 10 минут в атмосфере азота. Смесь охлаждают до 70°С и выливают в смесь воды (250 мл) и 12,5%-ного раствора NH3 (500 мл). Продукт экстрагируют этилацетатом (3×250 мл). Органическую фазу промывают несколько раз 12,5%-ным раствором NH3 и водой, сушат над Na2SO4 и концентрируют в вакууме.
1H ЯМР (400 МГц, ДМСО-d6): 3,86 (3H, с), 6,46 (2H, шир. с), 6,80 (1H, дд, 3J=8,5 Гц, 4J=2,4 Гц), 7,23 (1H, д, 4J=2,3 Гц), 7,51 (1H, д, 3J=8,5 Гц).
c) Метиловый эфир 5-((R)-3-бром-2-гидрокси-2-метилпропиониламино)-2-цианобензойной кислоты
Раствор тионилхлорида (3,9 мл, 5,3 ммоль) добавляют по каплям к раствору (2R)-3-бром-2-гидрокси-2-метилпропионовой кислоты (8,19 г, 44,8 ммоль, раствор приготовлен, как описано в WO 2005/000794) в 190 мл ТГФ и 5,8 мл N,N-диметилацетамида (DMAА) при 5°С в атмосфере азота. Раствор перемешивают в течение 3 часов при комнатной температуре. Раствор метилового эфира 5-амино-2-цианобензойной кислоты (7,50 г, 4,3 ммоль) в 75 мл TГФ добавляют и реакционную смесь выдерживают при 50°С в течение 3 часов и при комнатной температуре в течение 16 часов. Смесь выливают в воду, экстрагируют этилацетатом, промывают водой, сушат над Na2SO4 и выпаривают при пониженном давлении. Сырой продукт смешивают с толуолом и в результате фильтрации получают очищенное соединение.
1H ЯМР (400 МГц, ДМСО-d6): 1,48 (3H, с), 3,58 (1H, д, 2Jgem=10,3 Гц), 3,82 (1H, д, 2Jgem=10,3 Гц), 3,92 (3сH, с), 6,35 (1H, с, -OH), 7,95 (1H, д, 3J=8,5 Гц), 8,16 (1H, дд, 3J=8,5 Гц, 4J=2,2 Гц), 8,73 (1H, д, 4J=2,2 Гц), 10,40 (1H, с, -NHCO-).
d) Метиловый эфир 2-циано-5-[(S)-3-(4-циано-3-фторфенокси)-2-гидрокси-2-метилпропиониламино] бензойной кислоты
Смесь 2-фтор-4-гидроксибензонитрила (4,80 г, 35,0 ммоль), метилового эфира 5-((R)-3-бром-2-гидрокси-2-метилпропиониламино)-2-цианобензойной кислоты (8,41 г, 24,7 ммоль) и K2CO3 (8,51 г, 61,6 ммоль) в TГФ (150 мл) нагревают при 65°С в течение 5 часов в атмосфере азота. Смесь охлаждают до комнатной температуры и прибавляют воду. Продукт экстрагируют в этилацетат. Органическую фазу промывают водой, сушат над Na2SO4 и выпаривают. Сырой продукт очищают посредством флеш-хроматографии на силикагеле (элюент: гептан/этилацетат 7:3-6:4).
1H ЯМР (400 МГц, ДМСО-d6): 1,44 (3H, с), 3,91 (3H, с), 4,12 (1H, д, 2Jgem=10,1 Гц), 4,38 (1H, д, 2Jgem=10,1 Гц), 6,33 (1H, с, -OH), 6,96 (1H, дд, 3 J H,H=8,8 Гц, 4JH,H=2,3 Гц), 7,19 (1H, дд, 3JH,F=11,9 Гц, 4JH,H=2,3 Гц), 7,80 (1H, t, 3 J H,H=4JH,F=8,4 Гц), 7,95 (1H, д, 3J=8,5 Гц), 8,17 (1H, дд, 3J=8,5 Гц, 4J=2,2 Гц), 8,73 (1H, д, 4J=2,1 Гц), 10,47 (1H, с, -NHCO-).
e) 2-Циано-5-[(S)-3-(4-циано-3-фторфенокси)-2-гидрокси-2-метилпропиониламино] бензойная кислота
1М раствор LiOH (34 мл) прибавляют к раствору метилового эфира 2-циано-5-[(S)-3-(4-циано-3-фторфенокси)-2-гидрокси-2-метилпропиониламино] бензойной кислоты (4,52 г, 11,4 ммоль) в TГФ (50 мл) и метанол (6 мл) при температуре 16-18°С. Полученный раствор перемешивают при комнатной температуре в течение 2,5 часов. Растворители выпаривают и с помощью раствора HCl устанавливают pH 2. Продукт экстрагируют в этилацетат. Органическую фазу промывают водой, сушат над Na2SO4 и выпаривают. Осадок очищают флеш-хроматографией (элюент: CH2Cl2/MeOH 98:2). Растирают в порошок в горячем CH2Cl2, охлаждают до комнатной температуры и после фильтрованием получают названное соединение.
1H ЯМР (400 МГц, ДМСО-d6): 1,44 (3H, с), 4,11 (1H, д, 2Jgem=10,1 Гц), 4,37 (1H, д, 2Jgem=10,1 Гц), 6,32 (1H, с, -OH), 6,96 (1H, дд, 3 J H,H=8,8 Гц, 4JH,H=2,4 Гц), 7,20 (1H, дд, 3JH,F=11,9 Гц, 4JH,H=2,3 Гц), 7,80 (1H, т, 3 J H,H=4JH,F=8,4 Гц), 7,91 (1H, д, 3J=8,5 Гц), 8,14 (1H, дд, 3J=8,5 Гц, 4J=2,2 Гц), 8,67 (1H, д, 4J=2,1 Гц), 10,41 (1H, с, -NHCO-), 13,84 (1H, шир. с, COOH).
f) (S)-3-(4-Циано-3-фторфенокси)-N-(4-циано-3-гидроксиметилфенил)-2-гидрокси-2-метилпропионамид
(Бензотриазол-1-илокси)трис(диметиламино)фосфониум гексафторофосфат (BOP, 335 мг, 0,757 ммоль) прибавляют к раствору 2-циано-5-[(S)-3-(4-циано-3-фторфенокси)-2-гидрокси-2-метилпропиониламино] бензойной кислоты (250 мг, 0,652 ммоль) в безводный TГФ (8 мл) в атмосфере азота. N,N-диизопропилэтиламин (0,14 мл, 0,803 ммоль) прибавляют к смеси и перемешивают при комнатной температуре в течение 10 минут. Затем добавляют NaBH4 (30 мг, 0,793 ммоль) и перемешивают при комнатной температуре в течение 50 минут. Растворитель удаляют при пониженном давлении и осадок растворяют в этилацетате. Органическую фазу промывают 0,5М раствором HCl, концентрированным NaHCO3 и рассолом и сушат над Na2SO4. Растворитель удаляют при пониженном давлении и осадок очищают флеш-хроматографией на силикагеле с использованием в качестве элюента смеси дихлорометан/метанол (95:5) с тем, чтобы обеспечить получение желаемого спирта.
1H ЯМР (400 МГц, ДМСО-d6): 1,42 (3H, с), 4,09 (1H, д, 2Jgem=10,0 Гц), 4,35 (1H, д, 2Jgem=10,1 Гц), 4,59 (2H, д, 3J=5,6 Гц), 5,52 (1H, t, 3 J=5,5 Гц, -CH2OH), 6,23 (1H, с, -OH), 6,94 (1H, д, 3JH,H=8,8 Гц, 4JH,H=2,3 Гц), 7,16 (1H, дд, 3 J H,F=11,9 Гц, 4JH,H=2,3 Гц), 7,70 (1H, д, 3J=8,4 Гц), 7,78 (2H, м), 8,14 (1H, д, 4J=1,5 Гц), 10,09 (1H, с, -NHCO-).
g) (S)-3-(4-Циано-3-фторфенокси)-N-(4-циано-3-формилфенил)-2-гидрокси-2-метилпропионамид
(S)-3-(4-Циано-3-фторофенокси)-N-(4-циано-3-гидроксиметилфенил)-2-гидрокси-2-метилпропионамид (170 мг, 0,460 ммоль) и пиридиний хлорхромат (150 мг, 0,696 ммоль) в безводном CH2Cl2 (10 мл) перемешивают в течение 1 часа 45 минут при комнатной температуре. Затем растворитель выпаривают и осадок очищают посредством флеш-хроматографии на силикагеле (CH2Cl2/MeOH 96:4) с тем, чтобы получить (S)-3-(4-циано-3-фторфенокси)-N-(4-циано-3-формилфенил)-2-гидрокси-2-метилпропионамид.
1H ЯМР (400 МГц, ДМСО-d6): 1,44 (3H, с), 4,11 (1H, д, 2Jgem=10,1 Гц), 4,37 (1H, д, 2Jgem=10,0 Гц), 6,32 (1H, шир. с, -OH), 6,94 (1H, дд, 3 J H,H=8,8 Гц, 4JH,H=2,2 Гц), 7,16 (1H, дд, 3JH,F =11,9 Гц, 4JH,H=2,3 Гц), 7,78 (1H, т, 3 J H,H=4JH,F=8,3 Гц), 7,97 (1H, д, 3J=8,5 Гц), 8,18 (1H, дд, 3J=8,5 Гц, 4J=2,2 Гц), 8,61 (1H, д, 4J=1,9 Гц), 10,05 (1H, д, 4J=0,4 Гц, -CHO), 10,46 (1H, шир. с, -NHCO-).
1. Соединение формулы (I) ,которое представляет собой (2S)-3-(4-циано-3-фторфенокси)-Н-(4-циано-3-метилфенил)-2-гидрокси-2-метилпропионамид.
2. Фармацевтическая композиция, обладающая АР модулирующей активностью (действием, модулирующим активность андрогенных рецепторов), включающая терапевтически эффективное количество соединения по п.1, вместе с фармацевтически-приемлемым носителем.
3. Способ лечения или предупреждения состояний, обусловленных андрогенными рецепторами (АР), включающий введение терапевтически эффективного количества соединения по п.1 или композиции по п.2.