Производные бупренорфина и их применение
Иллюстрации
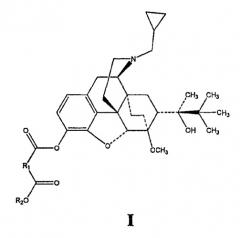
Показать всеИзобретение относится к соединениям общей формулы (I), в которой R1 представляет собой C1-С10-алкил с прямой или разветвленной цепью, необязательно замещенный ароматическим кольцом, или
-(СН2)nХ(СН2)n-, в котором каждое n равно целому числу от 0 до 2, Х представляет собой О, S, NH и где R2 представляет собой Н или C1-С6-алкил с прямой или разветвленной цепью. Также изобретение относится к применению сложноэфирных производных бупренорфина по гидроксильной группе фенола для лечения опиатной зависимости и/или боли, от умеренной до сильной, и к применению в качестве средства, высвобождающего терапевтическое количество бупренорфина в организме человека. Технический результат - новые производные бупренорфина по гидроксильной группе фенола для лечения опиатной зависимости и/или боли, от умеренной до сильной. 9 н. и 11 з.п. ф-лы, 7 ил., 1 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к производным бупренорфина и их применениям.
Уровень техники
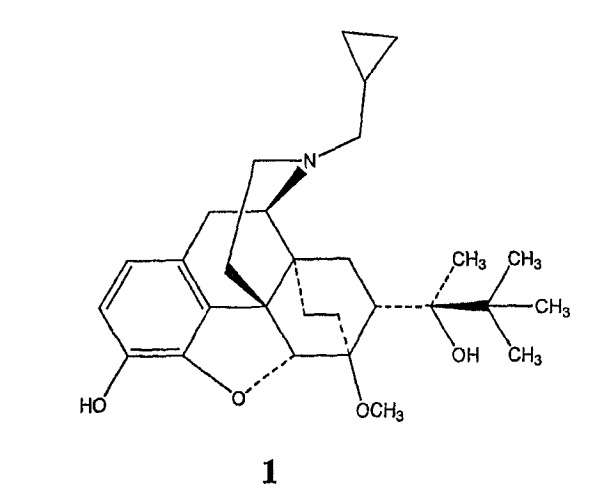
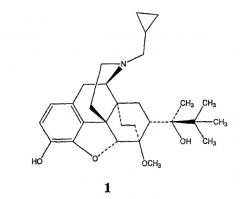
Лечение злоупотребления опиатами и опиатной зависимости путем замены опиата, используемого для злоупотребления, более безопасным, более длительно действующим опиоидом, часто является успешной стратегией медикаментозного лечения. Героин - опиат, широко используемый для злоупотребления, действует как агонист μ-опиоидного рецептора (MOR). При злоупотреблении героином часто применяют внутривенную инъекцию, часто приводящую к совместному использованию иглы наркоманами, которое зачастую является причиной распространения опасных для жизни инфекций, таких как гепатит C и ВИЧ/СПИД. В качестве заменителя агониста MOR был применен метадон. Метадон является активным при пероральном применении и обладает достаточной продолжительностью действия для того, чтобы обеспечить такое действие при введении в виде однократной суточной дозы. Совсем недавно для медикаментозного лечения был применен бупренорфин 1, 21-(циклопропил-7α-[(S)-1-гидрокси-1,2,2-триметилпропил])-6,14-эндоэтано-6,7,8,14-тетрагидроорипавин, частичный агонист MOR, (см., например, патент США № 4935428). В качестве частичного агониста MOR он имеет более низкий допустимый уровень воздействий, опосредованных MOR, чем полный агонист MOR (например, метадон). В результате бупренорфин имеет более высокий предел безопасности, чем полные агонисты MOR. Кроме того, бупренорфин также обладает большой продолжительностью действия. Повышенная безопасность бупренорфина в сочетании с его увеличенной продолжительностью действия обеспечивает относительно длительный интервал между приемами лекарственного средства, обычно каждые 24 часа, хотя он может быть увеличен до каждых 72 часов или более.
Благоприятный профиль безопасности бупренорфина по сравнению с метадоном позволил врачам назначать его амбулаторно, что существенно уменьшило стоимость лечения и увеличило число зависимых людей (наркоманов), подвергающихся медикаментозному лечению.
Для лечения злоупотребления опиатами и опиатной зависимости бупренорфин доступен в виде таблеток, разработанных для сублингвального введения, и продается под торговой маркой Subutex®. Суточная поддерживающая доза Subutex® находится в диапазоне 4-16 мг. Subutex® легко растворим в водных средах, что создает возможность для наркоманов злоупотреблять препаратом путем растворения таблеток в воде с последующей инъекцией полученного раствора. Чтобы противодействовать такому злоупотреблению, была разработана смесь бупренорфина с налоксоном - антагонистом MOR в отношении 4:1 (Suboxone®).
Сублингвальное введение бупренорфина имеет несколько недостатков, в частности необходимость избегать глотания таблетки из-за низкой биодоступности бупренорфина (~5%) при пероральном введении. Для сравнения, при сублингвальном всасывании биодоступность бупренорфина составляет приблизительно пятьдесят процентов (см., например, Jasinski and Preston, Buprenorphine, под ред. A Cowan, JW Lewis, Wiley-Lis, NY стр. 189-211).
Несколько сложноэфирных производных бупренорфина описаны Stinchcomb и др. в публикации Pharm. Res (1995), 12, 1526-1529. Описываются физико-химические свойства сложных эфиров и сравниваются со свойствами гидрохлорида бупренорфина и его свободного основания. В публикациях Stinchcomb и др. Biol.Pharm.Bull. (1996), 19, 263-267 и Pharm. Res. (1996), 13, 1519-1523 также описана трансдермальная абсорбция таких сложных эфиров. В опубликованной патентной заявке США № 2005/0075361 (автор Wang) также описаны некоторые производные бупренорфина, которые очевидно применимы для обезболивания при внутримышечном или подкожном введении.
Сущность изобретения
Описаны сложноэфирные производные бупренорфина 1 (структурная формула приведена выше) по фенольной гидроксильной группе. Обычно такие производные включают в себя фрагмент, который присоединяется к атому кислорода предшествующей фенольной гидроксильной группы. Фрагмент может включать, например, концевую группу в виде карбоновой кислоты или сложного эфира карбоновой кислоты. Как описано в данном описании, многие из таких производных, например сложный эфир дикарбоновой кислоты, содержащий подходящую удаляемую группу, например тозилат, иодид, бромид или хлорид, можно получать взаимодействием бупренорфина с дикарбоновой кислотой, соответствующим ангидридом или его эквивалентом. Новые сложные эфиры, например, в твердых дозированных формах можно применять для лечения субъектов, которые физически зависимы от опиатов, или субъектов, страдающих от боли, например сильной или хронической боли. Твердые дозированные формы могут обладать превосходными показателями безопасности, увеличенной продолжительностью действия и пониженной возможностью для злоупотребления.
В одном из аспектов изобретение относится к соединениям структурной формулы I или их солям.
R1 представляет собой
(1) C1-C10-алкил с прямой или разветвленной цепью, необязательно замещенный ароматическим кольцом,
(2) -(CH2)pCH=CH(CH2)p-, в котором каждое p независимо равно целому числу от 0 до 4,
(3) -(CH2)nX(CH2)n-, в котором каждое n равно целому числу от 0 до 2, X представляет собой O, S, NH, N(COOCH2Ph),
кольцо , имеющее замещение в 1,2-, 1,3- или 1,4-положениях, в котором Y представляет собой O, S или NH,
кольцо , имеющее замещение в 1,2-, 1,3- или 1,4-положениях, или
кольцо , в котором m равно целому числу от 1 до 4;
R2 представляет собой H или C1-C6-алкил с прямой или разветвленной цепью.
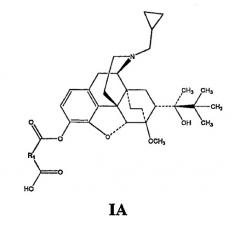
В еще одном аспекте изобретение относится к соединениям структурной формулы IA или их солям;
R1 представляет собой
(1) C1-C10-алкилен с прямой цепью,
(2) C1-C8-алкил с прямой цепью, замещенный 1-4 метильными группами или фенильной группой,
(3) -(CH2)pCH=CH(CH2)p-, в котором каждое p независимо равно целому числу от 0 до 3.
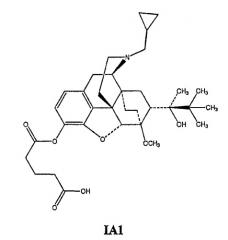
В еще одном аспекте изобретение относится к соединению структурной формулы IA1 или его солям:
В еще одном аспекте изобретение относится к соединению структурной формулы IA2 или его солям:
В еще одном аспекте изобретение относится к соединениям структурной формулы II или их солям;
Каждое n равно целому числу от 0 до 2, X представляет собой O, S, NH, N(COOCH2Ph),
кольцо , имеющее замещение в 1,2-, 1,3- или 1,4-положениях, в котором Y представляет собой O, S или NH,
кольцо , имеющее замещение в 1,2-, 1,3- или 1,4-положениях, или
кольцо , в котором m равно целому числу от 1 до 4.
Описанные в данном описании соединения и/или композиции включают в себя твердые дозированные формы, которые можно глотать, применять сублингвально и/или путем трансбуккального введения. Описанные в данном описании соединения и/или композиции также можно вводить с помощью других способов введения, таких как внутривенные, внутримышечные или трансдермальные способы.
В еще одном аспекте изобретение относится к способам лечения злоупотребления опиатами и/или опиатной зависимости субъекта путем введения субъекту терапевтически эффективного количества одного или нескольких описанных в данном описании соединений и/или композиций.
В еще одном аспекте изобретение относится к способам обезболивания или лечения боли у субъекта, например человека, путем введения субъекту терапевтически эффективного количества одного или нескольких описанных в данном описании соединений и/или композиций.
Аспекты или варианты осуществления изобретения могут иметь любое из следующих преимуществ или сочетание следующих преимуществ. Описанные в данном описании соединения и/или композиции применимы для лечения опиатной зависимости. Некоторые из соединений и/или композиций могут иметь пониженную возможность для злоупотребления, по меньшей мере, частично благодаря их пониженной гидрофильности и пониженной растворимости в воде. Способы лечения просты для применения и менее подвержены тому, чтобы быть использованными неправильным образом. Соединения и/или композиции можно использовать для лечения вне больницы (амбулаторно). Соединения и/или композиции являются сильнодействующими анальгетиками, которые могут облегчать боль, от умеренной до сильной. Соединения и/или композиции можно вводить с помощью различных традиционных способов введения, включая пероральное, сублингвальное, трансбуккальное, внутривенное, внутримышечное или трансдермальное введение. Соединения и/или композиции можно получать в различных состояниях, включая твердые вещества и жидкости. Соединения и/или композиции можно получать в различных традиционных формах, включая таблетки, порошки и пластыри. Соединения и/или композиции можно переводить в водорастворимое или водонерастворимое состояние. Композиции обладают повышенной биодоступностью при пероральном введении и увеличенной продолжительностью действия. Соединения и/или композиции по сравнению с бупренорфином могут обладать более медленным наступлением начала действия.
Если не оговорено иное, все применяемые в данном описании технические и научные термины имеют такое же значение, которое обычно подразумевается специалистом в данной области, к которой относится настоящее изобретение. Способы и материалы описаны в данном описании для применения в настоящем изобретении; также можно применять другие подходящие способы и материалы, известные в данной области. Материалы, способы и примеры предназначены только для иллюстрации и не имеют целью ограничивать изобретение. Все публикации, патентные заявки, патенты и другие, упоминаемые в данном описании ссылки, включены в данное описании в полном объеме путем ссылки. В случае противоречия настоящее описание, включая определения, будет проверяться.
Другие признаки и преимущества изобретения будут очевидны из следующего подробного описания и чертежей, а также из формулы изобретения.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1A приведен график, показывающий средние концентрации в плазме (нг/мл) полуадипата бупренорфина и бупренорфина, образующегося в результате его гидролиза, в зависимости от времени после перорального введения (проглатывания) дозы 1 мг/кг полуадипата бупренорфина первой группе собак породы бигль.
На фиг. 1B приведен график, показывающий средние концентрации бупренорфина в плазме (в нг/мл), в зависимости от времени после перорального введения (проглатывания) дозы 0,8 мг/кг бупренорфина второй группе собак породы бигль.
На фиг. 2A приведен график, показывающий средние концентрации в плазме (в нг/мл) полуглутарата бупренорфина и бупренорфина, образующегося в результате его гидролиза, в зависимости от времени после перорального введения (проглатывания) дозы 1 мг/кг полуглутарата бупренорфина первой группе собак породы бигль.
На фиг. 2B приведен график, показывающий средние концентрации бупренорфина в плазме (в нг/мл) в зависимости от времени после перорального введения (проглатывания) дозы 0,8 мг/кг бупренорфина второй группе собак породы бигль.
На фиг. 3A приведен график, показывающий средние концентрации в плазме (в нг/мл) полуадипата бупренорфина и бупренорфина, образующегося в результате его гидролиза, в зависимости от времени после перорального введения (проглатывания) дозы 63 мг/кг полуадипата бупренорфина первой группе собак породы бигль.
На фиг. 3B приведен график, показывающий средние концентрации бупренорфина в плазме (в нг/мл) в зависимости от времени после перорального введения (проглатывания) дозы 50 мг/кг бупренорфина второй группе собак породы бигль.
На фиг. 4 приведен график, показывающий фармакокинетический профиль высокой суточной дозы полуадипата бупренорфина, вводимой перорально в течение 28 дней собакам породы бигль.
ПОДРОБНОЕ ОПИСАНИЕ
Описаны новые сложноэфирные производные бупренорфина по фенольной гидроксильной группе. Новые сложные эфиры можно применять, например, для лечения субъектов, которые физически зависимы от опиатов. Можно получать различные твердые дозированные формы, которые включают в себя один или несколько новых сложных эфиров. Твердые дозированные формы можно, например, проглатывать или применять сублингвально.
Производные бупренорфина
Сложноэфирные производные обычно можно описать как соединения структурной формулы I или соли соединений структурной формулы I.
В структурной формуле I R1 представляет собой (1) C1-C10-алкильный фрагмент с прямой или разветвленной цепью, необязательно замещенный ароматическим кольцом, например карбоциклическим или гетероциклическим ароматическим кольцом; (2) фрагмент -(CH2)PCH=CH(CH2)P-, в котором каждое p независимо равно целому числу от 0 до 4; или (3) фрагмент -(CH2)nX(CH2)n-, в котором каждое n равно целому числу от 0 до 2, X представляет собой O, S, NH, 5-членное кольцо, представленное структурной формулой 2 (приведенной ниже), содержащее замещение в 1,2-положениях (приведенная ниже структурная формула 2A), 1,3-положениях (2B) или 1,4-положениях (2C); в котором Y представляет собой O, S или NH, бензольное кольцо, представленное структурной формулой 3 (приведенной ниже) и содержащее замещение в 1,2-положениях (3A), 1,3- положениях (3B) или 1,4-положениях (3C), или
5-, 6-, 7- или 8-членное алкильное кольцо, представленное структурной формулой 4 (приведенной ниже). В тех случаях, когда X представляет собой 5-, 6-, 7- или 8-членное алкильное кольцо, можно использовать все позиционные изомеры каждой из соответствующих кольцевых систем, например, замещенных в положениях 1,2- и 1,3- для 5-членного кольца. В структурной формуле I R2 представляет собой H или C1-C6-алкил с прямой или разветвленной цепью.
Некоторые примеры С1-C10-алкильных фрагментов с прямой или разветвленной цепью включают в себя, например, -CH2-, -CH2CH2-, -CH2CH2CH2-, -CH2CH2CH2CH2CH2- и структурные формулы 5, 6, 7 и 8, приведенные ниже.
Некоторые примеры С1-C10-алкильных фрагментов с прямой или разветвленной цепью, замещенных ароматическим кольцом, включают в себя структурные формулы 9, 10, 11 и 12, приведенные ниже.
Ароматическое кольцо может представлять собой, например, простое кольцо или конденсированное кольцо. Ароматическое кольцо может представлять собой карбоциклическое кольцо (например, бензольное кольцо или нафталиновую кольцевую систему), гетероциклическое кольцо (например, производное тиофена, производное фурана или производное пиррола) или конденсированное карбоциклическое и гетероциклическое кольцо.
В конкретных вариантах осуществления изобретения R1 представляет собой -CH2CH2-, -CH2CH2CH2-, -CH2CH2CH2CH2-, -CH2CH(CH3)CH2-, -CH2C(CH3)2CH2-, -CH2OCH2-, -CH2SCH2-, -CH2NHCH2- или -CH2N(COOCH2Ph)CH2-.
В тех случаях, когда R2 представляет собой C1-C6-алкильный фрагмент с прямой или разветвленной цепью, R2 может представлять собой, например, метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, т-бутил, амил, изоамил, 1,2-диметилпропил, 1,1-диметилпропил, пентил, гексил, 4-метилпентил, 1-метилпентил, 2-метилпентил, 3-метилпентил, 1,1-диметилбутил, 2,2-диметилбутил, 3,3-диметилбутил, 1,2,2-триметилпропил и 1,1,2-триметилпропил.
В некоторых вариантах осуществления изобретения R2 представляет собой H, обеспечивая соединения структурной формулы IA или их соли.
В таких случаях в структурной формуле IA R1 представляет собой (1) C1-C10-алкильный фрагмент с прямой цепью; (2) C1-C8-алкиленовый фрагмент с прямой цепью, замещенный 1-4 метильными группами или карбоциклическим ароматическим кольцом, например фенильной группой; или (3) фрагмент -(CH2)PCH=CH(CH2)P-, в котором каждое p независимо равно целому числу от 0 до 3.
В некоторых вариантах осуществления изобретения соединения или соли структурной формулы IA представляют собой соединения, в которых R1 представляет собой C2-C5-алкилен с прямой цепью, например -CH2CH2CH2-, -CH2CH2CH2CH2-, -CH2CH2CH2CH2CH2-, -CH2CH(CH3)CH2- или -CH2C(CH3)2CH2-.
В конкретных вариантах осуществления изобретения соединение представляет собой соединение структурной формулы IAl или IA2 или соль того или другого.
В некоторых вариантах осуществления изобретения R2 представляет собой H, и R1 представляет собой -(CH2)nX(CH2)n-, обеспечивая соединения структурной формулы II или их соли.
В таких случаях -(CН2)nX(CH2)n- может представлять собой любой из описанных выше фрагментов. В конкретных вариантах осуществления изобретения n в каждом случае равно 1, и X представляет собой S, NH, N(COOCH2Ph) или O.
Способ получения производных бупренорфина
Соединения структурной формулы I можно получать, например, из кислоты/свободного основания (IA) путем растворения кислоты/свободного основания в спирте, например, в метаноле или этаноле с последующей обработкой раствора кислоты/свободного основания требуемым диазоалканом (R2-H)N2 13 R2. В некоторых вариантах осуществления изобретения применяют избыток диазоалкана. В некоторых вариантах осуществления изобретения диазоалкан растворяют в простом эфире, например простом диэтиловом эфире. В некоторых вариантах осуществления изобретения диазоалкан добавляют к кислоте/свободному основанию при пониженной температуре, например менее 50°C, и после его добавления раствору дают нагреваться до комнатной температуры. Этерификация карбоновых кислот с помощью диазосоединений обсуждается в публикации Furrow, J.Amer. Chem.Soc, 126, 12222-12223 (2004). Очистку сложного эфира можно осуществлять путем пропускания неочищенной реакционной смеси через хроматографическую колонку, содержащую адсорбент, например оксид алюминия или диоксид кремния, и последующей перекристаллизации полученного материала.
Обычно соединения структурной формулы IA можно получать, например, из бупренорфина 1 или феноксисоединения в виде металлической соли IA (например, натриевой соли) бупренорфина с дикарбоновой кислотой 14 или с ее ангидридом 15. Например, дикарбоновая кислота может представлять собой малоновую кислоту, янтарную кислоту, глутаровую кислоту, 3-метилглутаровую кислоту, 3,3-диметилглутаровую кислоту, адипиновую кислоту, пимелиновую кислоту, дигликолевую кислоту, тиодигликолевую кислоту, имидодиуксусную кислоту, N-бензилоксикарбонилимидодиуксусную кислоту, терефталевую кислоту, изофталевую кислоту, 1,2-нафталиндикарбоновую кислоту, 1H-пиррол-2,5-дикарбоновую кислоту, тиофен-2,5-дикарбоновую кислоту и фуран-2,5-дикарбоновую кислоту.
В частности, соединения структурной формулы I получают, например, с помощью одного из трех способов. В первом способе получают и выделяют феноксисоединение в виде соли IA, такой как натриевая соль бупренорфина. Например, натриевую соль бупренорфина можно получать путем взаимодействия бупренорфина, который растворен в растворителе, таком как смесь этанол/вода, с гидридом натрия. Затем феноксисоединение в виде соли IA подвергают взаимодействию с требуемым ангидридом. Полученную при этом неочищенную соль превращают в гидрохлорид путем обработки разбавленной, например, 1 M хлористоводородной кислотой. Кислоту/свободное основание I можно получать из гидрохлорида путем нейтрализации. Во втором способе бупренорфин подвергают взаимодействию в сухом растворителе, например в смеси простого диэтилового эфира и ацетонитрила, с ангидридом требуемой кислоты. Обычно после выстаивания в течение ночи при комнатной температуре получают требуемый сложный полуэфир. В третьем способе сложные полуэфиры получают, применяя требуемую дикарбоновую кислоту путем объединения дикарбоновой кислоты, взятой в значительном избытке, например более чем 5-мольном избытке, с бупренорфином в сухом растворителе, таком как тетрагидрофуран, наряду с избытком связующего агента, такого как NN'-дициклогексилкарбодиимид (DCCI).
Характер действия производных бупренорфина
Вне связи с какой-либо конкретной теорией считается, что описанные в данном описании соединения, такие как сложные полуэфиры и их соли, являются пролекарствами, которые высвобождают активное лекарственное средство бупренорфин в организме (in vivo). Пролекарство можно определить как систему доставки исходного лекарственного средства, до которого пролекарство метаболически преобразуется после своего всасывания, например, посредством биотрансформации с высвобождением активного лекарственного средства, например, при гидролизе. Обычно пролекарство может защищать исходное лекарственное средство от преждевременной инактивации и экскреции до достижения места приложения действия лекарственного средства. Например, героин (3,6-диацетилморфин) является пролекарством, хотя в основном не для морфина, а для 6-ацетилморфина. В данном примере группа 6-ацетокси обычно более устойчива к метаболизму, чем группа 3-ацетокси.
В частности, считается, что открытые сложные полуэфиры являются пролекарствами, которые высвобождают бупренорфин после гидролиза в организме субъекта (как показано ниже).
Скорость гидролиза можно контролировать, варьируя гидрофильность сложного полуэфира. Поэтому соединения структурной формулы I при пероральном введении (путем проглатывания) субъекту могут продуцировать более высокие концентрации бупренорфина в крови, чем продуцируются эквивалентными дозами бупренорфина. Такой признак также может обеспечивать увеличенную продолжительность действия и более медленное наступление начала действия по сравнению с бупренорфином.
В ходе данной работы со ссылкой на фиг.1A, 1B, 2A и 2B на собаках породы бигль осуществляли фармакокинетические исследования, применяя меченный тритием полуадипат 16 и меченный тритием полуглутарат 17.
меченный тритием в положениях 15,16; 2- полуглутарат, меченный тритием в положениях 15,16; 3- T=тритий (3H))
На фиг. 1A приведен график, показывающий средние концентрации в плазме (в нг/мл) полуадипата бупренорфина и бупренорфина, образующегося в результате его гидролиза, в зависимости от времени после перорального введения (проглатывания) дозы 1 мг/кг полуадипата бупренорфина первой группе собак породы бигль. Для сравнения на фиг. 1B приведен график, показывающий средние концентрации бупренорфина в плазме (в нг/мл) в зависимости от времени после перорального введения (проглатывания) дозы 0,8 мг/кг бупренорфина второй группе собак породы бигль. На фиг. 2B приведен график, показывающий средние концентрации в плазме (в нг/мл) полуглутарата бупренорфина и бупренорфина, образующегося в результате его гидролиза, в зависимости от времени после перорального введения (проглатывания) дозы 1 мг/кг полуглутарата бупренорфина первой группе собак породы бигль. Для сравнения на фиг. 2B приведен график, показывающий средние концентрации бупренорфина в плазме (в нг/мл) в зависимости от времени после перорального введения (проглатывания) дозы 0,8 мг/кг бупренорфина второй группе собак породы бигль. Данные исследования показали, что при временах до 1 часа после введения 1 мг/кг сложного полуэфира бупренорфина (либо полуадипата, либо полуглутарата) в плазме присутствовали высокие концентрации исходного сложного эфира. Полученные уровни были выше, чем уровни высвобождаемого бупренорфина, хотя быстро падали, при этом через 2 часа становясь более низкими, чем уровни бупренорфина. В каждом исследовании (фиг.1B и 2B) другая группа животных принимала эквивалентную дозу неэтерифицированного бупренорфина. Уровень бупренорфина в плазме собак породы бигль после перорального введения доз, практически эквивалентных дозам сложных полуэфиров, был существенно более низким, чем уровни, полученные при введении сложных полуэфиров. Таким образом, каждый из сложных полуэфиров обеспечивал в 2-3 раза более высокие уровни бупренорфина в крови, чем уровни, полученные с помощью исходного лекарственного средства.
Фармацевтические композиции
Обычно фармацевтические композиции представляют собой композиции, которые в качестве активного ингредиента включают в себя, по меньшей мере, один описанный в данном описании сложный полуэфир бупренорфина и/или, по меньшей мере, одну его соль. Фармацевтические композиции обычно включают фармацевтически приемлемый носитель. Применяемая в данном описании формулировка "фармацевтически приемлемый носитель" включает в себя материал, такой как физиологический раствор, растворители, дисперсионные среды, покрывающие слои, инертные наполнители для таблеток, антибактериальные и противогрибковые средства, изотонические средства и средства, замедляющие всасывание, которые совместимы с введением фармацевтических средств. В композиции также можно включать дополнительные активные соединения. Примерами дополнительного активного соединения являются налоксон, налтрексон и налмефен.
Фармацевтические композиции обычно разрабатываются в соответствии с предлагаемым способом их введения. Примеры способов введения включают парентеральное, например внутривенное, интрадермальное или подкожное; пероральное; трансдермальное (местное) и трансмукозальное (например, сублингвально, путем ингаляции и ректально) введение.
Способы создания подходящих фармацевтических композиций описаны, например, в выпусках руководствах и монографиях: Drugs and Pharmaceutical Sciences: a Series of Textbooks and Monographs (Dekker, NY). Например, растворы или суспензии, применяемые для парентерального, интрадермального или подкожного введения, могут включать следующие компоненты: стерильный разбавитель, такой как вода для инъекции, физиологический раствор, нелетучие масла, полиэтиленгликоли, глицерин, пропиленгликоль или другие синтетические растворители; антибактериальные средства, такие как бензиловый спирт или метилпарабены; антиоксиданты, такие как аскорбиновая кислота или бисульфит натрия; хелатообразующие средства, такие как этилендиаминтетрауксусная кислота; буферы, такие как ацетаты, цитраты или фосфаты, и средства для регулирования тоничности, такие как хлорид натрия или декстроза. pH можно регулировать с помощью кислот или оснований, таких как хлористоводородная кислота или гидроксид натрия. Парентеральный препарат можно заключать в ампулы, одноразовые шприцы или флаконы для многократного введения, изготовленные из стекла или пластика.
Фармацевтические композиции, подходящие для инъекций, могут включать стерильные водные растворы (когда соединения водорастворимы) или дисперсии и стерильные порошки для немедленного приготовления стерильных инъецируемых растворов или дисперсии. Подходящие носители для внутривенного введения включают физиологический солевой раствор, антисептическую воду, Cremophor EL(TM) (BASF, Parsippany, NJ) или фосфатно-солевой буфер (ФСБ). Во всех случаях композиция должна быть стерильной и должна быть текучей настолько, чтобы быть способной легко проходить через шприц. Она должна быть устойчивой в условиях производства и хранения и должна быть защищена от инфицирующего действия микроорганизмов, таких как бактерии и грибки. Носитель может представлять собой растворитель или дисперсионную среду, содержащую, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль) и их подходящие смеси. Надлежащую текучесть можно поддерживать, например, путем применения покрывающего материала, такого как лецитин, путем сохранения требуемого размера частиц в случае дисперсии и с помощью применения поверхностно-активных веществ. Защиту от действия микроорганизмов можно обеспечить с помощью различных антибактериальных и противогрибковых средств, например парабенов, хлорбутанола, фенола, аскорбиновой кислоты и тимеросала. Во многих случаях в композицию будут предпочтительно включаться изотонические средства, например сахара, полиспирты, такие как маннит, сорбит и/или хлорид натрия. Пролонгированное всасывание инъецируемых композиций можно осуществлять, включая в композицию средство, замедляющее всасывание, например моностеарат алюминия и желатин.
Стерильные растворы для инъекций можно получать путем введения требуемого количества активного соединения в подходящий растворитель с одним ингредиентом или с комбинацией перечисленных выше ингредиентов, по желанию, с последующей стерилизацией фильтрованием. Дисперсии обычно получают путем введения активного соединения в стерильный наполнитель, содержащий основную дисперсионную среду и другие требуемые ингредиенты из перечисленных выше. В случае стерильных порошков для приготовления стерильных растворов для инъекций предпочтительными способами приготовления являются сушка в вакууме и лиофильная сушка, которые дают порошок активного ингредиента плюс любой дополнительно требуемый ингредиент из его раствора, предварительно стерилизованного фильтрованием.
В некоторых вариантах осуществления изобретения описанные композиции специально адаптированы для перорального введения. С целью перорального терапевтического введения одно или несколько активных соединений - сложных полуэфиров (или их солей) можно вводить с инертными наполнителями и применять в форме таблеток, пастилок или капсул, например желатиновых капсул; такие композиции обычно будут включать в себя инертный разбавитель или съедобный носитель. Композиции для перорального введения также можно приготовить для применения в виде жидкости для полоскания рта, применяя жидкий носитель. Фармацевтически совместимые связующие средства и/или вспомогательные материалы можно включать в виде части композиции. Таблетки, драже, капсулы, пастилки и т.п. могут содержать любые из следующих ингредиентов или соединений аналогичного характера: связующее, такое как микрокристаллическая целлюлоза, трагакантовая камедь или желатин; инертный наполнитель, такой как крахмал или лактоза, дезинтегрирующее средство, такое как альгиновая кислота или кукурузный крахмал; смазку, такую как стеарат магния; вещество, способствующее скольжению, такое как коллоидный диоксид кремния; подсластитель, такой как сахароза или сахарин; или ароматизатор, такой как перечная мята, метилсалицилат или апельсиновый ароматизатор.
Систематическое введение описанного в данном описании терапевтического соединения также можно осуществлять трансмукозальными или трансдермальными способами. Для трансмукозального или трансдермального введения в препарате применяются смачивающие вещества, подходящие для того, чтобы проникать через границу. Такие смачивающие вещества, например, для трансмукозального введения включают детергенты, соли желчных кислот и производные фусидовой кислоты. Трансмукозальное введение можно осуществлять через применение назальных спреев или суппозиториев. Для трансдермального введения разработаны одно или несколько активных соединений - сложных полуэфиров (и/или их солей), применяемых в мазях, бальзамах, гелях или кремах. Для введения путем ингаляции разработано одно или несколько активных соединений - сложных полуэфиров (и/или их солей) в форме аэрозольного спрея из находящегося под давлением контейнера или устройства для распыления, содержащего подходящий пропеллент, например газ, такой как диоксид углерода, или распылитель. Также можно применять материалы-носители, обычно применяемые в сухих порошкообразных препаратах, например моно- или дисахариды, такие как глюкоза, лактоза, моногидрат лактозы, сахароза или трегалоза, сахарные спирты, такие как маннит или ксилит, полимолочную кислоту или циклодекстрин, глюкозу, трегалозу и, в частности, моногидрат лактозы. В некоторых вариантах осуществления изобретения препараты также могут содержать два или более материала-носителя. Если требуется, дополнительно к невдыхаемым частицам носителя препарат также может содержать относительное количество вдыхаемых частиц носителя; например, дополнительно к относительно крупным частицам носителя моногидрата лактозы он может содержать относительное количество, например, от 0,1 до 10 мас.% тонкоизмельченного моногидрата лактозы, частицы которого могут иметь, например, размер диаметра не более 10 мкм, предпочтительно не более 5 мкм, по меньшей мере, для 50% частиц. Сухие порошкообразные препараты, включающие описанные в данном описании соединения, можно применять в ингаляторе сухого порошка, который известен в данной области, например ингаляторы сухого порошка для многократного приема, которые содержат резервуар для порошка, описаны в патентной заявке WO 97/20589. Ряд других способов и устройств, подходящих для доставки соединений путем ингаляции, описан, например, в патенте США № 6645466.
Фармацевтические композиции также можно получать в форме суппозиториев (например, с традиционными основами для суппозиториев, такими как масло какао и другие глицериды) или удерживающих клизм для ректальной доставки.
В некоторых вариантах осуществления изобретения терапевтические соединения получают с носителями, которые будут предохранять терапевтические соединения от быстрого удаления из организма, такие как препарат с контролируемым высвобождением, включая имплантаты и микрокапсулированные системы доставки. Можно применять биоразлагаемые, биосовместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, сложные полиортоэфиры и полимолочная кислота. Такие препараты можно получать, применяя стандартные методики. Также можно получать коммерческие материалы, например, от корпораций Alza Corporation и Nova Pharmaceuticals, Inc.
Способы лечения
Описанные в данном описании способы включают способы лечения злоупотребления опиатами и опиатной зависимостью. В некоторых вариантах осуществления изобретения опиат, применяемый для злоупотребления, представляет собой героин. Обычно описанные в данном описании способы включают в себя введение терапевтически эффективного количества сложного полуэфира бупренорфина субъекту, который нуждается в таком лечении, или субъекту, для которого была установлена необходимость подвергнуться такому лечению. Как применяется в данном контексте, "лечение" злоупотребления опиатами и опиатной зависимостью направлено на уменьшение или устранение зависимости субъекта от злоупотребляемого наркотика, удаление наркотического средства из организма субъекта, злоупотребляющего наркотиками, и до некоторой степени предотвращение субъекта от восстановления его зависимости от такого наркотика. Лечение также направлено на предупреждение или минимизацию абстинентных симптомов, испытываемых субъектом, или