Способ получения магнитоупорядоченного оксида железа (iii) ( -fe2o3) в высокодисперсном состоянии из водного раствора при комнатной температуре
Иллюстрации
Показать всеИзобретение может быть использовано в производстве магнитных материалов на основе оксидов металлов. Для получения высокодисперсного магнитоупорядоченного оксида железа (III) осаждение магнитной фазы γ-Fe2O3 проводят в присутствии воздуха в течение 24 ч при комнатной температуре и атмосферном давлении из щелочных водных растворов солей железа (II), циклодекстринов (ЦД) и соли фосфорноватистой кислоты, взятых в молярном отношении ЦД: Fe2+:NaH2PO2=1:100:100. Изобретение позволяет получить маггемит в высокодисперсном состоянии при комнатной температуре при атмосферном давлении, с повышением его чистоты. 2 ил.
Реферат
Предлагаемый способ относится к области технологии получения магнитных материалов на основе металлов или их оксидов, которые могут быть использованы в качестве магнитных детекторов, наполнителей, покрытий и магнитной среды в различных композитах как магнитные носители в электронной промышленности для создания магнитных сопротивлений, триггерных и запоминающих устройств, как звуконосители в малошумных магнитных лентах, в качестве компонентов в магнитных чернилах, тонерах, пигментах и красках для принтеров, в типографской промышленности, для изготовления красящих пленок на банковских магнитных картах и в других отраслях производства, где требуются вещества с магнитной упорядоченностью и высокой дисперсностью.
Известно, что железо образует несколько оксидов, среди которых Fe3O4 (магнетит) и γ-Fe2O3 (маггемит) обладают магнитными свойствами. Магнетит легко образуется и даже существует в природе, в то время как для получения маггемита требуются специальные условия. Окисление на воздухе, как правило, сопровождается формированием немагнитной фазы α-Fe2O3, устойчивой в широком температурном интервале, и оксо/гидроксо-форм, также не проявляющих ферромагнитных свойств.
Обычно магнитную модификацию оксида железа(III) получают в результате твердофазного высокотемпературного отжига немагнитной фазы α-Fe2O3 в узком температурном интервале.
Известен способ получения магнитной γ-Fe2O3 окислением порошка металлического железа при температуре 200-400°С в атмосфере, содержащей 5-20% кислорода [CN 1116976 A; CA 131:152888 (1998)]. Общим недостатком этого метода является многостадийность синтеза, включающего необходимость получения промежуточного высокодисперсного карбонильного порошка металлического железа из токсичного Fe(CO)5.
Описано получение магнитного оксида железа(III) γ-Fe2O3 окислением стеарата железа метилморфолин-N-оксидом в присутствии ПАВ при выдерживании в растворителе в течение нескольких часов при температуре 280-320°С [WO 2009002275 A1; CA 150:89105 (2009)]. Метод чрезвычайно сложен, требует предварительного получения стеарата железа и использования специальных органических веществ. Кроме того, к недостаткам можно отнести необходимость высокотемпературной обработки и значительную продолжительность синтеза.
Известен метод получения магнитной γ-Fe2O3 из солей железа(III) в растворе, содержащем органические амиды или гидразиды [IN 2001DE00532 А; CA 150:174359 (2008)]. Недостатком метода является использование микроволнового излучения и повышенной температуры, необходимых для получения устойчивой пены.
Магнитный порошок на основе γ-Fe2O3 получали дегидратацией FeOOH при 250-350°С [CN 1108424 А; CA 124:218365 (1996), JP 10025115 A2; CA 128:135648 (1996)]. Метод, однако, требует специальных условий, ограничивающих его использование. Так, например, осаждение FeOOH проводят в атмосфере азота в среде органического растворителя (метилового спирта). Кроме того, дегидратация оксогидроксида железа происходит при повышенной температуре (250-350°С), в результате чего образуется примесь магнетита, что требует дополнительной стадии доокисления продукта.
Известен способ получения тонкодисперсного порошка γ-Fe2O3 из водных растворов путем осаждения гидроксидов железа едким натром в присутствии NH4OH с последующим формированием геля в среде метанола и нагреванием в автоклаве [CN 1108425 А; СА 124:218364 (1996)]. Недостатками этого способа являются использование высокотоксичного органического растворителя и аппаратуры высокого давления.
Известен способ получения магнитной γ-Fe2O3 из водных растворов FeCl3 путем осаждения едким натром гидроксида железа(III) в присутствии полиэтиленгликоля как стабилизатора [CN 1789146 А; СА 145:179474 (2006)]. Существенным недостатком этого способа является необходимость проведения многочисленных процедур, включающих фильтрование, высушивание осадка, прокаливание в течение нескольких часов при температуре 300-400С°, последующее промывание водой и т.п.
Наиболее близким к заявляемому является способ получения магнитной γ-Fe2O3 [CN 101125684 А; СА 148:368571 (2006)] из водного щелочного раствора путем обработки солей двухвалентного железа едким натром в присутствии гидразингидрата с последующим выдерживанием смеси в автоклаве при 100-200°С в течение 4-100 часов и обработкой интермедиата (Fe3O4) гидропероксидом водорода. Существенными недостатками данного способа являются его многостадийность, проведение гидротермической реакции в автоклаве при повышенной температуре (100-200°С), а также неколичественный выход целевого продукта за счет образования примесной фазы магнетита, что требует дополнительной обработки сильным окислителем.
Задачей предлагаемого способа является прямое и количественное осаждение магнитной фазы маггемита (γ-Fe2O3) в высокодисперсном состоянии из водных растворов солей железа(II) при комнатной температуре без использования высокотемпературной обработки при атмосферном давлении в присутствии воздуха.
Данная задача решается предложенным способом, который состоит в том, что магнитную фазу γ-Fe2O3 получают при комнатной температуре и атмосферном давлении на воздухе осаждением из щелочного (рН 9-10) водного раствора солей железа(II) в присутствии циклодекстринов (ЦД) и солей фосфорноватистой кислоты (H3PO2) в молярном отношении ЦД:Fe(II):NaH2PO2=1:100:100 в течение 24 ч.
Отличием предложенного способа получения магнитной γ-Fe2O3 является проведение синтеза в присутствии воздуха, циклодекстринов и солей фосфорноватистой кислоты при комнатной температуре и атмосферном давлении.
Высокотемпературная обработка немагнитных образцов оксида железа(III) с целью получения магнитной фазы γ-Fe2O3, которая во всех известных методах синтеза является одной из ключевых стадий, требует специальных условий и значительно снижает экономическую эффективность процесса.
В предлагаемом способе синтез магнитной модификации γ-Fe2O3 проводят при комнатной температуре из растворов солей железа(II), в качестве которых могут быть использованы любые растворимые соли железа(II), например, FeCl2, FeSO4, соль Мора Fe(NH4)2(SO4)2·6H2O и т.п.
Особенностью предлагаемого метода является формирование оксида Fe2O3, т.е. окисленной формы железа, в присутствии сильного восстановителя и кислорода воздуха. Необходимость восстановителя в системе обусловлена химической спецификой данного процесса, который протекает через образование металлического железа как интермедиата. Без восстановителя образуются оксо/гидроксоформы железа, содержащие смесь железа(II) и железа(III), не обладающие магнитными свойствами.
Выбор гипофосфита в качестве восстановителя обусловлен высоким окислительно-восстановительным потенциалом пары Н2РО2 -/РО4 3-, обеспечивающим восстановление до металлического железа в щелочной среде.
Осаждение магнитной γ-Fe2O3 проводят в щелочном растворе с рН в интервале 9-10. Нижняя граница интервала рН определяется условием существования гидроксида железа Fe(OH)2. Верхняя граница зависит от устойчивости продукта взаимодействия частиц металла, образующихся при восстановлении гипофосфитом в щелочном растворе, и олигосахарида, специфически адсорбирующегося на поверхности металлического или оксидного зародыша. Природа щелочного металла (в составе щелочи или гипофосфита) не имеет значения. В качестве щелочи и гипофосфита могут быть использованы гидроксид и гипофосфит любого щелочного металла.
Механизм образования фазы оксида железа включает стадию восстановления гипофосфитом в щелочной среде согласно реакции:
Выбор исходных концентраций солей железа(II) и гипофосфита обусловлен индивидуальной растворимостью ингредиентов и в принципе неограничен при соблюдении условия оптимального соотношения Fe(OH)2:NaH2PO2 в реакционной смеси.
Известно, что циклодекстрины используют для стабилизации наночастиц некоторых оксидов в определенной кристаллической модификации. Например, получены наночастицы TiO2 в форме анатаза в присутствии (β-циклодекстрина [Chem. Asian J. 2006. 1, 664].
Образование магнитной γ-Fe2O3 в водном щелочном растворе происходит в присутствии циклодекстрина, в качестве которого могут быть использованы любые формы α-, β- и γ-ЦД и их производные. Молярное отношение ЦД:Fe(II) составляет 1:100.
Роль циклодекстрина при образовании магнитной γ-Fe2O3 в водном растворе состоит в стабилизации зародышей фазы металлического железа, образующейся в результате реакции (1), за счет торможения процессов агломерации и сращивания кристаллитов, с одной стороны, и ингибирования спонтанного окисления металлического железа в водной среде в присутствии растворенного кислорода в соответствии с уравнением реакции (2) - с другой.
Известно, что в присутствии некоторых органических соединений, таких, например, как поверхностно-активные вещества (высшие жирные кислоты и их соли), полиспирты, олигосахариды и др., скорость агломерации зародышей твердой фазы резко уменьшается, что приводит к образованию высокодисперсных осадков.
Рентгенофазовый анализ продукта, полученного заявляемым способом, свидетельствует об отсутствии фазы магнетита даже в следовых количествах. На рентгенограмме регистрируются рефлексы, принадлежащие исключительно фазе γ-Fe2O3.
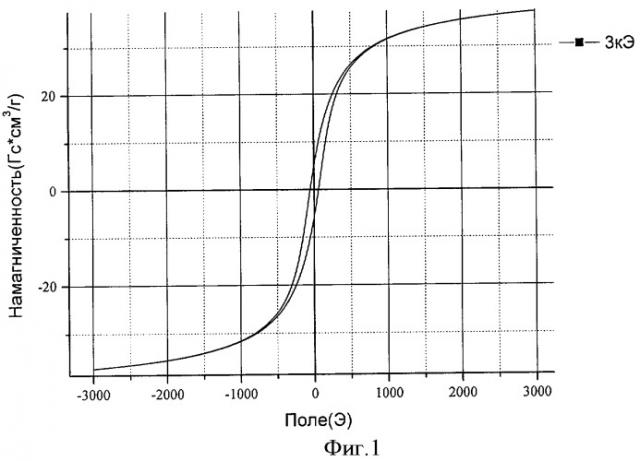
Магнитные свойства продукта, полученного заявляемым способом, охарактеризованы измерением намагничивания в зависимости от величины магнитного поля. Для типичного образца полученные данные представлены на фиг.1. Петля магнитного гистерезиса на кривой намагничивания указывает на ферромагнитные свойства образца. Величина коэрцитивной силы (Hc) и остаточного магнетизма составляют для данного продукта 70 Э и 4,5 Эмю/г соответственно.
Образование в описанном способе магнитной фазы γ-Fe2O3 подтверждается данными спектров Мёссбауэра, приведенными на фиг.2. Характер полученных мёссбауэровских спектров хорошо согласуется с известными литературными данными для стандартных образцов маггемита (γ-Fe2O3).
Таким образом, обработкой солей железа(II) при комнатной температуре на воздухе щелочным раствором циклодекстринов в присутствии восстановителя приводит к заявляемому технологическому эффекту, т.е. образованию высокодисперсного магнитного оксида γ-Fe2O3. Преимуществами изложенного способа являются простота «one-pot» синтеза, не требующего выделения промежуточных веществ, доступность и невысокая стоимость реагентов, безопасность технологического процесса, осуществляемого при комнатной температуре в водных растворах без использования органических растворителей.
Перечень иллюстративных материалов.
Фиг.1 Зависимость удельного намагничивания образца оксида железа(III) от напряженности магнитного поля при комнатной температуре
Фиг.2. Мессбауэровский спектр образца, полученного из щелочного водного раствора соли Мора в присутствии гипофосфита натрия и гидроксипропил-β-циклодектрина при комнатной температуре в присутствии воздуха
Заявляемый способ получения высокодисперсного магнитного оксида γ-Fe2O3 проиллюстрирован с помощью следующих примеров.
Пример 1
К 20 мл содержащего 24 мг р-циклодекстрина (0,02 ммоль), 627 мг Fe(NH4)2(SO4)2·6H2O (4 ммоль) и 16 ммоль NaOH, добавляют 20 мл водного раствора, содержащего 170 мг (4 ммоль) гипофосфита натрия. Смесь перемешивают при комнатной температуре в течение 24 ч. Отделяют осадок черного цвета с выходом 98%, в котором обнаруживают маггемит.
Пример 2
К 20 мл интенсивно перемешиваемого при комнатной температуре раствора, содержащего 24 мг гидроксипропил-β-циклодекстрина-1500 (0,04 ммоль), 627 мг Fe(NH4)2(SO4)2·6H20 (4 ммоль) и 16 ммоль NaOH, добавляют 20 мл водного раствора, содержащего 170 мг (4 ммоль) гипофосфита натрия. Смесь перемешивают при комнатной температуре в течение 24 ч. Отделяют осадок черного цвета с выходом 95%, в котором обнаруживают маггемит.
Пример 3
К 20 мл интенсивно перемешиваемого при комнатной температуре раствора, содержащего 30 мг диметил-β-циклодекстрина (0,02 ммоль), 627 мг Fe(NH4)2(SO4)2·6H2O (4 ммоль) и 16 ммоль NaOH, добавляют 20 мл водного раствора, содержащего 170 мг (4 ммоль) гипофосфита натрия. Смесь перемешивают при комнатной температуре в течение 24 ч. Отделяют осадок черного цвета с выходом 96%, в котором обнаруживают маггемит.
Пример 4
К 20 мл интенсивно перемешиваемого при комнатной температуре раствора, содержащего 30 мг α-циклодекстрина (0,03 ммоль), 627 мг Fe(NH4)2(SO4)2·6H2O (4 ммоль) и 16 ммоль NaOH, добавляют 20 мл водного раствора, содержащего 170 мг (4 ммоль) гипофосфита натрия. Смесь перемешивают при комнатной температуре в течение 24 ч. Отделяют осадок черного цвета с выходом 96%, в котором обнаруживают маггемит.
Пример 5
К 20 мл интенсивно перемешиваемого при комнатной температуре раствора, содержащего 30 мг γ-циклодекстрина (0,023 ммоль), 627 мг Fe(NH4)2(SO4)2·6H2O (4 ммоль) и 16 ммоль NaOH, добавляют 20 мл водного раствора, содержащего 170 мг (4 ммоль) гипофосфита натрия. Смесь перемешивают при комнатной температуре в течение 24 ч. Отделяют осадок бурого цвета, в котором обнаруживают маггемит.
Способ получения магнитоупорядоченного оксида железа (III) (γ-Fe2O3) в высокодисперсном состоянии, отличающийся тем, что осаждение магнитной фазы γ-Fe2O3 проводят в присутствии воздуха при комнатной температуре и атмосферном давлении из щелочных (рН 9-10) водных растворов солей железа (II), циклодекстринов и солей фосфорноватистой кислоты в молярном отношении ЦД:Fe(II):NaH2PO2=1:100:100 в течение 24 ч.