Агент, проявляющий свойства активатора когнитивных функций (варианты)
Иллюстрации
Показать всеПредложены агент, проявляющий свойства активатора когнитивных функций, представляющий собой 1,3-диметил-5-(пиридил-4-амино)метилен-барбитуровой кислоты (1), и агент того же назначения, 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидронафтиридинил)пиридиния хлорида (2) - варианты. Показана высокая биологическая активность в условиях скополаминовой амнезии предлагаемых агентов. 2 н.п. ф-лы, 1 табл.
Реферат
Изобретение относится к области химико-фармацевтической промышленности и медицины.
В настоящее время одной из фундаментальных проблем современной биологии является изучение закономерностей формирования памяти в головном мозге. В этом отношении важнейшей задачей является выяснение теоретического и практического вопроса о том, как именно активация нервных клеток обусловливает развитие памяти [1]. Вследствие этого принципиальным подходом к решению данной проблемы является синтез и биологическое исследование новых оригинальных соединений, способных активировать когнитивные функции, и выявление общих закономерностей получения таких веществ и возможности использовании их в медицинской практике.
Известно значительное число веществ, при помощи которых можно управлять многими функциями центральной нервной системы (ЦНС). К ним относятся разнообразные химические соединения, влияющие на психическое состояние и эмоции, уменьшающие восприятие болевых ощущений, способствующие развитию сна, вызывающие наркоз, обладающие противосудорожным действием и др.
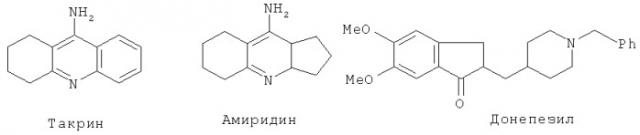
Известно, что при различных органических и функциональных нарушениях центральной нервной системы (астенические состояния, снижение интеллектуально-мнестических функций), которые сегодня еще не поддаются эффективному лечению терапевтическими средствами, могут применяться препараты, активирующие когнитивные функции. В последние годы было установлено, что при болезни Альцгеймера и других заболеваниях, включая различные виды старческих деменций, могут применяться такие антихолинэстеразные препараты, как такрин, амиридин, донепезил. Эти препараты используют при различных деменциях, правда, пока, в основном, как вспомогательные средства.
Болезнь Альцгеймера включает снижение рецепторной активности мускариновых м2 и никотиновых рецепторов. С повреждением холинергической системы связана сниженная при этой болезни активность ацетилхолинтрансферазы, высокий уровень обратного захвата ацетилхолина - все это приводит к ослаблению когнитивных функций. В настоящее время на моделях показано участие ацетилхолина в функциях познания и обучаемости.
Необходимо также рассматривать и другой подход, связанный с воздействием на один из подтипов глутаматных рецепторов - NMDA-рецепторы, гиперактивация которых может приводить к активизации нейродегенеративных симптомов [2, 3]. Было синтезировано значительное количество соединений, блокирующих суперактивацию этих рецепторов.
В частности, из уровня техники известны соединения, представляющие собой производные пиридина и лекарственные средства, обладающие селективной блокирующей активностью в отношении подвида NMDA-рецепторов на их основе, которые могут быть (патент РФ 2303037, опубл. 20.07.2007). Однако данные соединения могут вызвать ряд побочных эффектов.
Наиболее близкими по достигаемому результату являются соединения, представляющие собой 4-амино- и 2,4-диаминопиридиновые производные, стимулирующие когнитивные функции. Данные производные сочетают свойства антагонистов NMDA-рецепторов со свойствами умеренных ингибиторов ацетилхолинэстеразы и свойствами агонистов никотиновых рецепторов и симпатомиметиков (EA 200801639 (A1), опубл. 2009.08.28). Данный источник может быть указан в качестве ближайшего аналога.
Задача изобретения - поиск новых эффективных агентов, использование которых может обеспечить подходы к лечению таких заболеваний, а также изыскание новых средств, способных к положительному воздействию на функции памяти, т.е. поиск соединений, являющихся активаторами когнитивных функций.
Задача решается синтезом и биологическим исследованием новых соединений, которые проявляют высокую биологическую активность in vivo в отношении когнитивных функций. Эти вещества перспективны как агенты, на основе которых возможно создание новых оригинальных лекарственных препаратов, способных положительно модулировать активность Центральной Нервной Системы (ЦНС).
Среди множества синтезированных авторами веществ был проведен отбор по принципу наибольшей активности и высокому терапевтическому индексу (отношение эффективной дозы к токсической дозе) и выбрано два наиболее перспективных соединения (1, 2), которые могут быть использованы в качестве агентов, проявляющих свойства активаторов когнитивных функций.
Таким образом, объектами изобретения являются:
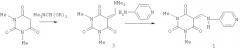
- агент, проявляющий свойства активатора когнитивных функций, который представляет собой 1,3-диметил-5-(пиридил-4-амино)метиленбарбитуровую кислоту формулы (1):
- агент, проявляющий свойства активатора когнитивных функций, который представляет собой 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидронафтиридинил)пиридиния хлорид формулы (2):
Методы синтеза целевых соединений предусматривают участие 4-аминопиридина в качестве промежуточного соединения для получения веществ, включающих в свои структуры 4-аминопиридиновый или 4-аминопиридиниевый фрагменты (соединения 1 и 2) и, соответственно, обеспечивающих технологически приемлемые условия получения целевых продуктов из доступного сырья и без применения особых условий проведения процесса.
Изобретение может быть проиллюстрировано следующими ниже представленными примерами осуществления:
Пример 1
Получение 1,3-диметил-5-(пиридил-4-амино)метиленбарбитуровой кислоты (1)
К суспензии 7,8 г 1,3-диметилбарбитуровой кислоты в 50 мл серного эфира прибавляют по каплям 14,7 мл диэтилацеталя диметилформамида (можно также использовать диметилацеталь диметилформамида), смесь перемешивают при комнатной температуре в течение 2 часов и отфильтровывают 9,82 г енамина 3. Смесь 1,05 г соединения 3 и 0,47 г 4-аминопиридина нагревают на масляной бане до температуры бани ≈160°C и затем выдерживают при 160-170°C в течение 30 мин, отфильтровывают 1,1 г (85%), т.пл. 233-235°C (из ДМФА).
Спектр 1HЯМР (D6 ДМСО): δмд 3,21 (6Н) (1,3-ди-Ме), 8,09, 8,74, 8,77 (аром. протоны и винильный протон), 12,13 (NH - уш. синглет, 1 Н).
Пример 2
Получение 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидронафтириди-нил)пиридиния хлорида (2)
Метод 1. Смесь 0.26 г (0.86 ммоль) 3-нитро-2-оксо-1-фенил-5-хлор-1,2-дигидро-1,6-нафтиридина (4) и 0.16 г (1.70 ммоль) 4-аминопиридина в 20 мл изопропанола кипятили 4 ч. Осадок при кипении не растворяется. После охлаждения реакционной массы до 20°C осадок отфильтровали, промыли изопропанолом, ДМФА. Получили 0.19 г (56%) соединения 2. Т.пл 326-329°C. Масс-спектр, m/z (ESI): 360 [М+Н]+; 719 [2М+Н]+; 285 [M-NO2-CO]. Спектр ЯМР 1H (ДМСО-d6, δ, м.д.): 6.70 (д, 1 H, H(8), 3Jo=6.02 Гц), 7.02 (д, 2 H, H(5''), H(5''), 3Jo=6.67 Гц), 7.38, 7.63 (оба м, по 2 H, 3 H, Ph), 8.38 (д, 2 H, H(5'), H(5'), 3Jo=7.20 Гц); 8.47 (д, 1 H, H(7), 3Jo=6.13), 8.71 (с, 1 H, H(4)); 8.92 (уш.с, 2 H, NH2). Найдено, (%): C, 57.57; H 3.99; N 17.70. C19H14N5O5Cl. Вычислено, (%):C, 57.66; H 3.57; N 17.69.
Метод 2. Смесь 0.15 г (0.50 ммоль) 3-нитро-2-оксо-1-фенил-5-хлор-1,2-дигидро-1,6-нафтиридина (4) и 0.05 г (0.50 ммоль) 4-аминопиридина в 15 мл ацетонитрила кипятили 86 ч. Контроль ТСХ. Осадок при кипении не растворяется. После охлаждения реакционной массы до 20°C осадок отфильтровали, промыли ацетонитрилом. Получили 0.14 г (72%) аналитически чистого образца 2. Температура плавления не дает депрессии с образцом, полученным по методу 1.
Пример 3
Изучение активности синтезированных соединений in vivo
Для изучения активности синтезированных соединений in vivo применялась одна из самых используемых методологий изыскания и оценки активации когнитивных функций - улучшение или облегчение выработки УРПИ (условный рефлекс пассивного избегания) у животных. Со времени исследования когнитивных свойств ноотропила и до сих пор пассивное избегание (УРПИ) используется чаще, чем другие поведенческие процедуры для изучения и скрининга лекарств с эффектом на процессы обучения и памяти на грызунах. УРПИ используется для исследования действия лекарств на обучение (при введении тестируемого вещества до тренировочной сессии), на сохранение или удержание в памяти (при введении веществ после тренировки) и на извлечение информации из памяти (введение веществ до тестирования памяти). Метод также используется для изучения и тестирования веществ на моделях нарушения обучения и памяти, обусловленного экспериментальными дисфункциями мозга (холинергической, ГАМК-ергической, вызванной холинергическим токсином AF64A), при алкоголь-бензодиазепиновой, электрошоковой, гипоксической, возрастной амнезиях, ингибировании синтеза белка и др. [4-6].
Таким образом, наряду с другими современными поведенческими методиками (оперантные, лабиринтные и др.) исследование методом УРПИ направлено на изучение и скрининг потенциальных препаратов, которые могут применяться при когнитивных расстройствах вследствие нейродегенеративных заболеваний у животных (болезнь Альцгеймера, мультиинфарктное слабоумие, болезнь Паркинсона, хорея Геттингтона, эпилепсия, множественный склероз и др.).
Поскольку в нейрохимические механизмы памяти и обучения вовлечена холинергическая нейромедиаторная система мозга, на первом этапе важно проведение изучения влияния отобранных соединений на рецепторы ацетилхолина никотинового типа.
Среди исследований, посвященных применению методологии УРПИ для изучения активации когнитивных функций, отметим также работы [7-13].
В результате проведенных исследований установлено, что заявляемые агенты проявляют мнемотропные свойства, что позволяет использовать их в плане создания препаратов для лечения расстройств когнитивных функций.
Сравнительное изучение особенностей влияния соединений 1 и 2 на обучение и память мышей в тесте условной реакции пассивного избегания (УРПИ) на модели амнезии, вызванной введением блокатора центральных холинорецепторов скополамина (Скоп.).
Исследования проведены на 470 мышах-самцах массой 20-22 г, по 20 животных на дозу. Обучение мышей УРПИ проводили по методу step down [1], в камере с электродным полом и площадкой для избегания. Параметры электрического раздражения для животного при сходе с площадки безопасности составляли 50 в/в течение 3-5 с. Критерием обучения и памяти являлось удержание животного на площадке в течение 1 минуты при тестировании через 2 и 24 часа после обучения.
Дефицит обучения создавали введением за 15 минут до обучения скополамина (1,0 мг/кг, в/б) и сокращением числа обучающих сессий у животных до двух вместо пяти (недотренированность).
Сохранение мнемотропного действия соединений в условиях дефицита обучения оценивали по количеству животных в группе (в %), удерживающихся на площадке безопасности (с иммобилизацией).
Для оценки влияния на различные фазы формирования памяти (фиксация, консолидация и воспроизведение) исследуемые соединения вводили непосредственно перед обучением (до скополамина) и сразу после обучения. Исследуемые соединения вводили внутрибрюшинно по двум схемам: первая - соединения в дозах 0,01-0,1 и 1,0 (или 3,0) мг/кг, за 40 мин до обучения и соответственно за 5 мин до скополамина, вторая - соединения в тех же дозах сразу после обучения. Контроль проводили параллельно в каждой серии экспериментов: одна контрольная группа вместо исследуемых веществ и скополамина получала физиологический раствор, вторая контрольная группа - скополамин по соответствующей схеме и в тех же обьемах.
Доза исследуемого вещества считалась эффективной, когда число положительных реакций значительно отличалось от реакций животных, которым вводили физиологический раствор и скополамин. Статистический анализ проводили с достоверностью различий от отрицательного контроля при p<0,05.
Как показали результаты исследований, обучаемость после 2-й тренировочной сессии у контрольных животных составляет в среднем 80% и не изменяется существенно при тестировании через 2 и 24 часа. Введение центрального холиноблокатора скополамина привело к снижению этого показателя в среднем до 28%, что свидетельствует о комбинированном действии препарата (амнезии) и недотренированности.
Исследуемые вещества 1 и 2 улучшали обучение и память экспериментальных животных в условиях скополаминовой амнезии. При этом существенных различий в эффективности при тестировании обучения и памяти через 2 и 24 часа не отмечалось. Соединения обладали максимальным эффектом у животных в весьма низкой дозе, 0,01 мг/кг и несколько менее выраженным - в дозах 0,1 и 1,0 мг/кг. Введение соединений до обучения и непосредственно после обучения существенно не изменило выраженности мнемотропного эффекта у животных.
| Таблица 1 | ||||
| Когнитивная активность и острое токсическое действие соединений формул 1 и 2 | ||||
| Исследуемые соединения | Дозы, мг/кг, в/б | Кол-во животных с УРПИ (%) | Острая токсичность в/б, мг/кг | Терапевтическая широта ЛД50/МЭД |
| Соед 1 | 0,01 | 90,0 | 15,3±2,6 | 1530 |
| 0,1 | 80,0 | (11,7-21,0) | ||
| 1,0 | 60,0 | P<0,05 | ||
| 10,0 | 50,0 | |||
| Соед 2 | 0,01 | 60 | 107,7±14,1 | 10770 |
| 0,1 | 80 | (84,5-137,3) | ||
| 1,0 | 70 | P<0,05 | ||
| 10,0 | 60 | |||
| Скополамин | 1,0 | 35 | - | - |
Таким образом, проведенные исследования показали способность соединений оказывать выраженное стимулирующее действие на процессы обучения и памяти у животных. Показано, что все соединения оказывают стимулирующее влияние как на процесс фиксации памятного следа, так и консолидацию или хранение информации.
Кроме того, представляется вероятным создание на их основе новых оригинальных лекарственных препаратов, положительно воздействующих на улучшение памяти и способность к обучению.
Список литературы
1. Цинь Д. В мире науки. 2007, №11, с.18-25.
2. Бачурин C.O. Вопросы медицинской химии. 2001, №2, 1-41.
3. Граник В.Г. Метаболизм экзогенных соединений. М.: Вузовская книга, 2006.
4. Nabeshima Т. - Ameliorating Effects of Nefiracetam (DM-9384) on Brain Dys-function // Drugs of Today, 1994, 30(5), 357-379.
5. Heise G.A. - Behavioral Methods for Measuring Effects of Drugs on Learning and Memory in Animals // Medicinal Research Review, 1984, 4, 535-558.
6. Sato T., Ishida T., Tanaka К. et. al. - Ameliorative and Exacerbating Effects of [pGlu4, Cyt6] AVP(4-9) on Impairment of Step-Through Passive Avoidance Task Performance by Group II Metabotropic Glutamate Receptor-Related Drugs in Mice // J.Pharmacol Sci, 2005, 97, 437-442.
7. Рябова С.Ю., Алексеева Л.М., Расторгуева H.A., Лисица Е.А., Папахин Д.М., Паршин В.А., Граник В.Г. Новый способ получения производных [1,4]диазепино[6,5-b]индола. Изв. Академии наук, Серия химическая, 2006, №12, стр.2193-2199.
8. Возякова Т.И., Алексеева Л.М., Паршин В.А., Калинкина М.А., Граник В.Г. Синтез и фармакологическое изучение производных 2,3,4-триаминопиридинов. Хим. фарм. журн., 2006, №12, 8-12.
9. Андреева Н.И., Головина С.М., Паршин В.А., Машковский М.Д. Новые данные о психофармакологических свойствах антидепрессанта азафена. Хим. фарм. журн., 1997, №3, 10-13.
10. Camps P., Munoz-Torrero D. Mini Reviews in Medicinal Chemistry, 2002, v.2, p.11.
11. Hsu R.S., Shutske G.M., Dileo E.M., Chesson S.M., Linville A.R., Allen R.C Drug. Metab. Disposit, 1990, v.18, №5, p.779.
12. Rohawski M.A., Wenk C.L. CNS Drug Reviews, 2003, v.9, №3, p.275-308.
13. Cumin R., Bandle E.F., Gamzu E. and Haefely W.E. // Psychopharmacology (Berl.), 1982. - V.78 - P.104-111.
1. Агент, проявляющий свойства активатора когнитивных функций, характеризующийся тем, что он представляет собой 1,3-диметил-5-(пиридил-4-амино)метиленбарбитуровую кислоту формулы (1)
2. Агент, проявляющий свойства активатора когнитивных функций, характеризующийся тем, что он представляет собой 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидронафтиридинил)пиридиния хлорид формулы (2)