Иммуногенная композиция, содержащая чужеродные антигены на поверхности сферических носителей, полученных при термической денатурации спиральных вирусов
Иллюстрации
Показать всеИзобретение относится к медицине, биологии, нанотехнологии, и касается получения иммуногенных композиций. Предложенная иммуногенная композиция содержит 1) платформу-носитель, в качестве которой используют сферические частицы, полученные путем термической структурной перестройки вирусов группы вируса табачной мозаики (тобамовирусы) или других растительных вирусов со спиральной структурой и 2) чужеродные белки/антигены/эпитопы, связанные с поверхностью сферических частиц. Предложенные композиции биологически безопасны, стабильны. При этом чужеродный антиген/эпитоп в составе комплекса со сферическими частицами проявляет высокую иммуногенность и сохраняет антигенную специфичность. 13 ил.
Реферат
Область применения изобретения.
Изобретение относится к области получения иммуногенных комплексов на основе использования в качестве платформ-носителей - сферических частиц (СЧ), продуктов термической денатурации спиральных вирусов, включая вирусы группы табачной мозаики (ВТМ) (тобамовирусы) и другие вирусы растений со спиральной структурой. Указанные платформы-носители представляют собой наночастицы с диаметром до 100 нм (СНЧ) и микрочастицы с диаметром до 800 нм и более (СМЧ), получаемые в процессе термической денатурации, структурной перестройки частиц нативного вируса.
Задача настоящего изобретения состояла в создании иммуногенных композиций на основе связывания различных целевых объектов (в частности, чужеродных антигенов/эпитопов) с поверхностью СЧ-носителей. Указанные СЧ могут применяться для создания композиций с чужеродными целевыми антигенами, антигенными детерминантами (эпитопами), ферментами, антибиотиками, синтетическими полимерами, металлами и другими объектами.
Указанные композиции предназначены для использования медицине, ветеринарии, иммунологии, вирусологии, безвирусном сельском хозяйстве и технике (последнее при необходимости создания бионеорганических комплексов или комплексов с синтетическими полимерами на основе СЧ-платформ).
В настоящем изобретении были созданы композиции, представляющие собой иммуногенные комплексы СЧ-платформ с чужеродными белками или эпитопами ряда вирусов. Показано, что все сферические частицы-платформы покрыты молекулами чужеродных белков/эпитопов упакованных на поверхности СЧ. Указанные комплексы могут быть использованы для получения вакцинных и диагностических препаратов для борьбы с вирусными и заболеваниями и болезнями иной природы.
Настоящее изобретение имеет прямое отношение к производству вакцинных препаратов и диагностических антител, открывая возможность быстрой сборки in vitro антигенно активных иммуногенных комплексов, состоящих из СЧ-платформ, поверхность которых связана с чужеродными антигенами/эпитопами целевого патогена.
Терминология
Технические и научные термины, использованные в описании изобретения, имеют тот же смысл и значение, которые обычно применяются в соответствующих областях науки и техники.
Термины «платформа, носитель» относятся к описываемым в настоящем изобретении сферическим частицам.
Термин «сферические наночастицы» (СНЧ) относится к сферическим частицам размером до 100 нм. Термин «сферические микрочастицы» (СМЧ) относится к сферическим частицам большего размера (800 нм и более).
Термин «сферические частицы» (СЧ) относится к обоим типам сферических частиц.
Термины «гетерологичный», «чужеродный» (например, «гетерологичные, или чужеродные белки» - это белки, антигенно неродственные белкам СЧ, использованные при создании комплекса (композиции) с СЧ носителем.
Чужеродные белки обычно (но не обязательно) закодированы не в геноме вируса, из которого получают СЧ, а в геноме другого вируса или альтернативного патогена, отличного от вируса (бактерии, грибы и т.п.).
Термин «антиген», используемый в изобретении, относится к чужеродным (целевым) белкам, которые применяются для образования нанокомплексов СЧ-белок.
Используемые в изобретении термины «эпитоп» и «антигенная детерминанта» относится к короткой области (участок, в настоящем изобретении, включающий в себя 12-32 аминокислотных остатка) чужеродного белка, применяемого для образования нанокомплекса СЧ-эпитоп. В принципе, размер эпитопа может значительно варьировать.
Термин «иммуногенный», используемый в изобретении, относится к способности СЧ индуцировать продукцию антител у мышей, других животных и человека.
Уровень техники.
Известны, так называемые, аффинно-конъюгированные антигенные системы. Такие системы включают: 1) химерные вирусы с БО, несущим участки связывания чужеродных целевых белков, антигенов, рецепторов, антител, специфически узнаваемых модифицированным чужеродным белком. В этих случаях ген вирусного белка оболочки генетически модифицировали в составе полногеномной копии или в изолированном гене БО введением вставок или делеций для получения афинных участков связывания целевых субстанций белковой природы. Например, вводили реактивный лизин в N-концевой участок БО ВТМ для связывания биотина с вирусным капсидом. В независимых опытах получали целевой белок, ковалентно связанный со стрептавидином. В результате специфического авидин-биотин взаимодействия получали частицы вируса, декорированного целевым белком-антигеном (Smith M.L., Lindbo J.A., Dillard-Telm S., Brosio P.M., Lasnikk A.B., McCormick A.A., Nguen L.V., Palmer K.E., 2006. Modified tobacco mosaic virus particles as scaffords for display of protein antigens for vaccine applications. Virology 348, 475-488. Известен биологически активный комплекс, состоящий из ВТМ, соединенного с водорастворимым полипептидом (US Patent, 20090053261). В этом комплексе используют нативный ВТМ с ковалентно связанным биотином. При этом в качестве целевого используют полипептид, содержащий ковалентно связанный авидин. При смешении вышеназванных компонентов в водной среде образуется единый биологически активный комплекс за счет взаимодействия биотиновых и авидиновых групп. Недостатком известного вакцинного препарата является сложность и высокая стоимость процедуры получения платформ ВТМ-биотин и эпитоп-авидин, а также его относительно невысокая биологическая активность US Patent Pub. N. 2009/0053261 A1, Feb.26, 2009; Lindbo JA, Palmer KE, Owensboro KY, Smith ML. Эта система включает этап аффинной сборки композиций на основе взаимодействия химически модифицированного рекомбинантного вируса-носителя и модифицированного чужеродного антигена. Несмотря на существенную разницу, эта система относительно близка заявляемому изобретению и может быть рассмотрена в качестве прототипа. Аффинно-конъюгированные антигенные системы рассматриваются также в более позднем патенте (Leclerc, D. 2010, Immunogenic affinity-conjugated antigen systems based on Papaya Mosaic Virus and used thereof. US Patent Application Publication, 2010/0047264 A1, Feb.25). (Leclerc, D.2010, Immunogenic affinity-conjugated antigen systems based on Papaya Mosaic Virus and used thereof. US Patent Application Publication, 2010/0047264 A1, Feb.25). Рассмотренная выше аффинно-конъюгированная антигенная система включает этап аффинной сборки композиций на основе взаимодействия химически модифицированных вируса-носителя и чужеродного антигена. Несмотря на существенную разницу, эта система относительно близка заявляемому изобретению и может быть рассмотрена в качестве прототипа.
Недостатки применения аффинно-конъюгированных систем: 1) относительно невысокая биологическая активность; 2) сложность и многоступенчатость процедуры, включающей: а) приготовление модифицированного биотином или стрептавидином (66 кДа белок) БО вируса и б) биотин- либо стрептавидин-меченного целевого белка/антигена с последующей, в) обязательной трехстадийной очисткой, то есть отделения биотин-меченного белка от модифицированных стрептавидином частиц и выделение комплекса «вирус-стрептавидин-биотин-белок».
3) Пользование этой системой осложняется генетической нестабильностью и другими трудностями, характерными для накопления химерных вирусов, рассмотренными выше.
4) Другим недостатком аффинно-конъюгированных антигенных систем является отсутствие универсальности - строгая специфичность, обусловленная специфичностью взаимодействия двух ее компонентов: модифицированной платформы-носителя (БО вируса) и модифицированного целевого белка (например, антигена). В определенных опытах высокая специфичность взаимодействия носителя с целевым белком полезна, облегчая очистку создаваемой композиции от ненужных примесей. Однако в настоящем изобретении, то есть при условиях отсутствия примесей за счет применения высокой степени очистки обоих компонентов композиции, специфичность должна резко ограничить возможности носителя (СЧ) одним типом целевого белка/антигена. Ниже показана способность СЧ образовывать композиции с различными структурно и функционально неродственными белками.
5) В отличие от прототипа, будучи раз получены, СЧ могут быть использованы для адсорбции разнообразных ЦБ. Обстоятельство, что, в отличие от вирусных частиц, поверхность СЧ обладает высокой сорбционной емкостью в отношении веществ различной химической природы. Это свойство СЧ иллюстрируется примерами 2, 3, 4, 5 настоящего изобретения. В силу этой особенности СЧ, способ приготовления композиции на их основе заключается в простом смешивании СЧ и ЦБ в соотношении, обеспечивающем образование монослоя ЦБ на поверхности СЧ. Упоминаемая в ряде примеров фиксация ЦБ на поверхности СЧ с помощью формальдегида имеет целью повышение стабильности композиции при ее применении для иммунизации. Таким образом, важным результатом изобретения является получение универсальных носителей (платформ) для создания различных комплексов и иммуногенных композиций.
Известно, что свободные от РНК вирусоподобные мультисубъединичные наночастицы (ВПЧ), несущие на своей поверхности чужеродные эпитопы, могут быть получены при полимеризации химерных субъединиц БО ("БО-чужеродный эпитоп") либо путем генетической модификации полноразмерного вирусного генома, содержащего ген белка оболочки, объединенный с чужеродным эпитопом. Результатом практической реализации этих принципов является создание химерных вирусных частиц, несущих на своей поверхности в качестве целевого пептида антигенную детерминанту (эпитоп) патогена либо иной функционально активный полипептид (McCormick А.А. and Palmer К.Е. (2008) Genetically engineered Tobacco mosaic virus as nanoparticle vaccines. Expert Rev Vaccines. 7(1), 33-41; Steinmetz N.F., Lin Т., Lomonossoff G.P. and Johnson J.E. (2009) Structure-based engineering of an icosahedral virus for nanomedicine and nanotechnology. Curr. Top. Microbiol. Immunol. 327, 23-58; Denis, N.Majeau, E.Acosta-Ramirez, C.Savard, M.-C. Bedard, S. Simard, K.Lecours, M.Bolduc, C.Pare, B.Willems, N.Shoukry, P.Tessier, P.Lacasse, A.Lamarre, R.Lapointe, C.L.Macias, and D. Leclerc (2007) Immunogenicity of papaya mosaic virus-like particles fused to a hepatitis С virus epitope: evidence for the critical function of multimerization. Virology 363, 59-68;. Turpen H.T. et al. US Patent 5977438, Nov. 1999. Production of peptides in plants as viral coat protein fusions; Leclerc. US Patent 7641896 B2, Jan.5 2010 Adjuvant viral particle; Werner S. et al. International Patent Application PCT/EP2006/009029 (WO/2007/031339). Следует отметить, что количество молекул чужеродного белка, присоединенных к индивидуальной частице ВТМ, весьма невелико (S.Werner, S.Marillonnet, G.House, V.Klimyuk and Yu. Gleba (2006) Immunoabsorbent nanoparticles based on a tobamovirus displaying protein A. Proc. Natl. Acad. Sci. USA 103 (47), 17678-17683).
Аннотация
Важно подчеркнуть, что во всех случаях, когда генетически модифицированные вирусы применяются в качестве платформы, используемой для получения вакцинных или других комплексов, морфология и общая архитектура нативного вируса остается неизменной. Другими словами, природная оболочка вируса (капсид) служит в качестве частицы-платформы, созданной в этом случае химерным БО.
В отличие от рассмотренных выше примеров, в настоящем изобретении для получения антигенно активных иммуногенных композиций и связывания с их поверхностью чужеродных антигенов/эпитопов применялись указанные СЧ носители (схемы на фиг.1-2), образуемые в результате термической денатурации и структурной перестройки ВТМ в СЧ. Для получения СЧ исходный раствор вируса разводили до нужной концентрации и распределяли по 50 мкл в полипропиленовых тонкостенных пробирках (для ПЦР) на 0,5 мл. Чтобы предотвратить испарения раствора (а следовательно, изменение [увеличение] концентрации вируса во время термической обработки), на поверхность раствора вируса наносили 30 мкл минерального масла. Далее, пробирки помещали в ячейки термоциклера «Терцик» (ДНК-Технология, Россия) и запускали программу, регулирующую температуру в каждой ячейке.
В изобретении показано, что СЧ являются перспективными платформами, обладая преимуществами для сборки иммуногенных комплексов in vitro (примеры 2-5 и фиг.3-6 и 8). Настоящее изобретение является первым, представляющим СЧ в качестве наночастиц-платформ для создания иммуногенных композиций.
Описание изобретения. Задача настоящего изобретения состояла в создании биологически активных композиций, состоящих из вышеуказанных сферических частиц (СЧ-платформ), способных ассоциировать с различными целевыми объектами, в частности, связывать чужеродные антигены/эпитопы с поверхностью указанных СЧ. В соответствии с этим аспектом настоящего изобретения, мы показали, что несколько типов антиген/эпитопов разного происхождения способны формировать антигенно активные и иммуногенные композиции с СЧ-носителем, включая 1) белок оболочки X вируса картофеля (фиг.3, Пример 2), 2) N-терминальный эпитоп М2е трансмембранного белка М2 вируса гриппа А человека (фиг.4, Пример 4), 3) эпитоп гликопротеида Е1 вируса краснухи (фиг.5, Пример 3), 4) тетраэпитоп гемагглютинина (НА) Н5 вируса гриппа А человека (фиг.6), 5) эпитоп 12 белка оболочки вируса оспы слив (фиг.8, Пример 5).
Комплексы «СЧ-антиген/эпитоп» стабилизировали с применением 0,05% формальдегида (ФА). Данные в пользу необходимости применения ФА при получении композиций получены на примере эпитопов вируса оспы (шарки) слив (ВОС) (потивирус) (фиг.7-8, Пример 7).
Для получения композиции с СЧ использовали рекомбинантный белок 1N, включающий БО ХВК с делегированным N-концом и 10-членный эпитоп БО ВОС (фиг.7 и 8). В изобретении показано, что иммуногенность комплекса «СЧ+антиген/эпитоп» весьма высока, однако она значительно возрастает после стабилизации комплекса обработкой формальдегидом. В результате обработки комплексов ФА титр антисыворотки составлял около 1:1000,000 (см. фиг.10 и Пример 7).
Важно, что поверхность всех СЧ вовлеченных в опыт была покрыта антигеном/эпитопами, использовавшимися в опыте. Последнее следует, в частности, из фиг.3 и фиг.6 и указывает на высокую эффективность связывания антигенов при сборке иммуногенных композиций на основе СЧ. Указанные композиции, состоящие из СЧ-платформы и чужеродных антиген/эпитопов, связанных с поверхностью СЧ-платформы, были иммуногенны и антигенно активны. Связанные с поверхностью СЧ-платформ чужеродные антиген/эпитопы специфично реагировали с антителами к соответствующему антигену/эпитопу, свидетельствуя о том, что специфичность связанных с СЧ антиген/эпитопов сохраняется в составе нанокомпозиции.
Результаты, представленные в настоящем изобретении, указывают на возможность использования СЧ-платформ для сборки in vitro антигенно активных иммуногенных комплексов-нановакцин. Композиции из СЧ, несущих на своей поверхности чужеродные эпитопы предоставляет ряд преимуществ в сравнении с аттенуированными, химически инактивированными и субъединичными вакцинами:
(i) Указанный выше подход исключает возможность рекомбинаций и реверсии патогенов.
(ii) Вакцины, полученные описанным выше способом, на основе термоденатурации вирусов растений, биологически безопасны, так как растения и животные не имеют общих патогенов.
(iii) Процедура получения СЧ-платформ основана на нагревании вируса при 94-98°С, то есть не требует дополнительной стерилизации частиц-платформ.
(iv) Вирус-донор СЧ (в частности, ВТМ) легко доступен, так как аккумулируется в листьях зараженных растений в очень больших количествах.
(v) Описанные в изобретении антигенно активные иммуногенные комплексы могут также применяться для производства дешевых диагностических моноклональных антител и в качестве диагностических препаратов для выявления инфекционных заболеваний человека и животных.
(vi) Применение стабилизированных формальдегидом иммуногенных комплексов сферической формы упрощает технологию получения и применения вакцинных или диагностических препаратов.
(vii) Создание метода «блочной» сборки иммуногенных комплексов вне клетки на платформе СЧ, несущих на своей поверхности эпитопы патогена позволит принципиально упростить и ускорить процесс производства вакцинных и диагностических препаратов различной природы для использования в медицине, ветеринарии и растениеводстве.
(viii) Настоящее изобретение позволяет осуществлять «сборку» иммуногенных комплексов, содержащих более одного типа чужеродных антигенов, то есть получать поливалентные антисыворотки.
Таким образом, важным результатом изобретения является получение универсальных носителей (платформ) для создания различного вида комплексов и иммуногенных композиций.
Предлагаемые биологически активные комплексы не описаны в литературе и являются новыми, что существенно расширяет ассортимент биологически активных комплексов.
Краткое описание чертежей
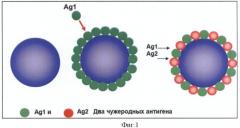
Фиг.1. представляет собой схематическое изображение одного или двух модельных антигенов (Ag1 and Ag2), связанных с СЧ-платформой
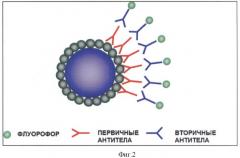
Фиг.2. представляет собой схематическое изображение детектирования посредством флуоресцентной микроскопии антигена Ag1, связанного с поверхностью СЧ-Ag1 комплекса. Показано, что первичные антитела реагируют с молекулами Ag1 на поверхности наноплатформы СЧ.
Фиг.3 иллюстрирует, что поверхность всех СЧ-платформ покрыта молекулами БО ХВК, (а) меченными флуоресцеинизотиоцианатом (ФИТЦ); (б) контроль, проходящий свет. Размер метки 3 мкм. Конфокальная микроскопия.
Фиг.4 иллюстрирует, что дегидрофолатредуктаза, слитая с М2е-эпитопом (23 аминокислоты) матриксного белка М2 вируса гриппа А человека (DHFR-M2e), связывается с поверхностью СЧ. Эпитоп М2е выявляется мышиными антителами к М2е и вторичными куриными антимышиными антителами, меченными флуорофором Alexa 488 зеленым. Размер метки 5 мкм. Флуоресцентная микроскопия.
Фиг.5 иллюстрирует, что тетраэпитоп белка Е1 вируса краснухи, связанный с поверхностью СЧ-платформы, выявляется первичными мышиными антителами к белку Е1 и вторичными куриными антимышиными антителами, конъюгированными с флуорофором Алекса 488 зеленым. Размер метки 3 мкм. Флуоресцентная микроскопия.
Фиг.6 иллюстрирует, что поверхность всех СЧ-платформ покрыта тетраэпитопами, состоящими из 4-х консервативных моноэпитопов гемагглютининина (НА) вируса гриппа А человека. Детекция первичными мышиными антителами к НА и вторичными куриными антимышиными антителами, конъюгированными с флуорофором. Контроль, проходящий свет (а); флуоресцентная микроскопия (б). Размер метки 3 мкм.
Фиг.7 иллюстрирует структуру двух рекомбинантных белков БО ХВК, слитых с двумя разными эпитопами БО ВОС: 1) 12-членником VNTNRDRDVDAG (Р2) и 2) 10-членником SMLNPIFTPA (1N), содержащих 6 гистидинов (6HIS) и эпитоп из БО ВОС на С-конце. Обозначение IEGR соответствует сайту действия протеиназы Ха при высвобождении «эпитопа-БО».
Фиг.8 иллюстрирует, что экспрессированный в бактериях 12-членный эпитоп вируса оспы сливы (ВОС 12), слитый с белком оболочки ХВК, связывается с поверхностью СЧ и выявляется с помощью первичных кроличьих антител к (ВОС 12) и вторичных ослиных антикроличьих антител, конъюгированных с флуорофором Alexa 555 красным. Размер метки 5 мкм. Флуоресцентная микроскопия.
Фиг.9 представляет собой график, иллюстрирующий результаты определения титра мышиных антисывороток к ВТМ и к СЧ и демонстрирующий более высокую иммуногенность СЧ по сравнению с частицами нативного ВТМ. Твердофазный иммуноферментный анализ (ИФА) (Пример 6).
Фиг.10 иллюстрирует иммуногенную активность композиции «СЧ+IN БО ВОС» (белок 1N содержит 10-членный эпитоп БО ВОС см. Фиг.7) и значительный рост этой активности при стабилизации композиции формальдегидом. Сравнение титров мышиных антисывороток к эпитопу ВОС в непрямом ИФА: 1) антисыворотка, полученная при иммунизации мышей рекомбинантным белком 1N; 2) антисыворотка, полученная при иммунизации СЧ, на поверхность которых белок 1N был помещен на основе электростатических взаимодействий; 3) антисыворотка, полученная при иммунизации мышей антигенными комплексами «СЧ-белок 1N», стабилизированных формальдегидом; контроль - нормальная мышиная сыворотка. Антисыворотку титровали относительно ВОС с концентрацией 10 мкг/мл. Ось-Х - разведение антисыворотки; Ось-Y - оптическая плотность при длине волны 405 нм.
Фиг.11 иллюстрирует иммуногенную активность композиции «СЧ+ БО ХВК», при стабилизации композиции формальдегидом и представляет собой график, на котором показаны результаты определения количества специфических антител в мышиных антисыворотках при иммунизации животных антигеном самим по себе или антигеном, фиксированным на поверхности СЧ различного размера.
Фиг.12 представляет собой график, иллюстрирующий результаты определения титра мышиных антисывороток к вирусу, полученных при иммунизации животных БО ХВК в смеси со СЧ или фиксированным на их поверхности. ИФА.
Фиг.13 представляет собой график, иллюстрирующий влияние дозы СЧ на интенсивность стимуляции иммунного ответа к антигену. ИФА.
ПРИМЕРЫ
Пример 1
Продукция белков/эпитопов в бактериальных клетках. В настоящем изобретении рекомбинантные антигены/эпитопы, экспрессированные в бактериальных клетках, были использованы для связывания с поверхностью СЧ. Все манипуляции с рекомбинантными ДНК проводились по стандартной методике (Sambrook J., Ftitsch E.F. and Maniatis Т. (1989) Molecular cloning: A laboratory Manual, 2nd edn. Cold Spring Harbor Laboratory, Cold Spring Harbor, NY). Для клонирования созданных конструкций и для их суперэкспрессии были использованы штаммы Е.coli DH5ot и M15[pREP4] соответственно. Рекомбинантные конструкции, экспрессирующие слитые с (His)6 - пептидом белки были получены путем клонирования в плазмидный вектор pQE ПЦР-фрагментов. Рестрикционные ПЦР-фрагменты были лигированы по соответствующим сайтам в экспрессирующий вектор, как было описано ранее (Ivanov К.I., Ivanov Р.А., Timofeeva Е.К., Dorokhov Yu.L. and Atabekov J.G. (1994). The immobilized movement proteins of two tobamoviruses form stable ribonucleoprotein complexes with full-length viral genomic RNA. FEBS Lett. 346, 217-220). Клетки Escherichia coli штамм M 15, трансформированные рекомбинантным вектором выращивали в культуральной жидкости при 37°С до OD600, равным 0.8-0.9. Экспрессию рекомбинантных белков индуцировали добавлением 1 мМ IPTG, культуру клеток растили дополнительно 3 часа при +37°С. Хроматографическую очистку (Н)6-рекомбинантных белков на Ni2+-нитрилотриацетатной агарозе (Ni-HTA) проводили согласно протоколу производителя (QIAGEN).
Пример 2
Образование комплекса «СЧ-ФИТЦ-меченный белок оболочки X вируса картофеля»
Белок оболочки (БО) Х-вируса картофеля (ХВК) выделяли обработкой вирусной суспензии в Трис-HCl буфере, рН 7.5 нейтральным солевым раствором LiCl, доводя его до конечной концентрации 2М, помещали на -20°С на ночь, центрифугировали при 10000 g. Супернатант диализовали против тридистилированной воды. Белок после диализа ультрацентрифугировали при 100,000 g. К 1 мг БО ХВК с концентрацией 1 мг/мл добавляли 18 мкг флуоресцеина изотиоцианата (ФИТЦ) и инкубировали 24 часа при 4°С, диализовали против воды для освобождения от не связавшейся флуоресцентной метки. Полученный белок, меченный ФИТЦ, использовали для образования комплекса с СЧ-носителем. Для этого 50 мкг СЧ инкубировали с 1 мкг белка в воде. Комплекс стабилизировали добавлением формальдегида до концентрации 0.05% (10 минут, 20°С). Связывание СЧ с БО фиксировали с помощью флуоресцентного микроскопа (LeicaDRMB), снабженного интегрированной камерой ORCAII-ERG2 (Hamamatsu, Japan).
Образование комплекса СЧ с ФИТЦ-меченным белком оболочки вируса X картофеля ХВК показано на фиг.3.
Пример 3
Образование комплекса «СЧ-носитель полиэпитоп А вируса краснухи»
Для образования комплекса с СЧ была использована антигенная детерминанта А гликопротеида Е1 вируса краснухи. Ниже приведена аминокислотная последовательность (32 аминокислотных остатка) эпитопа А гликопротеида Е1:
Область эпитопа А обозначена полужирным шрифтом.
Рекомбинантный белок (Мол. масса около 21-22 kD), содержащий на N-конце шесть аминокислотных остатков гистидина (His6) и представляющий собой четыре повтора эпитопа А (полиэпитоп А) Е1 гликопротеида был сконструирован на базе плазмиды pQE-BT-4A. Полиэпитоп А в составе комплекса с СЧ выявляли методом иммунофлуоресценции.
Комплекс СЧ-полиэпитоп А инкубировали при комнатной температуре 2 часа на покровных стеклах, предварительно обработанных поли-L-лизином. Для фиксации образцов их обрабатывали в течение 15 минут 4% параформальдегида при комнатной температуре, затем проводились три отмывки водой по 5 минут каждая. После отмывки образцы инкубировали в течение 30 минут в растворе, состоящем из 1% бычьего сывороточного альбумина (БСА), фосфатного буфера (PBS, состав: 7 мМ Na2HPO4, 1.5 мМ KH2PO4, рН 7.4, 137 мМ NaCl, 2.7 мМ KCl) и 0.05% Твин-20. Далее препараты инкубировали с первичными мышиными антителами к гликопротеиду Е1 вируса краснухи в течение 30 минут во влажной камере в PBS с 0.25% БСА и 0.05% твин-20. Контрольные образцы инкубировали в блокирующем растворе без добавления первичных антител. Не связавшиеся антитела отмывали раствором для отмывки (PBS с 0.25% БСА и 0.05% Твин-20) на качалке 3 раза по 5 минут. Связывание первичных антител с антигенными комплексами детектировалось при помощи вторичных противомышиных антител, конъюгированных с флуорофором Alexa-488 (Molecular Probes, Eugene, OR). Co вторичными антителами инкубацию проводили в течение 30 минут во влажной камере, от не связавшихся антител отмывались 3 раза по 5 минут в растворе для отмывки и один раз в PBS в течение 5 минут. После этого образцы заключали между покровными и предметными стеклами при использовании фотозащитной добавки 1,4 диазобицикло-[2,2,2]октана (DABCO), инкубировали 30 минут при +4°С. Полученные препараты анализировали при помощи флуоресцентного микроскопа (LeicaDRMB), снабженного интегрированной камерой ORCAII-ERG2 (Hamamatsu, Japan).
Образование комплекса СЧ с полиэпитопом А вируса краснухи продемонстрировано на Фиг.5.
Пример 4
Связывание СЧ-носителя с рекомбинантным белком ДГФР, слитым с эпитопом М2е вируса гриппа А.
Следующим для образовании комплекса «СЧ-эпитоп М2е» был использован рекомбинантный белок, состоящий из молекулы дегидрофолатредуктазы (ДГФР) слитой с М2е эпитопом вируса гриппа А человека длиной 23 аминокислотных остатка (J.Fan, X.Liang, М.Horton, Н.Perry, М.Citron, G.Heidecker, Т.Fu, J.Joyce, C.Przysiecki, P.Keller (2004) Preclinical study of influenza virus A M2 peptide conjugate vaccines in mice, ferrets, and rhesus monkeys. Vaccine 22, 2993-3003). Способность моноклональных антител, полученных против М2 белка (Mab) ослаблять репликацию вируса свидетельствует о том, что М2, а на самом деле внешний домен М2е, могут быть использованы в качестве мишени для получения вакцин (Tompkins S.M., Zhao Z-Sh., Lo, Ch-Yu., Misplon J.A., Liu T., Ye Z., Hogan R.J., Wu Zh., Benton K.A., Tumpey T.M. and Epstein S.L. (2007) Matrix Protein 2 Vaccination and Protection against Influenza Viruses, Including Subtype H5N1. EmergInfect Dis. 13, 426-435).
В представленном изобретении ДГФР служит носителем для М2е эпитопу (ДГФР-М2е).
Для того чтобы установить факт размещения (посадки) М2е пептида на поверхности СЧ был применен метод иммунофлуоресценции, схематически показанный на Фиг.1 и 2. Эпитоп М2е выявлялся мышиными антителами к М2е и вторичными куриными антимышиными антителами, меченными флуорофором Alexa 488 зеленым. Фиг.4 настоящего изобретения иллюстрирует, что М2е-эпитоп, связанный с СЧ сохранил свои антигенные свойства, и что использование рекомбинантного белка ДГФР-М2е, где ДГФР играет роль носителя, обеспечивает презентацию чужеродного целевого эпитопа (М2е) на поверхности сферических наночастиц.
Пример 5
Связывание с поверхностью СЧ комплекса «БО ХВК- эпитоп12-членник» (vntnrdrdvdag) вируса оспы слив (ВОС)
Эпитоп «12», длиной 12 аминокислотных остатков, белка оболочки вируса оспы (шарки) сливы (vntnrdrdvdag) (Fernández-Fernandez M.R., Martinez-Torrecuadrada J.L., Roncal F., Dominguez E., Garcia J.A. (2002) Identification of immunogenic hot spots within plum pox potyvirus capsid protein for efficient antigen presentation. J.Virol. 76, 12646-12653) был соединен с БО ХВК, и химерный белок Р2 «БО ХВК-эпитоп 12 ВОС» (см. Фиг.7) был экспрессирован в клетках Е. coli. Рекомбинантный белок «БО ХВК-эпитоп 12» был ковалентно соединен с поверхностью СЧ с помощью формальдегида, как указано выше. Для того чтобы выявить связывание эпитопа «12» вируса оспы сливы методом конфокальной флуоресцентной микроскопии были использованы первичные кроличьи антитела к БО вируса оспы сливы и вторичные ослиные антикроличьи антитела, конъюгированными с флуорофором Alexa 555 красным (Фиг.8).
Ген химерного белка «БО ХВК-эпитоп «12» ВОС был сконструирован на основе плазмиды pQE30. Полужирным шрифтом отмечены - 6His, подчеркнут - сайт гидролиза протеазы фактор Ха, курсивом и рамкой - антигенная детерминанта - эпитоп 12 вируса оспы сливы.
Аминокислотная последовательность химерного белка «БО ХВК- эпитоп 12 вируса оспы сливы»:
Методом флуоресцентной микроскопии показано, что поверхность СЧ покрыта чужеродным эпитопом ВОС 12 (Фиг.8).
Пример 6.
Сравнение иммуногенности СЧ и нативного ВТМ.
Мышей линии BALB/c в возрасте 6-8 недель иммунизировали внутрибрюшинно СЧ или вирионами ВТМ в дозе 100 мкг антигена на 1 инъекцию. Проведено 3 инъекции с двухнедельным интервалом между ними. При первой инъекции антиген вводили в смеси с равным объемом полного адъюванта Фрейнда, при 2 последующих - с равным объемом неполного адъюванта Фрейнда. Кровь, индивидуально от каждой мыши, брали из хвостовой вены через неделю после последней иммунизации. Кровь выдерживали 2 ч при комнатной температуре до формирования сгустка, помещали на ночь в холодильник и на следующий день сгусток отделяли центрифугированием 10000 g 10 мин. Полученную сыворотку использовали для определения титра антител к СЧ и к ВТМ. Титр определяли в пуле, полученном путем смешивания равных объемов антисывороток от каждого животного, с помощью непрямого метода иммуноферментного анализа (ИФА). На планшетах MaxiSorp (Nunc) сорбировали СЧ или ВТМ (6 мкг/мл в PBS: 0,05 М K2HPO4, 0,1 М NaCl, рН 7,4) в объеме 100 мкл на лунку. Планшеты выдерживали ночь в холодильнике, промывали PBST (PBS, 0,1% Твин 20, рН 7,4) 5 раз по 200 мкл на лунку и вносили тестируемые антисыворотки в двойных серийных разведениях, приготовленных на PBST, начиная с разведения 1/1000. В качестве отрицательного контроля использовали преиммунную мышиную сыворотку. Инкубировали 1 ч при 37°С на термостатируемом шейкере, промывали, как описано, и добавляли пероксидазный конъюгат (Promega) в рабочем разведении 1/20000, приготовленном на PBS, содержащем 0,5% бычьего сывороточного альбумина. Инкубировали 1 ч при 37°С на шейкере, промывали, как описано, и добавляли субстрат - ABTS с перекисью водорода в 0,05 М цитратно-фосфатном буфере рН 4,4. Оптическую плотность в лунках определяли на ридере Titerteck Multiscan при длине волны 405 нм через 20 мин после добавления субстрата. Титром антисыворотки считали ее последнее разведение, оптическая плотность в котором втрое превышала соответствующее значение преиммунной мышиной сыворотки. Данные, представленные на фиг.9, показывают, что титр антител к СЧ в 20 раз превышал титр антител к ВТМ.
Этот пример демонстрирует тот неочевидный факт, что СЧ обладают намного более высокой иммуногенностью, чем исходные частицы нативного ВТМ. Это обстоятельство имеет решающее значение для достижения цели настоящего изобретения. Известно, что для индукции гуморального иммунного ответа (синтеза антител) необходима кооперация В и Т-лимфоцитов, при которой рецепторы В-лимфоцитов распознают антиген, а Т-лимфоциты взаимодействуют с носителем. Известно также, что антительный ответ на антиген, присоединенный к носителю, прямо зависит от иммуногенности носителя. Таким образом, эффективность иммунизации (вакцинации) определенной композицией определяется не только иммуногенностью ЦБ, присоединенного к носителю, но и, главным образом, иммуногенностью самого носителя.
Пример 7
Иммуногенность композиции «СЧ-эпитоп 10-членник SMLNPIFTPA ВОС) возрастает при стабилизации комплекса формальдегидом.
В изобретении рассмотрена активность иммуногенной композиции, состоящей из частично делетированного с N-конца БО ХВК, слитого с эпитопом БО ВОС (см. 1N на Фиг.7). Была исследована возможность получения антител специфичных к эпитопу ВОС (SMLNPIFTPA), расположенного на N-конце рекомбинантного БО ХВК - 1N. Для иммунизации были использованы мыши линии BALB/c. В эксперименте было 4 группы мышей. Первую группу мышей иммунизировали раствором рекомбинантного белка 1N, Вторая группа мышей иммунизировали суспензией СЧ, на поверхность которых на основе электростатических взаимодействий был посажен рекомбинантный белок 1N. Электростатические взаимодействия между СЧ и рекомбинантным белком 1N могли оказаться нестабильными в физиологических условиях. В связи с этим, третью группу мышей иммунизировали антигенными комплексами, состоящими из СЧ и рекомбинантного белка 1N, дополнительно стабилизированных добавлением формальдегида. Количество рекомбинантного белка 1N во всех случаях составляло 28 мкг. Иммуногенный комплекс СЧ-АГ был образован при инкубации 100 мкг СЧ с 28 мкг рекомбинантного БО ХВК, несущего на N-конце эпитоп ВОС. В качестве контроля использовали раствор PBS. Были проведены 3 внутрибрюшинных иммунизации с двухнедельным интервалом между ними. Через неделю после последней иммунизации, полученную сыворотку использовали для определения титра антител к эпитопу ВОС с помощью метода непрямого ИФА.
Иммуногенность низкомолекулярного белка 1N была невелика (Фиг.10; 1N). Несколько более высокие титры антител удалось получить при иммунизации мышей СЧ, на поверхность которых путем электростатических взаимодействий был посажен белок 1N (Фиг.10; C4+1N).
Наиболее высокие титры были получены при иммунизации животных иммуногенными комплексами, стабилизированными формальдегидом. В этом случае титр антисывороток был значительно выше (Фиг.10; СЧ+1N (ФА) и составлял около 1: 1000,000. Это позволяет заключить, что формальдегид существенно повышал стабильность композиций, резко стимулируя их иммуногенность.
По видимому, в физиологических условиях комплексы СЧ-1N могли частично диссоциировать на СЧ и рекомбинантный белок 1N, что проявилось в заметном снижении титра сыворотки (Фиг.10).
Пример 8
Иммуногенность композиции «СЧ-БО ХВК».
Беспородных белых мышей иммунизировали внутрибрюшинно СЧ диаметром 100 или 500 нм, поверхность которых была покрыта монослоем антигена - БО ХВК. Доза СЧ составляла 500 мкг. Контрольную группу мышей иммунизировали по такой же схеме одним БО. Объем инъецируемой смеси составлял 0,5 мл на 1 животное. Каждая группа состояла из 5 животных. Проведено 3 иммунизации с двухнедельным интервалом между ними. Кровь, индивидуально от каждой мыши, брали из хвостовой вены через неделю после последней иммунизации. Кровь выдерживали 2 ч при комнатной температуре до формирования сгустка, помещали на ночь в холодильник и на следующий день сгусток отделяли центрифугированием 10,000 g 10 мин. Полученную сыворотку использовали для определения титра антител к БО.
Титр определяли в пуле, полученном путем смешивания равных объемов антисывороток от каждого животного, с помощью непрямого метода иммуноферментного анализа. На планшетах MaxiSorp (Nunc) сорбировали БО ХВК (6 мкг/мл в деионизованной воде) в объеме 100 мкл на лунку. Планшеты выдерживали ночь в холодильнике, промывали PBST (0,05 М K2HPO4, 0,1 М NaCl, 0,1% Твина 20, рН 7,4) 5 раз по 200 мкл на лунку и вносили тестируемые антисыворотки в двойных серийных разведениях, приготовленных на PBST, начиная с разведения 1/1000. В качестве отрицательного контроля использовали преиммунную мышиную сыворотку. Инкубировали 1 ч при 37°С на термостатируемом шейкере, промывали, как описано, и добавляли пероксидазный конъюгат (Promega) в рабочем разведении 1/20000, приготовленном на PBS, содержащем 0,5% бычьего сывороточного альбумина. Инкубировали 1 ч при 37°С на шейкере, промывали, как описано, и добавляли субстрат - ABTS с перекисью водорода в 0,05 М цитратно-фосфатном буфере рН 4,4. Оптическую плотность в лунках определяли на ридере Titerteck Multiscan при длине волны 405 нм через 20 мин после добавления субстрата. Титром антисыворотки считали последнее разведение, оптическая плотность в котором втрое превышала соответствующее значение преиммунной мышиной сыворотки.
Результаты определения титров мышиных антисывороток представлены на фиг.11. Эти результаты показывают, что СЧ разных размеров усиливают ИО на антиген, фиксированный на их поверхности. Иммунизация животных СЧ, покрытыми БО, приводит к пятнадцатикратному увеличению концентрации антител к БО ХВК в крови иммунизированного животного по сравнению с иммунизацией одним БО. Титр антител на 7 день после последней иммунизации составил 1/128000.
Пример 9
Образование антител к интактному вирусу при совместной иммунизации БО ХВК и СЧ
Антисыворотки к БО ХВК, полученные, как описано в примере 8, титровали методом ИФА на планшетах, покрытых интактным ХВК. На планшетах MaxiSorp (Nunc) адсорбировали ХВК (6 мкг/мл в PBS) в объеме 100 мкл на лунку. Остальные процедуры осуществляли, как описано в Примере 8.
Резуль