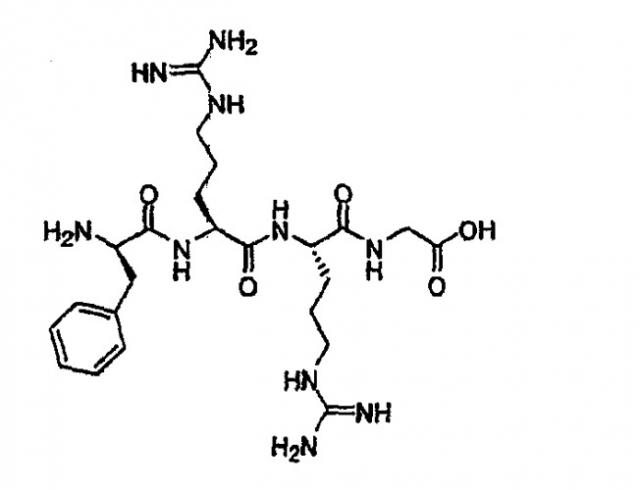
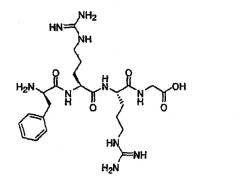
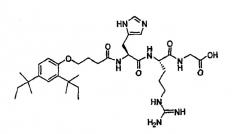
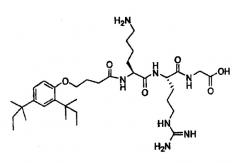
Аффинные лиганды, связывающие антитела
Иллюстрации
Показать всеОписан материал твердого носителя для выделения антител и их производных. На твердом носителе ковалентно иммобилизован аффинный лиганд, который содержит одну или несколько гидрофобных функциональных групп и одну или несколько катионных функциональных групп. По меньшей мере, одна гидрофобная функциональная группа отделена, по меньшей мере, от одной катионной функциональной группы расстоянием между связями от 5 Å до 20 Å. При этом лиганд имеет молекулярную массу не более 1000 Да, состоит из менее чем 5 остатков, обязательно содержащих структуру Х1-Х2-Х3. Указанная структура связана с твердым носителем линкером. Каждый из X1, Х2, Х3 выбирают из соответствующей группы соединений. Описаны также варианты твердого носителя со сходной структурой, но без линкера. Предложен также способ выделения антител или их производных на основе твердого носителя. Аффинная смола имеет емкость связывания более 5 мг моноклонального антитела на мл аффинной смолы и может найти применение в очистке антител и их производных. 4 н. и 9 з.п. ф-лы, 4 ил., 2 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к аффинным лигандам, ковалентно связанным с материалом твердого носителя, таким как полимерная матрица, и к их применению для очистки и/или выделения биологических молекул, таких как белки, в частности, антител, таких как моноклональные антитела. Аффинные лиганды содержат два различных домена или функциональных группы: (i) гидрофобный домен и (ii) катионный домен.
Уровень техники
Аффинная хроматография делает возможной селективную и обратимую адсорбцию биологических веществ, таких как моноклональные антитела, на комплементарном связывающем веществе, таком как аффинный лиганд, иммобилизованном на материале твердого носителя, помещенном в аффинную колонку.
Аффинные колонки часто содержат материал твердого носителя, обычно, пористую полимерную матрицу, к которой ковалентно присоединен соответствующий лиганд, непосредственно или посредством линкера. Образец, содержащий биологические вещества, имеющие сродство к лиганду, может приводиться в контакт с аффинным лигандом, ковалентно иммобилизованным на материале твердого носителя, при соответствующих условиях связывания, которые способствуют специфичному связыванию лиганда с биологическими веществами, имеющими сродство к лиганду. После этого колонка может промываться буфером для удаления несвязанного материала, и на следующей стадии биологические вещества, имеющие сродство к лиганду, могут элюироваться и получаться в очищенной или выделенной форме. Соответственно, лиганд должен предпочтительно демонстрировать характеристики специфичного и обратимого связывания с биологическим веществом, таким как антитело, которое является желаемым при очистке или выделении.
Антитела имеют одну или несколько копий Y-образной единицы, состоящей из четырех полипептидных цепей. Каждый Y содержит две идентичных копии "тяжелой" цепи и две идентичных копии "легкой цепи", названных так по их относительным молекулярным массам.
Антитела могут быть разделены на пять классов: IgG, IgM, IgA, IgD и IgE, на основе количества единиц Y и типа тяжелой цепи. Тяжелая цепь определяет подкласс каждого антитела. Тяжелые цепи IgG, IgM, IgA, IgD и IgE известны, как гамма, мю, альфа, дельта и эпсилон соответственно. Легкие цепи каждого антитела могут классифицироваться либо как тип каппа (κ), либо тип лямбда (λ) (описание молекулярной характеристики полипептида).
Для фармацевтических применений, наиболее часто используемое антитело представляет собой IgG, которое может расщепляться на три части, две области F(ab) и одну область Fc, посредством протеолитического фермента папаина, или на две части, одну область F(ab')2 и одну область Fc, посредством протеолитического фермента пепсина.
Области F(ab) содержат "ветви" антитела, которые являются критичными для связывания антигена. Область Fc содержит "хвост" антитела и играет роль при иммунной реакции, а также служит в качестве полезной "ручки" для манипуляций антителом во время некоторых иммунохимических процедур. Количество областей F(ab) на антителе соответствует его подклассу и определяет "валентность" антитела (в широком смысле - это количество "ветвей", с помощью которых антитело может связывать его антиген).
Термин "антитело" обозначает иммуноглобулин, либо природный, либо полученный синтетически, полностью или частично. Все его фрагменты и производные, которые сохраняют способность к специфичному связыванию, также включаются в термин. Типичные фрагменты представляют собой FC, FAB, тяжелую цепь и легкую цепь. Термин также охватывает любой полипептид, имеющий домен связывания, который является гомологичным или по большей части гомологичным, например, по меньшей мере, идентичным на 95%, если сравнивать аминокислотную последовательность с доменом связывания иммуноглобулина. Эти полипептиды могут быть получены из природных источников или получаться синтетически, частично или полностью. Антитело может быть моноклональным или поликлональным. Антитело может представлять собой член любого класса иммуноглобулинов, включая любой из классов, для человека: IgG, IgM, IgA, IgD и IgE. Производные класса IgG, однако, являются предпочтительными в одном из вариантов осуществления настоящего изобретения.
Термин "фрагмент антитела" относится к любому производному антитела, которое имеет менее чем полную длину. Предпочтительно, фрагмент антитела сохраняет, по меньшей мере, значительную часть способности к специфичному связыванию полноразмерного антитела. Примеры фрагментов антитела включают в себя, но, не ограничиваясь этим, Fab, Fab', F(ab')2, scFv, Fv, димерное антитело dsFv и фрагменты Fd. Фрагмент антитела может быть получен с помощью любых средств. Например, фрагмент антитела может быть получен ферментативно или химически посредством фрагментирования интактного антитела, или он может быть получен рекомбинантно из гена, кодирующего частичную последовательность антитела. Альтернативно, фрагмент антитела может быть получен синтетически, полностью или частично. Фрагмент антитела необязательно может представлять собой фрагмент антитела с одной цепью. Альтернативно, фрагмент может содержать множество цепей, которые связаны вместе, например, посредством дисульфидных связей. Фрагмент также необязательно может представлять собой мультимолекулярный комплекс. Функциональный фрагмент антитела будет, как правило, содержать, по меньшей мере, примерно 50 аминокислот, а более конкретно, будет содержать, по меньшей мере, примерно 200 аминокислот.
"Одноцепочечные Fv" (scFv) представляют собой рекомбинантные фрагменты антитела, состоящие только из вариабельной легкой цепи (VL) и вариабельной тяжелой цепи (VH), ковалентно связанных друг с другом посредством полипептидного линкера. Либо VL, либо VH могут представлять собой аминоконцевой домен. Полипептидный линкер может иметь переменную длину и состав, постольку, поскольку два вариабельных домена соединяются без серьезных стерических затруднений. Как правило, линкеры состоят в основном из цепей из остатков глицина и серина, с некоторым количеством остатков глутаминовой кислоты или лизина, включенными между ними для растворимости. "Димерные антитела" представляют собой димерные scFv. Компоненты димерных антител, как правило, имеют более короткие пептидные линкеры, чем большинство scFv, и они показывают предпочтение к ассоциации в виде димеров. Фрагмент "Fv" представляет собой фрагмент антитела, который состоит из одного домена VH и одного VL, удерживаемых вместе посредством нековалентных взаимодействий. Термин "dsFv" используется здесь для обозначения Fv с полученной посредством генной инженерии внутримолекулярной дисульфидной связью, для стабилизации пары VH-VL. Фрагмент "F(ab')2" представляет собой фрагмент антитела, по существу эквивалентный фрагменту, который получают из иммуноглобулинов (как правило, IgG) посредством расщепления с помощью фермента пепсина при pH 4,0-4,5. Фрагмент может быть получен рекомбинантно. Фрагмент "Fab'" представляет собой фрагмент антитела, по существу эквивалентный фрагменту, полученному посредством восстановления дисульфидного мостика или мостиков, соединяющих две части тяжелой цепи во фрагменте F(ab')2. Фрагмент Fab' может быть получен рекомбинантно. Фрагмент "Fab" представляет собой фрагмент антитела, по существу эквивалентный фрагменту, полученному посредством расщепления иммуноглобулинов (как правило, IgG) ферментом папаином. Фрагмент Fab может быть получен рекомбинантно. Сегмент тяжелой цепи фрагмента Fab представляет собой часть Fd. Область "Fc" представляет собой константную область конкретного класса антитела.
Связывание между антигенами и антителами зависит от водородных связей, гидрофобных связей, электростатических сил и сил Ван дер Ваальса. Они все представляют собой связи слабой, нековалентной природы, хотя некоторые взаимодействия между антигеном и антителом могут быть достаточно сильными. Соответственно, константа сродства связывания антитело-антиген может находиться в широких пределах, простирающихся от более низких, чем 105 моль-1, до больших, чем 1012 моль-1. Константы сродства зависят от температуры, pH и растворителя. Кроме сродства антитела к лиганду, общая стабильность комплекса антитело-лиганд определяется также валентностью антигена и антитела и структурным расположением взаимодействующих частей.
Точные константы сродства могут быть определены только для моноклональных антител, которые представляют собой генетически идентичные молекулы, распознающие один-единственный эпитоп на антигене, в то время как для поликлональных антител, широкое распределение сродства может вносить вклад в наблюдаемую константу сродства. В наблюдаемую константу сродства может также вносить вклад тот факт, что поликлональные антитела могут распознавать более одного-единственного эпитопа на одном и том же антигене. Поскольку антитела обычно прикрепляются более чем к одному домену связывания в молекуле, имеют место множественные, кооперативные связи между антителами и их антигенами; этот эффект называется авидностью. Поскольку моноклональные антитела взаимодействуют только с одним-единственным эпитопом на антигене, они более склонны к потере эпитопа во время химической обработки антигена, чем поликлональные антитела. Это может устраняться посредством объединения двух или более моноклональных антител к одному и тому же антигену.
Моноклональные антитела могут быть получены в результате слияния B-лимфоцитов с бессмертными культурами клеток, с получением гибридом. Гибридомы будут производить множество копий точно такого же антитела - главная особенность при разработке антител для терапевтических или диагностических применений.
В настоящее время, наиболее исследованный аффинный лиганд для очистки и выделения биологических молекул, таких как моноклональные антитела, представляет собой белок A. Белок A представляет собой широко используемый лиганд, однако лиганд может страдать несколькими недостатками, такими как проблемы, связанные с нестабильностью, с одновременным вымыванием из колонки, и необходимостью удалять его из конечного продукта или недостаточной смывкой с хроматографической смолы, и, кроме того, белок A является довольно дорогим.
Следовательно, имеется необходимость в новых, стабильных, недорогих лигандах для выделения антител, в частности моноклональных антител, или их аналогов, производных, фрагментов и предшественников, полученных либо из природных, либо из рекомбинантных источников.
Сущность изобретения
В одном из аспектов настоящего изобретения предусматривается материал твердого носителя, имеющий ковалентно иммобилизованный на нем аффинный лиганд, который содержит одну или несколько гидрофобных функциональных групп и одну или несколько катионных функциональных групп,
где, по меньшей мере, одна гидрофобная функциональная группа отделена от, по меньшей мере, одной катионной функциональной группы расстоянием между связями от 5 Å до 20 Å,
где указанный лиганд имеет молекулярную массу от 120 Да до 5000 Да.
В другом аспекте настоящего изобретения, предусматривается материал твердого носителя, имеющий ковалентно иммобилизованный на нем аффинный лиганд, который имеет одну или несколько гидрофобных функциональных групп и одну или несколько гетероароматических функциональных групп,
где, по меньшей мере, одна гидрофобная функциональная группа отделена от, по меньшей мере, одной гетероароматической функциональной группы расстоянием между связями от 5 Å до 20 Å, и
где указанный лиганд имеет молекулярную массу от 120 Да до 5000 Да.
В дополнительном аспекте настоящего изобретения, предусматривается способ выделения биологических молекул, таких как белки, например, антитела, в частности, моноклональные антитела или их производные, включающий стадии (i) предоставления материала твердого носителя, имеющего ковалентно иммобилизованный на нем аффинный лиганд, как определено здесь, (ii) предоставления образца, предположительно, содержащего антитело, имеющее сродство к указанному лиганду, (iii) приведения в контакт указанного лиганда с указанным образцом, предположительно, содержащим указанное антитело, (iv) селективного связывания указанного антитела, когда указанное антитело содержится в указанном образце, и (v) селективного выделения указанного антитела, когда указанное антитело содержится в указанном образце.
Краткое описание фигур
Фиг.1: анализ селективности смолы B2. 1 = супернатант от ферментирования, 2 = Прохождение растворителя через аффинный сорбент (цикл 1), 3 = элюирование (цикл 1), 4 = регенерация/смывка (цикл 1), 5 = промывка (цикл 2), 6 = элюирование (цикл 2), 7 = белка нет, 8 = эталонный образец mAb.
Фиг.2: анализ селективности смолы B3. 1 = супернатант от ферментирования, 2 = Прохождение растворителя через аффинный сорбент (цикл 1), 3 = элюирование (цикл 1), 4 = регенерация/смывка (цикл 1), 5 = промывка (цикл 2), 6 = элюирование (цикл 2), 7 = регенерация/смывка (цикл 2), 8 = эталонный образец mAb.
Фиг.3: анализ селективности смолы D1. 1 = эталонный образец mAb, 2 = супернатант от ферментирования, 3 = Прохождение растворителя через аффинный сорбент (цикл 1), 4 = элюирование (цикл 1), 5 = регенерация/смывка (цикл 1), 6 = промывка (цикл 2), 7 = элюирование (цикл 2), 8 = регенерация/смывка (цикл 2).
Фиг.4: анализ селективности смолы D2. 1 = эталонный образец mAb, 2 = супернатант от ферментирования, 3 = Прохождение растворителя через аффинный сорбент (цикл 1), 4 = элюирование (цикл 1), 5 = регенерация/смывка (цикл 1), 6 = промывка (цикл 2), 7 = элюирование (цикл 2), 8 = регенерация/смывка (цикл 2).
Подробное описание изобретения
Как описано выше, настоящее изобретение относится к новым материалам твердого носителя, имеющим ковалентно иммобилизованный на нем аффинный лиганд, где лиганд содержит конкретный набор функциональных групп. Такие материалы являются особенно полезными для очистки и выделения биологических молекул, таких как белки, например, антитела, в частности, моноклональные антитела или их производные.
Лиганды
Когда здесь используется, термин "лиганд" обозначает молекулу, которая может связывать целевое соединение, например, антитело, в частности, моноклональное антитело. Лиганды предпочтительно связываются со своими партнерами по связыванию, по меньшей мере, по существу специфически ("специфичное связывание").
"Специфичное связывание" относится к свойству лиганда: (1) связываться с партнером по связыванию, например, моноклональным антителом, (2) предпочтительно, таким образом, что относительная масса связанного партнера по связыванию, например, моноклонального антитела, по меньшей мере, в два раза, например, в 50 раз, например, в 100 раз, например, в 1000 раз, или более, больше, чем относительная масса других связанных частиц, иных, чем партнер по связыванию, например, моноклональное антитело. Под относительной массой связанного соединения подразумевается масса связанного соединения минус масса несвязанного соединения, деленная на общую массу партнера по связыванию, то есть
относительная масса связанного соединения = (масса связанного соединения - масса несвязанного соединения)/(масса связанного соединения + масса несвязанного соединения),
для соединения, являющегося партнером по связыванию, или других частиц.
Термин "партнер по связыванию" обозначает любую биологическую молекулу, которая связывается с конкретным лигандом, предпочтительно, по существу специфически. Партнер по связыванию может быть общим для одного или нескольких лигандов. Предпочтительные партнеры по связыванию представляют собой антитела, включая поликлональные антитела и моноклональные антитела. Дополнительными предпочтительными партнерами по связыванию являются фрагменты антител из моноклональных антител или поликлональных антител.
Лиганды в соответствии с настоящим изобретением включают в себя обогащенные или разделенные оптические изомеры по любому или по всем асимметричным атомам, как видно из настоящего описания или иллюстраций. Как рацемические, так и диастереомерные смеси, а также индивидуальные оптические изомеры могут выделяться или синтезироваться с тем, чтобы они по существу не содержали их энантиомерных или диастереомерных партнеров, и они находятся в рамках настоящего изобретения.
Эксперименты неожиданно показали, что определенные классы аффинных лигандов, в том числе такие, где лиганды содержат одну или несколько гидрофобных функциональных групп и одну или несколько катионных функциональных групп, селективно связываются с mAb. Другой обещающий класс аффинных лигандов представляет собой класс, где лиганды содержат одну или несколько гидрофобных функциональных групп и одну или несколько гетероароматических функциональных групп.
Кроме того, обнаружено, что, по меньшей мере, одна гидрофобная функциональная группа предпочтительно должна отделяться, по меньшей мере, от одной катионной функциональной группы расстоянием между связями от 5 Å до 30 Å, например, расстоянием между связями от 5 Å до 20 Å, таким как расстояние между связями от 5 до 19 Å, например, расстоянием между связями от 5 до 18 Å, таким как расстояние между связями от 5 до 17 Å, например, расстоянием между связями от 5 до 16 Å, таким как расстояние между связями от 5 до 15 Å, например, расстоянием между связями от 5 до 14 Å, таким как расстояние между связями от 5 до 13 Å, например, расстоянием между связями от 5 до 12 Å, таким как расстояние между связями от 5 до 11 Å, например, расстоянием между связями от 5 до 10 Å, таким как расстояние между связями от 6 до 14 Å, или таким как расстояние между связями от 7 до 20 Å, например, расстоянием между связями от 7 до 19 Å, таким как расстояние между связями от 7 до 18 Å, например, расстоянием между связями от 7 до 17 Å, таким как расстояние между связями от 7 до 16 Å, например, расстоянием между связями от 7 до 15 Å, таким как расстояние между связями от 7 до 14 Å, например, расстоянием между связями от 7 до 13 Å, таким как расстояние между связями от 7 до 12 Å, например, расстоянием между связями от 7 до 11 Å, таким как расстояние между связями от 7 до 10 Å, например, расстоянием между связями от 8 до 12 Å, или например, расстоянием между связями от 9 до 20 Å, таким как расстояние между связями от 9 до 18 Å, например, расстоянием между связями от 9 до 16 Å, таким как расстояние между связями от 9 до 14 Å, например, расстоянием между связями от 9 до 12 Å, таким как расстояние между связями от 9 до 11 Å, например, расстоянием между связями примерно 10 Å.
Расстояние между связями представляет собой самое короткое внутримолекулярное расстояние между ковалентно связанными химическими остатками вдоль химических связей. Оно вычисляется посредством сложения индивидуальных длин связей атом-атом вдоль кратчайшего внутримолекулярного пути. Типичные длины связей атом-атом равны от 1,2 Å до 1,4 Å.
Пространственное расстояние между, по меньшей мере, одной гидрофобной функциональной группой и, по меньшей мере, одной катионной функциональной группой лиганда предпочтительно меньше, чем 30 Å, например, меньше, чем 28 Å, например, меньше, чем 26 Å, например, меньше, чем 24 Å, например, меньше, чем 22 Å, например, меньше, чем 20 Å, например, меньше, чем 18 Å, например, примерно или меньше, чем 16 Å, например, меньше, чем 15 Å, например, примерно или меньше, чем 14 Å, например, меньше, чем 13 Å, например, примерно или меньше, чем 12 Å, например, меньше, чем 11 Å, например, примерно или меньше, чем 10 Å, например, примерно или меньше, чем 8 Å, например, примерно 6 Å, например, в пределах от 5 до 20 Å, такое как пространственное расстояние от 5 до 19 Å, например, пространственное расстояние от 5 до 18 Å, такое как пространственное расстояние от 5 до 17 Å, например, пространственное расстояние от 5 до 16 Å, такое как пространственное расстояние от 5 до 15 Å, например, пространственное расстояние от 5 до 14 Å, такое как пространственное расстояние от 5 до 13 Å, например, пространственное расстояние от 5 до 12 Å, такое как пространственное расстояние от 5 до 11 Å, например, пространственное расстояние от 5 до 10 Å, такое как пространственное расстояние от 7 до 20 Å, например, пространственное расстояние от 7 до 19 Å, такое как пространственное расстояние от 7 до 18 Å, например, пространственное расстояние от 7 до 17 Å, такое как пространственное расстояние от 7 до 16 Å, например, пространственное расстояние от 7 до 15 Å, такое как пространственное расстояние от 7 до 14 Å, например, пространственное расстояние от 7 до 13 Å, такое как пространственное расстояние от 7 до 12 Å, например, пространственное расстояние от 7 до 11 Å, такое как пространственное расстояние от 7 до 10 Å, например, пространственное расстояние от 9 до 20 Å, такое как пространственное расстояние от 9 до 18 Å, например, пространственное расстояние от 9 до 16 Å, такое как пространственное расстояние от 9 до 14 Å, например, пространственное расстояние от 9 до 12 Å, такое как пространственное расстояние от 9 до 11 Å.
Расстояния между связями и пространственные расстояния могут вычисляться или определяться специалистом в данной области в соответствии с состоянием технологий в данной области. Молекулярное моделирование также может использоваться для определения минимального расстояния между атомами различных функциональных групп лигандов. Молекулярное моделирование может осуществляться, например, с помощью Sybyl/Mendyl 5.4 (Tripos Associates, St. Louis, Mo.), с использованием компьютера Evans and Sutherland PS390 graphics, снабженного стереографическим устройством для просмотра. Структуры соответствующих лигандов могут создаваться посредством конструирования с помощью программы Concord или из библиотек, с последующей минимизацией энергии. Вычисления энергии могут производиться с помощью силового поля Sybyl/Mendyl и параметра Ван дер Ваальса 1,2 Å для водорода. Заряды могут вычисляться с использованием способа Гастайгнера-Хюккеля, который включает в себя сигма-связь и пи-связь.
Лиганд предпочтительно имеет молекулярную массу меньшую, чем 5000 Да, такую как меньшую, чем 4000 Да, например, меньше, чем 3500 Да, такую как меньшую, чем 3000 Да, например, меньше, чем 2500 Да, такую как меньшую, чем 2000 Да, такую как меньшую, чем 1800 Да, например, меньше, чем 1600 Да, такую как меньшую, чем 1500 Да, такую как меньшую, чем 1400 Да, например, меньше, чем 1300 Да, такую как меньшую, чем 1200 Да, такую как меньшую, чем 1100 Да, например, меньше, чем 1000 Да.
В дополнение к этому, лиганд предпочтительно имеет молекулярную массу, большую, чем 120 Да, такую как большую, чем 140 Да, например, большую, чем 160 Да, такую как большую, чем 180 Да, например, большую, чем 200 Да, такую как большую, чем 220 Да, например, молекулярную массу большую, чем 240 Да.
Для уменьшения уровня неспецифичного связывания с катионными группами, лиганд дополнительно может содержать одну или несколько анионных групп для компенсации некоторой части положительного заряда на лиганде. Анионные группы включают в себя, но, не ограничиваясь этим, карбоксилат, сульфонат, сульфат, фосфат и другие отрицательно заряженные ионизируемые группы, и могут, например, располагаться на боковых группах лиганда.
Функциональные группы лигандов
В одной из основных групп пригодных для использования лигандов, каждый лиганд содержит одну или несколько гидрофобных функциональных групп и одну или несколько катионных функциональных групп.
В другой основной группе пригодных для использования лигандов, каждый лиганд содержит одну или несколько гидрофобных функциональных групп и одну или несколько гетероароматических функциональных групп.
Как здесь используется, катионная функциональная группа представляет собой органическую группу, которая имеет положительный заряд в диапазоне pH 3-7. Первичные, вторичные и третичные амины представляют собой типичные примеры катионных групп. Гуанидин представляет собой дополнительный важный пример. Дополнительные примеры катионных функциональных групп приведены в разделе "Катионные функциональные группы" ниже.
Гидрофобная функциональная группа представляет собой органическую группу, способную связываться с поверхностью биологической молекулы, в основном, посредством гидрофобного взаимодействия. Гидрофобные функциональные группы отличаются тем, что они являются по существу неполярными и незаряженными при нормальных физиологических условиях. Гидрофобные остатки отталкиваются водным раствором так, что они стремятся занять внутренние положения в конформации лиганда, когда лиганд находится в водной среде. Также, гидрофобные остатки стремятся занять гидрофобные карманы или бороздки партнера по связыванию лиганда, когда лиганд ассоциируется с партнером по связыванию при нормальных физиологических условиях.
Когда он здесь используется, термин "нормальные физиологические условия" обозначает условия, которые являются типичными внутри живого организма или клетки. Хотя наблюдается, что некоторые органы или организмы создают экстремальные условия, окружающая среда внутри организма и внутри клетки обычно находится вблизи pH 7 (то есть, от pH 6,5 до pH 7,5), содержит воду в качестве преобладающего растворителя и существует при температуре выше 0°C и ниже 50°C. Будет понятно, что концентрация различных солей зависит от органа, организма, клетки или клеточного отдела, который упоминается.
Органические гидрофобные группы, как правило, имеют высокое содержание атомов углерода. Типичные примеры гидрофобных групп представляют сбой линейные и разветвленные алканы, циклические углеводороды, ароматические соединения и сочетания линейных и разветвленных алканов, циклических углеводородов и ароматических соединений. Также и замещенные варианты таких групп рассматриваются как гидрофобные, постольку, поскольку относительное содержание углерода выше определенного предела. Однако процент атомов углерода не является единственным параметром, который влияет на гидрофобность. Также положение и природа других атомов играет важную роль. Например, простой эфир, как правило, является более гидрофобным, чем спирт с таким же количеством атомов углерода и атомов кислорода, и сложный эфир является более гидрофобным, чем диол с таким же составом элементов. Когда один или несколько возможных атомов органической группы, иных, чем углерод, и иных, чем водород, находятся в первичных положениях, относительное количество атомов углерода должно быть выше для группы, которая должна быть гидрофобной, чем когда возможные атомы, иные, чем углерод, и иные, чем водород, находятся во вторичных, третичных или четвертичных положениях. Имея это в виду, авторы определяют гидрофобную группу как органические группы с 75% или более их атомов, иных, чем водород, являющимися атомами углерода, например, 80%, или более, предпочтительно, 85% или более их атомов, иных, чем водород, являются атомами углерода. Например, более низкое значение, 75%, применимо к простым эфирам и сложным эфирам, промежуточное значение, 80%, применимо к амидам и вторичным и третичным аминам, в то время как наивысшее значение, 85%, применимо к спиртам и первичным аминам. Примеры гидрофобных функциональных групп приведены ниже в разделе "Функциональные группы лиганда".
По меньшей мере, одна гидрофобная функциональная группа может содержать или состоять из одной или нескольких групп, выбранных из "алкила", "циклического алкила", "замещенного алкила", "арила", "замещенного арила", "алкенила", "замещенного алкенила", "алкинила", "замещенного алкинила", "аралкила", "замещенного аралкила", "гетероциклила", "замещенного гетероциклила", "гетероциклилалкила", "замещенного гетероциклилалкила", "алкиламиноалкила", "замещенного алкиламиноалкила", "диалкиламиноалкила", "замещенного диалкиламиноалкила", "гетероциклилоксиалкила", "замещенного гетероциклилоксиалкила", "ариламиноалкила", "замещенного ариламиноалкила", "гетероциклиламиноалкила", "замещеного гетероциклиламиноалкила", "алкиламиноалкокси", "замещенной алкиламиноалкокси", "диалкиламиноалкокси", "замещенной диалкиламиноалкокси", "гетероциклилокси" и "замещенной гетероциклилокси", как определено здесь ниже.
Гидрофобные функциональные группы, содержащие алифатические остатки
По меньшей мере, одна гидрофобная функциональная группа может содержать или состоять из необязательно замещенного алифатического остатка и/или необязательно замещенного ароматического остатка. Алифатические остатки, как правило, относятся к углеводородам, такие, например, как алкильные, алкиленовые и алкинильные остатки, которые могут быть замещенными или незамещенными.
"Алкил" как здесь используется, включает в себя алкильные группы с прямой цепью, такие как метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил, ундецил, додецил, и тому подобное. "Алкил" также включает в себя изомеры с разветвленной цепью алкильных групп с прямой цепью, включая, но, не ограничиваясь этим, следующие группы, которые приводятся в качестве примера: -CH(CH3)2, -CH(CH3)(CH2CH3), -CH(CH2CH3)2, -C(CH3)3, -C(CH2CH3)3, -CH2CH(CH3)2, -CH2CH(CH3)(CH2CH3), -CH2CH(CH2CH3)2, -CH2C(CH3)3, -CH2C(CH2CH3)3, -CH(CH3)CH(CH3)(CH2CH3), -CH2CH2CH(CH3)2, -CH2CH2CH(CH3)(CH2CH3), -CH2CH2CH(CH2CH3)2, -CH2CH2C(CH3)3, -CH2CH2C(CH2CH3)3, -CH(CH3)CH2CH(CH3)2, -CH(CH3)CH(CH3)CH(CH3)CH(CH3)2, -CH(CH2CH3)CH(CH3)CH(CH3)(CH2CH3) и другие.
Алифатический остаток может представлять собой необязательно замещенный линейный алифатический остаток или необязательно замещенный разветвленный алифатический остаток. Алифатический остаток также может представлять собой необязательно замещенный циклический алкил. "Циклический алкил" включает в себя группы, такие как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил, и такие кольца, замещенные алкильными группами с прямой и разветвленной цепью, как определено выше, а также включает в себя полициклические алкильные группы, такие как, но, не ограничиваясь этим, адамантил, норборнил и бицикло[2.2.2]октил, и такие кольца, замещенные алкильными группами с прямой и разветвленной цепью, как определено выше. Таким образом, незамещенные алкильные группы включают в себя первичные алкильные группы, вторичные алкильные группы и третичные алкильные группы. Незамещенные алкильные группы могут быть связаны с одним или несколькими атомами углерода, атомами кислорода, атомами азота и/или атомами серы в лиганде.
Циклический алифатический остаток может, например, содержать или состоять из C5-C16 циклоалкильной группы. Более короткие цепи также могут иметь место, как правило, когда циклоалкил является замещенным арильным или гетероарильным остатком.
"Замещенный алкил" относится к незамещенной алкильной группе, как определено выше, в которой одна или несколько связей с атомами углерода или водорода заменяется связью с атомами, иными, чем водород, и иными, чем углерод, такими как, но, не ограничиваясь этим, атом галогена в галогенидах, такой как F, Cl, Br и I; и атом кислорода в группах, таких как гидроксильные группы, алкокси группы, арилокси группы и сложноэфирные группы; атом серы в группах, таких как тиольные группы, алкил- и арилсульфидные группы, сульфоновые группы, сульфонильные группы и сульфоксидные группы; атом азота в группах, таких как амины, амиды, алкиламины, диалкиламины, ариламины, алкилариламины, диариламины, N-оксиды, имиды, и энамины; атом кремния в группах, таких как в триалкилсилильные группы, диалкиларилсилильные группы, алкилдиарилсилильные группы и триарилсилильные группы; и другие гетероатомы в различных других группах.
Замещенные алкильные группы также включают в себя группы, в которых одна или несколько связей с атомами углерода или водорода заменяется связью с гетероатомом, таким как кислород в карбонильных, карбоксильных и сложноэфирных группах; азот в группах, таких как имины, оксимины, гидразоны и нитрилы. Замещенные алкильные группы, также включают в себя, среди прочего, алкильные группы, в которых одна или несколько связей с атомом углерода или водорода заменяются одной или несколькими связями с атомом галогена. Другие замещенные алкильные группы включают в себя такие группы, в которых одна или несколько связей с атомом углерода или водорода заменяется связью с атомом кислорода, так что замещенная алкильная группа включает в себя гидроксильную, алкокси, арилокси группу или гетероциклилокси группу. Другие алкильные группы включают в себя алкильные группы, которые имеют группу амина, алкиламина, диалкиламина, ариламина, (алкил)(арил)амина, диариламина, гетероциклиламина, (алкил)(гетероциклил)амина, (арил)(гетероциклил)амина или дигетероциклиламина.
В одном из вариантов осуществления, алифатическая функциональная группа является предпочтительно замещенной арильной группой, такой как (C6-C12)арильная группа, рассмотренная здесь ниже, которая может, в свою очередь, также быть замещенной, как также описано здесь. Пример замещенной арильной группы включает в себя "аралкильную группу", которая может быть замещенной или незамещенной.
Соответственно, "аралкил" относится к незамещенным алкильным группам, как определено выше, в которых связь с атомом водорода или углерода незамещенной алкильной группы заменяется связью с арильной группой, как определено выше. Например, метил (-CH3) представляет собой незамещенную алкильную группу. Если атом водорода метильной группы заменяется связью с фенильной группой, как если атом углерода метила связывается с атомом углерода бензола, тогда соединение представляет собой незамещенную аралкильную группу (то есть, бензильную группу). Таким образом, включаются, но, не ограничиваясь этим, такие группы как группа бензила, дифенилметила и 1-фенилэтил (-CH(C6H5)(CH3)), 2-фенилэтильная группа, 2-нафтилэтильная группа, и тому подобное.
"Замещенный аралкил" имеет такое же значение по отношению к незамещенным аралкильным группам, какое замещенные арильные группы имеют по отношению к незамещенным арильным группам. Однако замещенная аралкильная группа также включает в себя группы, в которых связь с атомом углерода или водорода алкильной части группы, заменяется связью с атомом, иным, чем атом углерода, или иным, чем атом водорода. Примеры замещенных аралкильных групп включают в себя, но, не ограничиваясь этим, -CH2C(=O)(C6H5) и -CH2(2-метилфенил), среди прочих.
В одном из вариантов осуществления, необязательно замещенный алифатический остаток содержит или состоит из C5-C20 алкильной группы. Более короткие цепи также могут иметь место, как правило, когда алкил является замещенным арильным или гетероарильным остатком. Дополнительные примеры алкильных групп, замещенных арилом или гетероарилом, включают в себя, например, линейную (C1-C10), разветвленную (C4-C10) или циклическую (C5-C10) группу, такую как метильная группа, этильная группа, пропильная группа, такая как н-пропильная группа и изопропильная группа, бутильную группу, такую как н-бутильная группа, изобутильная группа, трет-бутильная группа, н-амильная группа, пентильную группу, такую как неопентильная группа, циклопентильная группа, гексильную группу, такую как н-гексильная группа, циклогексильная группа, гептильную группу, октильную группу, такую как н-октильная группа, нонильную группу, такую как н-нонильная группа, децильную группу, такую как н-децильная группа, ундецильная группа, додецильная группа, ментильную группа, 2,3,4-триметил-3-пентильную группа, 2,4-диметил-3-пентильную группу, и тому подобное.
В одном из вариантов осуществления, C5-C20 алкильная группа может также быть замещенной, например, атомом галогена, алкокси группой, арилокси группой, алкилтио группой или арилтио группой. Примеры атома галогена представляют собой атом фтора, атом хлора, атом брома и атом йода. Примеры алкоксильной группы включают в себя, например, (C1-C4) алкокси группу, такую как метокси группа, этокси группа, н-пропокси группа, трет-бутокси группа или что-либо по