Соединения имидазолотиазола для лечения заболеваний
Иллюстрации
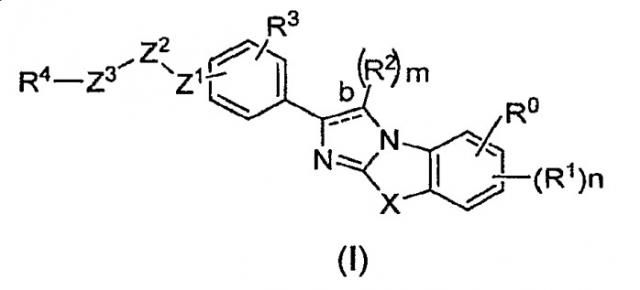
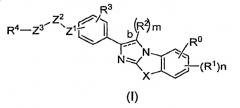
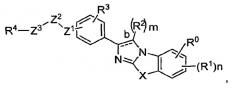
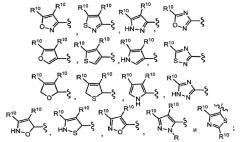
Показать всеИзобретение относится к соединениям общей формулы (I), где связь b представляет собой двойную связь; X представляет собой -S-; Z1 и Z3, каждый, независимо представляет собой прямую связь, -N(R5) - или - (CH2)q; Z2 представляет собой -С(О)- или -C(S)-; m представляет собой целое число, равное 1; n представляют собой целое число, равное 1; каждый из q независимо представляет собой целое число от 1 до 4; R0 представляет собой водород, галоген, гидрокси, незамещенный С1-С3алкил или незамещенный С1-С3алкокси; R1 независимо выбирают из группы, состоящей из галогена, необязательно замещенного С1-С3алкила, -R6OR7, -R6N(R7)2, -R6C(O)R7,
-R6C(O)OR7, -R6C(O)N(R7)R9N(R7)2,
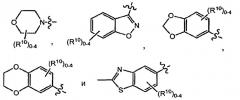
-R6OC(O)R8, -R6C(O)N(R7)2 или -R6OR9N(R7)2; R2 представляет собой водород; R4 выбирают из группы, состоящей из морфолинила, изоксазолила, тиазолила, оксазолила, бензизоксазолила, бензотиазолила, диоксинила, диоксолила, и необязательно замещенного фенила. Также изобретение относится к фармацевтически приемлемым солям соединений формулы (I) и к фармацевтической композиции, обладающей антипролиферативной активностью, содержащей соединения формулы (I).Технический результат - соединения формулы (I), обладающие антипролиферативной активностью. 2 н. и 19 з.п. ф-лы, 5 табл., 1 ил.
Реферат
Настоящая заявка заявляет приоритет предварительной заявки на патент США, серийный № 60/743543, поданной 17 марта 2006 года, озаглавленной "Imidazolothiazole Derivatives For The Treatment Of Disease". Описание упомянутой выше заявки включается сюда в виде ссылки во всей его полноте.
Область техники, к которой относится изобретение
Предлагаются новые низкомолекулярные соединения, композиции и способы лечения заболеваний. Предложенные соединения представляют собой модуляторы активности ферментов, таких как киназы, и являются пригодными для лечения, предотвращения или облегчения заболевания или расстройства, связанного с активностью фермента, или одного или нескольких его симптомов.
Уровень техники
Протеинкиназы (PK) представляют собой ферменты, которые катализируют фосфорилирование гидроксигрупп на тирозиновых, сериновых и треониновых остатках белков. Протеинкиназы, и в частности, относящиеся к семейству рецепторных тирозиновых протеинкиназ (RTK), действуют, прежде всего, как рецепторы факторов роста и играют центральную роль в путях передачи сигналов, регулирующих ряд клеточных функций, таких как клеточный цикл, клеточный рост, клеточная дифференциация и гибель клеток. Аберрантная или избыточная активность, или нарушение регуляции активности рецепторной тирозиновой протеинкиназы (RPTK) наблюдается при множестве болезненных состояний, включая доброкачественные и злокачественные пролиферативные расстройства, а также воспалительные расстройства и расстройства иммунной системы, которые возникают в результате неправильного активирования иммунной системы, вызывая, например, аутоиммунные заболевания.
Нарушение регуляции активности рецепторной тирозиновой киназы семейства рецепторов факторов роста тромбоцитов (PDGFR), в качестве одного из примеров, вовлечена в различные пролиферативные расстройства. Генная амплификация или положительная регуляция PDGFR происходит у пациентов с глиомами или саркомами (Kumabe et al., Oncogene, 7:627-633 (1992), Ostman and Heldin Cancer Res. 80:1-38 (2001)). Конститутивное активирование PDGFR-α обнаружено у пациентов с хронической миеломоноцитарной лейкемией (CMML) (Magnusson et al. Blood 100:1088-1091 (2002)). Увеличение числа функциональных мутаций и малых делеций в гене PDGFR-α также обнаружено у пациентов с желудочно-кишечными опухолями (GIST) (Heinrich et al. Science 299: 708-710 (2003)) и у пациентов с идиопатическим гиперэозинофильным синдромом (Cools et al. N. Engl. J. Med. 348:1201-1214 (2003)). PDGFR-β, как обнаружено, экспрессируется в строме опухоли для большинства солидных опухолей, что делает этот рецептор потенциальной мишенью для противоопухолевой терапии (Pietras et al. Cancer Cell 3:439-443 (2003), Pietras et al. Cancer Res. 62: 5476-5484 (2002)). PDGFR-β также, как обнаружено, экспрессируется в сосудистой системе опухоли, и исследования предполагают ингибирование PDGFR-β в качестве одного из механизмов антиангиогенной терапии (См. Bergers et al, J. Clin. Invest. 111(9): 1287-1295(2003), Saharinen et al. J. Clin. Invest. 111:1277-1280 (2003)).
Второй член семейства PDGFR, Flt3 (также называемый Flk2), играет важную роль в пролиферации и дифференциации гематопоэтических стволовых клеток и активирующая мутация или сверхэкспрессирование этого рецептора наблюдаются при AML (См. Heinrich Mini-Reviews in Medicinal Chemistry (2004) 4(3):255-271, Kiyoi et al. Int J Hematol (2005) 82:85-92). Разработано более дюжины известных ингибиторов Flt3, и некоторые из них показали перспективное клиническое воздействие против AML (См. Levis et al. Int J Hematol. (2005) 82:100-107). Рецептор Flt3 также экспрессируется в большой части предшественников дендритных клеток, и стимулирование рецепторов вызывает пролиферацию и дифференциацию этих предшественников в дендритные клетки (DC). Поскольку дендритные клетки являются главными инициаторами опосредованной T-лимфоцитами иммунной реакции, включая аутоиммунную реакцию, ингибирование Flt3 представляет собой механизм отрицательного регулирования опосредованных DC воспалительных и аутоиммунных реакций. Одно из исследований показывает, что ингибитор Flt3 CEP-701 является эффективным для уменьшения потерь миелина при экспериментальном аутоиммунном энцефаломиелите (EAE), мышиной модели для рассеянного склероза (см. Whartenby et al. PNAS (2005) 102: 16741-16746). Высокий уровень лиганда Flt3 обнаружен в сыворотке пациентов с гистиоцитозом клеток Лангерганса и при системной красной волчанке, что дополнительно свидетельствует о передаче сигналов с помощью Flt3 при нарушении регуляции предшественников дендритных клеток при этих аутоиммунных заболеваниях (См. Rolland et al. J Immunol. (2005) 174:3067-3071).
Третий член семейства PDGFR, рецептор колониестимулирующего фактора-1 (CSF-1R) (также называемый рецептором фактора стимулирования колоний макрофагов (M-CSFR) или fms) экспрессируется многими карциномами груди и раковыми заболеваниями эпителия человека, особенно репродуктивных органов женщин (Kacinski (1997) Mol. Reprod. Dev. 46:71-74), и представляет собой потенциальную мишень для терапии раковых заболеваний. Высокий уровень экспрессирования CSF-1 при солидных опухолях и лейкемиях также говорит о том, что CSF-1R может представлять собой терапевтическую мишень при раковых заболеваниях крови и солидных опухолях (Haran-Ghera (1997) Blood 89:2537-2545). Высокий уровень экспрессирования CSF-1 также обнаружен при гистиоцитозе клеток Лангерганса (Rolland et al. J Immunol. (2005) 174:3067-3071).
Kit (или рецептор фактора стволовых клеток, или SCFR) является другим членом семейства PDGFR, и присутствие мутаций kit представляет собой ключевой диагностический маркер для стромальных опухолей желудочно-кишечного тракта (GIST) (Duensing et al. (2004) Cancer Investigation 22(1): 106-116). Gleevec® (иматиниб мезилат или STI571), первый одобренный FDA ингибитор RPTK, изначально одобренный для опосредованной c-Abl-хронической миелоидной лейкемии, получил одобрение FDA для опосредованных Kit GIST в 2002 году и имеет доказанный на молекулярном уровне подход ингибирования Kit для лечения GIST (Giorgi and Verweij, Mol Cancer Ther 4(3):495-501(2005)). Увеличение функциональных мутаций рецептора Kit также связывается с лейкемией тучных клеток/миелоидной лейкемией и семиномами/дисгерминомами (Blume-Jensen Nature 411(17): 355-365(2001)). Мутации Kit также идентифицируются при определенных меланомах и определяются как потенциальная терапевтическая мишень для меланомы (Curtain et al. J Clin. Oncol. 24(26):4340-4346 (2006)).
Рецептор фактора роста эндотелия сосудов (VEGFR) представляет другое семейство RTK, которое вовлечено в ангиогенез опухолей. VEGF и его рецепторы VEGFR1 (также называемый Flt1) и VEGFR2 (также называемый KDR) сверхэкспрессируются в подавляющем большинстве клинически важных раковых заболеваний человека, включая раковые заболевания желудочно-кишечного тракта, поджелудочной железы, мочевого пузыря, почек, эндометрия, и при саркоме Капоши. VEGFR2 также активно экспрессируются при определенных интракраниальных опухолях, включая мультиформную глиобластому и спорадическую и связанную с синдромом фон Хиппеля-Ландау (VHL) капиллярную гемангиобластому. В настоящее время в клинической разработке находится более дюжины ингибиторов VEGFR2 для антиангиогенной терапии (Paz and Zhu, Frontiers in Bioscience 10:1415-1439 (2005)).
Другой член семейства VEGFR, VEGFR3 (также называемый Fit 4) идентифицируется как рецептор лимфангиогенного фактора роста, который играет ключевую роль в росте новых лимфатических сосудов (лимфангиогенезе). Активирование пути передачи сигналов VEGFR3, как показано, стимулирует метастатическое распространение клеток опухолей (см. Stacker et al. Nature Rev 2:573-583(2002)), и по этой причине его ингибирование могло бы стать основой для лечения состояний, отличающихся аномальным функционированием лимфатических сосудов (см. Stacker et al. Current Pharmaceutical Design 10:65-74 (2004), Achen et al. British Journal of Cancer 94:1355-1360 (2006)).
Киназа Ret представляет собой еще один RTK, который, как показано, экспрессируется при медуллярной тироидной карциноме, состоянии, которое является частью синдромов множественной эндокринной неоплазии 2A и 2B (MENS 2A и 2B). Ret является конститутивно активным при медуллярной тироидной карциноме (как при наследственной, так и при спорадической) и при папиллярной тироидной карциноме. Некоторые известные ингибиторы RTK, имеющие Ret-ингибиторную активность, как показано, являются эффективными при ингибировании роста опухоли на моделях голых мышей (Stock et al., Cancer Res 63:5559-5563 (2003)) и Carlomagno et al., Journal of the National Cancer Institute 98(5):326-334 (2006)).
В дополнение к этому, возможно, что ингибиторы определенных киназ могут быть пригодными для лечения заболеваний, когда киназа не подвергается нарушению регуляции, но, тем не менее, является критически важной для поддержания болезненного состояния. В таких случаях ингибирование активности киназы действовало бы либо как лекарство, либо как паллиатив для этих заболеваний. Например, множество вирусов, таких как вирус папилломы человека, разрушает клеточный цикл и перемещает клетки в S-фазу клеточного цикла (Vousden, FASEB Journal, 7:872-879 (1993)). Предотвращение вхождения клеток в фазу синтеза ДНК после вирусной инфекции посредством ингибирования основных активностей инициирования S-фазы может прервать жизненный цикл вируса посредством предотвращения репликации вируса. Такой же принцип может использоваться для защиты нормальных клеток организма от токсичности циклоспецифичных химиотерапевтических агентов (Stone et al., Cancer Research, 56:3199-3202 (1996); Kohn et al., Journal of Cellular Biochemistry, 54:44-452 (1994)).
Наконец, хотя сверхактивирование путей передачи сигналов RTK часто представляет собой основной механизм для ракового заболевания, ослабление дезактивации RTK, такое как ослабленная отрицательная регуляция RTK посредством индуцированного лигандами эндоцитоза или ослабление петель отрицательной обратной связи, также может представлять собой причину некоторых злокачественных образований. Другая стратегия использования молекул, обсуждаемых здесь, заключается по этой причине в исправлении и облегчении любого существующего механизма отрицательной регуляции RTK.
Принимая во внимание большое количество ингибиторов протеинкиназ и множество опосредованных PK пролиферативных, воспалительных и иммуннофункциональных заболеваний, имеется насущная необходимость в создании новых классов соединений, которые пригодны для использования в качестве ингибиторов PK и, таким образом, при лечении заболеваний, связанных с PK, как здесь обсуждается.
Сущность изобретения
Предлагаются соединения для применения при медицинском лечении, фармацевтические композиции и способы модулирования активности, связывания или субклеточного распределения киназ. В одном из вариантов осуществления соединения для использования в композициях и способах, представленных в настоящем описании, имеют формулу (I):
где
связь b представляет собой одинарную связь или двойную связь;
X представляет собой -S-, -N(R5) или -O-;
Z1 и Z3, каждый, независимо представляет собой -N(R5), -(CH2)q, -O-, -S- или прямую связь;
Z2 представляет собой -C(O) или -C(S);
m представляет собой целое число от 1 до 2;
n представляет собой целое число от 1 до 3;
каждый из q независимо представляет собой целое число от 1 до 4;
R0 представляет собой водород, галоген, гидрокси, необязательно замещенный алкил или необязательно замещенный алкокси;
каждый из R1 независимо выбирают из группы, состоящей из галогена, необязательно замещенного алкила, необязательно замещенного алкенила, необязательно замещенного алкинила, необязательно замещенного гетероциклилалкила, необязательно замещенного гетероциклилалкенила, необязательно замещенного гетероаралкила, необязательно замещенного гетероаралкенила, -R6OR7, -R6SR7, -R6S(O)tR8 (где t равно 1 или 2), -R6N(R7)2, -R6OR9OR7, -R6CN, -R6C(O)R7, -R6C(S)R7, -R6C(NR7)R7, -R6C(O)OR7, -R6C(S)OR7, -R6C(NR7)OR7, -R6C(O)N(R7)2, R6C(S)N(R7)2, -R6C(NR7)N(R7)2, -R6C(O)N(R7)R9N(R7)2, -R6C(O)SR8, -R6C(S)SR8, -R6C(NR7)SR8, -R6S(O)tOR7 (где t равно 1 или 2), -R6S(O)tN(R7)2 (где t равно 1 или 2), -R6S(O)tN(R7)N(R7)2 (где t равно 1 или 2), -R6S(O)tN(R7)N=C(R7)2, -R6S(O)tN(R7)C(O)R8 (где t равно 1 или 2), -R6S(O)tN(R7)C(O)N(R7)2 (где t равно 1 или 2), -R6S(O)tN(R7)C(NR7)N(R7)2 (где t равно 1 или 2), -R6N(R7)C(O)R8, -R6N(R7)C(O)OR8, -R6N(R7)C(O)SR8, -R6N(R7)C(NR7)SR8, -R6N(R7)C(S)SR8, -R6N(R7)C(O)N(R7)2, -R6N(R7)C(NR7)N(R7)2, -R6N(R7)C(S)N(R7)2, -R6N(R7)S(O)tR8 (где t равно 1 или 2), -R6OC(O)R8, -R6OC(NR7)R8, -R6OC(S)R8, -R6OC(O)OR8, -R6OC(NR7)OR8, -R6OC(S)OR8, -R6OC(O)SR8, -R6OC(O)N(R7)2, -R6OC(NR7)N(R7)2, -R6OC(S)N(R7)2, -R6OR9N(R7)2, -R6SR9N(R7)2, -R6N(R7)R9N(R7)2, -R6C(O)R9C(O)R7, -R5C(O)R9C(S)R7, -R6C(O)R9C(NR7)R7, -R6C(O)R9C(O)OR7, -R6C(O)R9C(S)OR7, -R6C(O)R9C(NR7)OR7, -R6C(O)R9C(O)N(R7)2, -R6C(O)R9C(S)N(R7)2, -R6C(O)R9C(NR7)N(R7)2, -R6C(O)R9C(O)SR8, -R6C(O)R9C(S)SR8, -R6C(O)R9C(NR7)SR8, -R6C(O), -R6C(O)R9N(R7)R9N(R7)2, -R6C(O)R9N(R7)R9OR7 и -R6C(O)N(R7)R9OR7;
каждый из R2 независимо выбирают из водорода, галогена, нитро, циано, необязательно замещенного алкила, -OR12, -SR12, -N(R12)2, -S(O)tR13 (где t равно 1 или 2), -C(O)R12, -C(O)OR12, -C(O)N(R12)2, -C(O)SR12 или -N(R12)S(O)tR13 (где t равно 1 или 2);
R3 представляет собой водород, галоген, нитро, циано, необязательно замещенный алкил, -OR12, -SR12, -N(R12)2, -S(O)tR13 (где t равно 1 или 2), -C(O)R12, -C(O)OR12, -C(O)N(R12)2, -C(O)SR12 или -N(R12)S(O)tR13 (где t равно 1 или 2);
R4 выбирают из группы, состоящей из необязательно замещенного алкила, необязательно замещенного гетероциклила, необязательно замещенного гетероарила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкенила и необязательно замещенного арила;
каждый из R5 независимо представляет собой водород или необязательно замещенный алкил;
каждый из R6 независимо представляет собой одинарную связь, необязательно замещенный алкилен с прямой или разветвленной цепью или необязательно замещенный алкенилен с прямой или разветвленной цепью;
каждый из R7 независимо выбирают из (i) или (ii) ниже
(i) R7 выбирают из группы, состоящей из водорода, необязательно замещенного алкила, необязательно замещенного алкенила, необязательно замещенного алкинила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного арила, необязательно замещенного аралкила, необязательно замещенного гетероциклила, необязательно замещенного гетероциклилалкила, необязательно замещенного гетероарила и необязательно замещенного гетероаралкила, или
(ii) два (R7) вместе с атомом, к которому они присоединены, образуют необязательно замещенный гетероциклил или необязательно замещенный гетероарил;
R8 независимо выбирают из группы, состоящей из необязательно замещенного алкила, необязательно замещенного алкенила, необязательно замещенного алкинила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного арила, необязательно замещенного аралкила, необязательно замещенного гетероциклила, необязательно замещенного гетероциклилалкила, необязательно замещенного гетероарила и необязательно замещенного гетероаралкила;
каждый из R9 независимо представляет собой необязательно замещенный алкилен с прямой или разветвленной цепью или необязательно замещенный алкенилен с прямой или разветвленной цепью;
каждый из R12 независимо выбирают из группы, состоящей из водорода, необязательно замещенного алкила, необязательно замещенного алкенила, необязательно замещенного алкинила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного арила, необязательно замещенного аралкила, необязательно замещенного гетероциклила, необязательно замещенного гетероциклилалкила, необязательно замещенного гетероарила и необязательно замещенного гетероаралкила; и
R13 независимо выбирают из группы, состоящей из необязательно замещенного алкила, необязательно замещенного алкенила, необязательно замещенного алкинила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного арила, необязательно замещенного аралкила, необязательно замещенного гетероциклила, необязательно замещенного гетероциклилалкила, необязательно замещенного гетероарила и необязательно замещенного гетероаралкила.
В одном из вариантов осуществления соединение выбирают при условии, что
(i) если -Z1Z2Z3R4 представляет собой -NHC(O)Bu, тогда R1 не может представлять собой этокси;
(ii) если -Z1Z2Z3R4 представляет собой -C(O)ORp, где Rp = метил или этил, тогда R1 не может представлять собой гидроксил, метокси или метоксикарбонил;
(iii) если -Z1Z2Z3R4 представляет собой -NHC(O)C(O)ORp, где Rp = метил или этил, тогда R1 не может представлять собой метокси;
(iv) если -Z1Z2Z3R4 представляет собой -CH2C(O)ORp, где Rp = метил или этил, тогда R1 не может представлять собой метокси или этокси;
(v) если -Z1Z2Z3R4 представляет собой -OC(O)CH3, тогда R1 не может представлять собой метил, метокси или этокси;
в виде индивидуального изомера, смеси изомеров, рацемической смесь изомеров, сольвата, гидрата или пролекарства, или в виде его фармацевтически приемлемой соли.
В одном из вариантов осуществления соединение, представленное в настоящем описании, представляет собой фармацевтически приемлемую соль соединения формулы (I). В одном из вариантов осуществления соединения, представленные в настоящем описании, представляют собой сольват соединения формулы (I). В одном из вариантов осуществления соединения, представленные в настоящем описании, представляют собой гидрат соединения формулы (I). В одном из вариантов осуществления соединение, представленное в настоящем описании, представляет собой пролекарство соединения формулы (I).
Такие соединения могут связываться с одной или несколькими киназами с высоким сродством и модулировать их активность. В определенном варианте осуществления такие соединения демонстрируют EC50, IC50 или сродство связывания менее чем 1 мкМ, а в определенных вариантах осуществления менее примерно чем 0,5 мкМ, 250 нМ, 100 нМ или 50 нМ. В одном из аспектов соединения, представленные в настоящем описании, являются селективными к конкретной киназе или к конкретному подмножеству киназ, то есть являются, по меньшей мере, в 5, 10 или, в другом аспекте, по меньшей мере, в 20, 50, 100 раз более активными, согласно измерению с помощью любого из анализов in vitro, описанных здесь, при связывании с желаемой киназой (киназами), по сравнению с непредпочтительной киназой или киназами. В одном из аспектов соединения селективно ингибируют желаемую киназу (киназы) без значительного воздействия на нежелательную киназу (киназы).
Также предусматриваются фармацевтические композиции, предназначенные для введения с помощью соответствующего способа, и средства, содержащие эффективные концентрации одного или нескольких соединений, представленных в настоящем описании, или их фармацевтически приемлемых солей, сольватов, гидратов и пролекарств, и необязательно содержащие по меньшей мере один фармацевтический носитель, наполнитель, основу, связывающее вещество, разбавитель, разрыхляющий агент, смазывающее вещество, глидант, подслащивающий агент или ароматизирующий агент.
Такие фармацевтические композиции доставляют количества, эффективные для лечения, предотвращения или облегчения заболеваний или расстройств, которые модулируются или подвергаются другому влиянию протеинкиназ (заболеваний, связанных с PK), или одного или нескольких их симптомов или причин. Такие заболевания или расстройства включают в себя, но не ограничиваясь этим,
A) Раковые заболевания, включая, но не ограничиваясь этим, рак головы и шеи (локализованный на губе, в ротовой полости, мезофаринксе, гипофаринксе, глотке, носоглотке, носовой полости и параназальных синусах слюнных желез); рак легких, включая мелкоклеточный рак легких, немелкоклеточный рак легких; раковые заболевания желудочно-кишечного тракта, включая рак пищевода, рак желудка, рак толстой и прямой кишки, рак заднего прохода, рак поджелудочной железы, рак печени, рак желчного пузыря, рак желчных проходов вне печени, рак фатеровой ампулы; рак груди; гинекологические раковые заболевания, включая рак шейки матки, рак матки, вагинальный рак, рак женских половых органов, рак яичников, гестационное трофобластическое раковое новообразование; рак яичек; раковые заболевания мочеполового тракта, включая рак почек, рак мочевого пузыря, рак простаты, рак пениса, рак уретры; неврологические опухоли; эндокринные новообразования, включая карциноидные опухоли и опухоли островковых клеток, феохромоцитому, кортикальную карциному надпочечников, карциному щитовидной железы и метастазы в эндокринные железы.
Дополнительные примеры раковых заболеваний представляют собой карциному базальных клеток; сквамозно-клеточную карциному; хондросаркому (рак, возникающий в клетках хрящей); мезенхимальную хондросаркому; саркомы мягких тканей, включая злокачественные опухоли, которые могут возникать в любой из мезодермальных тканей (мышцы, сухожилия, сосуды, которые переносят кровь или лимфу, суставы и жир); саркомы мягких тканей включают в себя саркому альвеолярных мягких тканей, ангиосаркому, фибросаркому, лейомиосаркому, липосаркому, злокачественную фиброзную гистиоцитому, гемангиоперицитому, мезенхимому, шванному, периферические нейроэктодермальные опухоли, рабдомиосаркому, синовиальную саркому; гестациональные трофобластические опухоли (злокачественное образование, при котором ткани, формируемые в матке, становятся раковыми после зачатия); лимфому Ходжкина и ларингиальный рак.
В одном из вариантов осуществления рак включает в себя различные типы лейкемий, таких как хроническая лимфоцитарная лейкемия, хроническая миелоцитарная лейкемия, острая лимфобластическая лейкемия, острая миелогенная лейкемия и острая миелобластическая лейкемия.
В некоторых вариантах осуществления острая лейкемия включает в себя, но не ограничиваясь этим, недифференцированную AML (M0), миелобластическую лейкемию (M1), миелобластическую лейкемию (M2), промиелоцитарную лейкемию (M3 или вариант M3 [M3V]), миеломоноцитарную лейкемию (M4 или вариант M4 с эозинофилией [M4E]), моноцитарную лейкемию (M5), эритролейкемию (M6), мегакариобластическую лейкемию (M7). В некоторых вариантах осуществления острая лимфоцитарная лейкемия (ALL) включает в себя лейкемию, которая возникает в бластических клетках костного мозга (B-лимфоциты), тимусе (T-лимфоциты) и лимфатических узлах. Острая лимфоцитарная лейкемия делится на категории как L1 выглядящие зрелыми лимфобласты (T-лимфоциты или пре-B- лимфоциты), L2 незрелые и плеоморфные (различной формы) лимфобласты (T-лимфоциты или пре-B-лимфоциты) и L3-лимфобласты (B-лимфоциты; клетки Беркета).
В одном из вариантов осуществления рак представляет собой рак желудка, желудочно-кишечного тракта, костей, яичников, толстой кишки, легких, мозга, глотки, лимфатической системы, мочеполового тракта, сквамозно-клеточную карциному, астроцитому, саркому Капоши, глиобластому, рак легких, рак мочевого пузыря, рак головы и шеи, меланому, рак простаты, рак груди, мелкоклеточный рак легких, лейкемию, глиому, рак толстой и прямой кишки, рак мочеполовой системы, рак желудочно-кишечной системы, гематологическое раковое заболевание или рак поджелудочной железы. В частности, острую миелогенную лейкемию (AML), острые лимфобластические лейкемии предшественников B-лимфоцитов, миелодиспластические лейкемии, острые лимфобластические лейкемии T-лимфоцитов и хронические миелогенные лейкемии (CML).
Раковые заболевания, подлежащие лечению, могут быть первичными или метастатическими. В одном из вариантов осуществления рак представляет собой солидную или возникающую в крови метастатическую опухоль. В другом варианте осуществления рак представляет собой метастатический рак костей.
B) Незлокачественные пролиферативные заболевания; атеросклероз, рестеноз после сосудистой ангиопластики и фибропролиферативные расстройства, такие как облитерирующий бронхиолит.
C) Воспалительные заболевания или расстройства, связанные с иммунной дисфункцией, включая иммуннодефицит, иммуномодуляцию, аутоиммунные заболевания, отторжение тканей, заживление ран, заболевание почек, аллергию, воспалительное заболевание желудка, красную волчанку, артрит, остеоартрит, ревматоидный артрит, астму и ринит.
D) Инфекционные заболевания, опосредованные либо вирусными, либо бактериальными патогенами.
В настоящем описании предусматриваются композиции и способы лечения заболевания, включающие введение субъекту эффективного количества соединения, модулирующего Kit или рецептор фактора стволовых клеток (SCFR). В одном из вариантов осуществления заболевание представляет собой рак. В другом варианте осуществления заболевание представляет собой карциному. В некоторых вариантах осуществления, рак представляет собой мелкоклеточный рак легких или рак груди. В другом варианте осуществления заболевание представляет собой карциному простаты. Еще в одном варианте осуществления рак представляет собой эндометриальный рак. В другом варианте осуществления рак представляет собой глиому. В другом варианте осуществления рак представляет собой злокачественную опухоль или гематологическое злокачественное состояние, такое как лейкемия и лимфома. В некоторых вариантах осуществления, лейкемия представляет собой острую миелогенную лейкемию (AML). В некоторых вариантах осуществления, лейкемия представляет собой лейкемию тучных клеток. В другом варианте осуществления заболевание представляет собой системный мастоцитоз. Еще в одном варианте осуществления заболевание представляет собой миелодиспластический синдром (MDS). В некоторых вариантах осуществления, злокачественная опухоль представляет собой опухоль половых клеток. В другом варианте осуществления опухоль половых клеток представляет собой семиому и/или дисгерминому. Еще в одном варианте осуществления заболевание представляет собой стромальную опухоль желудочно-кишечного тракта (GIST). Еще в одном варианте осуществления заболевание представляет собой опухоль тучных клеток, меланому или нейробластому.
В настоящем описании предусматриваются композиции и способы лечения заболевания, включающие введение субъекту, нуждающемуся в этом, эффективного количества соединения, модулирующего рецептор фактора роста, полученного из тромбоцитов (PDGF). В одном из вариантов осуществления заболевание представляет собой рак. В другом варианте осуществления заболевание представляет собой карциному. В другом варианте осуществления карцинома представляет собой карциному яичников. Еще в одном варианте осуществления карцинома представляет собой карциному груди. В другом варианте осуществления карцинома представляет собой карциному клеток надпочечников. Еще в одном варианте осуществления заболевание представляет собой саркому. В других вариантах осуществления, рак представляет собой злокачественную опухоль или гематологическое злокачественное состояние, такое как лейкемия и лимфома. В некоторых вариантах осуществления, лейкемия представляет собой острую лимфобластическую лейкемию (ALL). В другом варианте осуществления лейкемия представляет собой хроническую миелогенную лейкемию (CML). В некоторых вариантах осуществления, лимфома представляет собой лимфому T-лимфоцитов. В другом варианте осуществления заболевание представляет собой идиопатический гиперэозинофильный синдром (HES). В другом варианте осуществления заболевание представляет собой хроническую эозинофильную лейкемию (CEL). В некоторых вариантах осуществления, злокачественная опухоль представляет собой меланому или глиобластому. В другом варианте осуществления заболевание представляет собой ангиогенез опухоли. В дополнительном варианте осуществления заболевание представляет собой незлокачественное пролиферативное заболевание. В некоторых вариантах осуществления, незлокачественное пролиферативное заболевание представляет собой атеросклероз или рестеноз. Еще в одном варианте осуществления заболевание представляет собой фибропролиферативное расстройство. В некоторых вариантах осуществления, фибропролиферативное расстройство представляет собой облитерирующий бронхиолит. В другом варианте осуществления фибропролиферативное расстройство представляет собой идиопатический миелофиброз.
В настоящем описании предусматриваются композиции и способы лечения заболеваний, включающие введение субъекту, нуждающемуся в этом, эффективного количества соединения, модулирующего рецептор Flt-3. В одном из вариантов осуществления заболевание представляет собой рак. В другом варианте осуществления заболевание представляет собой карциному. В некоторых вариантах осуществления, рак представляет собой мелкоклеточный легких рак или рак груди. В других вариантах осуществления, рак представляет собой злокачественную опухоль или гематологическое злокачественное состояние, такое как лейкемия и лимфома. В другом варианте осуществления заболевание представляет собой гематологическое злокачественное состояние, такое как лейкемия и/или лимфома. В некоторых вариантах осуществления, лейкемия представляет собой острую миелогенную лейкемию (AML) или представляет собой хроническую миелоидную лейкемию (CML). В некоторых вариантах осуществления, рак представляет собой острую лимфобластическую лейкемию (ALL), миелодиспластическую лейкемию, острую лимфобластическую лейкемию T-лимфоцитов и острую лимфобластическую лейкемию B-лимфоцитов. В другом варианте осуществления расстройство представляет собой миелодиспластический синдром. Еще в одном варианте осуществления заболевание представляет собой расстройство иммунной системы и/или воспалительное заболевание. В другом варианте осуществления расстройство иммунной системы представляет собой системную красную волчанку. В другом варианте осуществления расстройство иммунной системы представляет собой воспалительное заболевание желудка. В другом варианте осуществления воспалительное заболевание желудка представляет собой болезнь Крона и/или язвенный колит. В другом варианте осуществления расстройство иммунной системы представляет собой хроническое обструктивное легочное заболевание.
В настоящем описании предусматриваются композиции и способы лечения заболевания, включающие введение субъекту, нуждающемуся в этом, эффективного количества соединения, модулирующего VEGFR. В одном из вариантов осуществления заболевание представляет собой рак. В другом варианте осуществления заболевание представляет собой карциному. В другом варианте осуществления заболевание представляет собой солидную опухоль. В другом варианте осуществления заболевание представляет собой метастатическую опухоль. В другом варианте осуществления заболевание представляет собой стромальные опухоли. Еще в одном варианте осуществления заболевание представляет собой нейроэндокринные опухоли. Еще в одном варианте осуществления заболевание или расстройство представляет собой ангиогенез опухоли. В другом варианте осуществления заболевание представляет собой саркому. В другом варианте осуществления саркома представляет собой саркому Капоши, гемангиосаркому и/или лимфангиосаркому.
В настоящем описании предусматриваются композиции и способы лечения заболевания, включающие введение субъекту, нуждающемуся в этом, эффективного количества соединения, модулирующего CSF-1R (или fms-). В одном из вариантов осуществления заболевание представляет собой рак. В другом варианте осуществления заболевание представляет собой карциному. Еще в одном варианте осуществления заболевание представляет собой метастатическую опухоль. В другом варианте осуществления метастатическая опухоль представляет собой метастазы в костях. Еще в одном варианте осуществления заболевание представляет собой гистиоцитоз клеток Лангерганса. Еще в одном варианте осуществления заболевание представляет собой расстройство иммунной системы и/или воспалительное заболевание. В другом варианте осуществления расстройство иммунной системы представляет собой системную красную волчанку. В другом варианте осуществления расстройство иммунной системы представляет собой воспалительное заболевание желудка. В другом варианте осуществления воспалительное заболевание желудка представляет собой болезнь Крона и/или язвенный колит. В другом варианте осуществления расстройство иммунной системы представляет собой ревматоидный артрит. Еще в одном варианте осуществления расстройство иммунной системы представляет собой рассеянный склероз. Еще в одном варианте осуществления расстройство иммунной системы представляет собой системную красную волчанку. Еще в одном варианте осуществления расстройство иммунной системы представляет собой аллергический ринит и/или астму. В другом варианте осуществления расстройство иммунной системы представляет собой диабет типа 1.
В настоящем описании предусматриваются композиции и способы лечения заболевания, включающие введение субъекту, нуждающемуся в этом, эффективного количества соединения, модулирующего Ret. В одном из вариантов осуществления заболевание представляет собой рак. В другом варианте осуществления заболевание представляет собой карциному. Еще в одном варианте осуществления карцинома представляет собой тироидную карциному. Еще в одном варианте осуществления тироидная карцинома представляет собой спорадическую или наследственную медуллярную карциному. В другом варианте осуществления тироидная карцинома представляет собой папиллярную тироидную карциному. Еще в одном варианте осуществления тироидная карцинома представляет собой карциному щитовидной железы. В другом варианте осуществления заболевание представляет собой множественную эндокринную неоплазию 2A или 2B.
В настоящем описании также рассматриваются комбинированные терапии с использованием одного или нескольких соединений или композиций, представленных в настоящем описании, или их фармацевтически приемлемых производных в сочетании с другими фармацевтическими активными агентами для лечения заболеваний и расстройств, описанных здесь.
В одном из вариантов осуществления такие дополнительные фармацевтические агенты включают в себя один или несколько из следующих агентов: противораковые агенты и противовоспалительные агенты.
Соединение или композиция, представленные в настоящем описании, или их фармацевтически приемлемое производное, может вводиться одновременно с введением одного или нескольких из указанных выше агентов, до или после него. Также предусматриваются фармацевтические композиции, содержащие соединение, представленное в настоящем описании, и один или несколько из указанных выше агентов.
При осуществлении этих способов эффективные количества соединений или композиций, содержащих терапевтически эффективные концентрации соединений, которые приготавливаются для системной доставки, включая парентеральную, пероральную или внутривенную доставку, или для локального или местного применения, вводятся индивидууму, демонстрирующему симптомы заболевания или расстройства, которое должно лечиться. Эти количества являются эффективными для облегчения или устранения одного или нескольких симпто