Рекомбинантный белок, несущий эпитопы вируса папилломы человека, встроенные в белок аденилатциклазу или его фрагмент, его терапевтическое применение
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, вирусологии и медицины. Описан рекомбинантный белок, содержащий один или несколько полипептидов, несущих один или несколько эпитопов одного или нескольких антигенов вируса папилломы человека ВПЧ. При этом указанные полипептиды встроены в один или в различные пермиссивные сайты белка аденилатциклазы (CyaA) или его фрагмента. Указанный фрагмент CyAa сохраняет свойство указанного белка аденилатциклазы направленно взаимодействовать с антиген-презентирующими клетками. Также описан полинуклеотид, кодирующий такой белок, и их использование в системах экспрессии для получения иммуногенных композиций и лекарственных средств. Изобретение может быть использовано в медицине. 17 н. и 43 з.п. ф-лы, 21 ил., 1 табл.
Реферат
Настоящая заявка относится к рекомбинантному белку, несущему эпитопы вируса папилломы, встроенные в белок аденилатциклазу или его фрагмент.
Соответственно, данное изобретение относится к рекомбинантным белкам, в которых белок аденилатциклаза (CyaA) действует как белковый вектор, для формирования иммунного ответа на эпитопы, полученные из антигенов вируса папилломы (папилломавируса), в частности - из антигенов вируса папилломы человека.
Изобретение относится, в частности, к применению полученных таким образом белковых векторов для доставки эпитопов в эукариотические клетки, предпочтительно - в клетки млекопитающих, в частности - в клетки человека.
Данное изобретение также относится к полинуклеотидам, кодирующим рекомбинантный белок согласно данному изобретению, векторам, содержащим указанные полинуклеотиды, а также клетками-хозяевами, содержащим указанные полинуклеотиды или векторы.
Изобретение относится также к способам применения упоминавшегося выше рекомбинантного белка или полинуклеотидов для лечения или профилактики ВПЧ-инфекции (инфекции, вызванной вирусом папилломы человека) у хозяина, а также для лечения или профилактики злокачественных эффектов, возникающих при инфицировании вирусом папилломы человека, у хозяина, в частности у хозяина, представляющего собой млекопитающее. В конкретном способе реализации, данное изобретение обеспечивает средство, пригодное для создания соединений, подходящих для иммунотерапии, в частности - иммунотерапии, направленной против опухоль-специфических антигенов вирусов папилломы (папилломавирусов).
Некоторые из многочисленных типов вирусов папилломы человека (ВПЧ, HPV), определяемые как высокоопасные, связаны с развитием злокачественных заболеваний эпителиальных тканей при персистировании инфекции в организме хозяина: (1) Рак шейки матки, второе по распространенности в мире опухолевое гинекологическое заболевание, (1) ассоциирован (>99%), в основном, с выявлением ДНК вирусов ВПЧ16 и ВПЧ18 (2). Онкогенный потенциал этих вирусов относят на счет продуктов экспрессии ранних генов, т.е. генов E6 и E7, экспрессия которых определяется на протяжении всего цикла репликации вируса и которая необходима для начала и поддержания злокачественной трансформации. Однако высокая частота аногенитальных инфекций, вызываемых этими высокоопасными типами ВПЧ (2) контрастирует с низкой долей лиц, у которых в конце концов развиваются злокачественные заболевания, ассоциированные с ВПЧ, что позволяет сделать предположение о том, что инфекции, вызываемые высокоопасными типами ВПЧ сдерживаются посредством иммунного ответа. Данное предположение подтверждают такие наблюдения, как: спонтанное обратное развитие (регрессия) большинства предраковых поражений (1), инфильтрация регрессирующих генитальных бородавок CD4+ Т-лимфоцитами и макрофагами (1), а также повышенное число инфицированных лиц, выявленных среди пациентов с иммуносупрессией или иммунодефицитом (1). Кроме того, в крови пациентов, у которых были диагностированы злокачественные заболевания, ассоциированные с ВПЧ 16-, также как в крови здоровых лиц (9, 10), выявили ответы CD4+ и CD8+ Т-лимфоцитов против эпитопов Е6 и/или Е7 ВПЧ16. Эти факторы в совокупности создают предпосылки для разработки иммунотерапии, направленной на белки Е6 и/или Е7 вируса ВПЧ16.
Было разработано много стратегий вакцинирования для предотвращения роста опухолей из HPV16 -Е6 и -Е7-положительных линий клеток опухоли у мышей C57BL/6 путем выработки иммунных ответов на фрагмент эпитопа H-2Db HPV16-E749-57. В этих подходах к вакцинации использовали плазмидную ДНК, вирусные или бактериальные векторы, химерные вирусоподобные частицы, синтетические пептиды и рекомбинантные белки (11). К сожалению, в отношении клинической регрессии, эти подходы дали слабо удовлетворительные результаты (3). Поэтому все еще представляет интерес разработка новых средств для обеспечения взаимодействия эпитопов ВПЧ с иммунной системой с целью стимулирования клеточного (иммунного) ответа.
Таким образом, существует потребность в новых векторах, пригодных для доставки эпитопов антигенов ВПЧ к клеткам-мишеням в условиях, подходящих для возникновения гуморального и/или клеточного иммунного ответа на указанные антигены организме хозяина. Авторы настоящего изобртения обнаружили, что белок аденилатциклаза может представлять интерес для создания такого вектора. Были сделаны разнообразные наблюдения с использованием белка аденилатциклазы бактерии Bordetella pertussis. Эти наблюдения привели к заключению, что этот белок может быть подходящей основой для создания эффективного вектора.
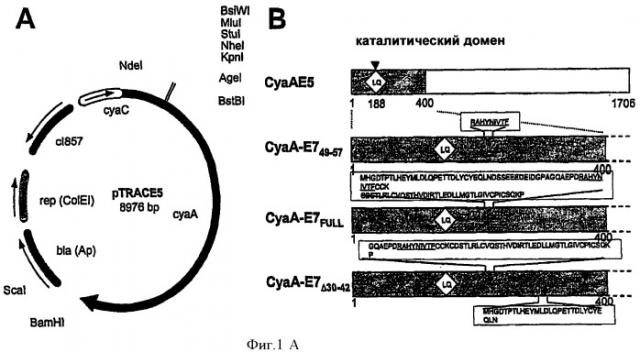
Аденилатциклаза (CyaA) бактерии Bordetella pertussis обладает способностью доставлять свой каталитический домен в цитозоль эукариотических клеток (12). Следовательно, эпитопы CD4+ и CD8+ Т-клеток, встроенные в каталитический сайт аденилатциклазы процессируются и презентируются белками основного комплекса гистосовместимости классов I и II, соответственно, на поверхность антиген-презентирующих клеток (АПК) (13). Кроме того, недавно было показано, что аденилатциклаза специфическим образом связывается с интегрином αмβ2 (CD11b/CD18) (14, WO 02/22169) и, следовательно, нацеливает эти эпитопы Т-клеток на CD11b+ субпопуляцию отросчатых клеток (15). Иммунизация мышей рекомбинантной аденилатциклазой, несущей соответствующие эпитопы стимулирует мощный ответ со стороны цитотоксических Т-лимфоцитов (ЦТЛ), полный иммунитет к летальному инфицированию вирусом и эффективный профилактический и терапевтический противоопухолевый иммунитет (16, 17). Белок аденилатциклаза (CyaA) и его приготовление по технологии рекомбинантных ДНК описаны, например - в международных заявках WO 93/21324 и WO 02/22169. В WO 02/22169 описано, что фрагменты аденилатциклазы, содержащие остатки с 373 по 1706 содержат структуру, необходимую для взаимодействия с рецептором CD11b/CD18.
Позднее было более конкретно описано, что последовательность аминокислот, протяженностью от остатка 1166 до остатка аминокислоты 1281, содержит детерминанту взаимодействия с рецептором CD11b/CD18, а более точно - что последовательность аминокислот, от остатка 1208 до остатка 1243, ответственна за взаимодействие этого токсина с CD11b/CD18 (Евразийские патенты ЕР 03291486.3 и 45).
Авторы настоящего изобретения определили и исследовали условия создания рекомбинантного белка CyaA, несущего, т.е. содержащего, эпитопы антигенов ВПЧ, который может доставлять указанные эпитопы в клетки-мишени, в особенности - к антиген-презентирующим клеткам хозяина, в том числе хозяина, страдающего ВПЧ-инфекцией и ее злокачественными трансформациями.
Соответственно, данное изобретение относится, в частности, к рекомбинантному белку, содержащему один или несколько полипептидов, несущих один или несколько эпитопов одного или нескольких антигенов ВПЧ, причем указанные полипептиды встроены в один или разные подходящие сайты белка аденилатциклазы (CyaA) или его фрагмента, причем указанный фрагмент аденилатциклазы сохраняет свойство белка аденилатциклазы взаимодействовать с клетками-мишенями CyaA, такими как антиген-презентирующие клетки, в частности клетками, имеющими фенотип CD11b/CD18, такими как отросчатые клетки. В конкретном способе реализации указанный фрагмент также сохраняет свойство CyaA обеспечивать перемещение встроенного в нее эпитопа или полипептида, содержащего указанный эпитоп, в цитозоль клетки-мишени. Перемещение эпитопа или полипептида, содержащего указанный эпитоп, становится возможным, если фрагмент CyaA содержит домен, который обеспечивает перемещение каталитического домена этого белка.
Рекомбинантный белок согласно настоящему изобретению можно приготовить, с использованием технологии рекомбинантных ДНК. Его можно также получить путем синтеза, в частности, путем химического синтеза. Следовательно, термин «рекомбинантный белок» относится к химерной форме белка.
Способность рекомбинантного белка взаимодействовать с CD11b/CD18 клетками можно оценить, в частности, способами, раскрытыми в ЕР 03291486.3 и (45) или в WO 02/22169. Кроме того, способность рекомбинантного белка перемещать эпитоп или полипептид, содержащий указанный эпитоп, в цитозоль клетки-мишени можно оценить при помощи способа, описанного в WO 02/22169.
В конкретном способе реализации фрагмент аденилатциклазы может состоять из двух разных частей белка CyaA, которые не представляют собой неперерывный фрагмент природного CyaA. В качестве примера можно привести каталитический домен CyaA, т.е. 400 остатков аминокислот N-концевой части CyaA, и фрагмент, содержащий остатки аминокислот 1208-1243, необходимые для взаимодействия с CD11b/CD18 антиген-презентирующими клетками.
В приведенном выше определении выражение «полипептид» описывает любую последовательность аминокислот, включая последовательности аминокислот, которые содержат посттрансляционные модификации, в частности, последовательность аминокислот, содержащую по меньшей мере шесть остатков аминокислот, и включая последовательность аминокислот, содержащую, например, от 5 до 500 остатков, или от приблизительно 5 до приблизительно 100, или от приблизительно 5 до приблизительно 200, или от приблизительно 10 до приблизительно 50 остатков, или от приблизительно 30, или приблизительно 50 до приблизительно 200 остатков, от приблизительно 100 до приблизительно 210, или от приблизительно 100 до приблизительно 200 остатков, при условии, что указанная последовательность аминокислот содержит по меньшей мере один эпитоп, т.е. последовательность аминокислот, которая может вызвать иммунный ответ при ее доставке к клетке-мишени, предпочтительно, в организме хозяина, в частности хозяина, представляющего собой млекопитающее. Следовательно, полипептиды согласно этому определению могут представлять собой просто эпитопы и даже - единственный эпитоп, либо могут содержать несколько разных или идентичных эпитопов, либо могут включать также полноразмерные антигены патогенов, т.е. вируса папилломы человека. В рамках настоящего изобретения эпитопы охватывают последовательности аминокислот, которые участвуют в гуморальном иммунном ответе и/или клеточном иммунном ответе, в частности в Т-клеточном иммунном ответе. Соответственно, эпитопы в составе полипептидов рекомбинантных молекул согласно настоящему изобретению включают эпитопы, процессируемые антиген-презентирующими клетками в организме хозяина, в частности эпитопы, распознаваемые в комплексе с молекулами ГКГС I (главным комплексом гистосовместимости первого типа), такие как эпитопы, направленные на CD8+ Т-лимфоциты, или эпитопы, распознаваемые в комплексе с молекулами ГКГС II, такие как эпитопы, направленные на CD4+ Т-лимфоциты.
В конкретном способе реализации несущий эпитопы полипептид содержит несколько эпитопов, полученных из разных антигенов, в частности из антигенов одного типа разных штаммов ВПЧ или из антигенов нескольких типов разных штаммов ВПЧ. Следовательно, полипептид, полученный из антигенов ВПЧ, может быть мультивалентным, в частности, бивалентным или тривалентным, т.е. запускающим иммунный ответ против нескольких антигенов.
Согласно настоящему изобретению антигены ВПЧ, из которых можно создать полипептиды, несущие один или несколько эпитопов, предпочтительно получены из белков, являющихся основными участниками возникновения и/или поддержания злокачественных последствий ВПЧ-инфекции, и включают так называемые опухолевые антигены, т.е. антигены, ассоциированные с развитием опухоли, связанной с ВПЧ-инфекцией, которые могут вызывать иммунный ответ в организме хозяина и реагировать специфическим образом с антителами или Т-лимфоцитами в организме хозяина.
Несущие эпитопы полипептиды согласно настоящему изобретению можно получить из нативных или зрелых антигенов ВПЧ, в том числе путем использования целого антигена или путем выбора фрагментов, в частности антигенных фрагментов, в частности эпитопов указанных антигенов, вместо использования целого белка, или путем модификации указанного антигена или отдельных его антигенных частей или эпитопов, в частности, с целью улучшения их способности стимулировать или вызывать иммунный ответ в организме хозяина совместно с белком CyaA в составе рекомбинантной молекулы. Соответственно, эти полипептиды включают эпитопы, которые фланкированы (окружены) последовательностями антигена, из которого они получены, причем указанные последовательности в природе могут быть фланкирующими или нефланкирующими, а также включают эпитопы или последовательности аминокислот, которые были химически модифицированы с целью улучшения их иммунных свойств, что иллюстрирует разнообразных возможных модификаций таких эпитопов. Эти модификации могут быть полезны для улучшения эффективности получаемых полипептидов в комплексе с белком CyaA.
Некоторые конкретные модификации описаны ниже в качестве примеров, в том числе - модификации, включающие изменение заряда полипептидов, в частности, путем вставки дополнительных положительно заряженных остатков аминокислот.
Соответственно к полипептидам согласно настоящему изобретению относятся также полусинтетические и синтетические полипептиды.
Согласно конкретному способу реализации полипептиды, полученные из антигенов ВПЧ, содержат, каждый в отдельности или совместно, приблизительно от 5 до 500, или приблизительно от 5 до 100, или приблизительно от 5 до 200, например, приблизительно от 10 до 50 остатков аминокислот, или приблизительно от 30 или приблизительно 50 до 200 остатков аминокислот или от приблизительно 100 до приблизительно 210, или от приблизительно 100 до приблизительно 200 остатков аминокислот.
Полипептид(ы) специально выбирают таким образом, чтобы он(и) вызывал(и) антиген-специфический ответ в составе рекомбинантного белка согласно настоящему изобретению.
Рекомбинантный белок согласно настоящему изобретению можно специально сконструировать таким образом, чтобы он содержал полипептид или несколько полипептидов, состоящих из измененного (нарушенного) нативного антигена ВПЧ, причем указанное нарушение состоит в делеции одного или нескольких остатков аминокислот кислотной области указанного антигена ВПЧ и/или во добавлении (инсерции) по меньшей мере двух полипептидных фрагментов указанного антигена ВПЧ в по меньшей мере два подходящих (пермиссивных) сайта аденилатциклазы.
В частности, изменение (нарушение), подпадающее под это определение, осуществляют путем вставки по меньшей мере двух фрагментов нативного антигена ВПЧ в по меньшей мере два пермиссивных сайта аденилатциклазы. Причем взаимное положение таких фрагментов обращено относительно их естественного положения в нативном антигене, т.е. фрагмент, который в нативном антигене располагается ближе к N-концу при вставке в CyaA или ее фрагмент располагается ближе к С-концу и наоборот.
Согласно наблюдениям изменение взаимного положения N-концевого и С-концевого фрагментов может увеличить эффективность стимулирования сильного и продолжительного защитного иммунитета, в частности, при иммунотерапии рака, что было показано при использовании фрагментов Е7Δ (т.е. фрагментов антигена Е7).
Согласно данному изобретению аденилатциклазу (CyaA) применяют в форме полноразмерного белка или его фрагмента, как описано выше.
Преимуществом является то, что белок CyaA или его фрагмент представляют собой белок (или его фрагмент), который является продуктом экспрессии двух генов cyaA и cyaC в клетке, в частности, в рекомбинантной клетке. В самом деле, было показано, что для того, чтобы CyaA обладал свойствами, позволяющими ему проникать в клетки-мишени (способностью к инвазии), необходимо, чтобы он претерпел посттрансляционные модификации, которые возможны только при экспрессии обоих генов: cyaA и cyaC (WO 93/21324).
В одном из способов реализации настоящего изобретения фрагменты белка CyaA представляют собой фрагменты, содержащие по меньшей мере 30 остатков аминокислот, и которые могут содержать до приблизительно 1300, в частности, до приблизительно 500 остатков аминокислот, предпочтительно приблизительно от 50 до 150 остатков аминокислот, причем в одном из вариантов реализации фрагменты содержат остатки аминокислот с 1166 по 1281 белка CyaA, или остатки аминокислот с 1208 по 1243 белка CyaA, для взаимодействия с клетками-мишенями, несущими CD11b/CD18. Таким образом, конкретный фрагмент включает всю С-концевую нативного белка или ее часть, ответственную за связывание этого белка с мембраной клетки-мишени и/или рецептором CD11b/CD18, а также за последующую доставку эпитопа, содержащегося в полипептиде/ах (или эпитопов, содрежащихся в полипептиде/ах) в цитозоль. (12). Фрагмент белка CyaA согласно настоящему изобретению содержит остатки аминокислот с 372 по 1706 белка CyaA. Другой вариант фрагмента представляет собой фрагмент, соответствующий белку CyaA, из которого удалили остатки аминокислот с 225 по 234, получив, таким образом, фрагмент CyaA, содержащий остатки с 1 по 224 и с 235 по 1706.
В конкретном способе реализации настоящего изобретения белок аденилатциклаза представляет собой бактериальный белок. В предпочтительном способе реализации белок CyaA получают из одного из видов Bordetella.
Согласно настоящему изобретению одним из видов Bordetella, представляющих интерес, является Bordetella pertussis. Другие представляющие интерес штаммы Bordetella: Bordetella parapertussis или Bordetella bronchiseptica. Последовательности белка CyaA В. parapertussis описаны, в частности под номером NC 002928.3 (как последовательность из 1740 аминокислот) и в Parkhill J. et al (Nat. Genet. DOI, 10 (2003), a последовательности В. bronchiseptica - в Betsou F. et al (Gene 1995, August 30; 162(1): 165-6).
Bordetella pertussis является возбудителем коклюша. Среди нескольких других секретируемых им токсинов - хорошо известный коклюшный токсин и (токсин) аденилатциклазу (CyaA), который является ключевым фактором вирулентности этой бактерии и представляет собой один из антигенов, защищающих от инфекции, вызываемой В. pertussis.
Белок аденилатциклаза бактерии Bordetella pertussis представляет собой токсин, описанный как бифункциональный белок, состоящий из 1706 остатков, содержащий N-концевой каталитический домен из 400 остатков аминокислот и С-концевую часть из 1306 остатков, которая ответственна за связывание этого токсина с мембраной клетки-мищени и последующую доставку каталитического фрагмента в цитозоль клетки (12).
Белок CyaA синтезируют в форме неактивного протоксина, который превращается в активный токсин в ходе посттрансляционного пальмитоилирования двух внутренних остатков лизина (лизины 860 и 983). Для этой посттрансляционной модификации необходима экспрессия вспомагательного гена, а именно гена cyaC, который расположен вблизи гена cyaA в хромосоме В. pertussis.
Аденилатциклаза Bordetella pertussis описана в виде последовательности аминокислот и в виде последовательности нуклеотидов в Glaser, P. et al, 1988, Molecular Microbiology 2(1), 19-30. Соответственно, когда в описании настоящего изобретения упоминаются последовательности остатков аминокислот или последовательности нуклеотидов белка CyaA бактерии В. pertussis, их позиции даны в соответствии с последовательностями, раскрытыми в указанной публикации Glasser et al. 1988.
В рекомбинантном белке согласно настоящему изобретению полипептиды, несущие один или несколько эпитопов одного или нескольких антигенов ВПЧ встроены в один или несколько подходящих (пермиссивных) сайтов белка CyaA.
В настоящем изобретении "пермиссивный сайт" обозначает сайт или последовательность белка CyaA, в который можно встроить (вставить) полипептид таким образом, что это встраивание не отразится существенно на функциональных свойствах белка CyaA, в частности - на его способности взаимодействовать с клетками, и конкретно - на направленном взаимодействии (нацеливании) аденилатциклазы с антиген-презантирующими клетками, в том числе на специфическом связывании рецептора CD11b-CD18, и, предпочтительно, не затрагивает домены этого белка, задействованные в процессе перемещения эпитопа (эпитопов) в клетку-мишень.
Пермиссивные сайты аденилатциклазы Bordetella pertussis, обеспечивающие перемещение каталитического домена аденилатциклазы и, следовательно, перемещение эпитопов, встроенных в такие пермиссивные сайты включают, без ограничения, остатки 137-138 (Val-Ala), остатки 224-225 (Arg-Ala), остатки 228-229 (Glu-Ala), остатки 235-236 (Arg-Glu) и остатки 317-318 (Ser-Ala) ((44) Sebo et al., 1995). Следующие дополнительные пермиссивные сайты также входят в способы реализации настоящего изобретения: остатки 107-108 (Gly-His), остатки 132-133 (Met-Ala), остатки 232-233 (Gly-Leu), а также 335-336 (Gly-Gln) и 336-337. (43)
Для других видов Bordetella соответствующие пермиссивные сайты можно определить путем сравнения последовательностей и выявления соответствующих остатков.
Согласно другому способу реализации полипептид можно встраивать дополнительно, или в качестве альтернативы, на одном и/или другом конце белка CyaA или его фрагмента.
Конкретные фрагменты белков CyaA для применения в целях настоящего изобретения представляют собой фрагменты длиной до 1300 аминокислот или приблизительно от 30 до 500 остатков аминокислот, предпочтительно, приблизительно от 50 до 150 остатков аминокислот, в частности такие фрагменты, включающие остатки аминокислот с 1166 по 1281 нативного белка CyaA, предпочтительно, остатки с 1208 по 1243 нативного белка CyaA.
Следовательно, согласно настоящему изобретению «встраивание» (вставка) полипептида в белок CyaA с целью получить так называемый рекомбинантный белок, называемый также «гибридным белком», включает генетическое встраивание, в частности, при помощи доступной ДНК-технологии. В качестве альтернативы "встраивание" включает также встраивание негентическими способами, включая химическое встраивание, например, ковалентное присоединение к одному из концов аденилатциклазы или ее фрагмента, или нековалентное присоединение. Негенетическое встраивание может, в частности, предоставлять интерес в случае, когда полипептид, который нужно ввести, является синтетическим или полусинтетическим. Способы присоединения лекарственного средства к полипептиду хорошо известны в данной области и включают, например, присоединение дисульфидной связью при помощи N-пиридилсульфонил-активированного сульфгидрила.
В частности, возможно присоединять молекулы, в том числе молекулы, содержащие полипептиды согласно настоящему изобретению, к аденилатциклазе посредством химической связи или генетической вставки, с целью нацеливания in vivo на клетки-мишени аденилатциклазы, такие как антиген-презентирующие клетки, например клетки, несущие CD11b/CD18, и в частности, в цитозоль указанных клеток. В самом деле, было обнаружено, что при присоединении молекулы, соответствующей данному CD8+ Т-клеточному эпитопу, к каталитическому домену обезвреженной аденилатциклазы либо дисульфидной связью, либо при помощи генетической вставки, эта рекомбинантная молекула способна вызывать in vivo специфический ответ цитотоксических Т-лимфоцитов, демонстрируя таким образом, что указанный эпитоп CD8+ Т-лимфоцита перемещается в цитозоль клеток, экспрессирующих CD11b.
В конкретном способе реализации рекомбинантная аденилатциклаза, применяемая для изготовления вектора на основе белка, представляет собой аденилатциклазу или ее фрагмент, в частности, модифицированные путем встраивания остатков цистеина, содержащих одну или более молекул, включающих, в частности, полипептиды согласно настоящему изобретению, химически связанные посредством дисульфидной связи со встроенными генетическими методами остатками (остатком) цистеина, расположенными в пределах каталитического домена указанной аденилатциклазы.
В самом деле, множество молекул, в ососбенности - содержащих полипептиды согласно настоящему изобретению, можно химически присоединить к аденилциклазе посредством образования дисульфидной связи с различными остатками цистеина, расположенными в различных пермиссивных сайтах в пределах каталитического домена.
С намерением предложить рекомбинантный белок, подходящий для создания препаратов, обладающих способностью вызывать иммунный ответ, в особенности клеточный иммунный ответ, в организме хозяина, и в частности - для создания препаратов, способных вызывать клеточный иммунный ответ, направленный против злокачественных эффектов, наблюдаемых в организме хозяина, инфицированного ВПЧ, авторы настоящего изобретения предложили получать полипептиды, несущие эпитопы, из высоко онкогенных штаммов ВПЧ, в особенности из антигенов штаммов, выбранных среди HPV16, HPV18, HPV31, HPV33, HPV35, HPV45, HPV52 и HPV58.
Среди этих штаммов особый интерес представляют штаммы HPV18 и HPV16. В частности, HPV16 благодаря своей связи с развитием рака шейки матки у млекопитающих, в частности у людей, представляет особый интерес в качестве мишени для лечения животного - хозяина, инфицированного HPV.
Приняв за основу эти штаммы ВПЧ, изобретатели предлагают получать полипептиды, несущие эпитопы из антигенов, выбранные среди белков L1, L2, Е1, Е2, Е4 и Е5.
В качестве альтернативы или дополнительно изобретатели предлагают также получать такие полипептиды, несущие эпитопы из белков Е6 или Е7 ВПЧ.
В конкретном способе реализации данного изобретения для создания полипептидов, несущих эпитопы применяют белки Е6 или Е7 ВПЧ16, либо белки Е6 или Е7 из ВПЧ18.
Конкретный белок ВПЧ, который можно использовать для создания полипептида, полученного из антигенов ВПЧ, - белок Е7 ВПЧ, в частности, ВПЧ16 или ВПЧ18. Согласно одному из способов реализации данного изобретения при получении полипептида используют несколько белков Е7 различных штаммов ВПЧ, в частности HPV16 и HPV18. Например, полипептид представляет собой полноразмерный белок Е7 вируса ВПЧ16 и HPV18, либо один или несколько фрагментов каждого из белков Е7 вирусов ВПЧ16 и ВПЧ18, включая мультимеры, в особенности димеры указанных фрагментов.
Данные белки ВПЧ, а также последовательности аминокислот и нуклеотидов этих белков раскрыты в Seedorf, К. et al (Human papillomavirus type 16 DNA sequence (Последовательность ДНК вируса папилломы человека 16 типа). Virology, 145: 181-185, 1985) для ВПЧ16, Cole S.T., Danos O. (Nucleotide sequence and comparative analysis of the human papillomavirus type 18 genome. Phylogeny of papillomaviruses and repeated structure of the E6 and E7 gene products (Последовательность нуклеотидов и сравнительный анализ генома вируса папилломы человека 18 типа. Филогенетика папилломавирусов и повторяющаяся структура продуктов генов E6 и E7). J. Mol. Biol. 193: 599-606 (1987)) или в Fernando GJ. et al (T-helper epitopes of the E7 transforming protein of cervical cancer associated human papillomavirus type 18 (HPV18) (Эпитопы Т-хелперов трансформирующего белка ассоциированного с раком шейки матки папилломавируса человека 18 типа (ВПЧ18) рака шейки матки) Virus Res. 1995 Апрель. 36(1): 1-13).
Белки E6 и E7 представляют собой онкобелки, экспрессируемые, в частности, вирусами ВПЧ16 или ВПЧ18 на протяжении всего цикла репликации вируса. Было показано, что они необходимы для начала и поддержания злокачественной трансформации клеток хозяина, следующей за инфицированием штаммом ВПЧ. Следовательно, оба эти опухоль-специфических антигена рассматриваются как возможные мишени для адаптивной иммунотерапии, опосредованной цитотоксическими Т-лимфоцитами.
Согласно конкретному способу реализации данного изобретения рекомбинантный белок содержит множество полипептидов, каждый из которых несет один или несколько эпитопов одного или нескольких антигенов ВПЧ.
Например, такие множественные полипептиды можно получить из белков E6 и E7 одного штамма HPV, в частности HPV16 или HPV18. Согласно другому примеру, такие множественные полипептиды могут содержать эпитопы, полученные из белков E6 или E7, из обоих вирусов HPV16 и HPV18.
Множественные полипептиды могут также состоять из разных эпитоп-определяющих фрагментов одного белка, например, белка E7 или E6, которые встроены в разные пермиссивные сайты представляющего интерес белка CyaA.
Другой конкретный рекомбинантный белок, соответствующий приведенным выше определениям, представляет собой рекомбинантный белок CyaA, в котором множественные полипептиды, несущие эпитопы, включают (содержат) фрагмент, содержащий остатки с 1 по 29 или фрагмент, состоящий из остатков с 1 по 29, либо фрагмент, содержащий остатки с 42 по 98, или фрагмент, состоящий из остатков с 42 по 98, белка Е7 вируса ВПЧ16, либо множественные полипептиды, состоящие из, или содержащие оба фрагмента, встроенные в разные пермиссивные сайты белка CyaA.
Другой рекомбинантный белок согласно данному изобретению представляет собой белок, указанные множественные полипептиды в котором включают фрагмент, который имеет последовательность аминокислот RAHYNIVTF (E749-57) и/или GQAEPDRAHYNIVTFCCKCDSTLRLCVQSTHVDIR (Е743-77).
Согласно наблюдениям число остатков аминокислот в полипептидах, встраиваемых в пермиссивные сайты белка CyaA, таково, что оно позволяет встраивать в белок CyaA или его фрагмент полипептиды, состоящие из полноразмерных антигенов, в частности полноразмерных белков Е6 или Е7 вируса папилломы человека.
Согласно конкретному способу реализации данного изобретения полипептид, всоставе рекомбинантной аденилатциклазы, представляет собой белок Е7, конкретно - белок Е7 вируса ВПЧ16, встроенный между кодонами 224 и 235 CyaA или между кодонами 319 и 320 CyaA.
В другом способе реализации рекомбинантный белок согласно настоящему изобретению содержит множественные полипептиды, некоторые из которых представляют собой полипептиды, несущие эпитоп или несколько эпитопов одного или нескольких ВПЧ, а другие полипептиды несут эпитопы других патогенов.
В другом частном способе реализации рекомбинантный белок согласно настоящему изобретению дополнительно содержит один или несколько эпитопов, полученных из разных патогенных агентов. Особый интерес может представлять объединение эпитопов, полученных из Chlamydia или из ретровируса ВИЧ или вируса папилломы человека, вируса гепатита В, вируса гепатита С, аденовируса Эпштейна-Барр, вируса герпеса, вируса Т-клеточной лимфомы человека 1 (HTLV.1) и цитомегаловируса с эпитопами, полученными из вируса папилломы человека.
Согласно другому частному способу реализации данного изобретения нативная последовательность аминокислот полипептидов, несущих эпитопы, была модифицирована, например, таким образом, чтобы уменьшить число отрицательно заряженных остатков аминокислот в последовательности. Такой модификации можно достичь путем удаления некоторых отрицательно заряженных остатков аминокислот или путем добавления нескольких положительно зараженных остатков аминокислот, например, в виде фланкирующих остатков эпитопов. Полипептиды, содержащие вследствие такой модификации меньшее число отрицательно заряженных остатков, могут обладать преимуществом при перемещении каталитического домена белка CyaA в цитозоль клеток-мишеней.
Полипептиды, несущие эпитопы, можно также сконструировать таким образом, чтобы при встраивании в аденилатциклазу они находились в «развернутом» (не сложенном) состоянии, что повышает эффективность внедрения рекомбинантного белка CyaA в клетки-мишени. Такого развертывания полипетидов, сворачиваение которых является следствием их аминокислотного состава, можно достичь, например, путем удаления или замещения остатков цистеина, что позволяет предотвратить образование дисульфидных связей, которые могут быть задействованы в свертывании полипептидов. В некоторых случаях можно предотвратить сворачивание полипептидов, готовя их в присутствии восстанавливающих агентов, что позволяет избежать повторного свертывания in vivo.
В отдельном способе реализации полипептиды, несущие эпитопы, могут представлять собой скрытые (криптические) эпитопы.
В отдельном аспекте данного изобретения, изобретатели фактически установили, что химерные белковые конструкции, полученные из рекомбинантных белков, которые содержат (i) аденилатциклазу (CyaA) или ее фрагмент согласно раскрытым выше определениям и (ii) полипептид, несущий один или несколько антигенных фрагментов одного или нескольких антигенов, обеспечивают иммуногенность скрытых эпитопов указанных антигенов как результат их презентации в составе рекомбинантной конструкции. В частности, указанные химерные конструкции, содержащие CyaA или ее фрагмент, охарактеризованные в настоящем изобретении, и полипептиды, полученные из антигенов, представляющих интерес для специфических криптических эпитопов антигена, которые могут стать иммуногенными, в частности, вызвать Т-клеточный ответ, в особенности, цитотоксических Т-лимфоцитов, в организме хозяина.
Таким образом, данное изобретение относится также к рекомбинантному белку, содержащему один или несколько полипептидов, несущих один или несколько эпитопов одного или нескольких антигенов, причем указанный полипептид (полипептиды) встроены в один и тот же или в разные пермиссивные сайты аденилатциклазы (белка CyaA) или его фрагмента, где указанный фрагмент аденилатциклазы сохраняет свойство указанного белка аденилатциклазы направленно взаимодействовать с антиген-презентирующими клетками, где по меньшей мере один из указанных эпитопов представляет собой субдоминантный криптический Т-клеточный эпитоп и где указанный рекомбинантный белок способен вызвать антиген-специфический ответ против указанного полипептида (полипептидов).
В частности, скрытые эпитопы происходят из антигена ВПЧ, в том числе из антигенов ВПЧ16 или ВПЧ18, в частности, входят в состав антигена Е7.
Определенный таким образом рекомбинантный белок, в частности, может содержать пептид, полученный из белка Е7 вируса ВПЧ18, т.е. пептид, который имеет последовательность аминокислот IDGVNHQHL.
Согласно одному из способов реализации настоящего изобретения криптический эпитоп может быть модифицирован, например, он может содержать замены в первых двух позициях и может иметь, например, аминокислотную последовательность: ASGVNHQHL.
Изобретение, в частности, относится к пептидам IDGVNHQHL.
Изобретение также относится к пептидам, которые содержат замены в этой последовательности, в частности в позициях 1 и/или 2, в частности к пептидам, которые имеют последовательность ASGVNHQHL.
Изобретение также охватывает варианты указанных пептидов, при условии, что они сохраняют иммуногенные свойства, в частности, если они способны вызывать Т-клеточный ответ, в частности ответ цитотоксических Т-лимфоцитов.
Для приготовления рекомбинантного белка согласно настоящему изобретению предпочтительно инактивировать ферментативную активность белка CyaA, т.е. его способность превращать АТФ в цАМФ. Такая инактивации может быть результатом генетической модификации. Например, генетический инактивации можно достичь, при встраивании дипептида в участок последовательности аденилатциклазы, который является частью каталитического сайта (например, между остатками 188 и 189). Некоторые варианты таких инактивированных белков CyaA приведены в последующих примерах.
Рекомбинантный белок согласно настоящему изобретению предпочтительно способен вызывать опосредуемый клетками иммунный ответ (клеточный иммунный ответ). Такой ответ включает активацию цитотоксических Т-лимфоцитов и Т-хелперов (Th-клеток), в частности ответ Th1, включая ответ CD4+ Т лимфоцитов и/или CD8+ Т-лимфоцитов.
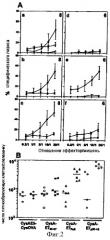
В частности, было показано, что способность рекомбинантного белка вызывать клеточный иммунный ответ достаточна для предотвращения роста опухоли in vivo, и даже для того, чтобы обеспечить регрессию опухоли у животного.
Изобретение также относится к полинуклеотиду, который кодирует описанный выше рекомбинантный белок.
Полинуклеотид согласно настоящему изобретению можно встроить в вектор экспрессии, чтобы получить рекомбинантный вектор, подходящий для экспрессии рекомбинантного белка согласно данному изобретению. Такие векторы экспрессии включают плазмиды, космиды, фагмиды и вирусные векторы.
Рекомбинантный вектор может представлять собой вектор, подходящий для экспрессии в прокариотических клетках, в частности в бактериях, или может представлять собой вектор экспрессии, подходящий для экспрессии в эукариотических клетках, в частности в клетках млекопитающих, и предпочтительно - в клетках человека.
Изобретение относится, в частности, к векторам, состоящим из плазмид, кодирующих рекомбинантный белок согласно настоящему изобретению, таким как:
pTRACE5-HPV16E7full(полноразмерный) (также обозначаемый CyaAE5-HPV16E7FULL), помещенный в Национальную коллекцию культур микроорганизмов CNCM (Париж, Франция)