Способ диагностики аксонально-демиелинизирующих полиневропатий
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к способу диагностики аксонально-демиелинизирующих полиневропатий методом прямого протеомного профилирования сыворотки крови больного на основе выявления в образце сыворотки биомаркеров данных заболеваний. Сущность способа заключается в том, что стадию фракционирования белков сыворотки крови проводят с использованием магнитных микрочастиц. Далее осуществляют масс-спектрометрический анализ образца элюата. Проводят сравнительный анализ полученных масс-спектров на предмет наличия или отсутствия набора пиков, соответствующих биомаркерам аксонально-демиелинизирующих полиневропатий, а именно синдрома Гийена-Барре и хронической воспалительной демиелинизирующей полиневропатии. Отсутствие характерных наборов пиков в масс-спектре свидетельствует об отсутствии у пациента аксонально-демиелинизирующей полиневропатии. Использование способа позволяет повысить точность диагностики аксонально-демиелинизирующих полиневропатий. 2 з.п. ф-лы, 6 табл., 6 ил.
Реферат
Изобретение относится к области медицины, а именно к неврологии, инфекционным болезням, лабораторной диагностике, и касается диагностики демиелинизирующих заболеваний периферической нервной системы, таких как синдром Гийена-Барре и хроническая воспалительная демиелинизирующая полиневропатия.
Аксонально-демиелинизирующие полиневропатии являются одной из наиболее серьезных и актуальных проблем современной медицины, как в России, так и во всем мире. В настоящее время выделяют две группы приобретенных аутоиммунных аксонально-демиелинизирующих полиневропатий, к которым относят синдром Гийена-Барре (СГБ) и хроническую воспалительную демиелинизирующую полиневропатию (ХВДП) [1].
Различные подходы к лечению больных СГБ и ХВДП требуют своевременной дифференциальной диагностики данных заболеваний, что в ряде случаев вызывает большие сложности, особенно на ранних этапах болезни, когда трудно распознать и прогнозировать дальнейший тип аутоиммунного процесса при ДПНП [2, 3]. Важно отметить, что до настоящего времени не существует четких дифференциально-диагностических критериев различных форм СГБ и ХВДП [4]. В результате неправильной диагностики пациентам не проводится адекватная патогенетическая терапия, что ведет к росту инвалидизации и ухудшению качества жизни больных [2, 5].
Известен способ диагностики синдрома Гийена-Барре, заключающийся в оценке совокупности клинико-лабораторных критериев, разработанных специалистами ВОЗ в 1993 году (таблица 1) [6]. Данный способ диагностики используется совместно со способом, основанным на данных электронейромиографии (таблица 2), позволяющим дифференцировать различные формы синдрома Гийена-Барре между собой.
| Таблица 1 | ||
| Диагностические критерии синдрома Гийена-Барре | ||
| Категория признаков | Признаки | |
| Признаки, необходимые для постановки диагноза СГБ | 1. Прогрессирующая мышечная слабость более | |
| чем в одной конечности. | ||
| 2. Сухожильная арефлексия. | ||
| Признаки, поддерживающие диагноз СГБ | А. Клинические признаки | 1. Прогрессирование: симптомы и признаки двигательных нарушений (мышечная слабость) развиваются быстро, но прекращают нарастать к концу 4-й недели от начала болезни. |
| 2. Относительная симметричность поражения. | ||
| 3. Нарушения чувствительности. | ||
| 4. Характерно поражение черепных нервов, парез мимических мышц. | ||
| 5. Восстановление обычно начинается через 2-4 недели после прекращения прогрессирования заболевания, но может задерживаться на несколько месяцев. Для большинства больных характерно полное восстановление функций нервной системы. | ||
| 6. Вегетативные нарушения: тахикардия, аритмии, постуральная артериальная гипотензия, артериальная гипертензия, вазомоторные расстройства. | ||
| 7. Отсутствие лихорадки в начале болезни (лихорадка в начале болезни у небольшого числа больных может быть связана с интеркуррентными инфекциями). Лихорадка не исключает СГБ, но ставит вопрос о возможности другого заболевания, в частности полиомиелита. | ||
| В. Варианты | 1. Выраженные нарушения чувствительности с болевым компонентом.2. Прогрессирование в течение более 4 недель, возможны рецидивы.3. Прекращение прогрессирования без последующего восстановления или сохранение выраженной стойкой резидуальной симптоматики.4. Функции сфинктеров: обычно сфинктеры не поражаются, но в некоторых случаях возможны нарушения мочеиспускания.5. Поражения ЦНС: достоверных доказательств возможности поражения ЦНС нет. У части пациентов могут быть глубокая атаксия мозжечкового характера, патологические стопные знаки разгибательного типа, дизартрия или нечеткий уровень сенсорных нарушений, что не исключает диагноза СГБ, если присутствуют другие типичные клинические симптомы. | |
| Признаки, поддерживающие диагноз СГБ | С. Изменения цереброспинальной жидкости | 1. Белок: через неделю после начала заболевания концентрация белка в ЦСЖ становится повышенной.2. Цитоз: содержание мононуклеарных лейкоцитов в ЦСЖ до 10 в 1 мкл. При содержании в 1 мкл ЦСЖ 20 и более лейкоцитов необходимо тщательное обследование. Если их содержание составляет 50 и более в 1 мкл, диагноз СГБ отвергают. |
| Признаки, вызывающие сомнения в диагнозе | 1. Выраженная сохраняющаяся асимметрия двигательных нарушений.2. Стойкие тазовые нарушения.3. Наличие тазовых нарушений в дебюте болезни.4. Содержание мононуклеарных лейкоцитов в ЦСЖ более 50 в 1 мкл.5. Наличие в ЦСЖ полиморфно-ядерных лейкоцитов.6. Четкий уровень расстройств чувствительности. | |
| Признаки, исключающие диагноз | 1. Злоупотребление в настоящее время летучими органическими растворителями.2. Нарушения обмена порфиринов, подразумевающие диагноз острой перемежающейся порфирии.3. Недавно перенесенная дифтерия.4. Наличие симптомов невропатии вследствие доказанной интоксикации свинцом (парез мышц верхней конечности, иногда асимметричный, с выраженной слабостью разгибателей кисти).5. Наличие исключительно сенсорных нарушений (однако некоторые авторы в качестве казуистически редкой атипичной формы СГБ рассматривают острую сенсорную невропатию, проявляющуюся исключительно нарушениями чувствительности).6. Достоверный диагноз другого заболевания, проявляющегося схожей с СГБ симптоматикой (полиомиелит, ботулизм, токсическая полиневропатия). |
| Таблица 2 | |
| Электронейромиографические (ЭНМГ) признаки различных форм синдрома Гийена-Барре | |
| Диагностическое значение признаков | Признаки |
| Признаки, характерные для острой воспалительной демиелинизирующей полиневропатии | Необходимо наличие 3 из 4 признаков: |
| 1) Снижение скорости проведения по двум и более двигательным нервам до: | |
| а)<80% от нижней границы нормы (при амплитуде М-ответа >80% от нижней границы нормы); | |
| b)<70% от нижней границы нормы (при амплитуде М-ответа <80% от нижней границы нормы). | |
| 2) Парциальный блок проведения или аномальная временная дисперсия - по крайней мере, в одном двигательном нерве. | |
| 3) Удлинение дистальной латенции более чем в двух нервах до: | |
| а)>125% от верхней границы нормы (при амплитуде М-ответа >80% от нижней границы нормы); | |
| b)>150% от верхней границы нормы (при амплитуде М-ответа <80% от нижней границы нормы); | |
| 4) Отсутствие F-волны или удлинение минимальнойлатенции F-волны в двух и более нервах до: | |
| а)>120% от верхней границы нормы (при амплитуде М-ответа >80% от нижней границы нормы); | |
| b)>150% от верхней границы нормы (при амплитуде М-ответа <80% от нижней границы нормы). | |
| Признаки, характерные для острой моторной аксональной невропатии | 1. Нет вышеперечисленных признаков демиелинизации ни в одном нерве (исключая один любой признак в 1 нерве, если амплитуда М-ответа <10% от нижней границы нормы).2. Амплитуда М-ответа <80% от нижней границы нормы (не менее чем в 2 нервах).3. Уменьшение сенсорного ответа или невозбудимые двигательные и чувствительные нервы. |
| Признаки, характерные для острой моторно-сенсорной аксональной невропатии | 1. Нет вышеперечисленных признаков демиелинизации ни в одном нерве (исключая один любой признак в 1 нерве, если амплитуда М-ответа <10% от нижней границы нормы).2. Амплитуда М-ответа <80% от нижней границы нормы (не менее чем в 2 нервах).3. Невозбудимые двигательные нервы. |
Недостатком представленных выше способов является низкая точность при изолированном поражении тонких нервных волокон, которое встречается у больных СГБ довольно часто.
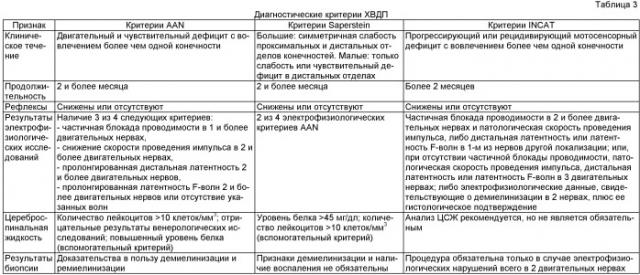
Известные же способы диагностики ХВДП, основывающиеся на критериях, разработанных Американской академией неврологии (AAN), Группой по изучению причин и лечению воспалительных нейропатий (INCAT), и критериях Saperstein, представленных в таблице 3, могут быть использованы только при диагностике ХВДП с типичным течением. Различить же ХВДП с острым началом и синдром Гийена-Барре в первые 4 недели болезни невозможно, что влечет за собой выбор неправильной тактики ведения пациента и, как следствие, развитие неблагоприятного исхода.
Таким образом, несмотря на существующие способы диагностики, даже при несомненных клинических признаках полиневропатии установить правильный нозологический диагноз бывает крайне сложно, а при атипичном течении болезни - невозможно и при самом тщательном исследовании, и удается лишь при дальнейшем прогрессировании заболевания [2].
Учитывая аутоиммунный характер развития аксонально-демиелинизирующих полиневропатий, важное место в их диагностике занимают иммунологические методы исследования. Однако наиболее перспективным представляется использование протеомных технологий, поскольку последние не требуют ориентации на специфичность взаимодействия антиген-антитело, которая при аутоиммунных процессах дает сбои из-за наличия множественных «перекрестных» неспецифичных реакций [7]. Системный подход, основанный на обнаружении в организме биомаркеров тех или иных патологических состояний методами протеомики, как правило, требует серьезной обработки результатов с использованием новейших достижений биоинформационных технологий, что еще больше повышает диагностическую значимость протеомных исследований [8].
Медицинские аспекты протеомики уже сейчас вышли на первое место. Такие диагностические инструменты протеомных исследований, как SELDI-TOF MS и MALDI-TOF MS технологии, успешно применяются для выявления биомаркеров различных заболеваний.
В литературе описаны примеры успешного применения SELDI-TOF MS для выявления биомаркеров, в первую очередь различных онкологических заболеваний (рака желудка, рака толстого кишечника и прямой кишки, гепатоклеточной карциномы, рака яичника, рака эндометрия, рака легкого, нефробластомы, опухолей щитовидной железы, рака простаты).
Обладая рядом преимуществ по отношению к SELDI, MALDI-TOF MS технология используется для определения биомаркеров колоректального рака, являясь очень чувствительным (95,2%) и специфичным (90%) методом диагностики данного заболевания [9]. MALDI анализ также используется для скрининговых исследований с целью формирования группы риска по развитию рака желудка [10], может быть применен для оценки доброкачественности или злокачественности опухолей молочной железы, зарегистрированных в процессе маммографии [11]. Этим методом определяются биомаркеры носоглоточной карциномы [12]. Приводятся доказательства высокой эффективности МАЛДИ масс-спектрометрии при определении биомаркеров I стадии рака яичников [13]. Данный метод используется для регистрации биомаркеров инфаркта миокарда (кардиотропины) [14], мозговых нарушений [15].
Успехи протемики в диагностике заболеваний нервной системы значительно скромнее, поскольку они потребовали предварительной расшифровки протеома не только плазмы крови, но и цереброспинальной жидкости на модели различных заболеваний [16]. В результате было установлено нарушение процессов гликозилирования белков при таких нейродегенеративных заболеваниях, как болезнь Крейтцфельда-Якоба, болезнь Альцгеймера, болезнь Паркинсона [17].
Известен способ диагностики сифилиса с использованием метода прямого протеомного профилирования сыворотки крови [18].
Применялись методы протеомного анализа и при синдроме Гийена-Барре [19, 20]. Проведены экспериментальные исследования спинномозговой жидкости (СМЖ) у больных синдромом Гийена-Барре с использованием двухмерного гель-электрофореза и времяпролетной MALDI-TOF масс-спектрометрии по общепринятым стандартным протоколам, с последующим выявлением аномальных белков спинномозговой жидкости и измерением концентрации данных белков методом ИФА по стандартной методике. Так, Chiang H.L. с соавторами в результате применения вышеописанного способа диагностики выявили увеличение уровня транстиретина в спинномозговой жидкости при СГБ и сделали вывод о том, что такая реакция может быть защитной на повреждение нервов [21]. A Yang Y.R. с соавторами выявили снижение концентрации цистатина С в СМЖ у больных СГБ и сделали вывод о том, что данный белок может быть вовлечен в патофизиологический процесс при СГБ и требует дальнейшего изучения его роли в патогенезе заболевания [22]. Являясь экспериментальными, результаты данных работ требуют дальнейшего подтверждения и не могут служить прототипом для наших исследований. При этом исследование СМЖ, используемой для диагностики, предполагает проведение инвазивной врачебной, нередко сопряженной с техническими трудностями, процедуры - люмбальной пункции. В то же время забор крови, используемой для наших исследований, может быть осуществлен средним медицинским персоналом и является рутинной процедурой.
Применяемый для диагностики других заболеваний метод МАЛДИ масс-спектрометрии предусматривает выполнение стандартных протоколов фракционирования белково-пептидных смесей, что обуславливает высокие требования к их воспроизводимости при протеомном анализе сыворотки крови [23], крайне редко достижимые в реальной клинической практике. Кроме того, классификационные модели, построенные на основе такого фракционирования, не всегда обладают высокими чувствительностью и специфичностью, что в таком случае не позволяет рекомендовать этот метод как способ диагностики.
Использование же в диагностике аксонально-демиелинизирующих полиневропатий (СГБ и ХВДП) протеомных технологий с применением предлагаемого нами усовершенствованного протокола фракционирования сыворотки крови больных с последующей МАЛДИ масс-спектрометрией и выявлением биомаркеров данных заболеваний позволит с высокими чувствительностью и специфичностью их верифицировать.
Задачей изобретения является повышение точности диагностики аксонально-демиелинизирующих полиневропатий, а именно синдрома Гийена-Барре и хронической воспалительной демиелинизирующей полиневропатии.
Технический результат заключается в выявлении в сыворотке крови пациента наборов масс-спектрометрических пиков, являющихся биомаркерами острой и хронической форм аксонально-демиелинизирующей полиневропатии.
Данный технический результат достигается за счет того, что у больного с подозрением на аксонально-демиелинизирующую полиневропатию проводят фракционирование белково-пептидных смесей образцов сыворотки крови с использованием магнитных микрочастиц, при этом образец элюата наносят на стальную полированную 384-точечную мишень в двух повторах и после высушивания на воздухе на образец наносят раствор матрицы, представленной смесью 2,4 мг 2,5-дигидроксибензойной кислоты и 3 мг α-цианогидроксикоричной кислоты на каждый миллилитр раствора метанол:ацетонитрил:вода, смешанных в соотношении 5:4:1; масс-спектрометрический анализ полученного образца элюата на предмет наличия или отсутствия набора пиков, соответствующих биомаркерам аксонально-демиелинизирующих полиневропатий, причем наличие в масс-спектре сыворотки крови набора пиков, характеризующегося значениями отношения молекулярной массы к заряду (m/z): 1945,26; 2787,18; 4477,75; 3985,3; 2843,56; 2239,51; 11784,46, свидетельствует о наличии у пациента синдрома Гийена-Барре, наличие набора пиков, характеризующегося значениями отношения молекулярной массы к заряду (m/z): 1945,29; 1886,18; 1490,03; 3985,32; 1552,5; 3401,42; 11783,91, свидетельствует о наличии у пациента хронической воспалительной демиелинизирующей полиневропатии, а отсутствие указанных наборов пиков в масс-спектре свидетельствует об отсутствии у пациента аксонально-демиелинизирующей полиневропатии. Применение магнитных частиц со слабой катионообменной поверхностью (MB-WBX) и проведение масс-спектрометрического анализа образца элюата по методу MALDI-TOF являются предпочтительными. Следует, однако, понимать, что для осуществления настоящего изобретения могут быть применены и другие типы микрочастиц, а также альтернативные методы масс-спектрометрии.
Для проведения исследований по поиску биомаркеров, специфичных для СГБ или ХВДП, обследовано 70 больных аксонально-демиелинизирующими полиневропатиями. Основную группу составили 40 больных синдромом Гийена-Барре (из них 20 мужчин и 20 женщин). В группу сопоставления вошли 30 больных хронической воспалительной демиелинизирующей полиневропатией (из них 14 мужчин и 16 женщин). Группа контроля - 25 практически здоровых доноров (из них 12 мужчин и 13 женщин).
Критериями включения больных в основные группы наблюдения были: подозрение на аксонально-демиелинизирующую полиневропатию (СГБ, ХВДП); возраст от 16 до 70 лет; информированное согласие пациента на обследование. Критериями исключения пациентов из исследования являлись: полиомиелит, ботулизм, дифтерия, ВИЧ-инфекция; миастения; токсическая полиневропатия; сахарный диабет; нарушение обмена порфиринов; хронический алкоголизм и/или наркомания; органические поражения ЦНС, исключенные по результатам клинико-лабораторных и инструментальных данных, а также отказ пациента от исследования.
У лиц, вошедших в контрольную группу, не выявлено сопутствующих хронических заболеваний нервной системы и на момент обследования не определялись какие-либо субъективные и объективные признаки острых заболеваний; в анамнезе не отмечено аллергических реакций и аутоиммунных состояний, а также алкоголизма и наркомании.
Методология исследования: 1) пробоподготовка (фракционирование белков сыворотки крови); 2) масс-спектрометрия; 3) анализ полученных данных.
1. Фракционирование белково-пептидных смесей образцов сыворотки крови проводили на специализированном роботе ClinProt (Bruker Daltonics GmbH, Германия) с использованием набора для профилирования, содержащего магнитные микрочастицы со слабой катионообменной поверхностью (MB-WCX), по протоколу, рекомендованному производителем, с небольшими модификациями, заключающимися в том, что элюаты наносили на стальную полированную 384-точечную масс-спектрометрическую мишень в двух повторах, после высушивания на воздухе на образец наносили раствор матрицы, представленной смесью 2,4 мг 2,5-дигидроксибензойной кислоты и 3 мг α-цианогидроксикоричной кислоты на каждый миллилитр раствора метанол:ацетонитрил:вода, смешанных в соотношении 5:4:1.
Вывод о предпочтительном использовании магнитных микрочастиц со слабой катионообменной поверхностью (MB-WCX) был сделан по результатам проведенных нами экспериментальных исследований контрольных образцов сыворотки крови (n=36). Для фракционирования белково-пептидных смесей образцов сыворотки крови использовали 3 вида магнитных микрочастиц: с обращенно-фазовой (MB-HIC 8, MB-HIC 18), слабой катионообменной (MB-WCX) и металло-аффинной (MB-IMAC Сu) функционализированными поверхностями. В результате сравнения масс-спектрометрических профилей образцов сыворотки крови, предварительно фракционированных на магнитных микрочастицах различного типа, мы остановили свой выбор на микрочастицах со слабой катионообменной поверхностью MB-WCX, как обеспечивающих регистрацию наибольшего количества, по сравнению с другими типами частиц, масс-спектрометрических пиков (фиг.1).
Затем была осуществлена отработка условий масс-спектрометрического анализа выделяемых с помощью магнитных микрочастиц белковых фракций сыворотки крови человека. Для чего из совокупности ароматических соединений, рекомендуемых для масс-спектрометрии белковых молекул (таблица 4), мы апробировали две матрицы: производные бензойной и коричной кислоты - 2,5-дигидроксибензойная и α-циано-4-гидроксикоричная кислота.
| Таблица 4 | |||
| Органические соединения, используемые в качестве основного вещества матрицы при МАЛДИ масс-спектрометрии белковых молекул и пептидов | |||
| Наименование соединения | Химическая формула | Длина волны поглощения (нм) | Область применения |
| α-циано-4-гидроксикоричная кислота | 337, 355 | Белки и пептиды с массой менее 10 кДа. Реже - липиды и олигонуклеотиды | |
| 3,5-диметокси-4-гидроксикоричная (синапиновая) кислота | 337, 355, 266 | Белковые молекулы массой более 10 кДа и гликопротеины | |
| 3-метокси-4-гидроксикоричная (феруловая) кислота | 337, 355, 266 | Высокомолекулярные белковые молекулы | |
| 3,4-дигидроксикоричная (кофейная) кислота | 337, 355, 266 | Высокомолекулярные белковые молекулы | |
| 2,5-дигидроксибензойная кислота | 337, 355, 266 | Широкий спектр белков и пептидов, в том числе фосфопептиды и гликопротеины, а также липиды и олигосахариды |
В силу лучшей ионизации небольших белковых молекул (до 10 кДа) на альфа-4-гидроксикоричной кислоте применение этой матрицы в отдельности не позволило получить равномерно богатый масс-спектр, наблюдался выраженный сдвиг в сторону малых масс. С другой стороны, при применении 2,5-дигидроксибензойной кислоты наблюдался равномерный масс-спектр белков с хорошим разрешением пиков. Однако для 2,5-дигидроксибензойной кислоты была характерна неравномерность кристаллизации на металлической пластине, что исключало автоматическое накопление масс-спектров, необходимое для стандартизации протокола.
Выход был найден в совместном использовании 2,5-дигидроксибензойной и α-циано-4-гидроксикоричной кислот. Такой композитный состав матрицы для ионизации обеспечивал равномерность накапливаемых масс-спектров, с одной стороны, и позволял сформировать с аналитом гомогенные кристаллы, пригодные для измерения в автоматическом режиме.
Модификация стандартного протокола фракционирования позволила значительно увеличить количество детектируемых в элюатах масс-спектрометрических пиков, а также качество и воспроизводимость получаемых масс-спектрометрических профилей, что иллюстрируется фигурами 2 и 3. На фигуре 2 приведены средние масс-спектрометрические профили образцов сыворотки крови после их фракционирования с использованием магнитных микрочастицах MB-WCX. На фигуре видно, что количество детектируемых компонентов в пептидно-белковых смесях, полученных после фракционирования сывороток крови по модифицированному протоколу разделения (А), значительно превышает количество компонентов в элюатах, полученных при фракционировании плазмы и сыворотки крови с использованием стандартного протокола (В), особенно ярко эти различия наблюдаются в диапазоне масс до 4 кДа (фиг.3).
2. Масс-спектрометрический анализ проводили с использованием времяпролетного MALDI-TOF масс-спектрометра Ultraflex (Bruker Daltonics GmbH, Германия). Десорбцию образцов осуществляли иррадиацией азотным лазером (длина волны 337 нм), работающим при частоте 25 Гц. Для удаления пиков матрицы использовали максимальный уровень подавления сигнала вплоть до 900 Да. Автоматическую регистрацию масс-спектров проводили в линейном режиме положительно заряженных ионов в диапазоне масс 1-15 кДа. Для калибровки использовали калибровочную смесь, содержащую пептиды и белки в диапазоне масс 1-17 кДа. Для увеличения чувствительности масс-спектрометрической детекции белков и пептидов избыток матрицы удаляли 10 импульсами лазера при мощности 45% с последующей аккумуляцией данных при мощности лазера 27%. Для каждого спектра суммировали результаты 720 лазерных импульсов (по 60 импульсов с 12 различных точек пятна). Суммировали спектры с отношением сигнал/шум >5 и разрешением >300. Для управления масс-спектрометром, включая установку режимов работы и регистрации масс-спектров, использовали программный пакет FlexControl 2.4 (Bruker Daltonics, Германия). На фигурах 4-6 в виде псевдогелей приведены масс-спектрометрические профили сравниваемых групп образцов сыворотки крови пациентов с СГБ и практически здоровых доноров, пациентов с ХВДП и практически здоровых доноров, а также пациентов с ХВДП и с СГБ соответственно. В результате интегрирования масс-спектрометрических профилей вышеперечисленных пар сравнения с использованием программы ClinProTools 2.1 было размечено соответственно 219, 222 и 236 пиков.
3. Анализ масс-спектрометрических данных
Анализ полученных данных проводили с использованием программного пакета для обработки данных масс-спектрометрических анализов ClinProTools версия 2.1 (Bruker Daltonics, Германия), отвечающего всем главным требованиям поиска биомаркеров в сложных биологических смесях и их валидации. В биоинформатической системе ClinProTools (версия 2.1) реализованы два метода построения классификационных моделей (классификаторов) для анализа распределения биомаркеров между группами: генетический алгоритм и управляемая нейронная сеть, являющиеся общепризнанными и эффективными методами математического анализа масс-спектрометрических данных для решения задач, связанных с построением классификаторов. Определение биомаркеров, выявляемых в моделях с помощью данных алгоритмов как масс-спектрометрические сигналы, осуществляется путем подбора оптимальных параметров алгоритмов: количество заданных масс-спектрометрических сигналов (пиков) и количество «соседей» (для обоих алгоритмов), количество итераций (для генетического алгоритма) до достижения наивысших показателей кросс-валидации и способности к распознаванию.
В результате масс-спектрометрического анализа белково-пептидных смесей сыворотки крови больных СГБ с использованием генетического алгоритма определены 7 значимых масс-спектрометрических пиков со следующими средними значениями отношения молекулярной массы к заряду (m/z): 1945,26; 2787,18; 4477,75; 3985,3; 2843,56; 2239,51; 11784,46, которые и вошли в классификационную модель и определены как биомаркеры СГБ (таблица 5).
| Таблица 5 | ||||
| Значения m/z пиков, вошедших в классификационную модель сывороток крови «СГБ-контроль», построенную с использованием генетического алгоритма | ||||
| Index | Mass | Start Mass | End Mass | Weight |
| 34 | 1945 | 1937 | 1950 | 2,006001001 |
| 60 | 2787 | 2780 | 2796 | 1,787940192 |
| 102 | 4478 | 4463 | 4482 | 1,349909864 |
| 87 | 3985 | 3976 | 3990 | 0,928244527 |
| 62 | 2844 | 2834 | 2851 | 0,738832543 |
| 45 | 2240 | 2234 | 2245 | 0,678443885 |
| 219 | 11784 | 11774 | 11797 | 0,266230980 |
| Index - порядковый номер пикаMass - значение m/z пикаStart Mass, End Mass - значения m/z, соответствующие началу и концу масс-спектрометрического пика соответственноWeight - статистический вес пика, соответствующий числовому значению коэффициента в алгебраическом выражении классификационной модели |
В результате масс-спектрометрического анализа белково-пептидных смесей сыворотки крови больных ХВДП с использованием генетического алгоритма определены 7 значимых масс-спектрометрических пиков со следующими средними значениями отношения молекулярной массы к заряду (m/z): 1945,29; 1886,18; 1490,03; 3985,32; 1552,5; 3401,42; 11783,91, которые и вошли в классификационную модель и определены как биомаркеры ХВДП (таблица 6).
| Таблица 6 | ||||
| Значения m/z пиков, вошедших в классификационную модель сывороток крови «ХВДП-контроль», построенную с использованием генетического алгоритма | ||||
| Index | Mass | Start Mass | End Mass | Weight |
| 34 | 1945 | 1940 | 1950 | 2,051317454 |
| 32 | 1886 | 1883 | 1891 | 1,923997493 |
| 19 | 1490 | 1486 | 1497 | 1,749895004 |
| 86 | 3985 | 3975 | 3989 | 1,454915710 |
| 23 | 1553 | 1549 | 1558 | 1,090828045 |
| 77 | 3401 | 3399 | 3412 | 1,082192700 |
| 222 | 11784 | 11768 | 11797 | 0,265484282 |
| Index - порядковый номер пика | ||||
| Mass - значение m/z пика | ||||
| Start Mass, End Mass - значения m/z, соответствующие началу и концу масс-спектрометрического пика соответственно | ||||
| Weight - статистический вес пика, соответствующий числовому значению коэффициента в алгебраическом выражении классификационной модели |
Сравнительный анализ полученных масс-спектрометрических данных проводили с помощью компьютерной программы ClinProTools 2.1 (Bruker Daltonics, Германия) с использованием математического генетического алгоритма, который позволил выявить характерные наборы пиков, согласованное изменение площадей которых с высокой специфичностью и чувствительностью дифференцировало масс-спектрометрические профили сыворотки крови пациентов с ДПНП и практически здоровых доноров (для СГБ значения этих характеристик достигали 100% и 100%, а для ХВДП 94,1% и 100% соответственно).
Анализ масс-спектрометрических профилей образцов сыворотки крови, полученных от пациентов с СГБ и ХВДП, позволил построить классификационную модель, различающую эти патологии друг от друга, со специфичностью 88,9% и чувствительностью 80%.
Таким образом, наличие в масс-спектре сыворотки крови больного набора пиков со следующими значениями отношения молекулярной массы к заряду: 1945,26; 2787,18; 4477,75; 3985,3; 2843,56; 2239,51; 11784,46, свидетельствует о наличии у пациента синдрома Гийена-Барре, наличие пиков со следующими значениями отношения молекулярной массы к заряду: 1945,29; 1886,18; 1490,03; 3985,32; 1552,5; 3401,42; 11783,91, свидетельствует о наличии у пациента хронической воспалительной полиневропатии, а отсутствие указанных наборов пиков в масс-спектре сыворотки крови свидетельствует об отсутствии у пациента аксонально-демиелинизирующей полиневропатии.
Изобретение иллюстрируется следующими графическими материалами.
Фиг.1. Усредненные масс-спектры образцов сыворотки крови, полученных от практически здоровых доноров после их фракционирования на магнитных микрочастицах МВ-HIС8 (A), MB-WCX (Б) и MB-IMAC Cu (В) с использованием модифицированного протокола.
Фиг.2. Средние масс-спектрометрические профили образцов сыворотки крови, фракционированных с использованием магнитных микрочастиц со слабой катионообменной поверхностью по модифицированному (А) и стандартному (B) протоколам.
Фиг.3. Средние масс-спектрометрические профили образцов сыворотки крови, фракционированных на магнитных частицах MB-WCX с использованием модифицированного (А) и стандартного (В) протоколов в диапазоне m/z от 1500 до 3500 Да.
Фиг.4. Усредненные масс-спектрометрические профили образцов сыворотки крови практически здоровых доноров (а) и пациентов с СГБ (б). Фракционирование образцов проводилось с использованием магнитных микрочастиц MB-WCX. По оси ординат отложена нормированная интенсивность масс-спектрометрических пиков, по оси абсцисс - отношение массы к заряду. Интенсивность окрашивания полос соответствует интенсивности пика в спектре. Данные приведены в виде псевдогеля. Во врезках вверху показаны усредненные масс-спектры наиболее значимых пиков, вошедших в классификационную модель, построенную с использованием генетического алгоритма.
Фиг.5. Усредненные масс-спектрометрические профили образцов сыворотки крови практически здоровых доноров (а) и пациентов с ХВДП (б). Фракционирование образцов проводилось с использованием магнитных микрочастиц MB-WCX. По оси ординат отложена нормированная интенсивность масс-спектрометрических пиков, по оси абсцисс - отношение массы к заряду. Интенсивность окрашивания полос соответствует интенсивности пика в спектре. Данные приведены в виде псевдогеля. Во врезках вверху показаны усредненные масс-спектры наиболее значимых пиков, вошедших в классификационную модель, построенную с использованием генетического алгоритма.
Фиг.6. Усредненные масс-спектрометрические профили образцов сывороток крови пациентов с ХВДП (а) и СГБ (б). Фракционирование образцов проводилось с использованием магнитных микрочастиц MB-WCX. По оси ординат отложена нормированная интенсивность масс-спектрометрических пиков, по оси абсцисс - отношение массы к заряду. Интенсивность окрашивания полос соответствует интенсивности пика в спектре. Данные приведены в виде псевдогеля. Во врезках вверху показаны усредненные масс-спектры наиболее значимых пиков, вошедших в классификационную модель, построенную с использованием генетического алгоритма.
Способ осуществляется следующим образом:
у больного с подозрением на аксонально-демиелинизирующую полиневропатию проводят прямое протеомное профилирование образца сыворотки крови с целью выявления биомаркеров демиелинизирующей полиневропатии (СГБ или ХВДП), предусматривающее: 1) фракционирование белково-пептидных смесей образцов сыворотки крови с использованием магнитных микрочастиц со слабой катионообменной поверхностью по стандартной методике на специализированном роботе (например, ClinProt, Bruker Daltonics GmbH, Германия), при этом элюаты наносят на стальную полированную 384-точечную масс-спектрометрическую мишень в двух повторах, после высушивания на воздухе на образец наносят раствор матрицы, представленной смесью 2,4 мг 2,5-дигидроксибензойной кислоты и 3 мг α-цианогидроксикоричной кислоты на каждый миллилитр раствора метанол:ацетонитрил:вода, смешанных в соотношении 5:4:1; 2) масс-спектрометрический анализ полученного образца элюата с использованием времяпролетного MALDI-TOF масс-спектрометра (например, Ultraflex, Bruker Daltonics GmbH, Германия); 3) сравнительный анализ полученных масс-спектров проводят с помощью программного пакета для обработки данных масс-спектрометрических анализов (например, ClinProTools 2.1, Bruker Daltonics, Германия) и при наличии в масс-спектре сыворотки крови набора дискриминантных пиков со следующими значениями отношения молекулярной массы к заряду (m/z): 1945,26; 2787,18; 4477,75; 3985,3; 2843,56; 2239,51; 11784,46, диагностируют у пациента синдром Гийена-Барре, при наличии дискриминантных пиков со следующими значениями отношения молекулярной массы к заряду (m/z): 1945,29; 1886,18; 1490,03; 3985,32; 1552,5; 3401,42; 11783,91, диагностируют у пациента хроническую воспалительную полиневропатию, а при отсутствии указанных наборов пиков в масс-спектре сыворотки крови наличие у пациента аксонально-демиелинизирующей полиневропатии отвергают.
Предложенный способ с высокими специфичностью и чувствительностью позволяет дифференцировать синдром Гийена-Барре и хроническую воспалительную демиелинизирующую полиневропатию и может быть внедрен в практику неврологической, инфекционной и многопрофильной клиник при сотрудничестве с научно-исследовательскими институтами, имеющими лабораторию по протеомным исследованиям.
Клинический пример 1
Пациентка Н., 46 лет, поступила в НЦН РАМН на 9 день болезни с жалобами на слабость в руках и ногах, боль в икроножных мышцах, легкое онемение кистей и стоп. При осмотре наблюдался тетрапарез со снижением силы в проксимальных отделах рук до 3 баллов, в дистальных - до 2 баллов, в проксимальных отделах ног - до 3 баллов, в стопах активные движения отсутствовали. Нарушение глубокой чувствительности проявлялось снижением вибрационной чувствительности в пальцах кистей и стоп. Также отмечалось отсутствие глубоких сухожильных рефлексов, повышенное потоотделение и симптомы поражения V, VII, IX, XI и XII черепных нервов в виде снижения силы жевательных и мимических мышц лица, мышц шеи и языка, нарушения речи и глотания.
Из анамнеза: за две недели до развития неврологической симптоматики перенесла острое респираторное заболевание с повышением температуры тела до 37,5°C и болью в горле при глотании. На фоне симптоматической терапии самочувствие нормализовалось в течение 3 дней. Через 10 дней после перенесенного ОРЗ появилось онемение в стопах, позже в кистях. На 3-й день появления неврологической симптоматики развилась слабость в верхних и нижних конечностях, которая медленно нарастала. На 8-й день не смогла ходить.
Хронические заболевания отрицает (в том числе сахарный диабет, алкоголизм и наркоманию).
При обследовании изменений в клиническом и биохимическом анализах крови и клиническом анализе мочи не выявлено. Порфобилиноген в моче не обнаружен.
Антитела к ВИЧ, вирусу гепатита С и HBsAg в сыворотке крови методом ИФА не выявлены. При исследовании сыворотки крови обнаружены антитела к асиало-GM1 и GM1 методом ИФА.
При ЭНМГ на 9-й день болезни выявлен первично демиелинизирующий процесс в периферических нервах верхних и нижних конечностей.
На МРТ признаков органического поражения ЦНС не