Рекомбинантная плазмидная днк pacyc-lans(km), штамм escherichia coli bl21(de3), трансформированный рекомбинантной днк pacyc-lans(km), и способ получения рекомбинантной l-аспарагиназы erwinia carotovora
Иллюстрации
Показать всеГруппа изобретений относится к биотехнологии и генной инженерии. Сконструирована рекомбинантная плазмидная ДНК pACYC_LANS(KM) для экспрессии в клетках Escherichia coli полипептида L-аспарагиназы Erwinia carotovora (rec-ASP-ECAR), предложен штамм-продуцент rec-ASP-ECAR, который получают путем трансформации компетентных клеток E.coli BL21(DE3) сконструированной рекомбинантной плазмидной ДНК pACYC_LANS(KM), разработан способ выращивания штамма с выделением и очисткой из полученной биомассы рекомбинантной L-аспарагиназы Erwinia carotovora. Изобретение позволяет обеспечить повышенный уровень биосинтеза полипептида rec-ASP-ECAR и достигнуть высокого выхода и чистоты целевого продукта при простом способе получения рекомбинантной аспарагиназы. 3 н. и 1 з.п. ф-лы, 4 ил., 2 табл.
Реферат
Группа изобретений относится к биотехнологии, в частности к генетической инженерии, и может быть использована для получения L-аспарагиназы Erwinia carotovora, обладающей цитотоксической активностью в отношении линий лейкозных клеток и солидных опухолей человека.
Бактериальные аспарагиназы 2-го класса (К.Ф. 3.5.1.1) являются периплазматическими ферментами, катализирующими гидролиз L-аспарагипа с образованием L-аспарагиновой кислоты и аммония. Две аспарагиназы, одна из Escherichia coli (EcA), другая из Erwinia chrysanthemi (ErA), уже более 30 лет широко используются в клинической практике в качестве противолейкозных препаратов для лечения, прежде всего, острой лимфобластной лейкемии, а также не-Ходжкинской лимфомы и лимфомы Беркита. Данные фармакогеномных и фармакопротсомных исследований указывают на возможность использования этого фермента и для лечения солидных опухолей. Считается, что оптимальной для клинического применения аспарагиназой должен являться фермент с высокой аспарагиназной и низкой глутаминазной активностями. Согласно этим критериям поиск наиболее эффективной для химиотерапии опухолей аспарагиназы продолжается в течение более 30 лет, однако до сих пор не достигнуто сколько-нибудь заметного позитивного результата.
L-Аспарагиназа из диких и рекомбинантных штаммов Erwinia carotovora представляет собой белок, построенный из 4-х нековалентно связанных идентичных субъединиц с мол. массой около 35 кДа, мономер фермента состоит из приблизительно 330 аминокислот. Значение удельной активности аспарагиназы Erwinia carotovora по данным различных авторов варьирует в диапазоне от 310 до 550 МЕ/мг белка. Мономер аспарагиназы не обладает каталитической активностью, поскольку активный сайт фермента формируется при образовании димера и расположен на его интерфейсе. Дальнейшая олигомеризация фермента приводит к образованию тетрамера, содержащего 4 идентичных некооперативных активных центра. В большинстве случаев ассиметричная кристаллическая ячейка аспарагиназы представляет собой гомотетрамер с С2-симметрией. Несмотря на то, что димер обладает всеми необходимыми структурными элементами для катализа, принято считать, что ферментативной активностью обладает только тетрамер аспарагиназы.
Известны, например, рекомбинатные полипептиды, имеющие аспарагиназную активность и повышенную термостабильность (US 7666652, 23.02.2010).
Известен способ промышленного получения рекомбинатного белка L-аспарагиназы ЕсА2 медицинского назначения, а также плазмида и рекомбинантный штамм Bacillus sereus для его получения (RU 2313575, 27.12.2007).
Известен ген L-аспарагиназы Erwinia carotovora и штамм Escherichia coli ВКПМ № В-8174 - продуцент L-аспарагипазы (RU 2221868, 20.01.2004).
Известна рекомбинантная плазмида pACYC_LANS, содержащая природную последовательность гена L-аспарагиназы Erwinia carotovora, которая находится под контролем промотора и терминатора РНК-полимеразы фага Т7 и кодирует полноразмерный предшественник фермента с сигнальным пептидом для экспорта белка в периплазму с последующим процессингом. Описан также способ получения и очистки рекомбинантной L-аспарагиназы (RU 2224797, 27.02.2004).
ECAR_LANS совмещает основные преимущества аспарагиназ ErA и ЕсА2, применяемых при лечении лейкозов. Этот фермент имеет такую же высокую специфичность к аспарагину, как и ЕсА2, значительно более низкое сродство к глутамину, а его удельная активность сравнима с активностью ErA. ECAR_LANS стабильна в широком диапазоне pH, при физиологических значениях pH активность фермента составляет 93-96% от максимальной величины. Плазмида pACYC_LANS имеет два гена резистентности к антибиотикам: bla (ApR) и kan (KmR), отвечающие соответственно за устойчивость к ампициллину и канамицину. При промышленном выращивании штамма продуцента аспарагиназы в качестве селективного агента в настоящее время используют только один антибиотик - ампициллин.
Однако β-лактамаза, обеспечивающая устойчивость к ампициллину, равно как и аспарагиназа, являются белками с периплазматической локализацией. Следовательно, активная выработка клетками β-лактамазы должна негативно сказываться на накоплении в периплазме аспарагиназы. Кроме того, процесс ферментации занимает много времени (15-17 часов). Недостатком известной плазмиды является также невысокий уровень биосинтеза.
Задачей настоящей группы изобретений, объединенных общим изобретательским замыслом, является увеличение уровня биосинтеза полипептида rec-ASP-ECAR, создание более продуктивного штамма-продуцента L-аспарагиназы и разработка простого способа получения рекомбинантной аспарагиназы с высоким выходом и чистотой целевого продукта.
Поставленная задача решается описываемой рекомбинантной плазмидной ДНК pACYC_LANS(KM) для экспрессии в клетках Escherichia coli фермента L-аспарагиназы Erwinia carotovora (rec-ASP-ECAR), имеющей молекулярную массу 29,61 Md, размер 4563 п.н., содержащей: фрагмент BamHI-NsbI (FspI) вектора pACYC177, несущий участок начала репликации плазмиды р15А и ген kan, обеспечивающий устойчивость к канамицину; BglII-PdiI (NaeI) - фрагмент вектора рЕТ23а, несущий промотор и терминатор РНК-полимеразы фага Т7 и полилинкер, в котором по сайтам XbaI - BamHI клонирован NheI-BamHI фрагмент вектора pBAD24, несущий последовательность Шайн-Дальгарно с клонированным EcoRI-фрагментом хромосомы Erwinia carotovora размером 1135 п.н., содержащим ген L-аспарагиназы Erwinia carotovora, при этом рекомбинантная плазмида pACYC_LANS(KM) содержит уникальные сайты узнавания рестрикционными эндонуклеазами, имеющими следующие координаты: Kpn I - 1146, BamHI - 1155, Nco - 1142, NotI - 1186, PvuI - 3525, Sac - 1167 п.н.
Поставленная задача решается также описываемым штаммом Escherichia coli BL21(DE3), трансформированным рекомбинантной ДНК pACYC_LANS(KM), охарактеризованной выше, который является продуцентом рекомбинантной L-аспарагиназы Erwinia carotovora.
Поставленная задача решается также описываемым способом получения рекомбинантной L-аспарагиназы Erwinia carotovora, заключающимся в том, что культивируют штамм-продуцент E.coli, трансформированный рекомбинантной плазмидой pACYC_LANS(KM), который охарактеризован выше, в оптимальных для синтеза данного фермента условиях, выделяют сконцентрированную биомассу, подвергают ее разрушению на Френч-Прессе, высаливают целевой продукт из полученного бесклеточного экстракта сернокислым аммонием в зоне 20-60% насыщения, проводят обессоливание сульфат-аммонийной фракции на колонке с Sephadex G-50, обессоленную фракцию подвергают ионообменной хроматографии на CM-Sepharose FF, осуществляют концентрирование целевого продукта в два этапа: вначале на колонке с DEAE-сорбентом, а затем на колонке с CM-Sepharose и лиофилизуют.
Предпочтительно культивирование штамма осуществляют при 37°С в питательной среде на основе бульона LB-M9 при рН=7, культуральную жидкость после охлаждения подвергают мембранному концентрированию и сепарации.
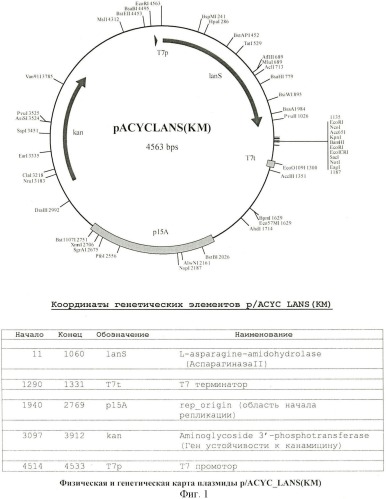
Заявленную рекомбинантную плазмиду, физическая и генетическая карта которой представлены на фиг.1, получают с помощью генно-инженерных манипуляций из плазмиды pACYC_LANS (описанной нами в RU 2224797, и принятой за прототип) путем удаления гена резистентности к ампициллину. В таблице 1 представлены уникальные сайты узнавания рестрикционными эндонуклеазами на ДНК плазмиды pACYC_LANS(KM).
Высокий уровень синтеза целевого полипептида обеспечивается тем, что плазмида pACYC_LANS(KM) лишена гена устойчивости к ампициллину.
Штамм-продуцент rec-ASP-ECAR получают путем трансформации компетентных клеток E.coli BL21(DE3) сконструированной рекомбинантной плазмидной ДНК pACYC_LANS(KM).
Полученный нами штамм бактерий, несущий плазмиду pACYC_LANS(KM), депонированный в ВКМП под коллекционным номером № В-10370, характеризуется следующими признаками:
Морфологические признаки: Клетки палочковидной формы, грамотрицательные, неспороносные.
Культуральные признаки: клетки хорошо растут на обычно используемых питательных средах. Время генерации около 30 мин в жидкой LB-среде. На 1,5%-ном питательном агаре «Дифко» образуются гладкие, серые, блестящие, круглые с ровным краем колонии. При росте на агаризованной LB-среде колонии круглые, гладкие, полупрозрачные, блестящие, серые, край ровный; диаметр колоний 3-5 мм; консистенция пастообразная. Рост в жидкой среде LB характеризуется равномерным помутнением среды.
Физиолого-биохимические признаки:
Клетки штамма продуцента могут расти в диапазоне температур 20-42°С, при этом оптимум составляет 37°С. Наиболее благоприятные для роста значения pH находятся в интервале 6,8-7,2. При росте в аэробных условиях культура может усваивать азот как органических соединений (пептон, триптон, аминокислоты, дрожжевой экстракт), так и аммонийных и нитратных солей. Углерод усваивается в форме углеводов и аминокислот.
Устойчивость к антибиотикам. Клетки проявляют устойчивость к канамицину (до 50 мкг/мл), обусловленную наличием в плазмиде pACYC_LANS(KM) гена kan.
Способ, условия и состав среды для хранения штамма. LB-бульон с 15% глицерином, при температуре -70°С, в криовиалах.
Существенными отличиями заявляемого способа получения от прототипа являются: использование более продуктивного нового штамма, оптимизация условий его культивирования и приемы выделения и очистки получаемой субстанции. Штамм Е.coli BL21(DE3)/pACYC_LANS(KM) обеспечивает устойчивый синтез полипептида L-аспарагиназы Erwinia carotovora с активностью не менее 95-102 МЕ/мл культуральной среды, что обуславливает высокую технологичность процесса.
Перечень фигур, иллюстрирующих изобретение.
На фиг.1. представлена физическая и генетическая карта рекомбинантной плазмиды pACYC_LANS(KM).
На фиг.2. - полная нуклеотидная последовательность гена L-аспарагиназы Erwinia carotovora, инициирующий и терминирующий кодоны выделены жирным шрифтом.
На фиг.3 - нуклеотидная последовательность гена lanS и аминокислотная последовательность L-аспарагиназы Erwinia carotovora.
На фиг.4 - картина рестрикционного расщепления плазмиды pACYC_LANS.
Заявленный штамм-продуцент Escherichia coli BL(DE3)/pACYC_LANS(KM) депонирован в ВКМП под коллекционным № В-10370.
Изобретение иллюстрируется следующими примерами:
Пример 1. Конструирование рекомбинантной плазмиды pACYC_LANS(KM).
Плазмида pACYC_LANS, используемая в настоящее время при получении аспарагиназы, имеет два гена резистентности к антибиотикам: bla (ApR) и kan (KmR), отвечающие соответственно за устойчивость к ампициллину и канамицину.
Для удаления из исходной плазмиды гена устойчивости к ампициллину ~10 нг ДНК плазмиды pACYC_LANS в 20 мкл расщепляют одновременно рестриктазами PdiI и NsbI. После этого ферменты инактивируют прогреванием при 65°С в течение 20 мин и проводят реакцию самолигирования (Self-circularization) в объеме 200 мкл. Лигазной смесью трансформируют штамм E.coli XLI Blue. Среди полученных клонов отбирают устойчивые к канамицину и чувствительные к ампициллину клоны. Из отобранных клонов выделяют плазмиды и проводят их рестрикционный анализ.
Структуру клонированного гена в отобранных клонах подтверждают определением нуклеотидной последовательности с использованием набора Cycle ReaderTM DNA Sequencing Kit (Fermentas, Литва). В результате получают экспрессионную плазмиду pACYC_LANS (KM) (фиг.1).
Получено 10 клонов E.coli BL21(DE3) с делегированным геном устойчивости к ампициллину (КМ).
По результатам проверки аспарагиназной активности у данных клонов для дальнейшего изучения отбирают наиболее активные клоны pACYC_LANS (KM).
На фиг.4 приведена картина рестрикционного расщепления плазмиды pACYC_LANS.
Анализ распределения ДНК-фрагментов плазмиды pACYC_LANS при рестриктазном гидролизе (см. фиг 4. и таблицу 1) указывает на структурную целостность плазмиды.
Пример 2. Получение штамма-продуцента.
Рекомбинантной плазмидной ДНК pACYC_LANS(KM) трансформируют компетентные клетки Escherichia coli BL21(DE3) («Novagen» Cat. №69387-3) и после выращивания рекомбинантных клонов на LB-агаре с канамицином при 37°С получают штамм-продуцент полипептида rec-ASP_BCAR.
Пример 3. Сравнительные данные продуктивности штаммов с плазмидами pACYC_LANS(KM) и pACYC_LANS.
Для сравнительного изучения продуктивности штаммов с плазмидами pACYC_LANS(KM) и pACYC_LANS проводят культивирование в колбах объемом 250 мл, содержащих 50 мл стандартной среды LB, при температуре 37°С и скорости перемешивания 180 об/мин. Посевной материал (ночная культура, выращенная на той же среде и в тех же условиях) вносят в среду в соотношении 1:100. Клон pACYC_LANS(KM) выращивают в присутствии 50 мг/мл канамицина. В качестве контроля используют клон с исходной плазмидой pACYC_LANS, культивируемый в присутствии одновременно ампициллина и канамицина. Клетки выращивают до ОП600=2,0-2,3, после чего вносят индуктор (ИПТГ) до конечной концентрации 0,5 мМ. Результаты сравнительного изучения продуктивности представлены в таблице 2. Как следует из таблицы 2, клон штамма-продуцента E.coli BL21 (DE3)/pACYC_LANS(KM) характеризуется примерно на 25% более высокими величинами накопления активности фермента в клетках и продуктивности, чем контрольные клоны E.coli BL21(DE3)/pACYC_LANS. Клон E.coli BL21 (DE3)/pACYC_LANS(KM) отбирают для выращивания рекомбинантного штамма E.coli в ферментере.
Пример 4. Выращивание штамма-продуцента E.coli BL21 (DE3)/pACYC_LANS(KM) в ферментере.
Единичную колонию рекомбинантного штамма E.coli BL21 (DE3)/pACYC_LANS(KM) инокулируют в 5 мл LB-среды, содержащей 20 мкг/мл канамицина, и выращивают в течение ночи при перемешивании со скоростью 180 об/мин и температуре 37°С. Инокулят для ферментации готовят, пересевая адаптированную культуру в 250 мл свежей среды, из расчета 1:50 и культивируют в условиях аэрации в течение 2-3 часов, до ОП=2-2,3 ОЕ, после чего вносят в ферментер.
Ферментацию культуры проводят после добавления в ферментер (рабочий объем 4 л) инокулята в соотношении 1:50 к объему среды при pH 7,2-7,5, температуре 37°С и аэрации (150 об/мин). Культуру выращивают до ОП600=1,8 (середина логарифмической фазы роста) и в среду вносят индуктор ИПТГ до конечной концентрации 0,5 мМ. Культивирование продолжают в течение 17 час, клетки собирают центрифугированием (5000 об/мин; 10 мин) и хранят при -80°С. Выход сырой биомассы составляет около 7 г/л. Содержание rec-ASP-ECAR в биомассе рекомбинантного штамма-продуцента составляет около 20% от суммарного белка клетки. Накопление фермента в клетках достигает 95-102 МЕ/мл культуральной среды.
Пример 5. Выращивание продуцента Escherichia coli BL(DE3)/pACYS_LANS(KM) в 300-литровом ферментере.
Для создания банка клеток используют отдельные клоны транформантов E.coli BL21(DE3)/pACYC_LANS(KM), полученные на LB-агаре с канамицином. Для закладки на хранение колонию продуцента выращивают в LB-бульоне до середины логарифмической фазы роста и полученную суспензию вносят в криовиалы, содержащие 30%-ный раствор глицерина, в соотношении 1:1. Смесь тщательно перемешивают и быстро замораживают при температуре -70°С.
Для отработки методики приготовления посевного материала для ферментации в 300-литровом ферментере используется схема, обеспечивающая оптимальные временные характеристики ведения процесса культивирования в сочетании с минимальным количеством пассажей продуцента на этапе масштабирования. В качестве исходного материала для ферментации используют ночную культуру продуцента, выращенную на среде с глюкозой и канамицином, которую после пересева в свежую питательную среду, выращивают до середины экспоненциальной фазы роста и вносят в 30-литровый инокулятор, после культивирования в котором продуцент поступает в 300-литровый ферментер.
Культивирование в ферментере объемом 300 л проведено при следующих условиях:
- Температура - 37°С
- Исходное значение pH среды - 7,0
- Условия аэрации: число оборотов мешалки 0-300 об/мин
Расход воздуха на аэрацию 150-70 л/мин
- Питательная среда на основе LB-M9 бульона
- Объем посевного материала 30 л (выращен в ферментере объемом 30 л)
- Оптическая плотность посевного материала при 560 нм - 4,70 ОЕ
- Объем культуральной жидкости в ферментере 260 л.
По окончании культивирования культуральную жидкость охлаждают до температуры 14-15°С проточной водопроводной водой, концентрируют в течение 3-х часов на мембранной установке (размер пор у мембран 0,25 мкм) до объема 30 л и сепарируют на сепараторе АСГ-3М при 9000 об/мин для получения влажной биомассы. Уровень активности аспарагиназы, определяемый методом прямой несслеризации, составил 140-150 МЕ/мл.
Пример 6. Очистка rec-ECAR_LANS из выращенной в ферментере биомассы.
Стадия 1. Разрушение биомассы на Френч-Прессе (получение бесклеточного экстракта).
Разрушение биомассы, проводят на Френч-Прессе в лизирующем буфере (10 мМ ЭДТА, pH 9,5), при соотношении клеток и лизирующего буфера 1:4 и рабочем давлении 1580-1600 бар. Выход на стадии бесклеточного экстракта составляет 80-93%.
Стадия II. Фракционирование сульфатом аммония и обессоливание.
Процесс солевого фракционирования проводят при температуре +4°С. При насыщении бесклеточного экстракта сульфатом аммония до 20% удается избавиться центрифугированием от части балластных белков, при дальнейшем насыщении сульфатом аммония надосадочной жидкости в интервале от 20 до 60% образуется осадок, который содержит почти всю аспарагиназную активность.
Для обессоливания используют колонку с Sephadex G-50 (coarse) объемом 5,5 л (14,0×35,5 см) в 20 мМ калий-фосфатном буфере, содержащем 1 мМ глицина и 1 мМ ЭДТА, pH 5,6. Обессоливание проводят при скоростях потока около 30 мл/мин.
Стадия III. Ионообменная хроматография на CM-Sepharose FF.
Обессоленную фракцию сульфат-аммонийного осадка разбавляют этим же буфером вдвое и наносят на колонку с CM-Sepharose FF (10×3,2 см), уравновешенную 20 мМ калий-фосфатным буфером, содержащим 1 мМ глицина и 1 мМ ЭДТА, pH 5,6 со скоростью около 400 мл/час. Проскок контролируют, определяя ферментативную активность качественно (микрометодом) с использованием реактива Несслера. После нанесения образца колонку промывают 20 мМ калий-фосфатным буфером, pH 6,3 с целью удаления балластных белков. Элюцию целевого вещества проводят 20 мМ калий-фосфатным буфером, pH 7,0 и 7,6. Завершающий этап хроматографической очистки полуфабриката аспарагиназы представляет собой стадию концентрирования образца, одновременно сопровождающуюся более глубокой степенью его очистки.
Стадия IV. Подготовка к лиофилизации.
Концентрирование проводят на колонке с CM-Sepharose FF (2,5×10,0 см), уравновешенной 20 мМ калий-фосфатным буфером, pH 6,3. В качестве предколонки используют колонку с DEAE-сорбентом СПС-DEAE-Био (5×6 см). Колонки с DEAE-сорбентом также уравновешивают 20 мМ калий-фосфатным буфером, pH 6,3.
Целевую фракцию, полученную с 250-миллилитровой колонки с СМ-Sepharose FF, разбавляют равным объемом 20 мМ KH2PO4, при этом pH фракции снижается с 7,0 до 6,3-6,4. Нанесение образца осуществляют через предколонку с DEAE-сорбентом на основную колонку с CM-Sepharose FF со скоростью потока 8 мл/мин. После нанесения образца колонку тщательно отмывают 20 мМ калий-фосфатным буфером, pH 6,3 до базовой линии, а затем элюируют белок 20 мМ калий-фосфатным буфером, pH 7,6.
Выход целевого вещества на этой стадии составляет 95-97%.
В качестве стабилизирующей добавки используют глюкозу, которую добавляют в препарат перед лиофилизацией до конечной концентрации 0,5%.
Стадия V. Лиофилизация.
Лиофилизацию проводят на лиофильной сушке Alpha ("Christ", Switzerland). В одних опытах концентраты, содержащие 0,5% глюкозы, лиофилизируют на полке при -10°С в течение 2 суток, затем полку нагревают до температуры 30°С. В других лиофилизацию проводят в колбах при комнатной температуре. Потери аспарагиназной активности при лиофилизации в обоих случаях составляют от 5 до 10%.
Выход целевого продукта при масштабировании процесса выделения и очистки составил 56%.
Полученный продукт полностью удовлетворяет требованиям, предъявляемым к иммунобиологическим рекомбинантным препаратам по содержанию примесных бактериальных белков E.coli и эндотоксинов.
Как видно из приведенных примеров, заявленная рекомбинантная плазмидная ДНК, штамм-продуцент Escherichia coli BL(DE3)/pACYC_LANS(KM), депонированный в ВКМП под коллекционным № В-103 70, обеспечивают возможность получения заявленным способом рекомбинантной L-аспарагиназы Erwinia carotovora с высоким выходом и достаточной чистотой.
| Таблица 1. | ||
| Уникальные сайты узнавания рестрикционными эндонуклеазами на ДНК плазмиды pACYC_LANS(KM) | ||
| Фермент | Сайт узнавания | Позиция на карте |
| BamHI | GGATC!С | 1155 |
| Bsp68I | TCG!CGA | 3183 |
| Bsp119I | TT!CGAA | 2026 |
| Bst11071 | GTA!TAC | 2751 |
| Bcu15I | AT!CGAT | 3218 |
| Eco52I | С!GGCCG | 1187 |
| Hin1I | GR!CGYC | 779 |
| KpnI | GGTAC!С | 1146 |
| Kpn2I | T!CCGGA | 1351 |
| KspAI | GTT!AAC | 286 |
| MluI | A!CGCGT | 689 |
| NcoI | С!CATGG | 1142 |
| NotI | GC!GGCCGC | 1186 |
| PdmI | GAANN!NNTTC | 2706 |
| Pfl23II | С!GTACG | 895 |
| Psp1406I | AA!CGTT | 713 |
| PvuI | CGAT!CG | 3525 |
| PvuII | CAG!CTG | 1026 |
| SacI | GAGCT!С | 1167 |
| SspI | AAT!ATT | 3451 |
| TatI | W!GTACW | 529 |
| XceI | RCATG!Y | 2187 |
| Таблица 2. | ||||
| Активность и продуктивность клонов E.coli/pACYC_LANS с делегированным геном резистентности к ампициллину | ||||
| №, п/п | Клоны | ОП600 нм | Активность, (МЕ/мл) | Продуктивность (МЕ/ОЕ) |
| 1 | pACYC_LANS(KM) | 4,2 | 81,5 | 19,4 |
| 2 | Контроль (среда с Ар) | 4,5 | 66,3 | 14,7 |
| 3 | Контроль (среда с Km) | 4,3 | 61,6 | 14,5 |
| 4 | pACYC_LANS (контроль, среда с Ар и Km) | 4,6 | 65,3 | 14,3 |
1. Рекомбинантная плазмидная ДНК pACYC_LANS(KM) для экспрессии в клетках Escherichia coli фермента L-аспарагиназы Erwinia carotovora (rec-ASP-ECAR), имеющая молекулярную массу 29,61 Md, размер 4563 п.н., содержащая: фрагмент BamHI - NsbI (FspI) вектора pACYC177, несущий участок начала репликации плазмиды р15А и ген kan, обеспечивающий устойчивость к канамицину; BglII-PdiI(NaeI) - фрагмент вектора рЕТ23а, несущий промотор и терминатор РНК-полимеразы фага Т7 и полилинкер, в котором по сайтам XbaI - BamHI клонирован NheI-BamHI фрагмент вектора pBAD24, несущий последовательность Шайн-Дальгарно с клонированным EcoRI-фрагментом хромосомы Erwinia carotovora размером 1135 п.н., содержащим ген L-аспарагиназы Erwinia carotovora; уникальные сайты узнавания рестрикционными эндонуклеазами, имеющими следующие координаты: Kpn I - 1146, BamHI - 1155, Nco - 1142, NotI - 1186, PvuI - 3525, Sac - 1167 п.н.
2. Штамм Escherichia coli BL21(DE3), трансформированный рекомбинантной плазмидной ДНК pACYC-LANS(KM), охарактеризованной по п.1 - продуцент рекомбинантной L-аспарагиназы Erwinia carotovora.
3. Способ получения рекомбинантной L-аспарагиназы Erwinia carotovora, характеризующийся тем, что культивируют в оптимальных условиях штамм-продуцент, охарактеризованный по п.2, выделяют сконцентрированную биомассу, подвергают ее разрушению на Френч-Прессе, высаливают целевой продукт из полученного бесклеточного экстракта сернокислым аммонием в зоне 20-60% насыщения, проводят обессоливание сульфат-аммонийной фракции на колонке с Sephadex G-50, обессоленную фракцию подвергают ионообменной хроматографии на СМ-Sepharose FF, осуществляют концентрирование целевого продукта в два этапа: вначале на колонке с DEAE-сорбентом, а затем на колонке с СМ-Sepharose FF и лиофилизуют.
4. Способ по п.3, отличающийся тем, что культивирование штамма осуществляют при 37°С в питательной среде на основе бульона LB-M9 при pH 7, культуральную жидкость после охлаждения подвергают мембранному концентрированию и сепарации.