Способ лечения вагинальных дисбиозов и вагинитов у женщин с хроническим сальпингоофоритом
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к гинекологии, физиотерапии. Способ включает магнитолазерное воздействие. Указанное воздействие осуществляют по влагалищной методике. Для этого используют инфракрасные светодиоды мощностью 60 мВт. Воздействие осуществляют с частотой 1500 Гц, напряженностью магнитного поля 30 мТл. В первый день продолжительность процедуры составляет 5 минут, в последующие дни по 10 минут. После каждой процедуры магнитолазерного воздействия во влагалище вводят иловую сульфидную грязь температурой 22-24°С в виде тампона, на 60 минут. После завершения процедуры остатки иловой сульфидной грязи удаляют спринцеванием минеральной водой. Процедуры проводят 1 раз в день. На курс - 10 процедур. Способ повышает эффективность лечения за счет активации клеточных ферментных систем, оказывает биостимулирующее воздействие на мембраны иммунокомпетентных клеток, обеспечивает создание тепловых, биохимических и механических градиентов. 1 табл., 2 ил.
Реферат
Изобретение относится к медицине, а именно к гинекологии и физиотерапии, и может быть использовано для лечения вагинальных дисбиозов и вагинитов у женщин с хроническим сальпингоофоритом.
Наиболее близким к предлагаемому является способ лечения бактериального вагиноза (БВ) путем применения низкочастотного ультразвука и низкоинтенсивного лазера по следующей методике: низкочастотная ультразвуковая терапия (санация) влагалища (далее НЧУЗС) проводится ультразвуковым аппаратом «ГИНЕТОН-2» через жидкую лекарственную среду (фиозиологический раствор), заливаемый во влагалище перед процедурой. Длительность одной процедуры НЧУЗС составляет 120 секунд. После этого отработанный раствор удаляется из влагалища, а его стенки тщательно протираются стерильным марлевым материалом. Первые 5 сеансов проводятся ежедневно. Затем делаются перерывы через день, через два дня и т.д., пока полностью не исчезают патологические выделения. Низкоинтенсивная магнитолазерная (МИЛ) терапия осуществляется инфракрасным лазерным аппаратом «МИЛТА-Ф». Процедуры МИЛ-терапии проводятся сразу после НЧУЗС с использованием специальной вагинальной насадки, которая рассеивает исходящее из терминала аппарата лазерное излучение во все стороны. Для соблюдения стерильности на насадку на время процедуры надевается презерватив. Время одной процедуры рассчитывают по стандартной формуле
,
где Т - время экспозиции, D - энергетическая экспозиция, S - площадь облучаемой поверхности, Р - мощность, К - коэффициент отражения лазерного излучения.
Время одной процедуры, составляет приблизительно 5 минут. Курс лечения МИЛ-терапией составляет 15 сеансов. Общий курс аппаратного лечения БВ занимает один межменструальный промежуток [1].
Недостатком данного способа является: длительность курса сочетанного применения низкочастотного ультразвука и низкоинтенсивного лазера по данной методике и осложнения: - в результате проведенного 25-дневного лечения у 72% женщин была элиминирована практически вся влагалищная флора; нормоценоз восстановился через месяц у 58% пациенток; также при лечении больных БВ с длительностью заболевания более 6 месяцев и наличием нескольких половых партнеров показано одновременное проведение курса терапии с применением низкочастотного ультразвука, и низкоинтенсивного лазера, и традиционной антибактериальной терапии.
Новая техническая задача - повышение эффективности лечения больных за счет уменьшения сроков лечения данной патологии; снижения медикаментозной терапии, связанной с применением антимикробных препаратов - и аппаратной терапии, обусловленной применением только одного метода аппаратной терапии, а второй метод является преформированным физическим фактором, нагрузки на организм; снижения полученной дозировки облучения за время курсового лечения; возможность проведения лечения в условиях больничной палаты, ЖК, амбулаторно; простота осуществления лечебного воздействия.
Для решения поставленной задачи в способе лечения вагинальных дисбиозов и вагинитов у женщин с хроническим сальпингоофоритом путем магнитолазерного воздействия на ткани влагалища магнитолазерное воздействие осуществляют по влагалищной методике с мощностью ИК-светодиодов 60 мВт, частотой 1500 Гц, напряженностью магнитного поля 30 мТл, в первый день продолжительность процедуры составляет 5 минут, затем по 10 минут; причем после каждой процедуры магнитолазерного воздействия вводят иловую сульфидную грязь в виде тампона влагалищно на 60 минут, с температурой пелоида 22-24°С, после завершения процедуры остатки иловой сульфидной грязи удаляют спринцеванием минеральной водой, процедуры проводят 1 раз в день, на курс - 10 процедур.
Способ осуществляют следующим образом.
В положении больной - лежа на спине, со слегка согнутыми в коленных и тазобедренных суставах и разведенными в стороны нижними конечностями, во влагалище женщины вводили специальную световодную оптическую гинекологическую стерильную насадку (вагинальный индуктор при этом помещен в презерватив) аппарата магнито-ИК-лазерного терапевтического с фоторегистратором и восемью частотами повторения импульсов лазерного излучения «МИЛТА-Ф-8-01» в задний свод влагалища до появления сопротивления тканей. Параметры проведения процедуры: мощность ИК-светодиодов 60 мВт, частота 1500 Гц, напряженность магнитного поля 30 мТл, в первый день продолжительность процедуры составляет 5 минут, затем по 10 минут. Суммарную поглощенную дозу с учетом расфокусирующей насадки рассчитывают по формуле
Du=(1-a)*(1-mmн/mon)*(0,1+0,6*10-6*F)*tэ [Дж],
где а - коэффициент потери насадки = 0,35, mmн - мощность при установленной насадке, mon - мощность на уровне апертуры, F - частота ИК-излучения, tэ - время экспозиции [2, 3].
Суммарная поглощенная доза за одну процедуру составляет соответственно 15,6 Дж при 5 минутах и 31,2 Дж при 10 минутах облучения. При этом плотность потока мощности составляет 0,6 мВт/см2. После введения оптической насадки женщину накрывают простыней. Затем (после каждой процедуры МИЛ-терапии) женщина располагалается на гинекологическом кресле. Далее раскрывают влагалище с помощью двустворчатого зеркала Куско; пинцетом вводят иловую сульфидную грязь, завернутую в стерильный бинт в виде тампона размером 5×3×3 см, температурой 22-24°С, на 60 минут. Используют иловую сульфидную грязь озера Малое Яровое (с М грязевого отжима 221,5 и его pH 7,48), содержащую слабоощущаемые песчаные частицы не более 0,25 мм в 0,14% (при норме 3%); объемный вес грязи составлял 1,59 г/см3, сопротивление сдвигу - 3924 дин/см2; pH среды грязи 7,30. Донные отложения по основным классификационным признакам соответствуют классу среднесульфидных соленасыщенных лечебных грязей Карачинской разновидности. Санитарно-биологическая оценка донных отложений проводилась в ФГУ «ТНИИКиФ ФМБА России» испытательной лабораторией природных лечебных ресурсов РОСС RU. 0001. 21ПЦ37. Согласно протоколу испытаний №231 М от 23.07.09 года, донные отложения соответствуют нормам МУ 143-9/316-7 МЗ 1989 года по всем показателям.
Нити тампона оставляют снаружи. Положение во время процедуры любое (по желанию женщины): она может лежать, сидеть, активно двигаться. После окончания процедуры тампон путем потягивания за нити извлекают из влагалища и выбрасывают. После удаления тампона остатки иловой сульфидной грязи удаляли спринцеванием минеральной воды. Для спринцевания используют слабоминерализованную воду, например, «ОМЕГА» с М 0,4 и pH 9,0 (за счет газации СО2 при бутилировании воды значение pH снижалось до 5,2). Процедуры проводят 1 раз в день, на курс - 10 процедур.
Выбор лечебных факторов и режим их применения основан на изучении данных научно-медицинской литературы и анализе данных клинических наблюдений
Сложный характер любого патологического процесса, сопровождающегося изменениями в различных органах и тканях, диктует необходимость комплексного подхода к физиотерапии. Только при комплексном применении правильно подобранных физических факторов можно получить выраженный терапевтический эффект или добиться полного выздоровления. Из двух возможных вариантов комплексного использования (комбинирование и сочетание) физических факторов предпочтение отдается сочетанной физиотерапии, т.е. одновременному воздействию несколькими факторами на одну и ту же область человеческого тела [4].
В последние годы при лечении инфекционных заболеваний все большее внимание уделяется системному подходу, заключающемуся в сочетанном применении средств, оказывающих специфическое и неспецифическое этиотропное действие, а также влияющих на патогенез воспалительного процесса и модулирующих функциональную активность иммунной системы пациентки [5]. К сожалению, антибактериальная терапия ведет к усилению процессов дисбиоза за счет еще большего угнетения нормальной микрофлоры и иммунологических реакций. Медикаментозное лечение данной патологии можно рассмотреть на примере применения «Тержинана в лечении бактериального вагиноза и урогенитального кандидоза». В статье представлены данные о лечении бактериального вагиноза и урогенитального кандидоза местным применением комбинированного препарата тержинана. Эффективность применения тержинана сравнивали с апробированными методами лечения данных заболеваний с использованием 2% далацина (вагинального крема) и йенамазола. Установлено, что излечение БВ констатировано у 82,8% и УГК - у 63,6% больных. Через 3 месяца после окончания курса лечения рецидивы отмечены соответственно у 18,8% с БВ и у 18,7% больных УГК. Однако следует отметить, что было бы неверно считать, будто применение тержинана и других аналогичных средств сразу решает проблему лечения БВ или УГК. Без последующей коррекции биохимического и биофизического профиля влагалищной среды, нормализации местного иммунитета и заместительной терапии эубиотиками неминуемы рецидивы. Тем не менее, можно констатировать, что тержинан является одним из препаратов выбора для лечения БВ и УГК на первом этапе. Удобство применения, отсутствие выраженных побочных и аллергических реакций, доступность, безопасность позволяют рекомендовать его не только для лечения некоторых влагалищных инфекций, но и как препарат для профилактики инфекционных осложнений после влагалищных операций и в послеродовом периоде [6]. Лишь при условии активации иммунной системы, создания благоприятных условий для репарации и эпителизации тканей возможно полное излечение, а следовательно - предупреждение развития осложнений репродуктивной системы как во время беременности, так и вне ее [7].
В качестве модифицирующего фактора выбрано сочетание инфракрасного лазера, магнитного поля и иловой сульфидной грязи.
Выбор аргументирован следующими фактами.
Последовательность происходящих изменений при лазеротерапии можно схематически представить следующим образом [8]: взаимодействие низкоэнергетического лазерного излучения со специфическими и неспецифическими фотоакцепторами - запуск комплекса фотофизических и фотохимических реакций - активация клеточных ферментных систем с усилением биоэнергетических и биосинтетических процессов - интенсификация пролиферации клеток - усиление регенерации, кроветворения, активности иммунной системы и системы микроциркуляции - генерализация местных эффектов лазеротерапии посредством нейрогуморальных и нервно-рефлекторных механизмов.
Известно, что генерализация воздействия лазерного облучения на целостный организм происходит посредством воздействия на форменные элементы крови прямым и опосредованным путями. Облучение этих клеток лазером приводит к увеличению количества Т-лимфоцитов и усилению активности Т-супрессоров, к подавлению или усилению (в зависимости от дозы) фагоцитарной функции и хемотаксиса нейтрофилов [9]. Таким образом, на молекулярном уровне можно выделить биостимулирующее воздействие на мембраны иммунокомпетентных клеток, усиление стимуляции цГМФ, активации процесса синтеза ДНК, индукцию цитокинов, запускающих каскад иммунных и нейро-эндокринных реакций. На системном уровне эффекты лазерного излучения выражаются также в позитивном влиянии на реологические свойства крови и микроциркуляцию. Известна высокая клиническая эффективность применения лазеротерапии при хронических воспалительных заболеваниях придатков матки и органов малого таза [2].
Магнитное поле всегда потенцирует лазерное воздействие. Основные механизмы действия сочетанного магнитолазерного излучения: увеличивается степень диссоциации электролитов тканей, происходит поляризация ионов в магнитном поле, уменьшается степень рекомбинации диссоциированных ионов. В результате: лазерное излучение проникает глубже, действует эффективнее и способствует созданию более мощных тепловых, биохимических и электрических градиентов.
Известна клиническая эффективность магнитолазера при гестозах; отработаны методы МЛТ при ишемии миокарда. Наиболее активно на процедуры МЛТ реагирует сосудистая система. Отмечается повышение скорости кровотока, увеличение числа функционирующих капилляров, появление почек роста капилляров и образование новых коллатералей в облучаемой ткани, что способствует усилению кислородного обмена и увеличению поглощения кислорода тканями. Клинически выявлено выраженное противовоспалительное, противоотечное и стимулирующее регенерацию тканей действие сочетанного лазерного или магнитного воздействия [9, 10, 11]. Работами Томских ученых Г.Ф.Плеханова и А.И.Торопцева за период с 1980 по 1990 годы обозначены подходы к получению максимального биологического эффекта и способы ликвидации негативных последствий электромагнитных воздействий. Таким образом, были основания надеять на получение иммуномодулирующего действия магнитолазера на эндометрий, слизистые оболочки.
В монографии Л.П.Шустова [12] указывается, что лечение нативной грязью и ее препаратами дает высокую терапевтическую активность, а применение пелоидов в сочетании с физическими воздействиями превосходит по эффективности нативную грязь. Таким образом, косвенно доказана целесообразность поиска действующего начала. Аналогию местного применения пеллоида можно провести с новым поколением иммуностимуляторов, действующим началом которых является синтетическая или натуральная антигенная детерминанта бактериального происхождения. К примеру, иммуномодулирующие свойства препарата гепон обусловлены структурой синтетического тетрадекапептида (НР1 - 14). Даже отдельные концевые фрагменты, пенталептиды, обладают иммуноадъювантным действием. Механизм действия препарата: гепон вызывает продукцию α- и β-IFN, мобилизует и активирует макрофаги, ограничивает выработку цитокинов воспаления (IL-1, IL-б, IL-8 и TNF), стимулирует продукцию антител к различным антигенам инфекционной природы, подавляет репликацию вирусов, повышает резистентность организма в отношении инфекций, вызванных вирусами, бактериями или грибами. С учетом вышеуказанного, для предлагаемого нами метода существенно важной и основной является химическая составляющая пелоида. В связи с этим мы пренебрегаем тепловым фактором (используя «холодную» иловую сульфидную грязь) и механической составляющей пелоида (нами предложена методика введения грязи в тампоне размером 5×3×3 см и отказ от большого объема данного природного фактора, вводимого во влагалище [4, 10, 11]).
Иловые сульфидные грязи образуются на дне минеральных (соляных) водоемов. Их грязевой раствор богат водорастворимыми солями и в нем содержится относительно малое количество органических веществ (менее 10%). Состав определяется высоким содержанием минеральных солей, сероводорода. Окисление метана (CH4) в анаэробных условиях объясняется деятельностью сульфатредуцирующих бактерий, использующих для этого кислород - сульфат иона морской (иловой) воды. Благодаря наличию в иловой грязи сульфатредудирующих бактерий образуется сернистое железо (сульфид железа - Fe(HS)2), придающее ей черный цвет; она обладает большой вязкостью и пластичностью (сметанообразная мелкодисперсная масса) со слабым запахом сероводорода. В результате сложных биохимических и физико-химических процессов сероводород соединяется с железом и образует гидротроиллит (Fe(HS)J) - один из основных компонентов сульфидных грязей. Содержание воды в этой грязи от 40 до 70%, засоренность частицами диаметром более 0,25 мм не выше 3%. Оптимальное значение величины сопротивления сдвигу до 2500 дин/см2, плотность 1,6 г/см3, значения окислительно-восстановительного потенциала отрицательны (~190 мВ); обладает бактерицидными свойствами. Сульфидные грязи содержат небольшое количество микроорганизмов. За счет присутствия сапрофитных микробов - антагонистов сульфидные грязи средней солености могут обладать достаточно выраженными бактериостатическими свойствами. В водных вытяжках сульфидной грязи установлено также наличие бактериофага, обладающего способностью лизировать дизентерийную кишечную палочку, стафилококки и протеи. Для иловых сульфидных грязей характерно присутствие небольшого количества органических веществ. Однако грязеобразовательный процесс тесно связан с жизнедеятельностью микро- и макроорганизмов, приводящих к накоплению разнообразных органических веществ. Благодаря его присутствию в пелоидах происходят сложные биохимические реакции с образованием ароматических продуктов, жирных кислот, аминокислот и др. Оно служит энергетическим источником такого важного процесса, как сульфатредукция с образованием сероводорода и гидротроиллита. В иловых грязях содержание органического вещества составляет 2-5%, иногда достигая и больших величин. Из сульфидной грязи выделено несколько пенициллиноподобных штаммов плесени, фолликулиноподобных веществ, всасывание которых через неповрежденную кожу практически доказано. Лечебный комплекс грязи содержит сложный липидный продукт, который продуцируют сине-зеленые водоросли. Липиды (липопротеиды) выполняют в организме роль энергетического резерва и служат основным материалом для построения клеточных мембран. Им отводится важная роль в созревании и старении организма, в создании защитно-компенсаторных механизмов при нарушении обмена, в развитии атеросклероза и других патологических состояний. Наряду с этим липидный комплекс обладает выраженной антибактериальной активностью в отношении тифозных, паратифозных, дизентерийных и дифтерийных микробов, а также некоторых штаммов патогенных грибков. Липиды грязей и их фракции принимают участие в противовоспалительном ответе организма. Адсорбционные свойства лечебной грязи проявляются в способности поглощать патогенную флору. В этом отношении на первом месте по адсорбции стафилококка находится иловая сульфидная грязь. Установлено, что анапская иловая сульфидная грязь адсорбирует стафилококк на 96-99%.
Пелоид как химическое вещество нормализует кислотно-щелочное состояние влагалища, как белковое разнообразие - обеспечивает иммуностимуляцию. Также доказано, что при воздействии пелоида, ингибиторы окислительных реакций, содержащиеся в липидной фракции грязи и обладающие актиоксидантным действием, не только ограничивают проокислительные свойства теплового фактора, но и тормозят ПОЛ в тканях, которое развивается при воспалительном процессе [4, 9 и другие]. Лазер в свою очередь обеспечивает мощную иммуно-, лимфостимуляцию и стимуляцию микроциркуляции; магнитное поле потенцирует действие двух первых факторов. Таким образом, накопленный ранее за десятилетия успешный опыт применения магнитных полей, лазерного излучения, пелоидотерапии прогнозировать хороший терапевтический эффект при лечении указанной патологии.
Применение иловой сульфидной грязи со сниженной до 22-24°С температурой предложено еще и в связи с тем, что при контакте тел и сред различной температуры между ними образуется тепловой поток в направление менее нагретой среды, при этом часть проходящего через ткани теплового потока будет расходоваться на их нагревание и повышение температуры различных элементов тканей [9]. При действии термических стимулов, температура которых меньше температуры организма человека, могут включаться все способы теплоотдачи организма. Модулированные термическими факторами афферентные импульсные потоки от рецепторов поступают на вставочные нейроны задних рогов. Отсюда по автономным и соматическим эфферентным проводникам своего спинального уровня поступают к соответствующим группам скелетных мышц и внутренним органам. Одновременно происходит активация по спиноретикулярным трактам гипоталамуса, через который и происходит управление тепловым балансом организма, которое осуществляется путем некоторых гормонов, БАВ и медиаторов. Факторы локальной сосудистой регуляции влияют преимущественно на тонус сосудов и перераспределение крови, при помощи которой осуществляется перенос тепловой энергии от внутренних органов к поверхности. Начальная активация симпатических волокон вызывает под действием холодовых факторов сужение артериол в течение нескольких минут, впоследствии происходит расширение сосудов. Вазоконстрикцию сосудов вызывают преимущественно локальные вазоактивные вещества (простагландин F). Такая реакция не оказывает существенного влияния на системную гемодинамику и сердечную деятельность. Кроме того, выделяющийся в месте воздействия из окончаний адренергических симпатических волокон норадреналин через бета-адренорецепторы активизирует процессы липолиза в тканях [4, 9]. При этом в кровь выделяются свободные жирные кислоты, окисление которых приводит к значительному выделению тепла; повышается теплоотдача в месте приложения фактора, для чего осуществляется локальная выработка эндогенного тепла в области больного органа.
Анализ данных клинических наблюдений:
В исследование вошла 51 женщина репродуктивного возраста (средний возраст 30 лет) вне беременности, постоянно проживающая на территории Томской области.
Пациентки были разделены на три группы по составу влагалищного биотопа и уровню воспалительной реакции. Наличие лейкоцитоза влагалищного мазка более 40 в отсутствие облигатных патогенов и венерических заболеваний позволяло включить пациентку в группу I с диагнозом вагинит, n=12. Редукция популяции лактобацилл, развитие условно-патогенной флоры при отсутствии воспалительной реакции являлась основанием включения пациентки в группу II с диагнозом бактериальный вагиноз, n=18. Наличие нормоценоза было критерием для формирования группы сравнения III, n=21.
Клинические исследования включали анкетирование, данные объективного осмотра и детального гинекологического статуса. В динамике в соответствующую фазу менструального цикла (через 26-30 дней от начала терапии) оценивались жалобы пациентки, общее состояние, характер вагинальных выделений. УЗИ органов малого таза выполнялось с цветным допплеровским картированием сосудов бассейна маточных артерий. Лабораторные методов исследования включали: общеклиническое обследование, бактериоскопическое и цитологическое исследование мазков из влагалища и цервикального канала; цитохомический метод выявления гликогена в клетках влагалищного эпителия (ШИК-реакция) с полуколичественной оценкой результатов из расчета на 100 клеток по Астальди [13], определение pH влагалищного секрета (с помощью универсальной индикаторной бумаги «LACH NER»); иммунный статус I уровня (CD 3, 4, 8, 19, IgG, IgA, IgM), определение уровня sIgA, IL-1-RA, IL-1β в цервикальной слизи методом ИФА с помощью наборов производства ЗАО «Вектор-Бест» (п. Кольцове, Новосибирская обл.). Обследование на инфекции, передающиеся половым путем (Chlamydia trachomatis, Mycoplasma genitalium) проводилось методом ПЦР с помощью наборов производства ООО «Интерлабсервис» (Москва).
Жалобы на изменившиеся выделения из половых путей (изменение количества, характера влагалищных выделений; появление запаха) до лечения предъявляли в I группе - 83% женщин, во II группе - 89%, в III группе - 5%. Жалобы на слабый зуд в области наружных половых органов отмечали пациентки только I и II групп в 17% и 6% случаев соответственно.
Соматическая патология в анамнезе чаще всего была представлена заболеваниями опорно-двигательного аппарата (остеохондроз позвоночника до 83%) и заболеваниями желудочно-кишечного тракта - хроническими гастритами и язвенной болезнью желудка. Во второй группе частота гастропатологии была значимо выше и составила 56%.
Достоверных различий паритета беременностей, родов и гинекологического анамнеза, в том числе и внематочной беременности между группами не выявлено; случаи замершей беременности в группе вагинитов зарегистрированы в 17% случаев, при наличии бактериального вагиноза - в 11%, в группе сравнения - 5%. Учитывая наличие хронического сальпингоофорита, логичным было обнаружение одинаково высокой частоты бесплодия (33%; 56% и 48% соответственно) и операций на органах малого таза в I группе - 50%, во II группе - 56%, в III группе - 57%.
Инфекции, передающиеся половым путем, в анамнезе чаще регистрировались в группе дисбиотических заболеваний. Наиболее частый возбудитель - Chlamydia trachomatis (33%). Среди условно-патогенных микроорганизмов чаще всего обнаруживались кандиды (56%), гарднереллы (44%), генитальные микоплазмы (19%).
При объективном исследовании достоверных различий между подгруппами в общеклинических, лабораторных показателях, состоянии матки, придатков, объеме регионарного кровотока исследовании не выявлено.
Все больные перенесли лечение хорошо. Патологической физиобальнеореакции не зарегистрировано. При оценке типа адаптационной реакции по Л.X.Гаркави [14] отрицательной динамики также не выявлено. В конце лечения все женщины отметили улучшение общего состояния.
При контрольном обследовании пациентки первой группы жалоб не предъявляли. Доля пациенток, отмечающих обильные выделения из влагалища во второй группе, сократилась с 89% до 17% (р<0,01). Необходимо отметить, что во всех клинических подгруппах к концу курса лечения бели изменили характер и стали слизистыми, исчезли зуд и раздражение вульвы.
При оценке состава влагалищного биотопа до лечения в группе воспалительных заболеваний преобладала Грам+ палочковая флора (50%), третью часть биотопа занимала Грам+/- кокковая флора (33%); в группе дисбиотических заболеваний на фоне сокращения количества Грам+ палочковой флоры выявлен рост дрожжеподобных грибов рода Candida (67%), Gardnerella (33%) и Грам+/- кокков (33%). В группе сравнения преобладающей являлась Грам+ палочковая флора (86%). После лечения зарегистрированы изменения, однотипные для всех групп: уменьшение Грам+ палочковой флоры в среднем на 10-11%, рост доли кокковой флоры, значительное угнетение популяции Gardnerella vaginalis и полная элиминация Candida.
Объяснение подобным изменениям получено при изучении динамики иммунологических и гистохимических показателей.
При оценке системного иммунитета в ходе лечения значимых изменений субпопуляций лимфоцитов не выявлено. В гуморальном звене отмечена тенденция к увеличению количества В-лимфоцитов и концентрации сывороточного IgA.
Изменения локального иммунитета у женщин с нормоценозом влагалищного биотопа были минимальными (Табл.1). Полостное применение магнитолазера в сочетании с пелоидом в этой группе дало значимое повышение продукции секреторного иммуноглобулина А. Небольшое повышение продукции IL-1 не сопровождалось миграцией лейкоцитов.
Наиболее благоприятное воздействие сочетание двух факторов оказало при исходном вагините. Собственная продукция sIgA слизистой (скорее всего с в сочетании с рекрутированием молекул иммуноглобулина из сыворотки) сопровождалось в данном случае достоверным снижением количества лейкоцитов влагалищного секрета. Супрессия лейкоцитарной реакции ассоциирована со снижением наработки IL-1 и выбросом его рецепторного антагониста.
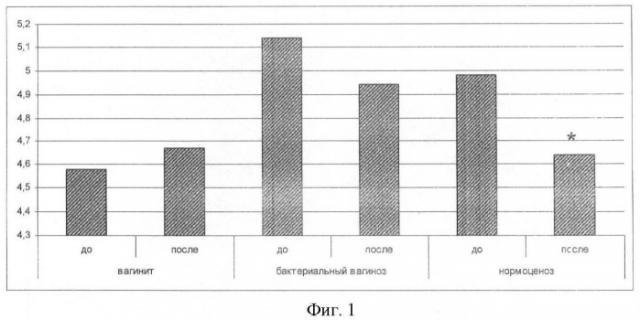
При бактериальном вагинозе применение данной методики дало другой эффект. Достоверное снижение уровня секреторного иммуноглобулина А объясняет замедленную редукцию популяций условно-патогенной флоры в данной группе. Учитывая характерное для бактериального вагиноза повышение pH, был проведен сравнительный анализ этого параметра до и после лечения (фиг.1).
Иловая сульфидная грязь имеет pH 7,30-7,48. Кислая среда влагалища, по мнению большинства авторов, достигается за счет продукции молочной кислоты палочковой флорой. В нашем наблюдении при нормоценозе после лечения выявлено одновременное снижение популяции лактобацилл и сдвиг реакции в кислую сторону. Одним из причин подобного сочетания может быть интенсификация метаболизма как клеток влагалищного эпителия, так и нормальной флоры влагалища. Подтверждение этому мы нашли в динамическом наблюдении за уровнем основного энергетического субстрата клеток - гликогена (фиг.2). В ходе лечения наблюдается снижение содержания гликогена. Наиболее выраженная потеря свойственна группе с местным воспалением.
Для оценки найденных изменений необходимо сопоставление механизмов действия изучаемых факторов. Магнитолазерное воздействие с успехом применяется при хроническом сальпингоофорите, однако его иммунотропное действие дозозависимо и может быть разнонаправленным [2, 8]. При воспалении выгодна частота, превышающая 1000 Гц, поскольку она оказывает противовоспалительное действие за счет значительного улучшения местной микроциркуляции. Применение полостных методик определяет максимум поглощения на слизистой органа. Исследованиями Т.Й.Кару показано, что поглощенная доза 0,001 Дж является порогом стимулирующего действия низкоинтенсивного лазерного излучения. Доза более 0,01 Дж позволяет достичь ускорение синтеза ДНК. Превышение дозы 0,6 Дж ведет к спаду активности ферментов митохондрий [15]. Таким образом, подобранная нами доза 0,36 Дж при 10 минутном облучении является оптимальной. Несмотря на это результаты исследования доказывают, что применение иловой сульфидной грязи при воспалительных заболеваниях репродуктивного тракта должно быть индивидуализировано по состоянию биоценоза влагалища. Так, при вагините механизм повышения pH в процессе лечения, скорее всего, основан на действии ингибиторов окислительных реакций, содержащихся в липидной фракции грязи и обладающих антиоксидантным действием. Используемая нами холодная грязь лишена проокислительных свойств теплового фактора. Блок продукции перекиси имеет протективное значение при воспалительном процессе, но одновременно будет приводить к повышению pH влагалищного секрета. При исходном бактериальном вагинозе pH влагалищного секрета снижается за счет интенсификации обменных процессов нормальной флоры крайне незначительно, учитывая ее малое количество, а противовоспалительный эффект используемых факторов снижает защитный уровень IgA.
Суммируя приведенные факты, можно полагать, что сочетание магнитолазерной и полостной пелоидотерапии обладает выраженным противовоспалительным действием, при этом происходят значительные потери гликогена клетками и изменяется pH среды.
Для получения максимального эффекта влагалищная пелоидотерапия должна сопровождаться дополнительным назначением метаболической терапии, про- и эубиотиков. Нерационально одновременное использование антиоксидантов в комплексе с местной магнитолазерной и пелоидотерапией.
При оценке эффективности получены следующие данные:
1. Без изменений - 9,09%.
2. Улучшение - 5,45%.
3. Значительное улучшение - 90,91%.
4. Ухудшение - 0%.
Эффективность лечения по непосредственным результатам составила 96,36% (в среднем). Приводим примеры на осуществление способа
Пример 1
Больная Б. (ИБ №70), 31 года, поступила на лечение в отделение репродуктологии ФГУ «ТНИИКиФ ФМБА России» 11 января 2010 года с диагнозом: «Хронический сальпингоофорит, стадия ремиссии. ВМС в полости матки (в течение 5 месяцев). Неспецифический вагинит». Жалобы при поступлении: на периодически возникающие боли тянущего характера в поясничной области, особенно перед началом менструации. Менструация с 14 лет, через 28-30 дней, по 5-6 дней, умеренные, болезненные. Дата последней менструации: 14 - 19.12.09 года. Половая жизнь с 17 лет. Замужем (брак 1 в течение 4,5 лет, в настоящее время брак 2 в течение 4 лет). Беременностей 6, родов 2, абортов 4.
Боли впервые появились в начале 2008 года, через несколько месяцев после аборта. При обращении в ЖК был поставлен диагноз: «Хронический сальпингоофорит». Была поставлена на диспансерный учет в ЖК. На протяжении 2 лет пациентка 1-2 раза в год получала противовоспалительную и рассасывающую терапию амбулаторно по месту жительства. Также, в 2008 году перенесла ДЭК по поводу эрозии шейки матки.
Из экстрагенитальных заболеваний имеет язвенную болезнь двенадцатиперстной кишки (ушивание язвенного дефекта в 2007 году) и остеохондроз шейного и поясничного отделов позвоночника. По поводу перечисленных заболеваний состоит на диспансерном учете по месту жительства.
При поступлении состояние удовлетворительное; кожные покровы и слизистые чистые, обычной окраски. В легких дыхание везикулярное, хрипов нет. Тоны сердца ясные, ритмичные; АД 110/70 мм рт. ст.; Ps 71 ударов в минуту. При пальпации живот мягкий, безболезненный. Симптомов раздражения брюшины нет. Симптом Пастернацкого отрицательный с обеих сторон.
При гинекологическом исследовании: наружные половые органы развиты правильно; рост волос - по женскому типу; промежность низкая; влагалище рожавшей; своды свободны. Шейка матки - усы ВМС, зев щелевидный, окраска обычная. Матка - в anteflexio - anteversio, не увеличена в размерах, незначительно ограничена в подвижности, плотная, гладкая, безболезненная. Придатки слева - не увеличены, уплотнены, незначительно болезненны при осмотре; справа - утолщены и несколько пастозны, незначительно болезненны при осмотре. Выделения - умеренные бели, слизисто - гнойного характера.
Мазок на степень чистоты влагалища: эпителиальные клетки в большом количестве; лейкоциты 40-60 в поле зрения, флора - кокко-бациллярная, обнаружен мицелий дрожжевого грибка рода Кандида; трихомонады и гонококки отсутствуют.
Мазок на цитологическое исследование: цитограмма без особенностей, но имеет воспалительный тип цитологического мазка.
Измерение pH влагалищной слизи = 5,5.
Мазок для гистохимической окраски на гликоген: индекс Каплоу = 2,35 у.е.
Исследование цервикальной слизи IL-1 = 339,50 нг/л; IL-1 RA = 3036,00 нг/л; s Ig A = 16,00 мг/л.
УЗИ ОМТ: матка в центре, кпереди, контуры ровные, структура, однородная. Размеры: 49×33×48 мм. М - эхо: 10 мм, эндометрий соответствует 2-й фазе м/ц. В полости матки - ВМК, занимает правильное положение. Правый яичник: 32×22×28 мм, не изменен. Левый яичник: 31×22×25 мм, не изменен. В заднем своде жидкость не определяется.
Общий анализ крови: Hb 127 г/л; эритроциты 3,9*1012/л; лейкоциты 5,0*109/л; формула: сегм. 62, пал. 2, лимф. 31, мок. 2, эоз. 3, СОЭ 7 мм/ч.
Общий анализ мочи: цвет светло - желтый; прозрачная; удельный вес 1012; белок - отр.; глюкоза - отр.; pH 6,0; лейкоциты 0-1 в поле зрения; клетки плоского эпителия единичные в поле зрения.
Биохимический анализ крови: общий белок 81,7 г/л; билирубин общий 9,2; билирубин прямой 0,7; глюкоза 4,3 моль/л: АСАТ 13,9; АЛАТ 9,5; креатинин 76.3.
Иммунологический анализ: В - лимфоциты 21%; Т - лимфоциты 38%, Т - хелперы 17%; Т - супрессоры 21%; Ig А 1,40 гул; Ig М 1,06 г/л; Ig G 8,63 г/л; ЦИК 75 у.е.
Индекс здоровья до лечения = 36,2
Лечение осуществляли согласно предлагаемому способу: пациентке в положении - лежа на спине, со слегка ссунутыми в коленных в тазобедренных суставах и разведенными в стороны нижними конечностями во влагалище вводили инициальную стерильную влагалищную насадку аппарата «МИЛТА-Ф-8-01». Процедуры проводили по следующим параметрам: мощность ИК-светодиодов 60 мВт, частота 1500 Гц, напряженность магнитного поля 30 мТл, в первый день продолжительность процедуры составляла 5 минут, затем по 10 минут. После введения оптической насадки женщину укрывали простыней. Затем женщина располагалась на гинекологическом кресле. Далее раскрывали влагалище с помощью двустворчатого зеркала пинцетом вводили иловую сульфидную грязь озера Малое Яровое, завернутую в стерильный бинт в виде тампона размером 5×3×3 см, температурой 24°С, на 60 минут. Нити тампона оставляли наружу. Во время процедуры пациентка принимала любое положение: она могла лежать, сидеть, активно двигаться. После окончания процедуры тампон путем потягивания за нити извлекался из влагалища. После удаления тампона остатки иловой сульфидной грязи удалялись спринцеванием минеральной воды «ОМЕГА». Процедуры проводили 1 раз в день, на курс - 10 процедур. Больная лечение перенесла хорошо. Физиобальнеореакции не наблюдалось в течение всего курса лечения.
При выписке из стационара: жалоб нет, состояние удовлетворительное.
При гинекологическом исследовании: наружные половые органы развиты правильно; рост волос по женскому типу; промежность низкая; влагалище рожавшей; своды свободны. Шейка матки - усы ВМС, зев щелевидный, окраска обычная. Матка в anteflexio, versio, не увеличена в размерах, стала более подвижной, плотная, гладкая, безболезненная. Придатки - не увеличены, пастозность отсутствует, стали менее плотными, безболезненны при осмотре. Выделения - скудное количество светлы