Способ лечения нейротрофических язв конечностей
Иллюстрации
Показать всеИзобретение относится к области медицины. Способ заключается в том, что на раневую поверхность однократно проводят трансплантацию аутологичных клеточных культур фибробластов пациента, обогащенных мультипотентными мезенхимальными стволовыми клетками (ММСК). Доля содержащихся в культуре ММСК составляет от 5 до 15%. Клетки наносят на рану капельным путем и фиксируют на месте тканевого дефекта с помощью фибриновой подложки под повязку, изготовленной из обогащенной тромбоцитами плазмы. Способ позволяет сократить сроки лечения, безопасен и высокоэффективен. 3 з.п. ф-лы, 2 ил., 1 табл., 1 пр.
Реферат
Изобретение относится к медицине, в частности к клеточным технологиям, и может быть использовано для лечения некротических тканевых дефектов, в частности, нейротрофических язв нижних конечностей при осложнениях сахарного диабета - (СД) II типа.
Известен способ лечения нейротрофических язв с помощью аллогенной трансплантации, при котором для наложения на язву используют криоконсервированные аллогеннные фибробласты человека, полученные из кожи крайней плоти новорожденных, выращенные на биосорбирующем сетчатом скафолде из полиглактина. Объявленная эффективность этой технологии 71% [Дермографт.55, 56, 57…Batool Kazmi, PhD; Christopher J. Inglefield, FRCS (Plast); Mark P. Lewis, PhD Autologus Cell Therapy: Current Therapy: Current Treatments and Future Prospects // Wounds. 2009 VOLUME: 21 PUBLICATION DATE: Sep 15 2009 pp 234-242].
Известен также способ лечения язв с помощью наложения (аппликации) двухслойного искусственного эквивалента кожи, состоящего из дермального (аллогенные фибробласты на коллагеновом гелевом матриксе) и эпидермального (кератиноциты, выращенные на предварительно сформированном дермальном слое) слоев, с объявленной эффективностью - 56%. [Batool Kazmi, PhD; Christopher J. Inglefield, FRCS (Plast); Mark P. Lewis, PhD Autologus Cell Therapy: Current Therapy: Current Treatments and Future Prospects // Wounds. 2009 VOLUME: 21 PUBLICATION DATE: Sep 15 2009 pp 234-242]/[Waymack P., Duff R.G., Sabolinski M. The effect of a tissue engineered bilayered living skin analog, over meshed split - thickness autografts on the healing of excised burn wounds. The Apligraf Burn Study Group. Burns. 2000; 26(7): 609-19. Kirsner R.S. The use of Apligraf in acute wounds. J. Dermatol. 1998; 25 (12): 805-11. Trent J.F., Krisner R.S. The engineered skin: Apligraf, a bi - layered living skin equivalent. J. Clin. Pract. 1998; 52 (6): 408-13].
Также известен способ лечения нейротрофических язв с помощью наложения аутологичных фибробластов, в котором для их культивирования используют трехмерную подложку из биосовместимого (поливинил и пр.) неорганического субстрата, а фибробласты предварительно трансферируются VEGF (фактор роста эндотелия сосудов), содержащим вектором. При этом биоконструкцию накладывают на поверхность язвы на 8 недель при ежедневной смене повязки [Naughton G.K., Mansbridge J.N., Pinney R.E., Zeltinger J. Methods for using a three - dimensional stromal tissue to promote angiogenesis. US 2003/0007954 Al. Jan. 9, 2003].
Задачей изобретения является ускорение и увеличение эффективности лечения длительно незаживающих нейротрофических язв конечностей при СД II типа с использованием аутопластики.
Задача решается тем, что при лечении длительно незаживающих нейротрофических язв конечностей при СД II типа для трансплантации используют культивированные аутогенные фибробласты. При этом однократно вносят на поверхность язвы капельным путем, выделенные и выращенные культуры фибробластов, обогащенные мультипотентными мезенхимальными стромальными клетками (ММСК), при этом доля ММСК в культуре достигает 5-15%, причем закрепление клеток на раневой поверхности производят с помощью накладывания фибриновой подложки из аутологичной обогащенной тромбоцитами плазмы из крови пациента и повязки для влажного заживления, которую меняют каждые три дня, а перед трансплантацией у пациента достигается состояние субкомпенсации по основному заболеванию до достижения показателей гликированного гемоглобина от 5,7 до 9,0% и наличия микробных тел на площади язвы не более 150 на квадратном сантиметре.
Новизной изобретения является то, что использование на всех этапах лечения аутологичных материалов с добавлением ММСК гарантирует отсутствие реакции отторжения и сокращает сроки лечения до 3-5 недель (в 3-2,5 раза) по сравнению с ближайшими аналогами и прототипом.
Достигаемый неочевидный лечебный эффект заключается в закрытии некротического кожного дефекта в течение более короткого срока по сравнению с описанными аналогами времени (3-5 недель) и более полного восполнения недостатка ткани в области самого дефекта, причем при использовании культуры обогащенных ММСК фибробластов наиболее полно восстанавливаются все слои дермы и подлежащие ткани, в частности подкожно-жировая клетчатка и фасции. Пролиферативный потенциал ММСК обеспечивает формирование нового микроциркулярного сосудистого русла.
Способ лечения осуществляется поэтапно следующим образом: сначала медикаментозными методами достигается состояние субкомпенсации по СД с помощью сахароснижающей терапии до достижения показателей гликированного гемоглобина от 5,7 до 9%. Параллельно проводится нейротропная, ангиотропная терапия, при необходимости проводится иммобилизация конечности при помощи разгрузочной повязки.
В процессе лечения независимо от стадии раневого процесса производят забор тканевого материала с ягодичной области или передней брюшной стенки (нижняя горизонтальная складка).
ММСК (мультипотентные мезенхимальные стромальные клетки) извлекают из подкожно-жировой клетчатки ферментативным способом и культивируют на питательной среде, ограничивающей дифференцировку. Параллельно культивируют в течение 30-38 дней фибробласты. За время культивирования клеток рана санируется с использованием антибиотиков, антимикотиков и санирующих разгрузочных повязок.
Культура фибробластов обогащается ММСК до 5-15% от общего объема и наносится капельным методом на раневую поверхность в виде смешанной культуры в количестве не менее 200 тыс. клеток на кв. см. Нанесенные клетки фиксируют на поверхности раны при помощи фибриновой подложки под повязку, полученной из обогащенной тромбоцитами плазмы, изготавливаемой из крови пациента непосредственно перед нанесением смешанной культуры клеток на рану. Наличие фибриновой подложки из крови пациента гарантирует задержку клеточных элементов в ране и обеспечение клеток факторами роста широкого спектра действия, содержащимися в тромбоцитах. Последние стимулируют пролиферативную активность клеток фибробластического дифферона и ММСК. За счет этого клетки смешанной аутологичной культуры быстрее восстанавливают тканевые дефекты, невзирая на недостаток трофического снабжения пострадавших участков кожи.
Основные показатели и ограничивающие параметры заявляемого способа, как: доля содержания ММСК во вносимой культуре от 5 до 15%; использование фибриновой подложки, изготовленной перед нанесением клеток из обогащенной тромбоцитами плазмы, полученной из крови пациента; количество клеток смешанной культуры, вносимой на поверхность язвы, не менее 200 тыс. на кв. см раны и требования к пациенту по состоянию субкомпенсации - определены и обоснованы практическим путем в результате многочисленных лабораторных опытов с учетом теоретической проработки аналогов, прототипов и опыта предыдущих исследований и клинических испытаний.
После детальной отработки в лабораторных условиях методик выращивания подготовка и культивирования фибробластов, клинические испытания предложенного способа были проведены в условиях областной клинической больницы №40 (г.Екатеринбург) у 10 пациентов с СД II типа тяжелой степени. Средний возраст пациентов составил 65,16 лет (от 50 до 79 лет). Стаж СД - 8,16 лет (2-25 лет). При обследовании у всех пациентов были выявлены осложнения СД - диабетическая микроангиопатия нижних конечностей и выраженная полинейропатия.
Отбор пациентов проводился при наличии добровольного информированного согласия, подписанного пациентами, на основании анамнестических данных, результатов врачебного осмотра, лабораторных исследований на предмет контаминации инфекционными агентами (ВИЧ, СМВ, гепатиты, мико- и токсоплазма (Axsym, Abbott laboratories).
Критерием включения в испытание являлось наличие язвенного дефекта площадью не менее 35x10 мм (на стопе) и 65x50 мм (на голени) в течение 6 и более месяцев и безуспешность проводимого ранее консервативного лечения.
Забор эксплантанта выполняли независимо от стадии раневого процесса под проводниковой анестезией. Эксплантацию кожи и подлежащей подкожно - жировой клетчатки производители с ягодичной области на 7-8 см ниже крыла подвздошной кости, эксплантант помещали в раствор PBS, содержащий двукратные концентрации культурных антибиотиков, хранили при температуре 4°С не более 12 часов.
Клетки культивировали при 37°С, концентрации СО2 5% и 95% влажности в среде ДМЕМ/Ham F-12 (Sigma) с добавлением 10% фетальной бычьей сыворотки (Ну Clone). Кроме культивирования клеток кожи из незначительного количества подкожно-жировой ткани (ЖТ) ферментативным способом извлекали мультипотентные мезенхимальные стромальные клетки (ММСК) с целью получения воспроизводимой клеточной линии. Ограниченный объем ЖТ обеспечил возможность получения трех таких линий: пациентов №2; 4 и 5. Принадлежность ММСК к стволовому пулу была подтверждена дифференцировкой клеток в фиброгенном, хондрогенном и остеогенном направлениях.
В период культивирования и наращивания клеточной массы (в среднем 37,6 суток) рану санировали с использованием стандартного перевязочного материала и атравматических повязок. В одном случае в клеточной культуре испытуемого была выявлена ДНК микоплазмы, в связи с чем данная культура была выбракована, а культивирование повторного изъятого эксплантанта осуществлялось с добавлением в среду 20-кратной (от культуральной) концентрации противопаразитарного антибиотика тилозина (Sigma), что привело к деконтаминации культуры к третьему пассажу.
Всем пациентам до трансплантации клеток проведена коррекция сахароснижающей терапии для достижения субкомпенсированного состояния по углеводному обмену. Показатели гликированного гемоглобина (HbAlc) колебались от 5,7 до 9,0% (в среднем 7,73%). Необходимым условием для трансплантации клеток являлось наличие «чистого» язвенного дефекта (количество микробных тел не более 150 на см2) и активных грануляций. Пациентам с локализацией язвы на стопе осуществлялась иммобилизация конечности с использованием разгрузочной повязки.
Для определения площади раневого дефекта использовали формулу вычисления площади круга: S=πR2. При неровности краев раны за радиус принимали среднее значение, получаемое путем сложения самого большого и самого малого радиусов дефекта с последующим делением полученного значения на два.
В рамках реализации программы безопасности перед клеточной терапией выполняли трехэтапный контроль полученных клеточных линий на вероятность наличия мутаций генов р53, k-ras, b-raf. Одновременно, среди клеток, собранных с культуральных поверхностей, определяли долю Stro-1 позитивных клеток (ММСК) иммунофлуоресцентным методом.
С целью обеспечения возможности повторного терапевтического применения полученных клеточных линий часть клеток криоконсервировали по стандартной методике.
При проведении испытаний было предпринято обогащение культур дермальных фибробластов линиями ММСК в аутогенном варианте. При этом доля Stro-1-позитивных клеток в культурах пациентов №№2; 4; 5 возросла десятикратно - до 0,6%. Трансплантация обогащенных культур в клинике ГКБ №40 производилась «слепым» методом с обязательным прохождением всех этапов предтрансплантационного контроля.
Для однократного нанесения на раневую поверхность использовали клеточную суспензию, содержащую не менее 8x106 живых клеток. Количество наносимых клеток варьировало в зависимости от величины язвенного дефекта.
Для фиксации клеток на поверхности язвы использовали аутологичную фибриновую подложку, обогащенную тромбоцитами, и специальную повязку, обеспечивающую «влажное» заживление раны. Изготовление аутологичной фибриновой подложки производилось непосредственно перед трансплантацией, практически у постели больного посредством центрифугирования крови пациента с последующим нагреванием сгустка до образования пленки.
Заживление язв отслеживали в динамике на протяжении 26 недель.
В таблице 1 представлены результаты наблюдений в клинике ГКБ №40 и динамика сокращения язвенных дефектов у пациентов.
| Таблица 1 | |||||||
| № пациента | До лечения, % | Итоги лечения - недели | |||||
| 1 нед. | 3 нед. | 5-6 нед. | 8-9 нед. | 11 нед. | 21 нед. | ||
| 1 | 0 | 54 | 73 | 90 | 100 | ||
| 2 (ММСК) | 0 | 75 | 89 | 98 | 100 | ||
| 3 | 0 | 10 | 80 | 100 | |||
| 4 (ММСК) | 0 | 50 | 100 | ||||
| 5 (ММСК) | 0 | 85 | 100 | ||||
| 6 | 0 | 4 | 40 | 75 | |||
| 7 | 0 | 36 | 77 | 98 | 100 | ||
| 8 | 0 | 46 | 69 | 98 | 100 | ||
| 9 | 0 | 60 | 96 | 100 | |||
| 10 | 0 | 35 | 58 | 80 | 100 |
Из таблицы 1 следует, что по прошествии первой недели после клеточной трансплантации сокращение язвенной поверхности более чем на 50% наблюдалось у половины пациентов (среднее арифметическое сокращения язвенного дефекта составило 45,5%). При этом у пациентов с трансплантацией культур, обогащенных ММСК, через семь дней зафиксировано уменьшение площади язвы на 75% (пациент №2), 50% (№4) и 85% (№5). К концу третьей недели у пациента №4 зафиксировано полное заживление язвы, а у восьми - сокращение язвенной поверхности более чем на 60%. Спустя шесть недель у испытуемого №5 была отмечена полная эпителизация раны, у №2 - закрытие площади язвы на 98%, а у остальных пациентов - от 58 до 80%. К концу второго месяца у пациента №2 наблюдалось полное заживление. К одиннадцатой неделе у 7 из 10 пациентов зафиксировано полное закрытие раневых дефектов, еще 2 находились на завершающем этапе заживления. Окончательная эпителизация у 9 пациентов была подтверждена к 21 неделе наблюдения. У одной пациентки на этом сроке наблюдалось 75% заживления. Полная эпителизация язвенного дефекта у данной испытуемой не была достигнута в связи с нарушением рекомендованной методики (использование для закрытия раневой поверхности сорбирующей марлевой повязки).
В одном случае через 6 дней после нанесения клеток у пациента отмечалось повышение температуры до фебрильных цифр. При проведении посевов раневого отделяемого выявлен рост Staphylococcus aureus, что потребовало назначения антибиотиков широкого спектра действия. Других осложнений у испытуемых не выявлено. Аллергических реакций за время исследования отмечено не было.
Средняя продолжительность лечения (с момента трансплантации аутофибробластов до эпителизации раны) при локализации язвы на стопе составила 9,5 недель, при локализации на голени - 19,3 недели. При этом средние сроки заживления при использовании обогащенных ММСК культур в аутогенном варианте составили 4,5±1,5 недели.
На фиг.1 и фиг.2 представлены фотоснимки этапов применения способа лечения нейротрофических язв конечностей у пациентов при клинических испытаниях в ОКБ №40 (г.Екатеринбург).
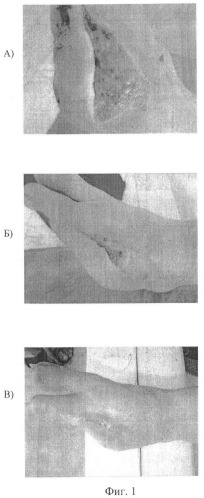
Фиг.1 - пациент №2, 50 лет. Сахарный диабет второго типа, выявленный в 1997 году, тяжелой степени, субкомпенсация.
СДС. Нейро-ишемический тип, (преобладание нейропатии) (ампутация).
Экзартикуляция третьего-пятого пальцев левой стопы (15.02.2008 г. по поводу гангрены). Трофическая язва правой стопы более 1 мес.
Взятие биоптата кожи 21.03.08. Культура обогащена ММСК.
24.04.08 выполнена имплантация смешанной культуры аутогенных фибропластов и ММСК на область дефекта кожи.
А - до лечения; Б - через неделю; В - через 3 недели.
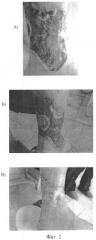
Фиг.2 - пациент №4, 69 лет. Сахарный диабет второго типа, впервые выявленный, тяжелой степени.
Трофическая язва правой голени с октября 2007 г., более 8 месяцев.
10.08.08 на нижней трети правой голени имеется язвенный дефект зведчатой формы 4,5 см ширина, 7.7 см ширина включая отрог, 7.5 см длина.
Выполнена трансплантация аутогенных фибропластов, обогащенных ММСК, на область язвенного дефекта.
А - до лечения; Б - через неделю; В - через 5 недель.
После эпителиализации язвы проводился ежемесячный контроль состояния рубца в течение 6 месяцев. Рецидивов заболевания за период наблюдения не отмечено.
Полученные результаты клинических испытаний по предложенному способу лечения нейротрофических язв у больных СД II типа тяжелой степени свидетельствуют о том, что обогащение ММСК культивируемых фибробластов и их применение в аутогенном варианте, по сравнению с использованием клеток фибробластического дифферона, сопровождается двукратным ускорением процесса заживления ран. Это подтверждает предположение об участии ММСК в оформлении дермального и эпителиального слоев кожи, а также сосудистого русла, предупреждающего повторное язвообразование.
Предложенный способ лечения, включающий однократное нанесение на поверхность язв при диабетической стопе культивированных дермальных фибробластов, обогащенных ММСК, в аутогенном варианте при закрытии фибриновой подложкой под повязку, сопровождается значительным усилением эпителиализации ран по сравнению с использованием необогащенных культур. Это позволяет предполагать ММСК-опосредованную активацию энграфмента транслантированных клеток и дифференцировки в области повреждения, их пролиферацию с ускоренным замещением зоны тканевой деструкции.
Проведенные клинические испытания предложенного способа по лечению язв нижних конечностей при СД II типа убедительно свидетельствуют о технической осуществимости способа и создании практической основы для разработки безопасной и эффективной технологии клеточной терапии нейротрофических язв, позволяющей значительно сократить сроки лечения при высокой ее результативности, расширяя возможности использования аутопластики клеточных культур при лечении нейротрофических язв конечностей.
1. Способ лечения нейротрофических язв конечностей, включающий подготовку пациента медикаментозными методами, нанесение на поверхность язвы клеточных культур, фиксацию клеточных культур на поверхности, закрытие повязкой и контроль хода лечения, отличающийся тем, что на раневую поверхность однократно проводят трансплантацию аутологичных клеточных культур фибробластов пациента, обогащенных мультипотентными мезенхимальными стволовыми клетками (ММСК), при этом доля содержащихся в культуре ММСК составляет от 5 до 15%, причем клетки наносят на рану капельным путем и фиксируют на месте тканевого дефекта с помощью фибриновой подложки под повязку, изготовленной из обогащенной тромбоцитами плазмы.
2. Способ лечения нейротрофических язв конечностей по п.1, отличающийся тем, что ММСК извлекают из подкожно-жировой клетчатки пациента ферментативным способом и культивируют на питательной среде, ограничивающей дифференцировку, при этом для нанесения на раневую поверхность используют смешанную культуру аутологичных фибробластов и аутологичных ММСК в количестве не менее 200 тыс. клеток на кв.см раны.
3. Способ лечения нейротрофических язв конечностей по пп.1 и 2, отличающийся тем, что обогащенную тромбоцитами плазму для изготовления фибриновой подложки получают из крови самого пациента, а раневой дефект с нанесенными на него клетками, фиксированными фибриновой подложкой, закрывают повязкой для влажного заживления, причем повязку меняют каждые три дня.
4. Способ лечения нейтротрофических язв конечностей по пп.1 и 2, отличающийся тем, что перед трансплантацией клеточных культур у пациента достигается состояние субкомпенсации по основному заболеванию до достижения показателей гликированного гемоглобина от 5,7 до 9,0% и наличия микробных тел на площади язв не более 150 на кв. см.