Материалы и способы лечения хронических фиброзных заболеваний
Иллюстрации
Показать всеГруппа изобретений относится к области фармацевтики. Способ включает уменьшение количества или активности CCL21 в фиброцитах и/или фибробластах, присутствующих в участке фиброзного повреждения при указанном фиброзном нарушении, где уменьшение количества или активности CCL21 предусматривает приведение данного млекопитающего в контакт со средством, уменьшающим количество или активность CCL21 в указанных фибробластах. Данное средство вводят в количестве, эффективном для облегчения одного или нескольких симптомов указанного хронического фиброзного нарушения. Группа изобретений позволяет снизить количество фиброзных повреждений и эффективно лечить симптомы фиброзных нарушений. 6 н. и 17 з.п. ф-лы, 16 ил., 5 пр.
Реферат
По настоящей заявке испрашивается приоритет предварительной заявки США номер 60/753647, поданной 23 декабря 2005 г, которая включена в настоящее описание в качестве ссылки в полном объеме.
Настоящее изобретение было сделано при поддержке правительства, грант № P50 HL-56402, выданный National Institutes of Health. Правительство имеет определенные права на настоящее изобретение.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к способам и композициям, эффективным для лечения хронических фиброзных нарушений. Более конкретно, настоящее изобретение относится к лечению хронических фиброзных нарушений путем иммунотерапевтического вмешательства.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Воспаление представляет собой координированный ответ на повреждение ткани или инфекцию. Воспаление начинается с высвобождения или локального высвобождения хемотаксических факторов, активации тромбоцитов и инициации путей коагуляции и комплемента. Эти события стимулируют локальный эндотелий, вызывая экстравазацию нейтрофилов и моноцитов. Вторая фаза воспаления характеризуется притоком в ткань клеток адаптивной иммунной системы, в том числе лимфоцитов. Последующая фаза разрешения, в которой происходит апоптоз избытка лимфоцитов и поглощение тканевыми макрофагами, также характеризуется восстановлением поврежденной ткани стромальными клетками, такими как фибробласты.
В процессе такого восстановления локальные покоящиеся фибробласты мигрируют в пораженный участок, продуцируют внеклеточные матриксные белки и активируют сокращение раны или фиброз. Также полагают, что циркулирующие клетки-предшественники фибробластов, фиброциты, которые присутствуют в крови, мигрируют к участкам повреждения или фиброза, где они дифференцируются и опосредуют восстановление ткани и другие фиброзные ответы. Фиброциты дифференцируются из популяции предшественников периферических моноцитов и экспрессируют маркеры как гематопоэтических клеток (CD45, MHC класса II, CD34), так и стромальных клеток (коллаген типа I и III и фибронектин). Зрелые фиброциты быстро проникают в участки повреждения ткани, где они секретируют воспалительные цитокины, а также белки внеклеточного матрикса, другие цитокины и проангиогенные молекулы, которые могут вызывать фиброз.
Дифференциация фиброцитов связана с рядом фиброзных заболеваний, включающих без ограничения склеродермию, келоидные рубцы, ревматоидный артрит, волчанку, нефрогенную фиброзную дермопатию и идиопатический фиброз легких. Они играют роль в образовании фиброзных повреждений после инфекции Schistosoma japonicum у мышей и участвуют в развитии фиброза, связанного с аутоиммунными заболеваниями. Фиброциты также участвуют в развитии патогенного фиброза, связанного с радиационным поражением, болезни Лима и фиброза легких, а также ремоделирования стромы в поджелудочной железе и стромального фиброза, тогда как отсутствие таких фиброцитов связано с опухолями поджелудочной железы и аденокарциномами. Фиброз также встречается у пациентов, страдающих от астмы и, возможно, других легочных заболеваний, таких как хроническое обструктивное заболевание легких, где фиброциты подвергаются дополнительной дифференциации в миофибробласты.
Конкретный ряд заболеваний, связанных с нерегулируемым фиброзным ответом, включает идиопатические интерстициальные пневмонии, которые относятся к другой группе хронических легочных заболеваний, характеризующихся различными уровнями фиброза легких. Основные факторы, участвующие в развитии доминантного легочного фиброзного ответа, связанного с рядом гистологически различных форм идиопатической интерстициальной пневмонии (IIP), до сих пор идентифицированы не полностью, что является одной из причин отсутствия эффективных клинических способов лечения указанных заболеваний (Green, Overview of pulmonary fibrosis. Chest 2002; 122(suppl. 6):334S-9S). Хотя многие из указанных заболеваний сопровождаются фибропролиферативным ответом в микросреде альвеол, приводящим к ухудшению дыхания, степень фиброзного изменения может сильно изменяться (Nicholason Am. J. Resp, Crit. Car Med. 2000:162:2213-7; Chapman J. Clin., Invest, 2004; 113:148-57). Также существуют противоречивые данные, указывающие на то, что противовоспалительные средства обеспечивают терапевтическое улучшение при менее тяжелых формах IIP, таких как неспецифическая интерстициальная пневмония (NSIP) и респираторное бронхолитическое/интерстициальное заболевание легких (RBILD), однако такие средства зачастую не способны предотвратить нарушение дыхания у пациентов с наиболее тяжелой и смертельной формой IIP - обычной интерстициальной пневмонией (UIP) (Flaherty et al., Am. J. Med., 110:278-282 (2001); Lynch et al., Curr. Opin. Pulm. Med., 7:298-308 (2001); Flaherty et al., Thorax, 58:143-148 (2003)).
Существование разных очагов фибробластов, или фибробластных очагов, является важным патологическим признаком, связанным с плохим прогнозом и смертельным исходом при идиопатической интерстициальной пневмонии (King et al., Am. J. Respir. Crit. Care Med., 164:1025-1032 (2001)). Новейшие способы лечения могут быть разработаны только после выяснения общих и отдельных событий, вносящих вклад в фиброзные изменения легких в процессе возникновения и развития IIP (van den Blink et al., Arch. Immunol. Ther. Exp. (Warsz), 48:539-545 (2000)). Хорошо известно, что рецептор 7 хемокина CC (CCR7; который связывает MIP-3b/CCL19 и 6-Ckine/CCL21 (Nagira et al., J. Biol. Chem., 272:19518-19524 (1997)) и рецептор 4 хемокина CX (CXCR4; который связывает SDF-1/CXCL12 (Forster et al., J. Immunol., 160:1522-1531 (1998)) относятся к рецепторам хемокинов, экспрессия которых ограничена клетками гематопоэтического происхождения (Kim et al., J. Leukoc. Biol., 66:455-461 (1999); Kim et al., J. Clin. Invest., 108:1331-1339 (2001)). В процессе иммунных ответов экспрессия CCR7 участвует в перемещении зрелых дендритных клеток (Sallusto et al., Eur. J. Immunol., 29:1617-1625 (1999)) к лимфоидным тканям, регулирует локализацию Т-хелперных клеток типов 1 и 2 в селезенке (Randolph et al., Science, 286:2159-2162 (1999)) и направляет Т-хелперные клетки типа 2 к аллергическому легкому (Hammad et al., J. Immunol., 169:1524-1534 (2002)). Экспрессия и действие CXCR4, как правило, ограничены иммунными клетками костно-мозгового происхождения (Ward et al., Biochem. J., 333:457-470 (1998); Gonzalo et al., J. Immunol., 165:499-508 (2000)). Полученные в последнее время данные, свидетельствующие о том, что экспрессия CCR7 и CXCR4 клетками опухоли молочной железы способствует метастазированию указанных клеток в легкие, позволяют изменить иммуноцентрическую модель (Muller et al., Nature, 410:50-56 (2001)). Клетки молочной железы не экспрессируют указанные рецепторы хемокинов или не отвечают на лиганды, которые связываются с ними (Muller et al., Nature, 410:50-56 (2001)). Данное наблюдение распространяется на некоторые типы метастазирующих опухолей, включая меланому (Murakami et al., J. Dermatol. Sci., 36:71-78 (2004)) и разные формы лейкемий (Tavor et al., Cancer Res., 64:2817-2824 (2004); Ghobrial et al., Mayo Clin. Proc, 79:318-325 (2004)).
Хронический фиброз легких возникает в результате рубцевания легких, которое может быть вызвано многими состояниями, включающими хронические воспалительные процессы (саркоидоз, грануломатоз Вегенера), инфекции, воздействие агентов окружающей среды (асбест, оксид кремния, воздействие некоторых газов), воздействие ионизирующей радиации (например, лучевой терапии, используемой для лечения опухолей молочной железы), хронические состояния (волчанка, ревматоидный артрит), а также воздействие некоторых лекарственных средств. При состоянии, известном как гиперчувствительный пневмонит, фиброз легких может развиваться вследствие усиления иммунной реакции на вдыхаемую органическую пыль или производственные химикаты. Данное состояние чаще всего возникает после вдыхания пыли, содержащей бактерии, грибки или животные продукты. Больной, страдающий некоторыми типами фиброза легких, такими как неспецифический интерстициальный пневмонит (NSIP), может отвечать на иммуносупрессивную терапию. Если, как это часто бывает, хроническое воспаление легких и фиброз развиваются без идентифицированной причины, больной, страдающий этим заболеванием, часто не отвечает на терапевтическое лечение. В особенности это справедливо для больных, страдающих идиопатическим фиброзом легких (IPF). Существует немного вариантов лечения идиопатического фиброза легких. Данные, свидетельствующие о том, что какие-либо лекарственные средства могут облегчать данное состояние, отсутствуют, поскольку после возникновения рубцевание присутствует постоянно. Трансплантация легкого является единственным доступным вариантом лечения. Постоянно проводятся научно-исследовательские работы с использованием разных лекарственных средств, которые могут уменьшать фиброзное рубцевание. Поскольку некоторые типы фиброза легких могут отвечать на кортикостероиды (такие как преднизон) и/или другие лекарственные средства, которые подавляют иммунную систему организма, эти лекарственные средства иногда прописывают для уменьшения процесса, приводящего к фиброзу. Тем не менее, хорошо известно, что в настоящее время не существует способов лечения фиброзных заболеваний. В стандартной клинической практике пациентам назначают преднизон и азатиоприн, однако не существует данных, свидетельствующих о том, что эти препараты обеспечивают терапевтическое улучшение. На самом деле побочные эффекты этих лекарственных средств могут вносить вклад в смертность пациентов с UIP.
Хотя хемокины могут участвовать в образовании фибробластных очагов и усилении фиброзного ответа при фиброзе легких, конкретная роль среды профиброзных медиаторов, присутствующих при хроническом фиброзе легких, остается неясной. Настоящее изобретение идентифицирует роль конкретных хемокинов и их рецепторов и предлагает новые методы и композиции, которые можно использовать для лечения, главным образом, идиопатических нарушений, устойчивых к терапевтическим способам лечения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам и композициям, эффективным для лечения фиброзных заболеваний. Более конкретно, настоящее изобретение демонстрирует, что ингибирование или другое уменьшение активности CCL21, одного или в сочетании с CCL19, эффективно уменьшает количество фиброзных повреждений и улучшает симптомы фиброзных нарушений.
Таким образом, конкретные варианты осуществления настоящего изобретения относятся к способам лечения у млекопитающего хронического фиброзного нарушения, включающим уменьшение количества или активности CCL21 в фиброцитах и/или фибробластах, присутствующих в участке фиброзного повреждения при указанном фиброзном нарушении. В некоторых вариантах осуществления способ может дополнительно включать уменьшение количества или активности CCL19 в фибробластах, связанных с указанным фиброзным нарушением. Например, уменьшения количества или активности CCL21 можно достичь путем приведения в контакт указанного млекопитающего со средством, которое удаляет CCL21 из указанных фибробластов, в количестве, эффективном для облегчения одного или нескольких симптомов указанного хронического фиброзного нарушения. Примером такого средства может быть антитело, способное к специфическому иммунному взаимодействию с CCL21, например такое антитело, которое лучше распознает эпитопы на CCL21, чем на других хемокинах.
В других вариантах осуществления уменьшения количества или активности CCL21 достигают путем приведения в контакт указанного млекопитающего со средством, которое уменьшает экспрессию CCL21 в указанных фибробластах, в количестве, эффективном для облегчения одного или нескольких симптомов указанного хронического фиброзного заболевания. Примером средства, используемого в таких вариантах осуществления, может служить молекула миРНК, направленная против CCL21.
С помощью способа по настоящему изобретению можно лечить фиброзное заболевание, выбранное без ограничения из группы заболеваний, включающих фиброз легких, хроническое обструктивное заболевание легких, фиброз печени, ревматоидный артрит, застойную сердечную недостаточность, хроническое заболевание почек, пневмонит с гиперчувствительностью, респираторный бронхолит/интерстициальное заболевание легких, инфекцию, вызванную шистосомой Мансона, первичную легочную гипертензию, вызваную плексиформными повреждениями, легочные проявления заболеваний, связанных с вирусом герпеса, дерматологические проявления заболеваний, связанных с вирусом герпеса, келоидные рубцы, волчанку, нефрогенную фиброзную дермопатию, фиброзные повреждения, связанные с инфекцией Schistosoma japonicum, аутоиммунные заболевания, патогенный фиброз, болезнь Лайма, реструктурирование стромы при панкреатите и стромальном фиброзе, фиброму матки, фиброз яичников, фиброз роговицы, застойную сердечную недостаточность и другие постишемические состояния, рубцевание после хирургической операции в брюшной полости, рубцевание после трабекулотомии при открытоугольной глаукоме, а также любые сочетания перечисленных заболеваний.
Характерная легочная гипертензия, лечение которой способом по настоящему изобретению может быть эффективно, включает первичную легочную гипертензию (РРН); вторичную легочную гипертензию (SPH); семейную РРН; спорадическую РРН; прекапиллярную легочную гипертензию; легочную артериальную гипертензию (РАН); гипертензию легочной артерии; идиопатическую легочную гипертензию; тромботическую легочную артериопатию (ТРА); плексогенную легочную артериопатию; функциональные классы I-IV легочной гипертензии; и легочную гипертензию, ассоциированную или связанную с дисфункцией левого желудочка, или вторичную по отношению к дисфункции левого желудочка, митральный порок сердца, констриктивный перикардит, аортальный стеноз, кардиомиопатию, фиброз средостения, неправильный дренаж легочной вены, окклюзионное заболевание легочной вены, коллагеновую болезнь сосудов, врожденный порок сердца, инфекцию ВИЧ, воздействие лекарственных средств и токсинов, таких как фенфлюрамины, врожденную болезнь сердца, легочную венозную гипертензию, хроническое обструктивное заболевание легких, интерстициальное заболевание легких, нарушение дыхания во сне, альвеолярную гиповентиляцию, хроническое воздействие большой высоты, неонатальное заболевание легких, альвеолярно-капиллярную дисплазию, серповидно-клеточное заболевание, другое нарушение коагуляции, хроническую тромбоэмболию, заболевание соединительной ткани, волчанку, шистосомоз, саркоидоз или легочный капиллярный гемангиоматоз.
Способ по настоящему изобретению, предпочтительно, можно использовать для лечения легочной гипертензии, связанной с нарушениями респираторной системы и/или гипоксимией, такими как хроническое обструктивное заболевание легких, интерстициальное заболевание легких, нарушение дыхания во сне, альвеолярная гиповентиляция, хроническое воздействие большой высоты, неонатальное заболевание легких, альвеолярно-капиллярная дисплазия, в особенности для лечения хронического обструктивного заболевания легких. В предпочтительных вариантах осуществления фиброзное нарушение представляет собой хронический фиброз легких.
В способах лечения соединение можно вводить местно в участок фиброзного повреждения. В более конкретных вариантах осуществления фиброзное поражение находится в легком, а композиция местно контактирует с указанным поражением. Предполагается, что в некоторых вариантах осуществления средство содержит фрагмент, обеспечивающий специфическую доставку указанного средства к участку фиброзного повреждения.
В конкретных вариантах осуществления антитело или композицию против CCL21 или CCL19 вводят способом, выбранным из группы, включающей местное введение, инъекцию, ингаляцию, непрерывное высвобождение посредством депо или насоса, или с помощью любого сочетания перечисленных способов.
Другой аспект настоящего изобретения относится к способу ингибирования пролиферации фибробластов и/или фиброцитов, включающему приведение в контакт указанных фибробластов и/или фиброцитов с композицией, которая содержит антитело против CCL21 или молекулу миРНК, направленную против CCL21. В некоторых вариантах осуществления способ дополнительно включает приведение в контакт указанного фибробласта с композицией, которая содержит антитело против CCL19 или молекулу миРНК, направленную против CCL19. В других вариантах осуществления способ дополнительно включает приведение в контакт указанного фибробласта с композицией, которая содержит антитело против CCR7 или молекулу миРНК, направленную против рецептора CCR7. Фиброциты и/или фибробласты можно обрабатывать in vitro или in vivo. Предпочтительно их обрабатывают in vivo. Более предпочтительно, обрабатываемые in vivo фибробласты находятся в легочной ткани.
Настоящее изобретение также относится к способам ингибирования миграции фиброцитов и/или активации фибробластов, включающим приведение в контакт указанных фиброцитов и/или фибробластов с композицией, ингибирующей активность CCL21. Эти способы позволяют ингибировать in vivo миграцию фиброцитов к легочной ткани млекопитающего и, как следствие, предотвращать избыточную продукцию внеклеточного матрикса. В данных способах фибробласты предпочтительно представляют собой резидентные легочные фибробласты, расположенные в легочной ткани млекопитающего, а указанные способы позволяют ингибировать активацию фибробластов в легочной ткани указанного млекопитающего, предотвращая таким образом избыточную продукцию внеклеточного матрикса.
В настоящем документе также описывается способ лечения фиброза легких, включающий ингибирование миграции фиброцитов и/или активации резидентных легочных фибробластов, расположенных в легочной ткани млекопитающего, страдающего от фиброзного заболевания легких, путем ингибирования активности или экспрессии CCL21 в указанных фиброцитах и/или фибробластах, и таким образом предотвращая избыточную продукцию внеклеточного матрикса и улучшение симптомов фиброза легких.
Изобретение также относится к способам лечения, ингибирования развития, улучшения одного или нескольких симптомов, обратного развития состояния или иным образом достижения терапевтического эффекта при индуцированном облучением легочном ламините и/или индуцированном облучением фиброзе легких у больного, такие способы включают введение указанному больному средства, уменьшающего количество или активность CCL21 в фиброцитах и/или фибробластах легочной ткани указанного больного, где упомянутое средство вводят до, во время или после лучевой терапии. Такой терапевтический способ может дополнительно включать введение средства, уменьшающего количество или активность CCL19 в легочной ткани указанного больного.
Другой аспект настоящего изобретения относится к способам лечения, ингибирования развития, улучшения одного или нескольких симптомов, обратного развития состояния или иным образом достижения терапевтического эффекта при индуцированном лекарственным средством фиброзе легких у больного, такие способы включают введение указанному больному средства, уменьшающего количество или активность CCL21 в фиброцитах и/или фибробластах легочной ткани указанного больного, где упомянутое средство вводят до, во время или после введения лекарственного средства. Опять же, в таком способе иногда желательно дополнительно вводить средство, уменьшающее количество или активность CCL19 в легочной ткани указанного больного. Существует множество средств, вызывающих фиброз, они включают без ограничения цитотоксические средства, антибиотики, противоаритмические средства, противовоспалительные средства и запрещенные наркотики. Примеры средств, вызывающих фиброз легких, включают без ограничения амфотерицин B, блеомицин, бромокриптин, бусульфан, карбамазепин, хлорамбуцил, кокаин, циклофосфамид, дифенилгидантоин, эрготамин, флекаинид, героин, мелфалан, метадон, метотрексат, метилфенидат, метилсергид, минеральное масло, нитрофурантоин, нитрозомочевины, прокарбазин, силикон, сульфазалазина токаинид, а также средства, принадлежащие к классу алкалоидов барвинка. В описанных в настоящем документе способах лечения иногда желательно использовать в качестве дополнительной терапии режим, в котором терапевтическое средство, воздействующее на CCL21 и/или CCL19, сочетают с кортикостероидным и/или иммуносупрессивным средством. В других способах комбинированная терапия может включать введение антикоагулянтов, диуретиков, сердечных гликозидов, блокаторов кальциевых каналов, сосудорасширяющих средств, аналогов простациклина, антагонистов эндотелина, ингибиторов фосфодиэстеразы, агонистов бета-2, антимускариновых средств, ингибиторов эндопептидазы, средств, снижающих уровень липидов, ингибиторов тромбоксана или их сочетаний.
Кроме того, настоящее изобретение дополнительно относится к применению средства, уменьшающего количество или активность CCL21 и/или CCL19 в фиброцитах и/или фибробластах, присутствующих в участке фиброзного повреждения, для получения лекарственного средства против хронического фиброзного нарушения.
В иллюстративных вариантах осуществления настоящее изобретение относится к применению средства, уменьшающего количество или активность CCL21, и, необязательно, средства, уменьшающего количество или активность CCL19 в фиброцитах и/или фибробластах, присутствующих в участке фиброзного повреждения, для получения лекарственного средства против хронического фиброзного нарушения у млекопитающего. В некоторых вариантах осуществления средство представляет собой антитело, способное к специфическому иммунному взаимодействию с CCL21, предпочтительно такое антитело, которое лучше распознает эпитопы на CCL21, чем на других хемокинах. В других вариантах осуществления средство представляет собой молекулу миРНК, направленную против CCL21. Промышленным способом получают лекарственное средство для лечения фиброзного заболевания, выбранного из группы, включающей фиброз легких, хроническое обструктивное заболевание легких, фиброз печени, ревматоидный артрит, застойную сердечную недостаточность, хроническое заболевание почек, пневмонит с гиперчувствительностью, респираторный бронхолит/интерстициальное заболевание легких, инфекцию, вызванную шистосомой Мансона, первичную легочную гипертензию, вызваную плексиформными повреждениями, легочные проявления заболеваний, связанных с вирусом герпеса, дерматологические проявления заболеваний, связанных с вирусом герпеса, келоидные рубцы, волчанку, нефрогенную фиброзную дермопатию, фиброзные повреждения, связанные с инфекцией Schistosoma japonicum, аутоиммунные заболевания, патогенный фиброз, болезнь Лайма, реструктурирование стромы при панкреатите и стромальном фиброзе, фиброму матки, фиброз яичников, фиброз роговицы, застойную сердечную недостаточность и другие постишемические состояния, рубцевание после хирургической операции в брюшной полости, рубцевание после трабекулотомии при открытоугольной глаукоме, а также любые сочетания перечисленных заболеваний. Предпочтительно фиброзное заболевание представляет собой хронический фиброз легких.
Предпочтительно на основе лекарственных средств получают композиции, подходящие для таких способов введения, как местное введение, инъекция, ингаляция, непрерывное высвобождение посредством депо или насоса, или любое сочетание перечисленных способов. Также предлагается применение композиции, содержащей антитело против CCL21 или молекулу миРНК, направленную против CCL21, и необязательно антитело против CCL19 или молекулу миРНК, направленную против CCL19, для получения лекарственного средства, ингибирующего пролиферацию фибробластов и/или фиброцитов. Применение может дополнительно включать применение композиции, содержащей антитело против CCR7 или молекулу миРНК, направленную против рецептора CCR7, в промышленном получении лекарственного средства, ингибирующего пролиферацию фибробластов и/или фиброцитов.
В другом аспекте настоящее изобретение относится к применению композиции, ингибирующей активность CCL21, в промышленном получении лекарственного средства, ингибирующего миграцию фиброцитов и/или активацию фибробластов. Также предлагается применение композиции, ингибирующей активность или экспрессию CCL21 в фиброцитах и/или активацию резидентных легочных фибробластов, в промышленном получении лекарственного средства для лечения фиброза легких путем предотвращения избыточной продукции внеклеточного матрикса и улучшения симптомов фиброза легких.
Кроме того, настоящее изобретение относится к применению средства, уменьшающего количество или активность CCL21, и, необязательно, средства, уменьшающего количество или активность CCL19 в фиброцитах и/или фибробластах легочной ткани, для промышленного получения лекарственного средства для лечения индуцированного облучением легочного ламинита и/или индуцированного облучением фиброза легких.
Также предлагается применение средства, уменьшающего количество или активность CCL21, и, необязательно, средства, уменьшающего количество или активность CCL19 в фиброцитах и/или фибробластах легочной ткани, для промышленного получения лекарственного средства для лечения индуцированного лекарственным средством фиброза легких. В таком применении промышленным способом получают лекарственное средство для лечения неидиопатического фиброза легких, индуцированного лекарственным средством, выбранным из группы, включающей цитотоксические средства, антибиотики, противоаритмические средства, противовоспалительные средства и запрещенные наркотики, например, лекарственное средство может быть выбрано из группы, включающей амфотерицин B, блеомицин, бромокриптин, бусульфан, карбамазепин, хлорамбуцил, кокаин, циклофосфамид, дифенилгидантоин, эрготамин, флекаинид, героин, мелфалан, метадон, метотрексат, метилфенидат, метилсергид, минеральное масло, нитрофурантоин, нитрозомочевины, прокарбазин, силикон, сульфазалазина токаинид, а также средства, принадлежащие к классу алкалоидов барвинка. В некоторых вариантах осуществления для получения лекарственного средства предлагается комбинированное применение средств, где лекарственное средство на основе CCL19 или CCL21 объединяют с кортикостероидом, иммуносупрессивным средством, антикоагулянтом, диуретиком, сердечным гликозидом, блокатором кальциевых каналов, сосудорасширяющим средством, аналогом простациклина, антагонистом эндотелина, ингибитором фосфодиэстеразы, агонистом бета-2, антимускариновым средством, ингибитором эндопептидазы, средством, снижающим уровень липидов, ингибиторами тромбоксана или их сочетаниями.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
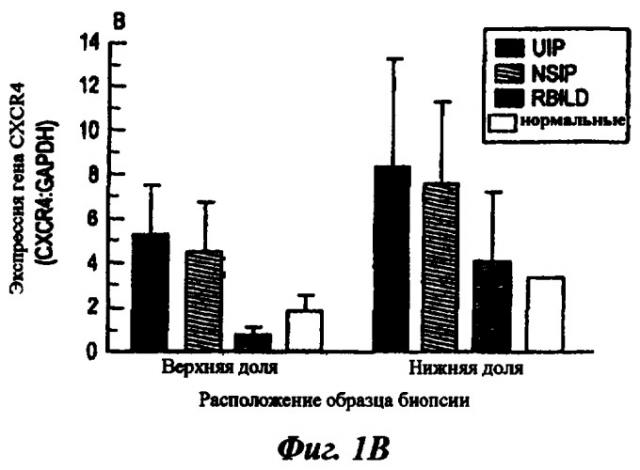
Фиг.1: Анализ с использованием макробиочипа SuperArray экспрессии генов (A) CCR7 и (B) CXCR4 в образцах биопсии, полученных хирургическим путем из верхней и нижней долей легких в группах пациентов с UIP (n=7), NSIP (n=6), RBILD (n=6) и обычной опухолью краевой зоны (n=5). Данные приведены в виде средних значений (SEM). Существенные различия отсутствуют. CCR7, рецептор 7 хемокина CC; CXCR4, рецептор 4 хемокина CX; GAPDH, глицеральдегид 3-фосфат дегидрогеназа; NSIP, неспецифическая интерстициальная пневмония; RBILD, респираторное бронхолитическое/интерстициальное заболевание легких; UIP, обычная интерстициальная пневмония.
Фиг.2: Анализ с использованием макробиочипа SuperArray экспрессии генов (A) CCL19, (B) CCL21 и (C) CXCL12 в образцах биопсии, полученных хирургическим путем из верхней и нижней долей легких в группах пациентов с UIP (n=7), NSIP (n=6), RBILD (n=6) и обычной опухолью краевой зоны (n=5). Данные приведены в виде средних значений (SEM). Существенные различия отсутствуют. CCL, лиганд рецептора хемокина CC; CXCL, лиганд рецептора хемокина CX; GAPDH, глицеральдегид 3-фосфат дегидрогеназа; NSIP, неспецифическая интерстициальная пневмония; RBILD, респираторное бронхолитическое/интерстициальное заболевание легких; UIP, обычная интерстициальная пневмония.
Фиг.3: Количественный анализ методом полимеразной цепной реакции Taqman экспрессии генов CCR7 и CCL21 в образцах биопсии, полученных хирургическим путем из верхней и нижней долей легких пациентов с UIP (n=18), NSIP (n=8), RBILD (n=6) и с обычной опухолью краевой зоны (n=6). Данные приведены в виде средних значений (SEM). **p (0,01 по сравнению с соответствующей долей пациента из группы с обычной опухолью краевой зоны). CCR7, рецептор 7 хемокина CC; CCL21, лиганд рецептора 4 хемокина CC; NSIP, неспецифическая интерстициальная пневмония; RBILD, респираторное бронхолитическое/интерстициальное заболевание легких; UIP, обычная интерстициальная пневмония.
Фиг. 4: Иммуноферментный твердофазный анализ CCL19, CCL21 и CXCL12 в образцах биопсии из верхней и нижней долей легких пациентов с UIP (n=18), NSLP (n=6), RBILD (n=6) и обычной опухолью краевой зоны (n=5). Данные приведены в виде средних значений (SEM). CCL, лиганд рецептора хемокина CC; CXCL, лиганд рецептора хемокина CX; NSIP, неспецифическая интерстициальная пневмония; RBILD, респираторное бронхолитическое/интерстициальное заболевание легких; UIP, обычная интерстициальная пневмония.
Фиг.5: Характерный иммуногистохимический анализ CCR7 в SLB групп пациентов с (A, B) UIP, (C, D) NSIP, (E, F) RBILD и (G, H) обычной опухолью краевой зоны. В секторах (A), (C), (E) и (G) показано контрольное окрашивание. Иммунореактивность CCR7 (красное окрашивание) наблюдается в фокальных участках SLB групп с (B) UIP, (D) NSIP и (F) RBILD, но не (H) с обычной опухолью краевой зоны. Исходное увеличение 6200. CCR7, рецептор 7 хемокина CC; NSIP, неспецифическая интерстициальная пневмония; RBILD, респираторное бронхолитическое/интерстициальное заболевание легких; SLB, хирургическая биопсия легкого; UIP, обычная интерстициальная пневмония.
Фиг.6: Характерный иммуногистохимический анализ CXCR4 в SLB групп пациентов с (A, B) UIP, (C, D) NSIP, (E, F) RBILD и (G, H) и обычной опухолью краевой зоны. В секторах (A), (C), (E) и (G) показано контрольное окрашивание. Иммунореактивность CXCR4 (красное окрашивание) наблюдается в мононуклеарных клетках, присутствующих в SLB пациентов с IIP и обычной опухолью краевой зоны. Исходное увеличение 6200. CXCR4, рецептор 4 хемокина CX; NSIP, неспецифическая интерстициальная пневмония; RBILD, респираторное бронхолитическое/интерстициальное заболевание легких; SLB, хирургическая биопсия легкого; UIP, обычная интерстициальная пневмония.
Фиг.7: Характерный иммуногистохимический анализ (B, E) CCR7 и (C,F) CD45 в серийных гистологических срезах в группах пациентов с (A-C) UIP и (D-F) NSIP. В секторах (A) и (D) показано контрольное окрашивание. В SLB пациентов с UIP иммунореактивность CCR7 (красное окрашивание в секторе B) частично перекрывается с иммунореактивностью CD45 (C), причем большая часть двойного окрашивания связана с мононуклеарными клетками (C). (A, F) В серийных гистологических срезах SLB NSIP не обнаруживается совместная локализация CCR7 и CD45. Исходное увеличение 6200. CCR7, рецептор 7 хемокина CC; NSIP, неспецифическая интерстициальная пневмония; SLB, хирургическая биопсия легкого; UIP, обычная интерстициальная пневмония.
Фиг.8: Характерный иммуногистохимический анализ CD34 в SLB групп пациентов с (A, B) UIP, (C, D) NSIP, (E, F) RBILD и (G, H) обычной опухолью краевой зоны. В секторах (A), (C), (E) и (G) показано контрольное окрашивание. Иммунореактивность CD34 (красное окрашивание) наблюдается в интерстициальных участках SLB всех пациентов. (D) Самая высокая экспрессия CD34 наблюдается в SLB пациентов группы NSIP. Исходное увеличение 6200. NSIP, неспецифическая интерстициальная пневмония; RBILD, респираторное бронхолитическое/интерстициальное заболевание легких; SLB, хирургическая биопсия легкого; UIP, обычная интерстициальная пневмония.
Фиг.9: Характерный иммуногистохимический анализ коллагена 1 в SLB групп пациентов с (A, B) ULP, (C, D) NSIP, (E, F) RBILD и (G, H) обычной опухолью краевой зоны. В секторах (A), (C), (E) и (G) показано контрольное окрашивание. Иммунореактивность коллагена (красное окрашивание) наблюдается в SLB пациентов с (B) UIP, (D) NSIP, (F) RBILD и (H) обычной опухолью краевой зоны. Исходное увеличение 6200. NSIP, неспецифическая интерстициальная пневмония; RBILD, респираторное бронхолитическое/интерстициальное заболевание легких; SLB, хирургическая биопсия легкого; UIP, обычная интерстициальная пневмония.
Фиг.10: Характерный иммуногистохимический анализ (B, E) коллагена 1 и (C, F) CCR7 в SLB групп пациентов с (A-C) UIP и (D-F) RBILD. В секторах (A) и (D) показано контрольное окрашивание. Иммунореактивность коллагена 1 (красное окрашивание) наблюдается в группах пациентов с (B) UIP и (E) RBILD. Однако в серийных гистологических срезах, участки которых являются иммунореактивными по отношению к коллагену 1, экспрессия CCR7 отсутствует (C, UIP; F, RBILD). Исходное увеличение 6200. CCR7, рецептор 7 хемокина CC; RBILD, респираторное бронхолитическое/интерстициальное заболевание легких; SLB, хирургическая биопсия легкого; UIP, обычная интерстициальная пневмония.
Фиг.11: Характерный иммуногистохимический анализ гладкомышечного актина (aSMA) в SLB групп пациентов с (A-C) UIP, (D-F) NSIP и (G-I) RBILD. В секторах (A), (D) и (G) показано контрольное окрашивание. Иммунореактивность CCR7 (красное окрашивание) наблюдается в фокальных участках SLB из групп пациентов с (B) UEP, (E) NSIP и (H) RBILD. Экспрессия aSMA (красное окрашивание) также наблюдается в серийных гистологических срезах тканей групп пациентов с (C) UIP, (F) NSIP и (I) RBILD. Однако перекрывание экспрессии CCR7 и aSMA не наблюдается. Исходное увеличение 6200. CCR7, рецептор 7 хемокина CC; NSIP, неспецифическая интерстициальная пневмония; RBILD, респираторное бронхолитическое/интерстициальное заболевание легких; SLB, хирургическая биопсия легкого; aSMA, гладкомышечный актин; UIP, обычная интерстициальная пневмония.
Фиг.12: Экспрессия транскрипта CCL21 в полученных хирургическим путем образцах биопсии легких пациентов с разными формами хронического фиброза легких по сравнению с пациентами, имеющими нефиброзные заболевания других типов. Экспрессия гена CCL21 (определяемая методом TAQMAN ПЦР) варьирует среди разных групп пациентов. Максимальная экспрессия CCL21 наблюдается в SLB при верхней и нижней обычной интерстициальной пневмонии (UIP), однако различие между SLB UIP и других групп наиболее четко выражено в нижних SLB. Вместе полученные данные позволяют предположить, что экспрессия CCR7 и CCL21 значительно увеличивается в процессе UIP. NSIP = неспецифическая интерстициальная пневмония; RBILD = респираторное бронхолитическое/интерстициальное заболевание легких.
Фиг.13: Экспрессия белка CCL21 в полученных хирургическим путем образцах биопсии легких пациентов с разными формами хронического фиброза легких по сравнению с пациентами, имеющими нефиброзные заболевания других типов. В данном описании приведены результаты анализа IIP и отличных от IIP образцов биопсии методом ELISA. В образцах биопсии верхней доли групп с UIP, NSIP и отличным от IIP заболеванием наблюдаются одинаковые уровни белка CCL21. Однако в образцах нижней доли (где фиброз легких является более агрессивным у пациентов с IIP) уровни CCL21 выше в группах IIP (т.е. в группах UIP, NSIP и RBILD по сравнению с группой, имеющей отличное от IIP заболевание).
Фиг.14: Миграция фибробластов UIP, но не отличных от IIP фибробластов, значительно увеличивается в присутствии CCL21. Данные эксперименты проводят путем добавления фибробластов человека в культуральный планшет с пористой системой transwell и подсчета фибробластов, мигрирующих при инкубации в течение 24 ч. Фибробласты UIP мигрируют через transwell ко дну лунки, причем миграция происходит гораздо интенсивнее, если на дно лунки добавлен CCL21, или фибробласты обработаны TNF, а на дно лунки добавлен CCL21. Присутствие антитела против CCL21 значительно снижает миграцию фибробластов в последних двух группах, но не влияет на фибробласты первой группы.
Фиг.15: В настоящем описании показаны результаты анализа влияния экзогенных CCL19 и CCL21 (концентрация обоих составляет 10 нг/мл) на пролиферативные ответы линий первичных фибробластов, выращенных из SLB нормальной ткани, гиперчувствительного пневмонита, саркоида и UIP. Обнаружено, что фибробласты UIP пролиферируют в ответ на присутствие лигандов CCL19 и CCL21.
Фиг.16: Поскольку обнаружено, что введение фибробластов IIP мышам SCID инициирует развитие интерстициального фиброза, с использованием данной модели проводят исследования, позволяющие определить антифиброзное действие антитела против CCL21. Группы из пяти мышей получают очищенные IgG или антитело против CCL21 путем в.б. инъекции начиная с 35 дня и затем через день до 63 дня. На 63 день ткани легких удаляют и делают показательные срезы. У мышей, обработанных IgG, отчетливо наблюдается интерстициальный фиброз и ремоделирование. И наоборот, по данным гистологического анализа в группах, обработанных антителом против CCL21, наблюдаются незначительные признаки фиброза легких.
Подробное описание предпочтительн