2-аминобензоксазолкарбоксамиды в качестве модуляторов 5-нт3
Иллюстрации
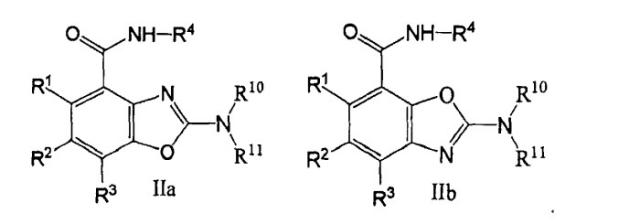
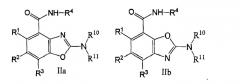
Показать всеИзобретение относится к соединениям общей формулы II, где R1, R2 и R3 независимо выбраны из группы, состоящей из водорода, галогена и низшего алкила, содержащего 1-6 атомов углерода; R4 представляет собой остаток, представленный в формуле изобретения; R5 представляет собой водород или метил; R10 выбран из группы, состоящей из: (i) водорода; (ii) (C1-С10)алкила; (iii) (С1-С10)алкила, замещенного одним или несколькими заместителями, независимо выбранными из группы, состоящей из -N(СН3)2, морфолинила, (C1-C4)алкокси, гидроксила, -CON(CH3)2 и галогена; (iv) моноциклического (С3-C8)циклоалкила, содержащего один гетероатом N; (v) 9-метил-9-азабицикло[3.3.1]нонана; (vi) фенила; (vii) фенила, замещенного одним или несколькими (С1-С4)алкокси; R11 выбран из группы, состоящей из водорода и (С1-С10)алкила; или R10, R11 и атом азота, к которому они присоединены, взятые вместе, образуют азотистый гетероцикл или замещенный азотистый гетероцикл, такие, как представлены в формуле изобретения. Также изобретение относится к фармацевтической композиции, обладающей способностью к модуляции рецептора серотонина типа 3 и способу лечения расстройства, которое зависит от модуляции рецептора серотонина типа 3. Технический результат - соединения формулы II в качестве модуляторов рецептора серотонина типа 3. 3 н. и 15 з.п. ф-лы, 1 табл., 159 пр.
Реферат
Перекрестная ссылка на родственные заявки
Настоящая заявка заявляет приоритет предварительной заявки на патент США №60/821646, поданной 7 августа 2006 г., полное содержание которой включено сюда в виде ссылки.
Область техники, к которой относится изобретение
Данное изобретение относится к группе 2-аминобензоксазолкарбоксамидов, которые являются применимыми при лечении индуцированной химиотерапией тошноты и рвоты (CINV) и при лечении синдрома раздраженного кишечника с преобладающей диареей (IBS-D).
Уровень техники
Тошнота и рвота, вызванные химиотерапией, принадлежат к наиболее неприятным побочным действиям у пациентов, подвергающихся лечению по поводу рака. В зависимости от химиотерапевтических агентов или принятых схем их приема до 90% пациентов могут страдать некоторой формой индуцированной химиотерапией тошноты и рвоты (CINV). Симптомы CINV могут быть очень изнурительными и часто приводят к отказу пациентов от дальнейших курсов химиотерапии с явно неблагоприятными последствиями в отношении прогрессирования рака. Кроме того, CINV является нагрузкой на систему здравоохранения, расходующую время врачебного персонала, который мог бы в противном случае оказывать помощь другим пациентам или уделять внимание другим медицинским проблемам.
CINV подразделяют на две основные категории: острая CINV и замедленная CINV. Острая CINV имеет место в пределах первых 24 часов лечения; замедленная CINV имеет место от 24 часов до 120 часов после лечения. Замедленная CINV остается часто проявляемым при лечении побочным действием у пациентов, подвергаемых химиотерапии, хотя здравоохранение имеет тенденцию занижать число пациентов, которые испытывают замедленную CINV. Кроме того, замедленная CINV значительно снижает способность пациентов проявлять заботу о себе после того, как они были выписаны из лечебного учреждения.
Соединения, которые ингибируют рецепторы серотонина, являются в настоящее время наиболее эффективными противорвотными средствами; они обуславливают единственный наиболее значительный успех в устранении тошноты и рвоты у пациентов с раковым заболеванием и имеют дополнительное применение при индуцированной излучением тошноте и рвоте (RINV) и послеоперационной тошноте и рвоте (PONV). По-видимому, блокирование рецептора 5-НТ3 в результате сигнала серотонина, вызванного индуцированным химиотерапией повреждением энтерохромаффинных клеток кишечника, в котором находится основная часть запасов серотонина организма, либо посредством периферического, либо центрального механизма, предотвращает острую рвоту. За исключением палоносетрона (алокси®), ингибиторы 5-НТ3 разрешены для лечения острой CINV и являются наиболее эффективными для такого лечения. Палоносетрон, который следует вводить внутривенно, является в настоящее время единственным ингибитором 5-НТ3, разрешенным для профилактики как острой, так и замедленной CINV. Постулируется, что эффективность палоносетрона против замедленной рвоты обуславливается его длительным периодом полувыведения из сыворотки. Поэтому специалисты в данной области признают, что ингибиторы 5-НТ3, которые имеют длительные периоды полувыведения из сыворотки, могут быть эффективными терапевтическими агентами как для острой, так и замедленной CINV, тогда как ингибиторы 5-НТ3, которые имеют короткие периоды полувыведения, могут быть применимыми для лечения острой CINV. Кроме того, обнаружено, что комбинация палоносетрона, ингибитора 5-НТ3 и апрепитанта (эменда®), антагониста нейрокинина, является очень эффективной при профилактике как острой, так и замедленной CINV после различных схем химиотерапии со рвотой от умеренной до очень сильной при клинических испытаниях. Особенно комбинированная терапия с применением либо антагонистов NK1, либо антагонистов 5-НТ3 с кортикостероидами, такими как дексаметазон, повышает эффективность этих лекарственных средств против острой или замедленной рвоты. По существу, маркировка эменд® указывает на то, что дозу данного лекарственного средства вводят с кортикостероидом и антагонистом 5-НТ3.
Синдром раздраженного кишечника (IBS) обычно существует в виде трех типов: с преобладающей диареей (IBS-D), с преобладающей констипацией (IBS-C) и IBS с чередующимися симптомами, названный IBS-A, или со смешанными симптомами (IBS-M). Синдром раздраженного кишечника с преобладающей диареей является ослабляющим организм, хотя и редко смертельным заболеванием. Типичный страдающий IBS-D пациент проявляет первичные симптомы, включающие множественные и ежедневные эксплозивные приступы диареи и тяжелые ежедневные спазмы брюшной полости. Наиболее обычные вторичные побочные действия включают панические приступы, депрессию, отказ от социальной и семейной активности и недостаточность или нарушение питания.
В настоящее время соединения, которые ингибируют рецепторы 5-НТ3, являются единственными эффективными средствами для лечения IBS-D. Единственным лекарственным средством, в настоящее время разрешенным для лечения IBS-D, является алосетрон, который был введен в употребление Glaxo, изъят из применения Департаментом по контролю за качеством пищевых продуктов, лекарственных и косметических средств США (FDA), поскольку он, по-видимому, вызывает ишемический колит, затем восстановлен в применении FDA, поскольку потребность в лечении IBS-D была также высокой. В 2002 г. Департамент по контролю за качеством пищевых продуктов, лекарственных и косметических средств США разрешил применение таблеток гидрохлорида алосетрона (лотронекс®) при ограниченных состояниях для женщин, в которых медицинская польза перевешивает риски. Ограничения по разрешению применения отражают серьезные желудочно-кишечные неблагоприятные случаи, которые описаны при применении алосетрона. Вторым структурно родственным ингибитором 5-НТ3 является цилансетрон, который прошел через клинические испытания, но недавно было получено письмо от FDA, не разрешающее его применение. Для лечения IBS-D могут быть применимыми новые, структурно неродственные ингибиторы IBS-D.
Ясно, что существует потребность в улучшенной терапии как для CINV, так и IBS-D.
Сущность изобретения
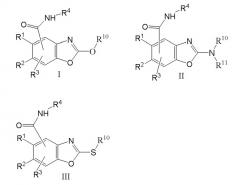
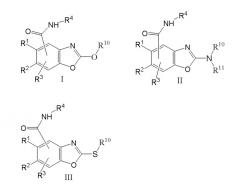
Теперь обнаружено, что соединения формул I, II и III являются сильнодействующими и селективными ингибиторами рецептора 5-НТ3:
В этих соединениях R1, R2 и R3 независимо выбраны из водорода, галогена, циано, алкил- или арилсульфоксида, алкил- или арилсульфона, амино, алкиламино, диалкиламино, ациламино, морфолинила, низшего О-алкила, гидрокси, низшего алкила, низшего фторалкила, низшего О-фторалкила, метилендиокси, этилендиокси, алкокси-низшего алкила и низшего гидроксиалкила.
R4 представляет собой насыщенный азотистый гетероцикл или замещенный метилом насыщенный азотистый гетероцикл, у которого атом азота является третичным, причем указанный гетероцикл содержит по меньшей мере одно 5- или 6-членное кольцо;
R10 выбран из группы, состоящей из
(i) водорода;
(ii) (С1-С10)алкила;
(iii) замещенного (С1-С10)алкила;
(iv) гетероциклила;
(v) замещенного гетероциклила;
(vi) арила и
(vii) замещенного арила;
R11 выбран из группы, состоящей из водорода и (С1-С10)алкила; или
R10, R11 и атом азота, к которому они присоединены, взятые вместе, образуют азотистый гетероцикл или замещенный азотистый гетероцикл.
В другом аспекте изобретение относится к фармацевтическим композициям, включающим фармацевтически приемлемый носитель и терапевтически эффективное количество соединения формулы I, II или III. Композиции могут содержать дополнительный противорвотный агент, особенно антагонист нейрокинина. Композиции могут содержать также кортикостероид.
В другом аспекте изобретение относится к способу лечения расстройства, возникающего из-за неподходящей активности рецептора серотонина типа 3 или зависящего от модуляции рецептора серотонина типа 3. Способ включает введение терапевтически эффективного количества соединения формулы I, II или III. Примеры расстройств, возникающих из-за неподходящей активности рецептора серотонина типа 3 или зависящих от модуляции рецептора серотонина типа 3, включают рвоту, особенно CINV, IBS-D, послеоперационную тошноту и рвоту и индуцированную излучением тошноту и рвоту. Другие такие нарушения включают физиологические нарушения, ожирение, нарушения, связанные со злоупотреблением различных веществ, деменцию, связанную с нейродегенеративным заболеванием, потерю познавательной способности, боль, синдром фибромиалгии и синдром хронической усталости (см. опубликованную заявку на патент США 2004/0204467). Известно также, что антагонисты рецептора серотонина типа 3 являются применимыми для профилактики и лечения бронхиальной астмы, нервной булимии, приступов апноэ во сне, зуда и мигрени (см. Costall and Naylor, Current Drug Targets - CNS & Neurological Disorders, 2004:3 27-37 и Israili, Current Med. Chem. - CNS Agents, 2001:1 171-199). Известно также, что антагонисты рецептора серотонина типа 3 являются применимыми для профилактики и лечения эпилепсии. Применение таких соединений для лечения эпилепсии демонстрируется в международной патентной заявке РСТ/GB2006/002733.
Подробное описание изобретения
На всем протяжении данного описания заместители имеют значения, указанные при первом упоминании, и сохраняют свои указанные значения.
В первом аспекте изобретение относится к соединениям формулы I, II или III:
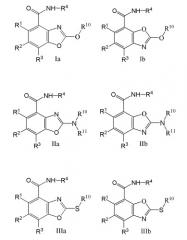
В общем, было обнаружено, что соединения вышеуказанных формул являются сильнодействующими и селективными ингибиторами рецептора 5-НТ3. Каждый из трех типов соединений можно разделить на два подтипа: 4-карбоксамиды (Ia, IIa и IIIa) и 7-карбоксамиды (Ib, IIb и IIIb):
В этих соединениях R4 представляет собой насыщенный азотистый гетероцикл или замещенный метилом насыщенный азотистый гетероцикл, у которого атом азота является третичным. Азотсодержащий гетероцикл (называемый также азотистым гетероциклом) является гетероциклом, содержащим по меньшей мере один атом азота в кольце; он может содержать дополнительные атомы азота, а также другие гетероатомы. Азотистые гетероциклы включают пиперидин, метилпиперидин, тропан, 9-азабицикло[3.3.1]нонан-3-он и , в которой Х представляет собой NCH3, O, S, SO или SO2. В некоторых вариантах осуществления R4 представляет собой
и
в которых m равно 1, 2, 3 или 4; n равно 0, 1, 2, 3 или 4; Q представляет собой N(CH3) или -О- и R5 представляет собой водород или метил. Например, R4 может быть хинуклидином, тропаном, азабицикло[3.3.1]нонаном, метилазабицикло[3.3.1]нонаном, диметилдиазабицикло[3.3.1]нонаном, метилпиперидином или метил-3-окса-9-азабицикло[3.3.1]нонаном.
В некоторых вариантах осуществления R1, R2 и R3 представляют собой водород и в других один из R1, R2 и R3 представляет собой галоген.
В некоторых вариантах осуществления R10 выбран из группы, состоящей из водорода и (С1-С3)алкила. В других вариантах осуществления типа II R11 представляет собой Н или СН3 и R10 выбран из группы, состоящей из фенила, замещенного фенила, (С1-С6)алкила, 4-7-членного моноциклического азотистого гетероцикла, содержащего 4-10 атомов углерода бициклического азотистого гетероцикла, 4-7-членного моноциклического азотистого гетероцикла, замещенного одним или несколькими (С1-С6)алкилами, содержащего 4-10 атомов углерода бициклического азотистого гетероцикла, замещенного одним или несколькими (С1-С6)алкилами, диметиламино(С1-С6)алкила, 4-7-членного моноциклического азотистого гетероциклил(С1-С6)алкила, (С1-С6)алкокси(С1-С6)алкила, гидрокси(С1-С6)алкила и диалкиламинокарбонил(С1-С6)алкила.
В других вариантах осуществления R10 и R11, взятые вместе, образуют азотистый гетероцикл или замещенный азотистый гетероцикл. Примеры их включают морфолин, пиперазин, пиперидин, диазепан, тетрагидрохиноксалин, азабицикло[3.3.1]нонан, триазолопиразин, диазабицикло[2.2.1]гептан или любой из вышеуказанных гетероциклов, замещенный одним, двумя или тремя заместителями, независимо выбранными из (С1-С6)алкила, галоген(С1-С6)алкила, (С1-С6)алкоксифенила, гетероарила, замещенного гетероарила, гетероциклила и замещенного гетероциклила.
Соединения, находящиеся в пределах вышеуказанной группы соединений и ее подгрупп, являются применимыми в качестве ингибиторов 5-НТ3. В процессе экспертизы можно обнаружить, что соединения, которые в настоящее время не исключены из формулы изобретения, являются непатентоспособными для авторов изобретения в данной заявке. В этом случае исключение отдельных соединений и подгрупп из формулы изобретения следует рассматривать как непреднамеренные дефекты делопроизводства, которые не отражают идею и описание авторами их изобретения. Изобретением в качестве объекта «вещество» являются все соединения формул I, II и III, за исключением (а) тех соединений, которые находятся в общественном достоянии, и (b) конкретного соединения примера 55, находящегося в пределах подгруппы IIa, в котором R10, R11 и атом азота образуют кольцо морфолина и R4, по-видимому (на основании данных ЯМР), является эндо-3,9-диметил-3,9-диазабицикло[3.3.1]нонан-7-илом. Такое соединение не проявляет уровень активности, установленный как пороговый для скрининга.
Определения
Предполагается, что алкил включает неразветвленные, разветвленные или циклические углеводородные структуры и их комбинации. Низший алкил относится к алкильным группам, содержащим 1-6 атомов углерода. Примеры низших алкильных групп включают метил, этил, пропил, изопропил, бутил, втор- и трет-бутил и тому подобное. Предпочтительными алкильными группами являются алкильные группы С20 или ниже. Циклоалкил является подгруппой алкила и включает циклические углеводородные группы с 3-8 атомами углерода. Примеры циклоалкильных групп включают циклопропил, циклобутил, циклопентил, норборнил и тому подобное. Некоторые группы требуют точного определения. Утверждение, что термин алкил предназначается для включения неразветвленных, разветвленных или циклических углеводородных структур и их комбинаций, означает, что нижеследующую комбинацию неразветвленных и циклических структурных элементов
(и подобные комбинации) считают «алкильной» группой. С1-С20углеводород включает алкил, циклоалкил, алкенил, арил и их комбинации. Примеры его включают фенетил, циклогексилметил, камфорил и нафтилэтил.
Алкокси или алкоксил относится к группам с 1-8 атомами углерода неразветвленной, разветвленной или циклической структуры и их комбинациям, присоединенным к «основной» структуре через атом кислорода. Примеры их включают метокси, этокси, пропокси, изопропокси, циклопропилокси, циклогексилокси и тому подобное. Низший алкокси относится к группам, содержащим от одного до четырех атомов углерода.
Оксаалкил относится к алкильным остаткам, у которых один или несколько атомов углерода заменены атомами кислорода. Примеры его включают метоксипропокси, 3,6,9-триоксадецил и тому подобное.
Ацил относится к группам с 1-8 атомами углерода неразветвленной, разветвленной, циклической структуры, насыщенным, ненасыщенным и ароматическим, и их комбинациям, присоединенным к «основной» структуре через карбонильную функциональную группу. Один или несколько атомов углерода в ацильном остатке могут быть заменены атомом азота, кислорода или серы, пока место присоединения к «основной» структуре остается у карбонила. Примеры его включают ацетил (Ас), бензоил, пропионил, изобутирил, трет-бутоксикарбонил, бензилоксикарбонил и тому подобное. Низший ацил относится к группам, содержащим от одного до четырех атомов углерода.
Арил и гетероарил означают 5- или 6-членное ароматическое или гетероароматическое кольцо, содержащее 0-3 гетероатома, выбранных из О, N или S; бициклическую 9- или 10-членную систему ароматических или гетероароматических колец, содержащую 0-3 гетероатома, выбранных из О, N или S; или трициклическую 13- или 14-членную систему ароматических или гетероароматических колец, содержащую 0-3 гетероатома, выбранных из О, N или S. Ароматические 6-14-членные карбоциклические кольца включают, например, бензол, нафталин, индан, тетралин и флуорен, и 5-10-членные ароматические гетероциклические кольца включают, например, имидазол, пиридин, индол, тиофен, бензопиранон, тиазол, фуран, бензимидазол, хинолин, изохинолин, хиноксалин, пиримидин, пиразин, тетразол и пиразол.
Арилалкил относится к остатку, в котором арильная часть присоединена к «основной» части молекулы через алкил. Примерами его являются бензил, фенетил и тому подобное. Толил не является арилалкилом; толил является алкиларилом. Гетероарилалкил означает гетероарильный остаток, присоединенный к «основной» части через алкил. Примеры его включают, например, пиридинилметил, пиримидинилэтил и тому подобное.
Гетероцикл означает циклоалкильный или арильный остаток с кольцами от одного до трех, у которого от одного до четырех атомов углерода заменены гетероатомом, выбранным из группы, состоящей из N, O и S. Гетероатомы азот и сера могут быть необязательно окислены и гетероатом азот может быть необязательно кватернизован. Примеры гетероциклов включают пирролидин, пиразол, пиррол, индол, хинолин, изохинолин, тетрагидроизохинолин, бензофуран, бензодиоксан, бензодиоксол (обычно называемый метилендиоксифенилом при присутствии в качестве заместителя), тетразол, морфолин, тиазол, пиридин, пиридазин, пиримидин, тиофен, фуран, оксазол, оксазолин, изоксазол, диоксан, тетрагидрофуран и тому подобное. Азотистыми гетероциклами являются гетероциклы, содержащие по меньшей мере один атом азота. Они могут дополнительно включать другие гетероатомы и несколько атомов азота. Примеры их включают хинуклидин, тропан, пиперидин, пиперазин, морфолин, хинолин, бензо[b][1,4]оксазин, 1,2,4-триазоло[4,3-a]пиразин, пергидрохиноксалин и тиазол. Следует отметить, что гетероарилы являются подгруппой гетероциклов, в которой гетероцикл является ароматическим. Дигидрогетероарилы являются, как предполагает их название, гетероарильными остатками, формально восстановленными одним молем водорода. Примером дигидрогетероарильного остатка является 2,3-дигидробензофуран.
Замещенный алкил, арил, циклоалкил, гетероциклил и т.д. относится к алкилу, арилу, циклоалкилу или гетероциклилу, где до четырех атомов Н в каждом остатке заменены галогеном, галогеналкилом, гидрокси, низшим алкокси, карбокси, алкоксикарбонилом (COOR), оксо, карбоксамидо (-CONR2), сульфонамидо (-SO2NR2), циано, карбонилом, нитро, амино, алкиламино, диалкиламино, меркапто, алкилтио, сульфоксидом, сульфоном, ациламино, амидино, фенилом, бензилом, гетероциклилом, гетероциклилкарбонилом, фенокси, бензилокси или гетероарилокси. В предшествующем перечне R представляет собой водород или алкил.
Термин «галоген» означает атом фтора, хлора, брома или иода.
Некоторые из описанных здесь соединений могут содержать один или несколько асимметричных центров и могут, таким образом, обуславливать существование энантиомеров, диастереомеров и других стереоизомерных форм, которые можно обозначить в терминах абсолютной стереохимии как (R)- или (S)-изомеры. Имеется в виду, что настоящее изобретение включает все такие возможные изомеры, а также их рацемические и оптически чистые формы. Оптически активные (R)- и (S)-изомеры можно получить с применением хиральных синтонов или хиральных реагентов или разделением смесей с применением общепринятых способов. Когда соединения, описанные здесь, содержат олефиновые двойные связи или другие центры геометрической асимметрии и, если не указано иначе, имеется в виду, что соединения включают как Е-, так и Z-геометрические изомеры. Подобным же образом имеется в виду, что соединения включают все таутомерные формы. Конфигурация любой углерод-углеродной двойной связи, показываемая в них, выбрана только для удобства и не предполагается, что она означает конкретную конфигурацию, поэтому углерод-углеродная связь, изображенная здесь произвольно как транс, может быть Z-, E-конфигурацией или смесью двух конфигураций в любом отношении.
Должно быть понятно, что соединения данного изобретения могут существовать в форме, меченной радиоизотопом, т.е. соединения могут содержать один или несколько атомов, имеющих атомную массу или массовое число, отличное от атомной массы или массового числа, обычно обнаруживаемого в природе. Радиоизотопы водорода, углерода, фосфора, фтора, хлора и иода включают 3H, 14C, 35S, 18F, 36Cl и 125I, соответственно. Соединения, которые содержат такие радиоизотопы и/или другие радиоизотопы других атомов, находятся в пределах объема данного изобретения. Радиоизотопы тритий, т.е. 3Н, и углерод-14, т.е. 14С, являются особенно предпочтительными вследствие легкости их получения и детектируемости. Меченные радиоизотопом соединения данного изобретения обычно получают способами, хорошо известными специалисту в данной области. Такие меченные радиоизотопом соединения можно получить подходящим образом проведением методик, описанных в примерах и на схемах, заменой немеченного радиоактивным изотопом реагента легко доступным, меченным радиоактивным изотопом реагентом.
Терминология, относящаяся к «защите», «снятию защиты» и «защищенным» функциональным группам встречается на всем протяжении данной заявки. Такая терминология хорошо понятна специалистам в данной области и ее применяют в контексте способов, которые включают последовательную обработку рядом реагентов. В таком контексте защитная группа относится к группе, которую применяют для маскирования функциональной группы во время стадии способа, в которой она может в противном случае реагировать, но в которой реакция является нежелательной. Защитная группа предотвращает реакцию на данной стадии, но ее можно затем удалить для получения первоначальной функциональной группы. Удаление защитной группы или «снятие защиты» имеет место после завершения реакции или реакций, которым может препятствовать упомянутая функциональная группа. Таким образом, когда указывается последовательность применения реагентов, как это имеет место в способах изобретения, специалист в данной области может легко определить те группы, которые могут быть подходящими в качестве «защитных групп». Подходящие группы для такой цели обсуждаются в стандартных пособиях в области химии, таких как публикация Protective Groups in Organic Synthesis by T. W. Greene [John Wiley & Sons, New York, 1991], которая включена здесь в качестве ссылки.
Термин «профилактика», применяемый здесь, относится к введению лекарственного средства заранее для предотвращения или смягчения приступа. Специалист в области медицины (к которой относятся пункты формулы изобретения на способ) понимает, что термин «профилактика» не является абсолютным термином. Понятно, что в области медицины он относится к профилактическому введению лекарственного средства, чтобы существенно уменьшить вероятность появления или серьезность состояния, и этот термин имеет смысл, предполагаемый здесь. Фактически в издании 2006 г. публикации the Physician's Desk Reference, которая является стандартным пособием в данной области, применяют термин «проводить профилактику» или «профилактика» не менее 10 раз в его описании критериев палоносетрона.
Графические изображения рацемических, амбискалемных и скалемных или энантиомерно чистых соединений, применяемых здесь, взяты из Maehr J. Chem. Ed. 62, 114-120 (1985): сплошные и прерывистые клинья применяют для обозначения абсолютной конфигурации хирального элемента; волнистые линии означают исключение любого стереохимического значения, которое связь, его представляющая, могла бы образовывать; сплошные и четкие ломаные линии являются геометрическими дескрипторами, показывающими относительную конфигурацию, но обозначающими рацемический характер; и клиновидные контуры и пунктирные или прерывистые линии означают энантиомерно чистые соединения неопределенной абсолютной конфигурации. Простая сплошная линия ничего не говорит о стереохимии. Например, на иллюстрации для примера 2 в приведенной ниже таблице показана сплошная линия, но соединение примера фактически является индивидуальным энантиомером с S-конфигурацией и его можно правильно изобразить как
Предполагается, как и должно быть понятно специалисту в данной области, что применяемый здесь термин «соединение» включает соли, сольваты и комплексы включения такого соединения. Термин «сольват» относится к соединению формулы I в твердом состоянии, у которого молекулы подходящего растворителя включены в кристаллическую решетку. Подходящий растворитель для терапевтического введения является физиологически переносимым при вводимой дозе. Примерами подходящих растворителей для терапевтического введения являются этанол и вода. Когда растворителем является вода, сольват называют гидратом. В общем, сольваты получают растворением соединения в подходящем растворителе и выделением сольвата охлаждением или применением антирастворителя. Сольват обычно сушат или подвергают азеотропной перегонке в условиях окружающей среды. Комплексы включения описаны в публикации Remington: The Science and Practice of Pharmacy 19th Ed. (1995) volume 1, page 176-177, которая включена здесь в качестве ссылки. Наиболее обычно применяемыми комплексами включения являются комплексы с циклодекстринами, и все комплексы с циклодекстринами, природными и синтетическими, в частности, включены в формулу изобретения.
Термин «фармацевтически приемлемая соль» относится к солям, полученным из фармацевтически приемлемых нетоксичных кислот или оснований, включающих неорганические кислоты и основания и органические кислоты и основания. Когда соединения настоящего изобретения являются основными, соли можно получить из фармацевтически приемлемых нетоксичных кислот, включающих неорганические и органические кислоты. Подходящие фармацевтически приемлемые кислотно-аддитивные соли для соединений настоящего изобретения включают соли, образованные уксусной, бензолсульфоновой (безилат), бензойной, камфорасульфоновой, лимонной, этансульфоновой, фумаровой, глюконовой, глутаминовой, бромистоводородной, хлористоводородной, изетионовой, молочной, малеиновой, яблочной, миндальной, метансульфоновой, слизевой, азотной, памовой, пантотеновой, фосфорной, янтарной, серной, винной, п-толуолсульфоновой кислотой и тому подобное. Когда соединения содержат кислотную боковую цепь, подходящие фармацевтически приемлемые основно-аддитивные соли соединений настоящего изобретения включают соли металлов алюминия, кальция, лития, магния, калия, натрия и цинка или органические соли, полученные из лизина, N,N'-дибензилэтилендиамина, хлорпрокаина, холина, диэтаноламина, этилендиамина, меглумина (N-метилглюкамина) и прокаина.
Полный список аббревиатур, применяемый специалистами органической химии, представлен в первом номере каждого тома Journal of Organic Chemistry. Список, который обычно представляют в таблице, озаглавленной «Стандартный список аббревиатур», включен здесь в качестве ссылки.
Обобщенные синтетические схемы представлены ниже.
Общие методики модификации кольца бензоксазола
Условия: А) амин, растворитель; В) основание гидроксид; С) амин, EDCI, HOBt, ДМФА или HBTU, ДМФА; D) HCl, MeOH или Et2O
Общая методика (GP-A) аминирования кольца бензоксазола
Смесь подходящего 2-хлорбензоксазола, А1 (1 экв) и подходящего амина (2 экв) и необязательного основания (например, К2СО3, триэтиламина, диизопропиламина, 1,8-диазабицикло[5.4.0]ундецена или гидрида натрия) в ТГФ (или DME, ДМФА) нагревают в диапазоне 20-80°С в течение вплоть до 24 час. После охлаждения до комнатной температуры реакционную смесь концентрируют при пониженном давлении. Сырой продукт очищают колоночной хроматографией на силикагеле (типичные элюенты включают смесь 9:1 дихлорметан/метанол, этилацетат, гексаны), получая при этом требуемый продукт, 2-аминобензоксазол. Структуру продукта подтверждают 1Н ЯМР или анализом масс.
Общая методика (GP-B1) гидролиза метилового эфира
Смесь метилового эфира А2 в 2 н. NaOH и ТГФ перемешивают при комнатной температуре в течение 12 час. Реакционную смесь нейтрализуют 2 н. HCl и затем экстрагируют дихлорметаном. Объединенные органические слои сушат (Na2SO4), фильтруют и концентрируют, получая при этом требуемую карбоновую кислоту А3. Структуру продукта подтверждают либо 1Н ЯМР, либо анализом масс.
Общая методика (GP-B2) гидролиза метилового эфира (карбоксилатная соль лития)
Смесь метилового эфира А2 и моногидрата гидроксида лития (1-3 экв) в смеси метанол/вода (3:1) перемешивают при комнатной температуре до завершения реакции по данным ЖХ-МС. Растворитель удаляют в вакууме и сырую литиевую соль А3 сушат при высоком вакууме и затем применяют без дополнительной очистки. Структуру продукта подтверждают 1Н ЯМР или анализом масс.
Общая методика (GP-B3) гидролиза метилового эфира
Смесь метилового эфира А2, моногидрата гидроксида лития (1-3 экв) и смеси метанол/вода или ТГФ/вода (3:1 - 5:1) перемешивают при комнатной температуре до завершения реакции по данным ЖХ-МС. Реакционную смесь концентрируют при пониженном давлении. Образовавшийся остаток разбавляют водой, подкисляют (рН 1-5) 3н хлористоводородной кислотой и концентрируют досуха. Твердое вещество растирают в дихлорметане и фильтрат концентрируют при пониженном давлении, получая при этом требуемую карбоновую кислоту А3. Структуру продукта подтверждают либо 1Н ЯМР, либо анализом масс.
Общая методика (GP-C1) амидирования
Смесь карбоновой кислоты или карбоксилатной соли лития А3 (1 экв), подходящего амина (например, дигидрохлорида эндо-3-амино-9-метил-9-азабицикло[3.3.0]нонана (1 экв), гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида (2 экв)), и 1-гидроксибензотриазола (2 экв) в ДМФА перемешивают при комнатной температуре в течение 5 мин, затем добавляют триэтиламин (2-4 экв). Образовавшуюся реакционную смесь перемешивают при комнатной температуре в течение 12 час. Смесь разбавляют дихлорметаном и затем промывают насыщенным раствором бикарбоната натрия. Водный слой далее экстрагируют дихлорметаном. Объединенные органические слои сушат (Na2SO4), фильтруют и концентрируют. Сырое вещество очищают хроматографией на силикагеле (типичные элюенты: смесь этилацетат/гексаны, этилацетат/метанол, дихлорметан, смесь дихлорметан/метанол или дихлорметан/метанол/концентрированный гидроксид аммония), получая при этом требуемый карбоксамид А4. Структуру продукта подтверждают 1Н ЯМР.
Общая методика (GP-C2) амидирования
Смесь карбоновой кислоты или карбоксилатной соли лития А3 (1 экв), подходящего амина (например, дигидрохлорида эндо-3-амино-9-метил-9-азабицикло[3.3.0]нонана) (1 экв), и HBTU (1,3-2 экв) в ДМФА перемешивают при комнатной температуре в течение 5 мин, затем добавляют триэтиламин (2-4 экв). Образовавшуюся реакционную смесь перемешивают при комнатной температуре в течение 12 час. Смесь разбавляют дихлорметаном и затем промывают насыщенным раствором бикарбоната натрия. Водный слой далее экстрагируют дихлорметаном. Объединенные органические слои сушат (Na2SO4), фильтруют и концентрируют. Сырое вещество очищают хроматографией на силикагеле (типичные элюенты: смесь этилацетат/гексаны, этилацетат/метанол, дихлорметан, смесь дихлорметан/метанол или дихлорметан/метанол/концентрированный гидроксид аммония), получая при этом требуемый карбоксамид А4. Структуру продукта подтверждают 1Н ЯМР.
Общая методика (GP-D1) превращения в соль HCl
К охлажденному льдом раствору карбоксамида A4 (1 экв) в дихлорметане и этиловом эфире добавляют хлорид водорода (2 экв) в метаноле. Смесь перемешивают при комнатной температуре в течение 5 мин и затем разбавляют безводным этиловым эфиром. Смесь выдерживают при комнатной температуре в течение 2 час и затем образовавшийся осадок собирают фильтрованием и промывают этиловым эфиром. Твердое вещество сушат в вакууме, получая при этом требуемую гидрохлоридную соль А4. Структуру продукта подтверждают 1Н ЯМР.
Общая методика (GP-D2) превращения в соль HCl
Охлажденный льдом раствор Вос-защищенного карбоксамида из GP-C (1 экв) обрабатывают избытком либо TFA, либо HCl (в диэтиловом эфире, диоксане или метаноле) в дихлорметане. Сырую соль разбавляют метанолом и загружают в колонку с катионообменной смолой (колонка с 10 г изолюта SCX-2). Колонку промывают метанолом (50 мл) и продукт затем элюируют 2 н. гидроксидом аммония в метаноле (50 мл). Раствор концентрируют при пониженном давлении. Сырое вещество очищают хроматографией на силикагеле (типичные элюенты: смесь дихлорметан/метанол, дихлорметан/метанол/концентрированный гидроксид аммония), получая при этом требуемый карбоксамид. Карбоксамид затем обрабатывают HCl (1-2 эквивалента) в дихлорметане и концентрируют при пониженном давлении. Аморфную гидрохлоридную соль лиофилизуют в смеси ацетонитрил/вода (6:1), получая при этом требуемую гидрохлоридную соль А4. Структуру продукта подтверждают анализом массы и 1Н ЯМР.
Общая методика (GP-E) ацилирования эндо-N-(9-метил-9-азабицикло[3.3.1]нонан-3-ил)-2-((2S,6S)-2,6-диметилпиперазин-1-ил)бензоксазол-4-карбоксамида
К охлажденной льдом смеси эндо-N-(9-метил-9-азабицикло[3.3.1]нонан-3-ил)-2-((2S,6S)-2,6-диметилпиперазин-1-ил)бензоксазол-4-карбоксамида и триэтиламина в CH2Cl2 добавляют подходящий ацилхлорид, хлорформиат или сульфонилхлорид. Смеси дают возможность нагреться до температуры окружающей среды и затем перемешивают в течение вплоть до дополнительных 24 час. Реакционную смесь гасят смесью СН3ОН/насыщенный раствор соли и образовавшуюся смесь экстрагируют дихлорметаном (2×). Объединенные органические слои промывают последовательно 10% лимонной кислотой и насыщенным раствором соли, затем сушат (Na2SO4), фильтруют и концентрируют при пониженном давлении. Очистка колоночной хроматографией (силикагель, от смеси 9:1 CH2Cl2/СН3ОН до смеси 90:9:1 CH2Cl2/СН3ОН/NH4OH), дает соответствующий эндо-N-(9-метил-9-азабицикло[3.3.1]нонан-3-ил)-2-((2S,6S)-2,6-диметил-4-ацилпиперазин-1-ил)бензоксазол-4-карбоксамид.
Получение метил-2-хлорбензоксазол-4-карбоксилата
Условия: (А) TMSCHN2; (B) О-этилксантат калия, пиридин; (С) PCl5, POCl3.
Стадия А: К охлажденной льдом суспензии гидробромида 2-амино-3-гидроксибензойной кислоты (3,0 г, 12,8 ммоль) в толуоле (30 мл) и метаноле (30 мл) медленно добавляют (триметилсилил)диазометан (16,0 мл, 2 М раствор в этиловом эфире, 32,0 ммоль), затем смесь перемешивают при 0°С в течение 20 мин. В реакционную смесь при 0°С добавляют уксусную кислоту (5 мл), затем смесь перемешивают при комнатной температуре в течение 0,5 час. Реакционную смесь концентрируют при пониженном давлении и затем сырой продукт растворяют в этилацетате и промывают насыщенным раствором бикарбоната натрия и насыщенным раствором соли. Органический слой сушат (Na2SO4), фильтруют и концентрируют. Сырой продукт очищают колоночной хроматографией (силикагель, смесь 1:1 гексаны/этилацетат), получая при этом требуемый сложный эфир (2,04 г, 95%) в виде светло-коричневого твердого вещества. 1Н ЯМР (500 МГц, CDCl3) δ 7,48 (дд, J=8,0, 1,5 Гц, 1H), 6,81 (дд, J=7,5, 1,5 Гц, 1H), 6,50 (т, J=8,0 Гц, 1H), 5,80 (ушир.с, 2H), 3,87 (с, 3H); MC (ESI+) m/z 168 (M+H).
Стадия В. Смесь метил-2-амино-3-гидроксибензоата со стадии А (2,04 г, 12,2 ммоль) и О-этилксантата калия (1,37 г, 8,56 ммоль) в пиридине (8 мл) кипятят с обратным холодильником а течение 2 час, зат