Производные азапептидов
Иллюстрации
Показать всеИзобретение относится к новым производным сульфата атазанавира - ингибитора ВИЧ протеазы. Данное изобретение также относится к фармацевтическим композициям, обладающим противовирусной активностью в отношении ВИЧ. 2 н. и 17 з.п. ф-лы, 5 ил., 11 табл., 20 пр.
Реферат
РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет согласно предварительной заявке на патент США № 60/934201, поданной 12 июня 2007 года, и предварительной заявки на патент США № 61/067627, поданной 29 февраля 2008 года. Описания указанных заявок во всей полноте включены в настоящее описание посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
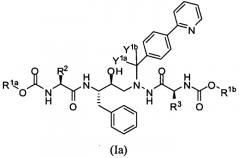
Атазанавира сульфат, известный также как сульфат диметилового эфира (3S,8S,9S,12S)-3,12-бис(1,1-диметилэтил)-8-гидрокси-4,11-диоксо-9-(фенилметил)-6-[[4-(2-пиридинил)фенил]метил]-2,5,6,10,13-пентаазатетрадекандионовой кислоты, предотвращает образование зрелых вирионов ВИЧ в клетках, инфицированных ВИЧ-1, селективным ингибированием вирус-специфического процессинга некоторых полипротеинов (вирусных полипротеинов Gag и Gag-Pol). В настоящее время атазанавира сульфат утвержден в качестве лекарственного средства для лечения ВИЧ инфекции.
Противопоказанием для применения атазанавира является совместное применение с лекарственными средствами, которые являются высокозависимыми от CYP3A для клиренса и для которых повышенные концентрации в плазме связаны с серьезными и/или опасными для жизни событиями. Вследствие ингибиторного действия атазанавира на CYP3A, CYP2C8 и UGT1A1 для пациентов, принимающих атазанавир, предписывается осторожность при назначении лекарственных средств, метаболизируемых, главным образом, CYP3A, CYP2C8 и UGT1A1. Обычно неблагоприятные эффекты, связанные с атазанавиром, включают гипербилирубинемию, быстропроходящую сыпь, тошноту, головную боль и желтуху/склеральную желтуху. Неблагоприятные последствия, которые испытывают некоторые пациенты и причинная взаимосвязь которых не была установлена, включают сахарный диабет/гипергликемию, увеличение продолжительности PR интервала, гемофилию и перераспределение жира.
Несмотря на полезные активные свойства атазанавира существует потребность в новых соединениях для лечения указанных выше заболеваний и состояний.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым соединениям, которые представляют собой азапептиды, и их фармацевтически приемлемым солям. Точнее, изобретение относится к новым азапептидам, представляющим собой производные атазанавира сульфата, который является ингибитором ВИЧ протеазы. Данное изобретение предоставляет также апирогенные композиции, содержащие одно или несколько соединений согласно изобретению и носитель, и применение заявленных соединений и композиций в способах лечения заболеваний и состояний, которые лечатся введением ингибиторов ВИЧ протеазы. Изобретение также относится к применению одного или нескольких заявленных соединений в качестве реагентов в аналитических исследованиях, которые включают применение атазанавира.
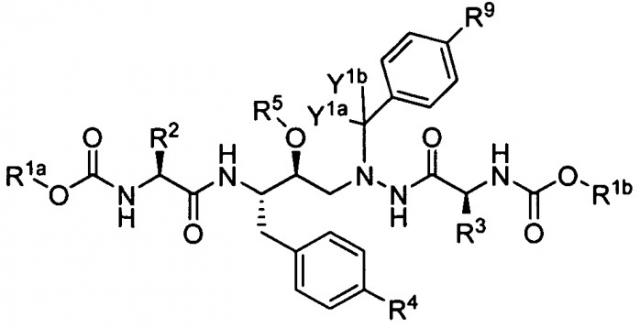
Соединения согласно настоящему изобретению представляют собой соединения формулы А:
(А)
или их соли, гидраты или сольваты, где
каждый из R1a и R1b независимо выбран из С1-С3 алкила, где один или несколько атомов водорода в алкиле необязательно заменены атомом дейтерия;
каждый из R2 и R3 независимо выбран из изопропила, втор-бутила и трет-бутила, где один или несколько атомов водорода в изопропиле, втор-бутиле или трет-бутиле необязательно заменен(ы) атомом дейтерия;
R4 выбран из Н, ОН и -О-(СR6R7-O)n-R8;
R5 выбран из Н и -(СR6R7-O)n-R8, где:
каждый R6 и R7 независимо выбран из Н, С1-С6 алкила, С2-С6 алкенила, С2-С6 алкинила и С3-С7 циклоалкила; или
R6 и R7 вместе с атомом углерода, к которому они присоединены, образуют 3-7-членный циклоалкил;
каждый R8 независимо выбран из -С(О)Н, -С(О)-(С1-С7 алкила), -Р(О)-(ОН)2, -S(O)-OH, -S(O)2-OH и A-R11, где
А представляет собой остаток α-аминокислоты; и
R11 выбран из Н, С1-С6 алкила, -С(О)-(С1-С7 алкила), А-R12,
где R12 выбран из Н, С1-С6 алкила и -С(О)-(С1-С7 алкила);
n равно 0 или 1;
где любой алкил в R5 является необязательно замещенным;
каждый из Y1a и Y1b независимо выбран из Н и D;
R9 выбран из 2-тиенила, 3-тиенила, тиазол-5-ила, тиазол-2-ила, пиридин-2-ила, пиридин-3-ила, пиридин-4-ила, пиразин-2-ила, 2-метил-2Н-тетразол-5-ила, 2-(d 3-метил)-2Н-тетразол-5-ила, 1-метил-1Н-тетразол-5-ила и 1-(d 3-метил)-1Н-тетразол-5-ила; и
по меньшей мере, одна из переменных R1a, R1b, R2, R3 или Y включает атом дейтерия.
Соединения, их фармацевтически приемлемые соли и композиции согласно изобретению могут применяться для лечения заболеваний, которые эффективно лечатся соединением, являющимся ингибитором ВИЧ протеазы. Само по себе настоящее изобретение включает способ лечения заболевания, чувствительного к лечению соединением, которое является ингибитором ВИЧ протеазы, причем способ включает введение субъекту, нуждающемуся в таком лечении, эффективного количества: (i) соединения или его фармацевтически приемлемой соли; или (ii) апирогенной композиции (например, фармацевтической композиции) согласно настоящему изобретению.
Заболевания или состояния, чувствительные к лечению соединением, обладающим ингибиторной активностью в отношении ВИЧ протеазы, включают, но без ограничения, ВИЧ инфекцию.
Соединения или композиции согласно настоящему изобретению могут также применяться в качестве реагентов в способах определения концентрации атазанавира сульфата в растворе, исследованиях метаболизма атазанавира сульфата и других аналитических исследованиях. Дополнительная возможность применения соединений любой из приведенных в описании формул включает их применение в качестве внутренних стандартов для определения точной концентрации атазанавира сульфата в биологических матрицах, таких как плазма.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
ФИГ.1 представляет собой график, показывающий стабильность соединений согласно данному изобретению в микросомах печени человека по сравнению с атазанавиром.
ФИГ.2 представляет собой график, показывающий стабильность соединений согласно настоящему изобретению в микросомах печени человека по сравнению с атазанавиром.
ФИГ.3 представляет собой график, показывающий стабильность соединений согласно настоящему изобретению в микросомах печени человека по сравнению с атазанавиром.
ФИГ.4 представляет собой график, показывающий уровни содержания в плазме соединений согласно изобретению после перорального введения шимпанзе по сравнению с атазанавиром.
ФИГ.5 представляет собой график, показывающий уровни содержания в плазме соединений согласно настоящему изобретению после перорального введения шимпанзе по сравнению с атазанавиром.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Термины «улучшать» и «лечить» используются взаимозаменяемо и включают как терапевтическое лечение, так и профилактическое лечение (снижение вероятности развития). Оба термина означают снижение, подавление, ослабление, уменьшение, приостановку или стабилизацию развития или прогрессирования заболевания (например, заболевания или расстройства, определенного в описании), снижение тяжести заболевания или ослабление симптомов, связанных с заболеванием.
Термин «заболевание» означает любое состояние или расстройство, которое наносит ущерб или причиняет вред нормальной функции клетки, ткани или органа.
Следует представлять, что некоторое изменение природной изотопной распространенности имеет место в синтезированном соединении в зависимости от источника химических веществ, используемых в синтезе. Таким образом, препарат атазанавира будет по существу содержать небольшие количества дейтерированных изотопологов. Концентрация стабильных изотопов водорода, которая имеет место согласно природной распространенности, несмотря на такое отклонение, является небольшой и незначительной по сравнению со степенью стабильного изотопного замещения соединений согласно настоящему изобретению (см., например, Wada E. et al., Seikagaku 1994, 66:15; Ganes L.Z. et al., Comp. Biochem. Physiol. Mol. Integr. Physiol. 1998, 119:725).
Если не определено иначе, когда положение обозначено конкретно как «Н» или как «водород», следует представлять, что это положение содержит водород согласно природной распространенности его изотопного состава. Также если не определено иначе, когда положение точно определено как «D» или как «дейтерий», следует представлять, что положение содержит дейтерий в количестве, которое, по меньшей мере, в 3500 раз превышает природное содержание дейтерия, равное 0,015% (т.е., по меньшей мере, 52,5% введения дейтерия).
Термин «фактор изотопного обогащения», когда используется в данном описании, означает соотношение между изотопным избытком D в конкретном положении в соединении согласно настоящему изобретению и природным содержанием данного изотопа. Природное содержание дейтерия составляет 0,015%.
В других вариантах осуществления изобретения соединение согласно настоящему изобретению имеет фактор изотопного обогащения для каждого дейтерия, присутствующего в сайте, указанном в качестве возможного сайта дейтеризации на соединение, равный, по меньшей мере, 4000 (60% введения дейтерия), по меньшей мере, 4500 (67,5% введения дейтерия), по меньшей мере, 5000 (75% введения дейтерия), по меньшей мере, 5500 (82,5% введения дейтерия), по меньшей мере, 6000 (90% введения дейтерия), по меньшей мере, 6333,3 (95% введения дейтерия), по меньшей мере, 6466,7 (97% введения дейтерия), по меньшей мере, 6600 (99% введения дейтерия) или, по меньшей мере, 6633,3 (99,5% введения дейтерия). Следует представлять, что фактор изотопного обогащения каждого дейтерия, присутствующего в сайте, обозначенном в качестве сайта дейтеризации, не зависит от других дейтерированных сайтов. Например, если в соединении имеются два сайта дейтеризации, один сайт может быть дейтерированным на 52,5%, в то время как другой может быть дейтерированным на 75%. Тогда полученное соединение рассматривается как соединение, в котором фактор изотопного обогащения равен, по меньшей мере, 3500 (52,5%).
Термин «изотополог» относится к соединению, которое отличается от конкретного соединения согласно изобретению только изотопным составом. Изотопологи могут отличаться уровнем обогащения изотопов в одном или нескольких положениях и/или положением(ями) изотопного обогащения.
Следует представлять, что термин «соединение», когда относится к соединениям согласно данному изобретению, относится к совокупности молекул, имеющих идентичную химическую структуру, за исключением того, что может иметь место изменение изотопного состава атомов, образующих молекулу. Таким образом, специалисту в данной области техники должно быть понятно, что соединение, представленное конкретной химической структурой и включающее указанные атомы дейтерия, будет также содержать меньшие количества изотопологов, содержащих атомы водорода в одном или нескольких указанных положениях дейтерия в данной структуре. Относительное количество таких изотопологов в соединении согласно настоящему изобретению будет зависеть от ряда факторов, включая изотопную чистоту дейтерированных реагентов, использованных для получения соединения, и эффективности введения дейтерия на различных стадиях синтеза, используемых для получения соединения. Однако, как показано выше, относительное количество таких изотопологов будет составлять менее 47,5% соединения.
Подразумевается также, что термин «соединение» включает любые сольваты или гидраты данного соединения.
Соль соединения согласно настоящему изобретению образуется между кислотной и оснóвной группой соединения, такой как функциональная аминогруппа, или основанием и кислотной группой соединения, такой как функциональная карбоксильная группа. В соответствии с другим вариантом осуществления изобретения соединение представляет собой фармацевтически приемлемую кислотно-аддитивную соль.
Термин «фармацевтически приемлемый», когда используется в данном описании, относится к компоненту, который в пределах области действия стандартной медицинской оценки подходит для использования в контакте с тканями людей и других млекопитающих без избыточной токсичности, раздражения, аллергической реакции и т.п. и обладает приемлемым соотношением «польза/риск». Термин «фармацевтически приемлемая соль» означает любую нетоксичную соль, которая при введении реципиенту способна предоставлять непосредственно или опосредованно соединение согласно настоящему изобретению. Термин «фармацевтически приемлемый противоион» относится к ионной части соли, которая является нетоксичной, когда высвобождается из соли при введении реципиенту.
Кислоты, обычно используемые для получения фармацевтически приемлемых солей, включают неорганические кислоты, такие как сероводородная кислота, хлористоводородная кислота, бромистоводородная кислота, йодистоводородная кислота, серная кислота и фосфорная кислота, а также органические кислоты, такие как пара-толуолсульфоновая кислота, салициловая кислота, винная кислота, аскорбиновая кислота, малеиновая кислота, бензолсульфоновая кислота, фумаровая кислота, глюконовая кислота, глюкуроновая кислота, муравьиная кислота, глутаминовая кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, молочная кислота, щавелевая кислота, пара-бромфенилсульфоновая кислота, угольная кислота, янтарная кислота, лимонная кислота, бензойная кислота и уксусная кислота, а также родственные неорганические и органические кислоты. Следовательно, такие фармацевтически приемлемые соли включают сульфат, пиросульфат, бисульфат, сульфит, бисульфит, фосфат, моногидрофосфат, дигидрофосфат, метафосфат, пирофосфат, хлорид, бромид, йодид, ацетат, пропионат, деканоат, каприлат, акрилат, формиат, изобутират, капрат, гептаноат, пропиолат, оксалат, малонат, сукцинат, суберат, себакат, фумарат, малеат, бутин-1,4-диоат, гексин-1,6-диоат, бензоат, хлорбензоат, метилбензоат, динитробензоат, гидроксибензоат, метоксибензоат, фталат, терефталат, сульфонат, ксилолсульфонат, фенилацетат, фенилпропионат, фенилбутират, цитрат, лактат, β-гидроксибутират, гликолят, малеат, тартрат, метансульфонат, пропансульфонат, нафталин-1-сульфонат, нафталин-2-сульфонат, манделат и другие соли. В одном варианте осуществления изобретения фармацевтически приемлемые кислотно-аддитивные соли включают соли, полученные с минеральными кислотами, такими как хлористоводородная кислота и бромистоводородная кислота, в частности соли, полученные с органическими кислотами, такими как малеиновая кислота.
Для соединений согласно изобретению, включающих -P(O)-(OH)2, -S(O)-OH, -S(O)2-OH, подходящие катионные фрагменты для образования фармацевтически приемлемых солей включают, но без ограничения, щелочные металлы, такие как натрий, калий и литий; щелочноземельные металлы, такие как кальций и магний; другие металлы, такие как алюминий и цинк; аммиак и органические амины, такие как моно-, ди- или триалкиламины; дициклогексиламин; трибутиламин; пиридин; N-метил-, N-этиламин; диэтиламин; триэтиламин; моно-, бис- или трис-(2-гидрокси-низший алкил)амины, такие как моно-, бис или трис-(2-гидроксиэтил)амин, 2-гидрокси-трет-бутиламин или трис-(гидроксиметил)метиламин, N,N-ди-низший алкил-N-(гидрокси низший алкил)амины, такие как N,N-диметил-N-(2-гидроксиэтил)амин или три-(2-гидроксиэтил)амин; N-метил-D-глюкамин; аминокислоты, такие как аргинин, лизин и т.п., и цвиттерионы, такие как глицин и т.п.
Термин «гидрат», когда используется в данном описании, относится к соединению, которое дополнительно включает стехиометрическое или нестехиометрическое количество воды, связанной нековалентными внутримолекулярными силами.
Термин «сольват», когда используется в данном описании, относится к соединению, которое дополнительно включает стехиометрическое или нестехиометрическое количество растворителя, такого как вода, ацетон, этанол, метанол, дихлорметан, 2-пропанол и т.п., связанного нековалентными внутримолекулярными связями.
Заявленные соединения могут существовать в различных стехиометрических формах. Стереоизомеры представляют собой соединения, которые различаются только расположением их атомов в пространстве. Энантиомеры представляют собой пары стереоизомеров, «зеркальные изображения» которых не могут совмещаться при наложении, в большинстве случаев ввиду того, что они содержат асимметрически замещенный атом углерода, который действует как хиральный центр. Термин «энантиомер» относится к одной из пары молекул, которые являются зеркальными изображениями друг друга и не совмещаются при наложении. Диастереомеры представляют собой стереоизомеры, которые не являются «зеркальными изображениями», главным образом, так как они содержат два или несколько асимметрически замещенных атомов углерода. Символы «R» и «S» означают конфигурацию заместителей относительно одного или нескольких хиральных атомов углерода.
Когда стереохимия заявленных соединений названа или представлена структурой, названный или изображенный стереоизомер составляет, по меньшей мере, 60%, 70%, 80%, 90%, 99% или 99,99% из расчета на чистую массу относительно других стереоизомеров. Когда единственный энантиомер назван или представлен структурой, представленный структурой или названный энантиомер является, по меньшей мере, на 60%, 70%, 80%, 90%, 99% или 99,9% оптически чистым. Оптическая чистота, выраженная в процентах по массе, представляет собой отношение массы энантиомера к суммарной массе энантиомера и его оптического изомера.
Когда заявленное соединение названо или представлено структурой без указания стереохимии и содержит, по меньшей мере, один хиральный центр, следует представлять, что название или структура включает один энантиомер соединения, свободный от соответствующего оптического изомера, рацемическую смесь соединения и смеси, обогащенные одним энантиомером относительно соответствующего оптического изомера («скалемические смеси»).
Когда заявленное соединение названо или представлено структурой без указания стереохимии и содержит, по меньшей мере, два хиральных центра, следует представлять, что название или структура включает диастереомер, свободный от других диастереомеров, пару диастереомеров, свободную от других диастереомерных пар, смеси диастереомеров, смеси диастереомерных пар, смеси диастереомеров, в которых один диастереомер обогащен относительно другого(их) диастереомера(ов), и смеси диастереомерных пар, в которых одна диастереомерная пара обогащена относительно другой(их) диастереомерной(ных) пары (пар).
Выражение «по существу свободен от других стереоизомеров», когда используется в описании, означает, что присутствует менее 25% других стереоизомеров, предпочтительно менее 10% других стереоизомеров, более предпочтительно менее 5% других стереоизомеров и наиболее предпочтительно менее 2% других стереоизомеров или менее «Х»% других стереоизомеров (где Х представляет собой число в интервале от 0 до 100).
Термин «стабильные соединения», когда используется в данном описании, относится к соединениям, которые обладают стабильностью, достаточной для их производства, и которые сохраняют целостность в течение достаточного периода времени для того, чтобы применяться для целей, подробно описанных далее (например, для введения в терапевтические препараты, получения промежуточных продуктов для применения при получении соединений, обладающих терапевтическими свойствами, для выделения или хранения промежуточных продуктов, для лечения заболевания или состояния, чувствительного к терапевтическим средствам).
Символ «D» относится к дейтерию. Термин «стереоизомер» относится как к энантиомерам, так и диастереомерам. Приставка «трет»-, символы «t» и «t-» означают «третичный». Аббревиатура «США» означает Соединенные Штаты Америки. Аббревиатура “FDA” означает Управление по контролю за продуктами и лекарствами. Аббревиатура “NDA” означает Заявку на новое лекарственное средство.
Термин «необязательно замещенный» относится к возможной замене одного или нескольких атомов водорода другим фрагментом. За исключением особо оговоренных случаев, любой атом водорода, включая концевые атомы водорода, может быть необязательно заменен.
Термин «галоген» относится к любому элементу из -Cl, -F, -Br или -I.
Термин «оксо» относится к группе =О.
Термин «алкокси» относится к -О-алкилу.
Термин «алкиламино» относится к -NH-алкилу.
Термин «диалкиламино» относится к N(алкил)алкилу, где два алкильных фрагмента являются одинаковыми или различающимися.
Термин «алкил» относится к прямым или разветвленным алкильным цепям, содержащим от 1 до 12 атомов углерода, предпочтительно от 1 до 8 атомов углерода, более предпочтительно от 1 до 4 атомов углерода, если не указано иного. Примеры алкильных групп с прямой или разветвленной цепью включают метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил, пентил, гексил, гептил и октил. Алкил может быть необязательно замещенным.
Алкильная или арильная группы, которые являются необязательно замещенными, обычно будут содержать от одного до четырех заместителей, которые выбраны независимо. Примеры необязательных заместителей включают С1-7 алкил, галоген, цианогруппу, гидроксильную группу, карбоксигруппу, алкоксигруппу, оксогруппу, аминогруппу, алкиламиногруппу, диалкиламиногруппу, гетероциклоалкил, алкилгетероциклоалкил, арил, алкиларил, гетероарил и алкилгетероарил.
Термин «гетероциклоалкил» относится к неароматической моноциклической, бициклической, трициклической, спироциклической или тетрациклической кольцевой системе, которая включает один или несколько гетероатомов, таких как атом азота, атом кислорода или атом серы, по меньшей мере, в одном из циклов. Каждый цикл может быть четырех-, пяти-, шести-, семи- или восьмичленным. Примеры таких гетероциклоалкилов включают тетрагидрофурил, тетрагидротиофенил, морфолино, тиоморфолино, пирролидинил, пиперазинил, пиперидинил и тиазолидинил, а также циклические формы сахаров.
Термин «алкилгетероциклоалкил» относится к гетероциклоалкильной группе, включающей алкильный заместитель. Примеры алкилгетероциклоалкилов включают 4-метилпиперазин-1-ил и 4-метилпиперидин-1-ил.
Термин «арил» относится к карбоциклическим ароматическим группам, таким как фенил и нафтил.
Термин «алкиларил» относится к арильной группе, связанной с основной частью молекулы через алкильную цепь.
Термин «гетероарил» относится к моноциклическим ароматическим группам, содержащим в цикле один или несколько гетероатомов, таких как атом азота, атом кислорода или атом серы, и включает имидазолил, тиенил, фурил, пиридил, пиримидил, пиранил, пиразолил, пирролил, пиразинил, тиазолил, оксазолил и тетразолил. Гетероарильные группы включают также конденсированные полициклические ароматические кольцевые системы, в которых, по меньшей мере, один цикл включает один или несколько гетероатомов, таких как атом азота, атом кислорода или атом серы. Примеры гетероарильных групп включают бензотиенил, бензофурил, индолил, хинолинил, бензотиазол, бензоксазол, бензимидазол, хинолинил, изохинолинил и изоиндолил.
Термин «алкилгетероарил» относится к гетероарильной группе, связанной с основной частью молекулы через алкильную цепь.
Термин «остаток α-аминокислоты» относится к группе общей формулы -С(О)-CHR-NH- и включает остаток природных и синтетических аминоксилот с D- или L-конфигурацией.
За исключением особо оговоренных случаев термин «α-аминокислота» включает α-аминокислоты с (D)-, (L)- или рацемической (D,L)-конфигурацией. Следует представлять, что когда переменная R8 представляет собой α-аминокислоту, она связана с остальной частью молекулы через атом углерода карбонильной группы, непосредственно связанный с α-углеродом аминокислоты. Согласно структуре формулы I такая связь приводит к образованию сложного эфира.
В данном описании переменная может обозначаться общим символом (например, «каждый R») или может обозначаться более точно (например, R1, R2, R3 и т.д.). За исключением особо оговоренных случаев считается, что указанное обозначение включает все специфические варианты осуществления данной конкретной переменной.
Соединения согласно изобретению представляют собой соединения, представленные формулой А:
(А)
или их соль, гидрат или сольват,
где
каждый из R1a и R1b независимо выбран из С1-С3 алкила, в котором один или несколько атомов водорода необязательно заменен(ы) атомом дейтерия;
каждый из R2 и R3 независимо выбран из изопропила, втор-бутила и трет-бутила, где один или несколько атомов водорода в изопропиле, втор-бутиле или трет-бутиле заменен(ы) атомом дейтерия;
R4 выбран из Н, ОН и -О-(CR6R7-O)n-R8;
R5 выбран из Н и -О-(CR6R7-O)n-R8, где
каждый из R6 и R7 независимо выбран из Н, С1-С6 алкила, С2-С6 алкенила, С2-С6 алкинила и С3-С7 циклоалкила, или
R6 и R7 вместе с атомом углерода, к которому они присоединены, образуют 3-7-членный циклоалкил;
каждый R8 независимо выбран из -C(O)H, -C(O)-(C1-C7 алкила), -P(O)-(OH)2, -S(O)-OH, -S(O)2-OH и A-R11, где
А представляет собой остаток α-аминокислоты; и
R11 выбран из С1-С6 алкила, -С(О)-(С1-С7 алкила), А-R12,
где R12 выбран из Н, С1-С6 алкила и -С(О)-(С1-С7 алкила); и
n равно 0 или 1;
где любой алкил в R5 является необязательно замещенным;
каждый Y1a и Y1b независимо выбран из Н и D;
R9 выбран из 2-тиенила, 3-тиенила, тиазол-5-ила, тиазол-2-ила, пиридин-2-ила, пиридин-3-ила, пиридин-4-ила, пиразин-2-ила, 2-метил-2Н-тетразол-5-ила, 2-(d 3-метил)-2Н-тетразол-5-ила, 1-метил-1Н-тетразол-5-ила и 1-(d 3-метил)-1Н-тетразол-5-ила; и
по меньшей мере, одна из переменных R1a, R1b, R2, R3 или Y содержит атом дейтерия.
Конкретные варианты осуществления формулы А включают соединения, где
а) один или оба из R2 и R3 содержат атом дейтерия;
b) каждый из R2 и R3 независимо выбран из -C(CH3)3, -C(CD3)3, -CH(CH3)2, -CD(CD3)2, -CH2CH2(CH3)2 и -CD2CD2(CD3);
с) один или оба из R1a и R1b содержат атом дейтерия;
d) каждый из R1a и R1b независимо выбран из -CH3, -CD3, -CH2CH3, -CD2CD3, -CD2CD2CD3 и -CH2CH2CH3;
е) R5 представляет собой H, P(O)-(OH)2, -CH2-O-P(O)-(OH)2 или их фармацевтически приемлемую соль;
f) R2 выбран из -C(CD3)3, -CD(CD3)2 и -CD2CD2(CD3)2; или
g) имеют место одновременно два или несколько из параметров, описанных в пунктах а)-f), представленных выше.
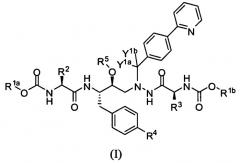
В одном варианте осуществления изобретения соединения согласно изобретению представляют собой соединения формулы I:
или их фармацевтически приемлемую соль, где:
каждый из R1a и R1b независимо выбран из CH3, CH2D, CHD2 и CD3;
каждый из R2 и R3 независимо представляет собой -С(СН3)3, где от 1 до 9 атомов водорода необязательно заменены атомом дейтерия;
R4 выбран из Н, ОН и -О-(CR6R7-O)n-R8;
R5 выбран из Н и -(CR6R7-O)n-R8, где:
R6 и R7 независимо выбраны из Н и С1-С3 алкила;
каждый R8 независимо выбран из α-аминокислоты, -C(O)H, -C(O)-(C1-C7 алкила), где указанный C1-C7 алкил является необязательно замещенным, -P(O)-(OH)2 и -S(O)-OH;
n равно 0 или 1;
Y1a и Y1b независимо выбраны из Н и D; и
по меньшей мере, одна из переменных R1a, R1b, R2, R3 или Y содержит атом дейтерия.
Конкретные варианты соединений формулы I включают соединение, где:
i. каждый из R1a и R1b независимо выбран из СН3 и CD3;
ii. каждый из R2 и R3 независимо выбран из -С(СН3)3 и -C(CD3)3;
iii. R2 представляет собой -С(СD3)3;
iv. Y1a и Y1b являются одинаковыми;
v. каждый из Y1a и Y1b представляет собой дейтерий;
vi. R4 выбран из Н и -O-(CR6R7-O)n-R8;
vii. R4 и R5 одновременно представляют собой Н;
viii. каждый R6 и каждый R7 представляет собой Н;
ix. каждый R8 независимо выбран из α-аминокислоты с (L)-конфигурацией; -С(О)Н; -С(О)-(С1-С3 алкила), где указанный С1-С3 алкил является необязательно замещенным цианогруппой, гидроксильной группой, карбоксигруппой, алкоксигруппой, аминогруппой, алкиламиногруппой, диалкиламиногруппой, гетероциклоалкилом, алкилгетероциклоалкилом, арилом, алкиларилом, гетероарилом и алкилгетероарилом; -Р(О)-(ОН)2; или соли -Р(О)-(ОН)2, где катион выбран из Na+, Mg2+ или аммония; -S(O)-OH; и соли -S(O)-OH, где катион выбран из Na+, Mg2+ или аммония;
х. каждый R8 независимо выбран из L-серина, L-лизина, L-тирозина, L-валина, L-глутаминовой кислоты, L-аспаргиновой кислоты, L-3-пиридилаланина, L-гистидина, -С(О)Н, -С(О)-(С1-С3 алкила), -C(O)CH2OCH3; -C(O)CH2CH2OCH3; -C(O)CH2CH2C(O)OH; -C(O)CH2CH2NH2; -С(О)СН2СН2NHCH3; -C(O)CH2CH2N(CH3); ; ; ; -Р(О)-(ОН)2; соли -Р(О)-(ОН)2, где катион выбран из Na+, К+ или Са2+; -S(O)-OH; и соли -S(O)-OH, где катион выбран из Na+, К+ или Са2+; или
xi. в соединении присутствуют два или несколько параметров i.-x.
Примеры вариантов осуществления изобретения, где встречаются два или несколько из указанных выше параметров, включают, но без ограничения, следующие конкретные варианты осуществления изобретения.
В одном конкретном варианте осуществления R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3, и R1a и R1b независимо выбраны из СН3 и CD3.
В другом конкретном варианте осуществления изобретения R2 представляет собой -C(CD3)3, и R1a представляет собой CD3.
В еще одном конкретном варианте осуществления изобретения R2 представляет собой -C(CD3)3, R1a представляет собой CD3, и R1b представляет собой CD3.
В еще одном варианте осуществления изобретения Y1a и Y1b являются одинаковыми (т.е. оба одновременно представляют собой дейтерий или одновременно представляют собой Н), и либо каждый из R1a и R1b независимо выбран из СН3 и CD3, либо R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3. В более точно определенном варианте осуществления Y1a и Y1b являются одинаковыми (например, оба представляют собой дейтерий), R1a и R1b независимо выбраны из СН3 и CD3, и R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3.
В еще одном более точно определенном варианте осуществления изобретения R4 выбран из Н и -O-(CR6R7-O)n-R8; и либо R1a и R1b независимо выбраны из СН3 и CD3, либо R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3. В более точно определенном варианте осуществления R4 выбран из Н и -O-(CR6R7-O)n-R8; R1a и R1b независимо выбраны из СН3 и CD3, R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3.
В еще одном конкретном варианте осуществления изобретения R4 выбран из Н и -O-(CR6R7-O)n-R8; и Y1a и Y1b являются одинаковыми. В более точно определенном варианте осуществления изобретения R4 выбран из Н и -O-(CR6R7-O)n-R8; и Y1a и Y1b представляют собой дейтерий. В еще одном более точно определенном варианте осуществления изобретения R4 выбран из Н и -O-(CR6R7-O)n-R8, Y1a и Y1b являются одинаковыми (т.е. оба одновременно представляют собой дейтерий или одновременно представляют собой Н), и либо R1a и R1b независимо выбраны из СН3 и CD3, либо R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3. В наиболее точно определенном варианте осуществления изобретения R4 выбран из Н и -O-(CR6R7-O)n-R8, Y1a и Y1b являются одинаковыми (т.е. оба одновременно представляют собой дейтерий или одновременно представляют собой Н), R1a и R1b независимо выбраны из СН3 и CD3, и R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3.
В еще одном конкретном варианте осуществления изобретения каждый из R6 и R7 представляет собой Н, и либо R1a и R1b независимо выбраны из СН3 и CD3, либо R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3. В более точно определенном варианте осуществления изобретения каждый R6 и R7 представляет собой Н, R1a и R1b независимо выбраны из СН3 и CD3, и R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3.
В еще одном конкретном варианте осуществления изобретения каждый из R6 и R7 представляет собой Н, и Y1a и Y1b являются одинаковыми. В более точно определенном варианте осуществления изобретения каждый из R6 и R7 представляет собой Н, и Y1a и Y1b представляют собой дейтерий. В еще более точно определенном варианте осуществления изобретения каждый из R6 и R7 представляет собой Н, Y1a и Y1b являются одинаковыми (т.е. оба одновременно представляют собой дейтерий или одновременно представляют собой Н), и либо R1a и R1b независимо выбраны из СН3 и CD3, либо R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3. В наиболее точно определенном варианте осуществления изобретения каждый из R6 и R7 представляет собой Н, Y1a и Y1b являются одинаковыми (например, оба представляют собой дейтерий), R1a и R1b независимо выбраны из СН3 и CD3, R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3.
В еще одном конкретном варианте осуществления изобретения каждый из R6 и R7 представляет собой Н, и R4 выбран из Н и -O-(CR6R7-O)n-R8. В более точно определенном варианте осуществления изобретения каждый из R6 и R7 представляет собой Н, R4 выбран из Н и -O-(CR6R7-O)n-R8, и либо R1a и R1b независимо выбраны из СН3 и CD3, либо R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3. В наиболее точно определенном варианте осуществления изобретения каждый из R6 и R7 представляет собой Н, R4 выбран из Н и -O-(CR6R7-O)n-R8, R1a и R1b независимо выбраны из СН3 и CD3, и R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD3)3.
В еще одном конкретном варианте осуществления изобретения каждый из R6 и R7 представляет собой Н, R4 выбран из Н и -O-(CR6R7-O)n-R8, Y1a и Y1b являются одинаковыми. В более точно определенном варианте осуществления изобретения каждый из R6 и R7 представляет собой Н, R4 выбран из Н и -O-(CR6R7-O)n-R8, Y1a и Y1b представляют собой дейтерий. В еще более точно определенном варианте осуществления изобретения каждый из R6 и R7 представляет собой Н, R4 выбран из Н и -O-(CR6R7-O)n-R8, Y1a и Y1b являются одинаковыми (т.е. оба одновременно представляют собой дейтерий или оба одновременно представляют собой Н), и либо R1a и R1b независимо выбраны из СН3 и CD3, либо R2 и R3 независимо выбраны из -С(СН3)3 и -C(CD