Ген, вовлеченный в иммортализацию раковой клетки человека, и его применение
Иллюстрации
Показать всеИзобретение относится к биотехнологии. Описан маркерный ген для определения иммортализации раковой клетки, причем маркерный ген представляет собой полинуклеотид, обладающий последовательностью, по меньшей мере, из 15 последовательных оснований. Представлен способ определения иммортализованной раковой клетки. Описан маркер иммортализации раковой клетки, представляющий собой полипептид. Представлено антитело к описанному маркеру. Описаны реагент для определения иммортализованной раковой клетки, включающий в себя, по меньшей мере, один член, выбранный из группы, состоящей из маркерного гена и антитела. Представлен способ скрининга вещества на супрессию пролиферации иммортализованных раковых клеток. Представлен ингибитор роста иммортализованной раковой клетки, содержащий в качестве активного ингредиента описанный полинуклеотид. Изобретение позволяет определять иммортализованную раковую клетку. 12 н. и 4 з.п. ф-лы, 28 ил., 3 табл., 2 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к гену (определяющему иммортализацию гену), вовлеченному в иммортализацию раковых клеток человека, и к способу, применимому для избирательной терапии рака, нацеленной на иммортализованную раковую клетку, обладающую геном. Более конкретно, настоящее изобретение относится к способу распознавания иммортализованной раковой клетки с использованием определяющего иммортализацию гена в качестве показателя и реагента для распознавания. Кроме того, настоящее изобретение относится к способу для скрининга активного ингредиента избирательного противоракового лекарственного средства (ингибитора роста иммортализованной раковой клетки), нацеленного на иммортализованные раковые клетки, и к противораковому лекарственному средству (ингибитору роста иммортализованной раковой клетки).
УРОВЕНЬ ТЕХНИКИ
Пациенты получают плохой прогноз для солидного рака человека, если не проводить радикального хирургического вмешательства. Это в основном происходит из-за недостаточного эффекта современной химиотерапии. Поскольку существующие химиотерапевтические лекарственные средства в основном влияют на биосинтез нуклеиновых кислот, ДНК, микротрубочки и т.д., так как они ингибируют процесс синтеза от нуклеиновой кислоты до белка, они неминуемо разрушают в дополнение к раковым клеткам здоровые клетки, которые находятся в процессе роста. Недавнее исследование идентифицировало ряд молекул, которые специфически экспрессируются в раковых клетках, и ингибиторы, нацеленные на эти специфические молекулы, могут оказывать минимальное неблагоприятное действие на здоровые клетки. Это преимущество позволяет использовать более высокую дозу лекарственного средства. Однако несмотря на его активное развитие, такое нацеленное на молекулу лекарственное средство обладает следующим главным дефектом. Нацеленное на молекулу лекарственное средство не обязательно обещает конкретный эффект для большинства случаев рака; эффект может сильно меняться для каждого случая. Более того, обычно является сложным точно оценить эффект до введения. Такое сильное изменение для нацеленного на молекулу терапевтического лекарственного средства в каждом случае может происходить из-за того факта, что лекарственное средство направлено на молекулы генов, вовлеченных в канцерогенез или метастазирование. Канцерогенез меняется для различных типов рака и даже в пределах одного и того же рака; таким образом предполагают, что эффект, оказываемый молекулами-мишенями на развитие рака, отличается в каждом случае. В противоположность этому развитие нацеленного на молекулу терапевтического лекарственного средства, которое может обладать универсальным эффектом для множества видов рака, должно стать возможным посредством идентификации молекулы, обладающей универсальным и первичным эффектом для различных типов рака.
У всех позвоночных, включая человека, каждый конец хромосомы содержит простую повторяющуюся последовательность: «TTAGGG» (приблизительно 10 т.п.о. у человека и в несколько раз больше у мышей). Эта концевая последовательность не может до конца воспроизводиться при каждой дупликации ДНК при делении клетки и постепенно укорачивается (из расчета приблизительно 200 оснований у человека). Эта концевая часть названа «теломерой». Когда теломера укорачивается до определенной длины (приблизительно 5 т.п.о. в незлокачественных клетках человека) посредством повторяющихся делений клетки, деление клетки в конечном счете прекращается. Деление клетки снова становится возможным посредством злокачественного перерождения клетки, однако затем когда укорачивание в конечном итоге достигает предельного уровня (приблизительно 2 т.п.о.), клетка погибает. Как описано в непатентном документе 1, обратная транскриптаза «теломеразы» служит для удлинения укороченной теломеры для стабилизации длины теломеры, таким образом продлевая предел делений клетки. Поскольку теломераза не экспрессируется в здоровой клетке, деление клетки для здоровой клетки ограничено несколькими десятками раз. Однако теломераза является высокоэкспрессированной как в способной к размножению клетке, так и в и иммортализованной раковой клетке. Все раковые клетки привыкли рассматривать как иммортализованные; однако, опубликованы сообщения, что некоторые виды клинически выраженного рака не обладают активностью теломеразы (см. непатентные документы 2, 3 и т.д.). Опубликованы также другие сообщения, что вынужденная экспрессия ферментного компонента теломеразы TERT в незлокачественной клетке не приводит к получению раковой клетки (см. непатентный документ 4). Соответственно к настоящему времени злокачественное перерождение и иммортализацию рассматривают как различные феномены:
[Непатентный документ 1] Harley CB, Mutation Res, 256: 271-82, 1991
[Непатентный документ 2] Kim NW et al., Science 266: 2011-5, 1994
[Непатентный документ 3] Hiyama K et al., J Natl Cancer Inst 87: 895-902, 1995
[Непатентный документ 4] Morales CP et al., Nat Genet 21: 115-8, 1999
[Непатентный документ 5] Shay JW, Bacchetti S, Eur J Cancer 33: 787-91, 1997
[Непатентный документ 6] Hiyama K et al., J Immunol 155: 3711-5, 1995
[Непатентный документ 7] Hiyama E et al., Int J Oncol 9: 453-8, 1996
[Непатентный документ 8] Forsyth NR et al., Aging Cell 2: 235-43, 2003
[Непатентный документ 9] Bodnar AG et al., Exp Cell Res 228: 58-64, 1996
[Непатентный документ 10] Hiyama K et al., Int J Oncol 27: 87-95, 2005
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Техническая проблема
Настоящее изобретение относится к способу распознавания иммортализованной раковой клетки и к реагенту, применяемому для распознавания. Кроме того, настоящее изобретение относится к способу скрининга активного ингредиента для ингибитора роста иммортализованной раковой клетки, который является применимым в качестве избирательного противоракового лекарственного средства благодаря его эффекту специфической супрессии роста иммортализованной раковой клетки; и к ингибитору роста иммортализованной раковой клетки.
Техническое решение
Чтобы разработать нацеленное на молекулу терапевтическое лекарственное средство, которое является эффективным для лечения рака, особенно лекарственное средство, которое, как ожидают, обладает универсальным эффектом для многих типов рака, авторы настоящего изобретения сфокусировали свое внимание на другом признаке рака - «иммортализации», который отличается от «перерождения в рак (злокачественного изменения)». Конкретно, даже если раковые клетки обнаружены, они не будут распространяться или метастазировать, чтобы погубить хозяина, если их неограниченный рост можно остановить. Супрессия неограниченного роста также увеличивает возможность естественной смерти раковых клеток, при условии, что число оставшихся раковых клеток снижено до некоторой степени посредством химиотерапии или нерадикального хирургического вмешательства, поскольку ожидают, что время деления раковой клетки будет истекать до начала роста следующей клетки. Опубликовано, что эту экспрессию теломеразы наблюдали в 80% или более из нескольких тысяч клинических образцов (см. Непатентный документ 5); экспрессию теломеразы подтверждали при различных типах рака, исследованных до настоящего времени; а также экспрессию теломеразы наблюдали в большинстве штаммов клеток, происходящих из видов рака человека (см. Непатентный документ 2). На основании этих сообщений и известного факта, что раковые клетки с экспрессией теломеразы никогда естественным образом не станут отрицательными снова, феномен иммортализации, по-видимому, существует как универсальный и широко распространенный во многих раковых клетках, в отличие от большого разнообразия канцерогенеза. Соответственно посредством нацеливания на молекулу, которая регулирует иммортализацию, становится возможным супрессировать неограниченный раковый рост с универсальным эффектом для многих типов рака. На основании этого принципа тестировали противораковую стратегию, сфокусированную непосредственно на теломеразе.
Однако авторы настоящего изобретения уже обнаружили, что клетка-предшественник, лимфоцит и т.д., из регенерирующего органа обладает активацией теломеразы даже в нормальной здоровой клетке (см. Непатентные документы 6 и 7). Также известно, что иммортализация клеток не всегда является индуцированной вынужденной экспрессией TERT (ферментный компонент теломеразы) в незлокачественных клетках (см. Непатентный документ 8); и что здоровая клетка-предшественник или лимфоцит, экспрессирующие теломеразу, не являются иммортализованными, но обладают увеличенным временем жизни (см. Непатентные документы 6 и 9). Соответственно такое обнаружение активации теломеразы в здоровых клетках, очевидно, представляет собой просто экспрессию теломеразы, а не иммортализацию клетки. Более конкретно, хотя иммортализация клетки человека по существу требует активации фермента теломеразы, который служит для удлинения теломеры на конце хромосомы, иммортализация является индуцированной не только активацией теломеразы, но также присутствием специфических молекул для иммортализации. Молекулы, по-видимому, функционируют, в частности, в раковых клетках. Фактически, авторы настоящего изобретения подтвердили, что ген, который подвергается специфической экспрессии и изменению в клоне, который был иммортализован вынужденной экспрессией теломеразы посредством введения TERT в здоровые клетки, полностью отличается от опубликованных экспрессии и изменений, наблюдаемых в раковых клетках (см. Непатентный документ 10). Существует другой факт, показывающий, что ген, вовлеченный в иммортализацию здоровых клеток, отличается от гена, вовлеченного в иммортализацию раковых клеток. Если лекарственное средство направлено на теломеразу, оно супрессирует способность к делению лимфоцита, клетки-предшественника крови, клетки крипт слизистой оболочки кишечника и т.д., и таким образом проявляет тенденцию нарушать иммунность, кроветворную способность и функционирование желудочно-кишечного тракта, что, как известно, является неисправимым вредом при лечении рака. Однако если лекарственное средство направлено на определяющий иммортализацию фактор, который действует только в раковых клетках, становится возможным блокировать специфическую неограниченную пролиферацию раковых клеток без разрушения здоровых клеток организма/клеток-предшественников, обладающих активностью теломеразы.
На основании этой теории авторы настоящего изобретения провели интенсивное исследование для обнаружения генов, которые являются универсально вовлеченными в иммортализацию раковых клеток человека. В результате исследования авторы настоящего изобретения в конечном итоге поняли, что эти гены не являются вовлеченными в увеличение продолжительности жизни клеток в результате активации теломеразы в здоровых клетках, но являются специфически вовлеченными в постоянную пролиферацию раковых клеток. Затем авторы изобретения идентифицировали тринадцать определяющих иммортализацию генов (Таблица 1) следующим образом. Сначала гены с универсальной экспрессией и усилением в различных типах рака выделяли анализом на микрочипах. Среди полученных генов выбрали тринадцать видов генов на основании их более сильной экспрессии в органе с клиническим раком, состоящем из иммортализованных раковых клеток, чем экспрессия в раковой ткани, состоящей из неиммортализованных раковых клеток и на основании того, что они не подвергаются экспрессии или повышению уровня в здоровых клетках, экспрессирующих теломеразу посредством ее введения. Затем авторы изобретения подтвердили, что супрессия экспрессии тринадцати генов с использованием миРНК супрессирует пролиферацию иммортализованных раковых клеток.
Далее авторы настоящего изобретения провели более подробное исследование на основании вышеуказанной теории и в конечном итоге завершили настоящее изобретение. Конкретно настоящее изобретение включает в себя следующие формы.
Пункт 1. Маркерный ген для определения иммортализации раковой клетки, причем маркерный ген содержит полинуклеотид, обладающий последовательностью, по меньшей мере, из 15 оснований, которая специфически гибридизуется с непрерывной последовательностью, по меньшей мере, из 15 оснований внутри любой из последовательностей оснований, представленных SEQ ID NO:1-13.
Пункт 2. Маркерный ген по пункту 1, где маркерный ген представляет собой зонд или праймер.
Пункт 3. Способ определения иммортализованной раковой клетки, включающий в себя стадии:
(1) связывания маркерного гена по п.1 или 2 с РНК, приготовленной из биологического образца, который является выделенным из тестируемого субъекта и который может содержать раковую клетку, или с производным РНК;
(2) измерения количества РНК или производного, связанных с маркерным геном, с использованием маркерного гена в качестве показателя; и
(3) сравнения количества РНК или ее производного, обнаруженных на стадии (2) (в общем обозначаемого как «количество РНК» здесь и далее), с количеством (в общем обозначаемым как «сравнительное количество РНК» здесь и далее) соответствующей РНК или ее производного в неиммортализованной здоровой или раковой клетке.
Пункт 4. Способ определения иммортализованной раковой клетки по пункту 3, дополнительно включающий в себя стадию:
(4) определения, что раковая клетка тестируемого субъекта является иммортализованной, когда количество РНК, обнаруженное на стадии (2), выше, чем сравнительное количество РНК, и определения, что раковая клетка тестируемого субъекта не является иммортализованной, когда количество РНК, обнаруженное на стадии (2), не превышает сравнительное количество РНК.
Пункт 5. Антитело для распознавания полипептида, обладающего любой из аминокислотных последовательностей, представленных SEQ ID NO:14-26. Антитело является пригодным для применения для определения иммортализованной раковой клетки.
Пункт 6. Способ определения иммортализованной раковой клетки, включающий в себя стадии:
(1') связывания содержащей белок фракции, содержащей полипептид, полученной из биологического образца, который является выделенным из тестируемого субъекта и который может содержать раковую клетку с антителом по пункту 5;
(2') измерения количества полипептида, связанного с антителом, с использованием антитела в качестве показателя; и
(3') сравнения количества (в общем обозначаемого как «количество полипептида» - здесь и далее) полипептида, обнаруженного на стадии (2'), с количеством (в общем обозначаемым как «сравнительное количество полипептида» - здесь и далее) соответствующего полипептида в неиммортализованной здоровой или раковой клетке.
Пункт 7. Способ определения иммортализованной раковой клетки по пункту 6, дополнительно включающий в себя стадию:
(4') определения, что раковая клетка тестируемого субъекта является иммортализованной, когда количество полипептида, обнаруженного на стадии (2'), выше, чем сравнительное количество полипептида, и определения, что раковая клетка тестируемого субъекта не является иммортализованной, когда количество полипептида, обнаруженное на стадии (2'), не превышает сравнительное количество полипептида.
Пункт 8. Набор реагентов для определения иммортализованной раковой клетки, включающий в себя, по меньшей мере, один член, выбранный из группы, состоящей из маркерного гена по пункту 1 и антитела по пункту 5.
Пункт 9. Способ скрининга вещества на супрессию пролиферации иммортализованных раковых клеток, включающий в себя стадии:
(A) приведения тестируемого материала в контакт с клеткой, которая может экспрессировать один из определяющих иммортализацию генов, представленных SEQ ID NO:1-13;
(B) измерения уровня экспрессии определяющего иммортализацию гена в клетке, приведенной в контакт с тестируемым материалом;
(C) сравнения уровня экспрессии определяющего иммортализацию гена, обнаруженного на стадии (B), с уровнем экспрессии (в общем обозначаемым как «сравнительный уровень экспрессии» - здесь и далее) определяющего иммортализацию гена в клетке, не находящейся в контакте с тестируемым материалом; и
(D) выбора тестируемого материала в качестве вещества-кандидата для супрессии пролиферации иммортализованных раковых клеток, когда уровень экспрессии, обнаруженный на стадии (B), ниже, чем сравнительный уровень экспрессии.
Пункт 10. Способ скрининга вещества на супрессию пролиферации иммортализованных раковых клеток, включающий в себя стадии:
(A') приведения тестируемого материала в контакт с полипептидом, обладающим одной из аминокислотных последовательностей, представленных SEQ ID NO:14-26;
(B') измерения активности полипептида, обладающего одной из аминокислотных последовательностей, представленных SEQ ID NO:14-26, приведенного в контакт с тестируемым материалом;
(C') определения степени активности полипептида, обнаруженной на стадии (B'), путем сравнения активности полипептида, обнаруженной на стадии (B'), с активностью (в общем обозначаемой как «сравнительная активность» - здесь и далее) полипептида, не находящегося в контакте с тестируемым материалом; и
(D') выбора тестируемого материала в качестве вещества-кандидата для супрессии пролиферации иммортализованных раковых клеток, когда активность полипептида, обнаруженная на стадии (B'), ниже, чем сравнительная активность.
Пункт 11. Ингибитор роста иммортализованной раковой клетки, содержащий в качестве активного ингредиента полинуклеотид, обладающий последовательностью, по меньшей мере, из 15 оснований, которая специфически гибридизуется с непрерывной последовательностью, по меньшей мере, из 15 оснований внутри любой из последовательностей оснований, представленных SEQ ID NO:1-13.
Пункт 12. Ингибитор роста иммортализованной раковой клетки по пункту 11, где полинуклеотид обладает одной из последовательностей оснований, представленных SEQ ID NO:27-76.
Пункт 13. Способ противоракового лечения, включающий в себя стадию введения ингибитора роста иммортализованной раковой клетки по пункту 11 или 12 в раковые клетки пациента.
Пункт 14. Применение полинуклеотида, обладающего последовательностью, по меньшей мере, из 15 оснований, которая специфически гибридизуется с непрерывной последовательностью, по меньшей мере, из 15 оснований внутри одной из последовательностей оснований, представленных SEQ ID NO:1-13, для получения ингибитора роста иммортализованной раковой клетки.
Пункт 15. Применение по пункту 14, где полинуклеотид обладает одной из последовательностей оснований, представленных SEQ ID NO:27-76.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
По настоящему изобретению выявили гены, которые универсальным образом определяют иммортализацию многих различных раковых клеток. Гены обладают специфически повышенной экспрессией в иммортализованных раковых клетках при множестве видов рака. Настоящее изобретение относится к способу распознавания иммортализованных раковых клеток и к реагенту, который применяют для способа распознавания, который позволяет измерение уровня экспрессии определяющих иммортализацию генов. По отношению к измеренному уровню становится возможным отличить иммортализованные раковые клетки от клеток с ограниченным числом делений. Это разделение никогда не являлось возможным при общепринятых общих патологических диагнозах. Таким образом разделение обладает большим потенциалом для клинического применения, которое является применимым для ранней диагностики, новых возможностей лечения, прогнозирования и т.п. для различных видов рака.
Кроме того, с помощью способа скрининга, нацеленного на определяющий иммортализацию ген, по настоящему изобретению получают активный ингредиент противоракового лекарственного средства, специфически супрессирующего пролиферацию иммортализованных раковых клеток.
НАИЛУЧШИЙ СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
(I) Определяющий иммортализацию ген
По настоящему изобретению термин «неиммортализованные раковые клетки» относится, среди раковых клеток вообще, к клеткам с ограниченным числом делений, обладающим (1) отсутствием активации теломеразы, (2) сниженной длиной теломеры и (3) не поддающейся детекции экспрессией белка теломеразы. Кроме того, по настоящему изобретению термин «иммортализованная раковая клетка» относится к клетке, в которой отсутствует по меньшей мере одно из вышеупомянутых условий; более конкретно, к клетке, обладающей активацией теломеразы, к клетке, обладающей увеличенной длиной теломеры, и/или к клетке с поддающейся детекции экспрессией белка теломеразы. Такая «иммортализованная раковая клетка» является способной к неограниченной пролиферации клетки.
По настоящему изобретению термин «определяющий иммортализацию ген» относится к гену, который определяет иммортализацию раковых клеток.
Настоящее изобретение не ограничивает конкретно тип раковой клетки в качестве мишени и относится к клеткам, происходящим, например, из рака легкого, рака молочной железы, рака пищевода, рака головы и шеи, рака желудка, рака толстого кишечника, рака прямой кишки, рака печени, рака желчного пузыря и желчных протоков, рака поджелудочной железы, рака мочевого пузыря, рака предстательной железы или карциномы шейки матки.
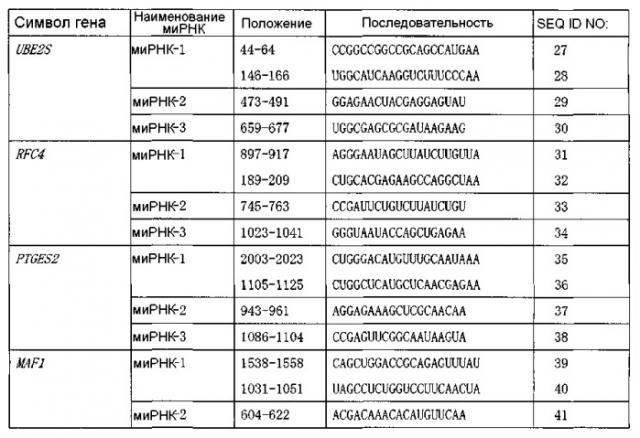
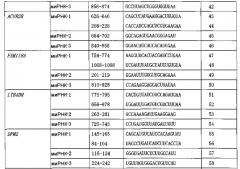
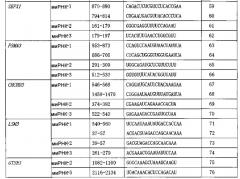
Определяющими иммортализацию генами являются конкретно (1) ген UBE2S, (2) ген RFC4, (3) ген PTGES2, (4) ген MAF1, (5) ген ACVR2B, (6) ген FAM119A, (7) ген LTB4DH, (8) ген DPM2, (9) ген SEPX1, (10) ген PSMA3, (11) ген CHCHD3, (12) ген LSM3 и (13) ген GTSE1. В таблице 1 показаны регистрационный номер в GenBank, официальное наименование гена и символ гена, и SEQ ID NO:, обозначающие последовательности оснований генов. В таблице 1 наименование гена, символ гена и т.д. основаны на данных NCBI, описанных в Интернет (http://www.ncbi.nlm.nih.gov/).
| Таблица 1 | |||
| SEQ ID NO: | Регистрационный № в GenBank | Наименование гена | Символ гена |
| 1 | NM_014501 | присоединяющий убиквитин фермент E2S | UBE2S |
| 2 | NM_002916 | фактор репликации C (активатор 1) 4, 37 кДа | RFC4 |
| 3 | NM_025072 | простагландин E-синтаза 2 | PTGES2 |
| 4 | NM_032272 | гомолог MAF1 (S. cerevisiae) | MAF1 |
| 5 | NM_001106 | рецептор активина A, тип IIB | ACVR2B |
| 6 | NM_145280 | семейство со сходством последовательностей 119, член A | FAM119A |
| 7 | NM_012212(D49387, BQ214856) | 12-гидроксидегидрогеназа лейкотриена B4 | LTB4DH |
| 8 | NM_003863 | полипептид 2 маннозилтрансферазы долихилфосфата, регуляторная субъединица | DPM2 |
| 9 | NM_016332 | селенопротеин X, 1 | SEPX1 |
| 10 | NM_002788 | субъединица протеасомы (просомы, macropain), типа альфа, 3 | PSMA3 |
| 11 | NM_017812 | домен, содержащий двойную спираль-спираль-двойную спираль-спираль 3 | CHCHD3 |
| 12 | NM_014463 | гомолог LSM3, связанный с малой ядерной РНК U6 (S. cerevisiae) | LSM3 |
| 13 | NM_016426 | экспрессирующийся в G-2 и S-фазе 1 | GTSE1 |
Как показано в примере 1, перечисленные выше определяющие иммортализацию гены все являются высокоэкспрессированными в иммортализованных раковых клетках, полученных из множества видов рака, включая рак легкого, рак пищевода и рак молочной железы. Как показано в примере 2, когда экспрессию этих тринадцати генов супрессировали посредством миРНК в иммортализованных раковых клетках, в каждом случае пролиферация иммортализованных раковых клеток являлась супрессированной. Это показывает, что тринадцать определяющих иммортализацию генов определяют иммортализацию раковых клеток (определяющий иммортализацию ген).
(II) Реагент для оценки иммортализации раковых клеток (маркерный ген)
Как описано выше, определяющие иммортализацию гены ((1)-(13)), обладающие последовательностями оснований, представленными SEQ ID NO:1-13, все обладают сильной экспрессией, специфической для иммортализованных раковых клеток. Таким образом, с использованием тринадцати генов в качестве маркерных генов можно оценивать иммортализацию/смертность раковых клеток.
Настоящее изобретение относится к определяющему иммортализацию маркерному гену (сокращенному как «маркерный ген» по настоящему изобретению) в качестве средства (реагента), которое подходящим образом используют для оценки иммортализации раковых клеток. Маркерный ген конструируют как полинуклеотид по меньшей мере из 15 оснований, который специфически гибридизуется с непрерывной последовательностью, по меньшей мере, из 15 оснований среди одной из последовательностей оснований, определяющих иммортализацию генов, представленных SEQ ID NO:1-13. Маркерный ген по настоящему изобретению может обладать произвольной формой в соответствии с объектом и может представлять собой любое из одноцепочечной ДНК, одноцепочечной РНК, двухцепочечной ДНК, двухцепочечной РНК и гибрида ДНК:РНК.
Маркерный ген содержит зонд или праймер, применимый для детекции возникновения экспрессии определяющего иммортализацию гена и/или уровня (уровня экспрессии) в раковых клетках, чтобы позволять распознавание иммортализованных раковых клеток. Кроме того, проба или праймер является также применимой в качестве средства (реагента для детекции) для детекции изменения экспрессии определяющего иммортализацию гена для скрининга материала, супрессирующего пролиферацию иммортализованных раковых клеток.
(II-1) Зонд
Иммортализацию раковых клеток распознают посредством детекции по меньшей мере одного из вышеупомянутых определяющих иммортализацию генов: (1) гена UBE2S, (2) гена RFC4, (3) гена PTGES2 и (4) гена MAF1, (5) гена ACVR2B, (6) гена FAM119A, (7) гена LTB4DH, (8) гена DPM2, (9) гена SEPX1, (10) гена PSMA3, (11) гена CHCHD3, (12) гена LSM3 и (13) гена GTSE1, которые обладают сильной экспрессией, специфической для иммортализованных раковых клеток.
При детекции определяющих иммортализацию генов в качестве зондов используют полинуклеотиды, каждый из которых специфически гибридизуется с последовательностью оснований одного из вышеупомянутых определяющих иммортализацию генов. По настоящему изобретению олигонуклеотид, обладающий последовательностями множества оснований, включен в разряд «полинуклеотид».
Каждый полинуклеотид сконструирован, чтобы специфически гибридизоваться с непрерывной последовательностью оснований одного из определяющих иммортализацию генов. Более конкретно, для каждого из вышеупомянутых определяющих иммортализацию генов соответствующий полинуклеотид специфически гибридизуется с непрерывными основаниями, по меньшей мере, 15 основаниями, предпочтительно, 20 основаниями, и более предпочтительно, 30 основаниями из общей длины оснований определяющего иммортализацию гена. Соответственно каждый полинуклеотид обладает длиной в основаниях, соответствующей определенной длине в основаниях.
На протяжении настоящего описания и формулы изобретения «специфическая гибридизация» относится к гибридизации, где образуется только специфический гибрид и не образуется неспецифического гибрида в строгих условиях гибридизации. Строгие условия гибридизации определяют обычным образом, например, на основании температуры плавления (Tm) нуклеиновой кислоты, при которой образуется гибрид. Типичные условия отмывки для обеспечения состояния гибридизации представляют собой приблизительно «1×SSC, 0,1% SDS, 37°C», более строгие «0,5×SSC, 0,1% SDS, 42°C», и еще более строгие «0,1×SSC, 0,1% SDS, 65°C».
Полинуклеотид (зонд) предпочтительно обладает последовательностью оснований, которая является комплементарной непрерывной последовательности, по меньшей мере, из 15 оснований из определяющего иммортализацию гена; однако зонд не всегда должен являться полностью комплементарным указанной непрерывной последовательности оснований, при условии, что специфическая гибридизация является возможной. Полинуклеотид обладает идентичностью, по меньшей мере, 70%, предпочтительно, не менее, чем 80%, более предпочтительно, не менее, чем 90%, еще более предпочтительно, не менее, чем 95%, и еще более предпочтительно, не менее, чем 98%, по отношению либо к полинуклеотиду, обладающему непрерывными основаниями по меньшей мере из 15 оснований внутри последовательности оснований определяющего иммортализацию гена, либо к комплементарному ему полинуклеотиду. Идентичность каждой последовательности оснований можно вычислить посредством поиска идентичности, программы выравнивания, BLAST, FASTA, ClustalW или подобных.
Примеры зондов, подходящих по настоящему изобретению, включают в себя олигонуклеотиды и полинуклеотиды, обладающие непрерывной последовательностью из 15 оснований, предпочтительно, 20 оснований, и более предпочтительно, 30 оснований из определяющего иммортализацию гена, который гибридизуется по меньшей мере с одним полинуклеотидом (однако когда полинуклеотид представляет собой РНК, основание «t» в последовательности заменено на «u»), выбранные из группы, состоящей из следующего (1)-(13):
(1) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:1) гена UBE2S.
(2) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:2) гена RFC4.
(3) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:3) гена PTGES2.
(4) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:4) гена MAF1.
(5) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:5) гена ACVR2B.
(6) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:6) гена FAM119A.
(7) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:7) гена LTB4DH.
(8) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:8) гена DPM2.
(9) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:9) гена SEPX1.
(10) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:10) гена PSMA3.
(11) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:11) гена CHCHD3.
(12) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:12) гена LSM3.
(13) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:13) гена GTSE1.
Эти полинуклеотиды (зонды) можно получать известным способом, например, с использованием коммерчески доступного синтезатора нуклеотидов, на основании последовательности оснований - мишени из определяющего иммортализацию гена. Полинуклеотиды (зонды) можно получать также способом ПЦР с использованием последовательности оснований - мишени из определяющего иммортализацию гена в качестве матрицы.
Более предпочтительно, для упрощения детекции определяющих иммортализацию генов каждый зонд можно метить радиоактивным материалом, флуоресцентным материалом, химическим люминесцентным веществом или ферментом (описанными позднее более подробно).
Кроме того, каждый зонд можно иммобилизовать на любой твердой фазе перед использованием.
Соответственно зонды, подходящие для настоящего изобретения, включают в себя зонд, в котором вышеупомянутый полинуклеотид иммобилизован на твердой фазе (например, иммобилизованный зонд, включая генный чип, микрочип кДНК, чип олиго-ДНК, или мембранный фильтр). Этот зонд является пригодным для чипа ДНК для использования для детекции определяющего иммортализацию гена, или более конкретно, для использования для детекции иммортализованной раковой клетки.
Твердая фаза иммобилизованного зонда (полинуклеотида) не является конкретно ограниченной, при условии, что она иммобилизует полинуклеотид. Примеры твердых фаз включают в себя стеклянную пластину, нейлоновую мембрану, микробусины, кремниевый кристалл, капилляр и другие субстраты. Полинуклеотид можно иммобилизовать на твердой фазе посредством размещения синтетического полинуклеотида на твердой фазе или посредством синтеза полинуклеотида - мишени на твердой фазе. Иммобилизация представляет собой хорошо известный способ в данной области, и можно использовать любой подходящий способ в соответствии с типом иммобилизованного зонда. Например, коммерчески доступное устройство для печати чипов (изготовленное Cosmobio Co., Ltd. и т.д.) часто используют для получения микрочипа ДНК. (Например, синтез полинуклеотида in situ с использованием фотолитографического способа (AFFYMETRIX CO.), или способ распыления (ROSETTA INPHARMATICS CO.)
(II-2) Праймер
Настоящее изобретение относится к полинуклеотиду в качестве праймера, который служит маркерным геном для специфической амплификации области последовательности оснований каждого определяющего иммортализацию гена.
Полинуклеотид, как правило, представляет собой полинуклеотид, который обладает непрерывной последовательностью, по меньшей мере, из 15 оснований, предпочтительно, 15-100 оснований, более предпочтительно, 15-50 оснований, еще более предпочтительно, 15-35 оснований, и который специфически гибридизуется с частью по меньшей мере одного полинуклеотида (однако когда полинуклеотид представляет собой РНК, основание «t» в последовательности заменено на «u»), выбранного из группы, состоящей из следующего (1)-(13), так чтобы амплифицировать часть полинуклеотида или весь полинуклеотид:
(1) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:1) гена UBE2S.
(2) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:2) гена RFC4.
(3) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:3) гена PTGES2.
(4) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:4) гена MAF1.
(5) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:5) гена ACVR2B.
(6) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:6) гена FAM119A.
(7) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:7) гена LTB4DH.
(8) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:8) гена DPM2.
(9) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:9) гена SEPX1.
(10) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:10) гена PSMA3.
(11) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:11) гена CHCHD3.
(12) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:12) гена LSM3.
(13) Полинуклеотид с непрерывной последовательностью, обладающей, по меньшей мере, 15 основаниями из последовательности оснований (SEQ ID NO:13) гена GTSE1.
Как и в случае зонда, каждый из определенных полинуклеотидов (праймеров) предпочтительно обладает последовательностью оснований, комплементарной непрерывной последовательности, по меньшей мере, из 15 оснований в одном из определяющих иммортализацию генов; однако пока возможна специфическая гибридизация, он не должен являться полностью комплементарным. Полинуклеотид обладает идентичностью по меньшей мере 70%, предпочтительно, не менее, чем 80%, более предпочтительно, не менее чем 90%, еще более предпочтительно, не менее чем 95%, и еще более предпочтительно, не менее чем 98%, по отношению либо к полинуклеотиду, обладающему непр