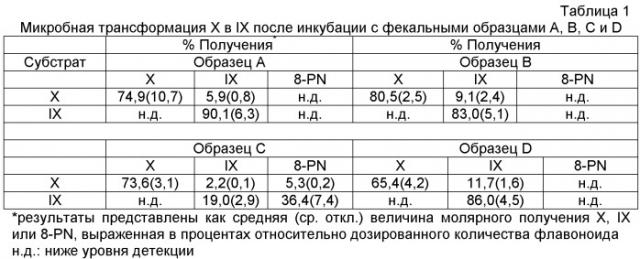
Ферментативное деметилирование флавоноидов
Иллюстрации
Показать всеИзобретение относится к биотехнологии. Способ получения 8-пренилнарингенина in vitro включает: а) предоставление первой композиции, включающей культуру бактериальных клеток вида Eubacterium limosum или вида Peptostreptococcus productus, имеющей 5-алкоксифлавоноид-деалкилирующую активность, и b) приведение в контакт второй композиции, включающей 5-алкоксифлавоноиды, с указанной первой композицией, так чтобы сделать возможным деалкилирование указанных 5-алкоксифлавоноидов с помощью указанной культуры бактериальных клеток. Представлена комбинация для получения 8-пренилнарингенина in vitro и применение культуры бактериальных клеток вида Eubacterium limosum или вида Peptostreptococcus productus имеющей 5-алкоксифлавоноид-деалкилирующую активность, для получения 8-пренилнарингенина in vitro. Способ обогащения 5-алкоксифлавоноид-деалкилирующей активности культуры бактериальных клеток вида Eubacterium limosum или вида Peptostreptococcus productus включает стадию посева указанной культуры бактериальных клеток на среду, включающую 5-алкоксифлавоноиды, и стадию селекции колонии, имеющей наивысшую 5-алкоксифлавоноид-деалкилирующую активность. Штамм Eubacterium limosum LMG Р-23546 имеет 5-алкоксифлавоноид-деалкилирующую активность и способен к превращению изоксантогумола в 8-пренилнарингенин. Изобретение позволяет повысить эффективность получения фитоэкстрагена, такого как 8-пренилнарингенина. 5 н. и 9 з.п. ф-лы, 9 ил., 4 табл., 6 пр.
Реферат
Область техники
Настоящее изобретение относится к фитоэстрогенам и их получению, а также к фармацевтическим композициям и пищевым добавкам, которые включают такие фитоэстрогены.
Уровень техники
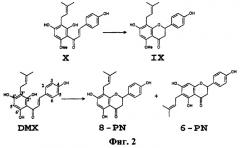
Хмель (Humulus Lupulus L.) применяли веками в качестве основного сырья для пивоварения, которое придавало пиву горьковатый вкус и особый запах. В последние несколько лет это растение привлекло к себе повышенное внимание в качестве источника пренилфлавоноидов, подкласса флавоноидов, содержащих неполярную пренильную боковую цепь, связанную с одним из фенольных колец. Они присутствуют в лупулиновых железах, обнаруженных в основании брактеолей шишек хмеля женского растения. Из этих пренилфлавоноидов наибольшее внимание сейчас привлекают два халкона (ксантогумол (Х) и дезметилксантогумол (DMX)) и три флавонона (изоксантогумол (IX), 8-пренилнарингенин (8-PN) и 6-пренилнарингенин (6-PN)) (Фиг.2) благодаря их потенциальным оздоровительным свойствам. Х идентифицировали как сильный противораковый агент, тогда как для 8-PN было показано, что он является одним из наиболее сильнодействующих фитоэстрогенов, идентифицированных до настоящего времени, со значительно более высокой активностью, чем у хорошо известных соевых фитоэстрогенов. Было продемонстрировано, что 8-PN in vivo проявляет эстрогенную активность, предупреждая потерю костной массы у крыс, ингибируя ангиогенез и метастазирование, а также было показано, что 8-PN проявляет антиандрогенную активность.
Х присутствует в качестве доминирующего пренилхалкона в женских хмелевых шишках в концентрации до 1% (вес./вес.), тогда как DMX присутствует в более низких концентрациях (De Keukeleire et al. (2003) J. of Agric. and Food Chem. 51, 4436-4441). Соотношение X/DMX различается у разных сортов хмеля. Путем изомеризации Х трансформируется в IX, и DMX превращается в 8-PN и 6-PN.
Эстрогенные эффекты хмеля были обнаружены в последние десятилетия. Хмелевые ванны применяли для лечения гинекологических заболеваний, а у женщин, собиравших хмель, часто наблюдались менструальные нарушения. В 1999 году Milligan et al. [J. Clin. Endocrinol. Metab. 84, 2249-2252] идентифицировали новый фитоэстроген хмеля, 8-пренилнарингенин. Хотя он гораздо слабее, чем 17β-эстрадиол (<1%), он является одним из наиболее сильнодействующих фитоэстрогенов, идентифицированных до настоящего времени, со значительно большей активностью, чем у других фитоэстрогенов, полученных из сои, таких как соединения генистеин и даидзеин.
Обсуждалось, действительно ли воздействие эстрогенов из пищи и/или окружающей среды представляет собой фактор риска для здоровья, такой как эндокринное нарушение. В случае хмелевых пренилфлавоноидов пиво является их главным пищевым источником. В Соединенных Штатах в 2001 году среднее потребление пива на человека составило по расчетам примерно 225 мл пива в день (USDA, 2003). Когда предположили, что если бы такое количество потреблялось в виде самого распространенного в США бренда легкого пильзенского пива (500-1000 мкг пренилфлавоноидов/л пива), то ежедневное потребление пренилфлавоноидов составило бы около 0,14 мг. Однако обнаруженные в пиве концентрации (и, таким образом, среднее потребление) сильно зависят от процесса пивоварения, так крепкие сорта пива содержат до 4 мг пренилфлавоноидов/л. Хотя Х представляет собой доминирующий пренилфлавоноид, присутствующий в хмеле (0,1-1% от сухого веса), большая его часть трансформируется в IX путем термической изомеризации в процессе пивоварения. Таким образом, IX является самым распространенным пренилфлавоноидом, обнаруженным в пиве, и присутствует в концентрациях от 500 мкг/л (легкого пильзенского пива) до 4 мг/л (крепкого пива). Подобным образом, DMX превращается в 8-PN, достигая конечных концентраций в пиве до 100 мкг 8-PN/Л. Но, несмотря на высокую активность 8-PN, общая эстрогенная активность в пиве остается в 500-1000 раз меньше, чем концентрация, представляющая опасность с точки зрения in vivo активности (~100 мг/л) (Milligan et al. (2002) Reproduction 123, 235-242). Кроме того, многие сорта пива готовят сейчас с применением экстрактов хмеля вместо цельного хмеля, что обеспечивает пониженные концентрации 8-PN или его полное отсутствие. Таким образом, в основном это согласуется с тем, что, основываясь на современных знаниях, никакие вредные для здоровья эффекты не могут быть обусловлены фитоэстрогенами при среднем потреблении пива.
С другой стороны, сейчас многие данные соотносят преднамеренное потребление фитоэстрогена с возможной пользой для здоровья (Magee & Rowland (2004) Br. J. Nutr. 91, 513-531). Кроме пива, продаются пищевые добавки на основе хмеля с заявлением таких эффектов, как увеличение груди или уменьшение приливов. Все воздействия фитоэстрогенов на здоровье потенциально являются результатом действия комбинации многих индивидуальных фитохимикатов с разнообразными и, возможно, аддитивными или противодействующими активностями. До настоящего момента только изофлавоны и лигнаны считали значимыми фитоэстрогенами в питании человека, особенно потому что концентрации в пиве 8-PN считали слишком низкими для положительных или отрицательных воздействий на здоровье.
Несколько патентных публикаций описывают благотворные воздействия на здоровье пищевых флавоноидов, например, применение IX для предупреждения понижения плотности костной ткани (WO04089359), применение экстрактов хмеля в лекарственных средствах, имеющих эстрогенные свойства (WO02085393), и применение IX или X в пищевых продуктах с заявлением противовоспалительных или антивозрастных свойств (патент WO03090555). Кроме того, также предлагалось применение 8-PN в косметических средствах для ухода за кожей (СА2426467).
Для того чтобы in vivo осуществить воздействия, выявленные in vitro, пищевые флавоноиды должны всосаться из кишечника и достичь своих мишеней без изменений. В основном мономерные флавоноиды проходят без модификаций через желудок в тонкий кишечник, где может происходить всасывание из кишечника в мезентериальную кровеносную систему. Исследования in vitro выявили при всасывании существенную биотрансформацию X в печени (Yilmazer et al. (2001a) FEBS Lett. 491, 252-256) и 8-PN (Nicolic et al. (2004) Drug Metabolism and Disposition 32, 272-279). Однако степень пищевого всасывания полифенолов в тонком кишечнике довольно ограниченная (10-20%), таким образом, предполагается, что большая часть флавоноидов достигает толстой кишки. Нарингенин, не пренилированный аналог 8-PN, продемонстрировал интенсивную микробную биотрансформацию в кишечнике, включая расщепление кольца и дегидроксилирование (Rechner et al. (2004) Free Radic. Biol. Med. 36, 212-225) с последующим всасыванием и мочевыделением. Мало известно о кишечных трансформациях пренилфлавоноидов. Nookandeh et al. (2004) Phytochemistry 65, 561-570, вводили Х крысам по 1000 мг/кг веса тела и выделили 22 метаболита из фекалий. Однако большую часть (89%) из полученных флавоноидов представлял собой не измененный Х. Оставшаяся фракция состояла из малых количеств различных метаболитов, включая некоторое количество IX. Avula et al. (2004) [J. Chromatogr. Sci. 42:378-382] осуществили подобный эксперимент с крысами и обнаружили преимущественно не измененный Х, а также некоторое количество не идентифицированных метаболитов.
Возможность того, что IX может действовать как проэстроген, предположили Coldham et al. (2002) Food Addit. Contam. 19:1138-1147. Предположение было основано на способности печени к разносторонней биотрансформации, которая включает деметилирование. Однако воздействие на IX микросом печени не приводило к увеличению эстрогенной активности, из чего заключили, что 8-PN не производился. Напротив, Nicolic et al. описывают, что микросомы печени могут деметилировать IX, но не X (Nicolic et al. (2005) J. of Mass Spectrom. 40, 289-299). Однако было показано, что кроме деметилирования микросомы также модифицируют боковую пренильную цепь с получением, в конечном счете, большого разнообразия минорных продуктов деградации. Schaefer et al. (2003) (J. Steroid Biochem. Mol. Biol. 84, 359-360) идентифицировали низкий уровень 8-PN в моче двух тестируемых субъектов после перорального потребления IX, и связали этот факт с деметилированием в печени.
Кроме печени, толстая кишка человека также является важным местом трансформации веществ в теле человека. Толстая кишка содержит ~1012 микроорганизмов/см3 (около 400 различных видов) с огромным каталитическим и гидролитическим потенциалом. Важность этого микробного сообщества в метаболизме фитоэстрогенов в основном хорошо изучена. Wang et al. (2000) Chem. Pharm. Bull. 48, 1606-1610, идентифицировали два вида бактерий, ответственных за трансформацию лигнанов, и Decroos et al. (2005) Arch. Microbiol. 183, 45-55, недавно выделили микробный консорциум, способный к трансформации соевого фитоэстрогена даидзеина в эквол. Кроме того, было показано, что биодоступность фитоэстрогенов усиливают некоторые кишечные бактерии, так как они содержат β-глюкозидазы, которые необходимы для гидролиза гликозидов фитоэстрогенов (Rowland et al. (2003) Br. J. Nutr 89, s45-S58). Таким образом, предполагается, что микробиота кишечника является важным фактором для биодоступности фитоэстрогенов (Turner et al. (2003) Nutr. Rev. 61, 204-213).
Так как экономический интерес представляют только присутствующие в женских хмелевых шишках эфирное масло и альфа-кислоты, как важные ингредиенты пивоварения, то были разработаны различные методы экстракции хмеля с целью специфически экстрагировать только эти соединения. С одной стороны, СО2 в настоящий момент является наиболее общепринятым растворителем при производстве экстрактов хмеля (Palmer & Ting (1995) Food Chem. 52, 345-352). По сравнению со способами, в которых применяют традиционные органические растворители (этанол, гексан, метанол или метилен хлорид), СО2-экстракция обеспечивает более селективные экстракты, которые при производстве пива могут применяться в качестве хорошей альтернативы цельному хмелю или хмелевым гранулам. СО2-экстракты образуют основу для большого числа дополнительно выделенных и очищенных продуктов, таких как изо-альфа-кислоты и восстановленные производные. Другой способ для дополнительной очистки СО2-экстрактов путем удаления нежелательных пренилфлавоноидов описан в патенте US3794744.
С другой стороны, различные способы были разработаны для специфического получения и очистки пренилфлавоноидов (главным образом Х). Примеры этих способов экстракции описаны в патенте US 4121040 и в немецком патенте DE19939350. Применяя эти процессы, можно было легко получить ксантогумол, поэтому проявлялся небольшой интерес к разработке способа химического синтеза Х. Однако 8-PN гораздо труднее получить из натуральных экстрактов из-за его низких концентраций, присутствующих в хмелевой шишке. Таким образом, были разработаны стратегии синтеза, чтобы получить 8-PN путем пренилирования коммерчески доступного нарингенина. Сначала 8-PN получили из нарингенина или из флороацетофенона путем малопродуктивного не селективного прямого С-пренилирования. Эффективный мелкомасштабный синтез был выполнен с помощью перегруппировки Кляйзена, катализируемой европием(III) (Gester et al. (2001) Tetrahedron 57, 1015-1018). Недавно в европейском патенте EP1524269 была описана продукция в промышленном масштабе, основанная на этом способе.
Несмотря на всестороннее промышленное применение хмеля и экстрактов хмеля, не существует эффективного способа получения из натурального источника биоактивных пренилированных фитоэстрогенов, таких как 8-PN.
Сущность изобретения
Целью настоящего изобретения является предложение эффективного способа продукции биоактивных пренилированных фитоэстрогенов, таких как 8-PN, из 5-алкоксифлавоноидов, которые могут быть получены из натурального источника, а также предложение фармацевтических композиций и пищевых добавок, в которых используют такие биоактивные пренилированные фитоэстрогены.
В первом аспекте в настоящем изобретении предлагаются композиции, имеющие 5-алкоксифлавоноид-трансферазную (5-AO-FT) и/или 6'-алкоксихалкон-трансферазную (6'-AO-CT) активность. Более конкретно, в изобретении предлагаются композиции, имеющие 5-метоксифлавоноид-трансферазную (5-MO-FMT) и/или 6'-метоксихалкон-трансферазную (6'-MO-CMT) активность. Следующее воплощение настоящего изобретения относится к композициям, способным деалкилировать пренилированные 5-алкоксифлавоноиды и/или пренилированные 6'-алкоксихалконы. В конкретном воплощении настоящего изобретения предлагаются композиции, способные деалкилировать 6'-алкоксихалкон ксантогумол (Х) и/или 5-алкоксифлавоноид изоксантогумол (IX). Таким образом, композиции по настоящему изобретению способны к продукции биоактивных фитоэстрогенов, более конкретно пренилированных фитоэстрогенов, более конкретно 8-PN.
Согласно конкретному воплощению композиции, имеющие 5-алкоксифлавоноид- и/или 6'-алкоксихалкон деалкилирующую активность, представляют собой композиции, включающие или полученные из материала не животного происхождения, более конкретно прокариотического происхождения. Более конкретно композиции по настоящему изобретению включают бактериальные клетки или экстракты, супернатант или другой очищенный или частично очищенный материал таких бактериальных клеток. Конкретное воплощение настоящего изобретения относится к композиции, включающей гомоацетогенную бактерию, такую как Eubacterium sp. или Peptostreptococcus sp., более конкретно Eubacterium limosum или Peptostreptococcus productus или их экстракты, супернатант или другой очищенный или частично очищенный материал на их основе.
Другое конкретное воплощение изобретения включает бактериальные штаммы и/или композиции, включающие клетки, их экстракты, супернатант или другой очищенный или частично очищенный материал на их основе, с помощью которого обогащали продукцию 5-алкоксифлавоноид-трансферазной (5-AO-FT) и/или 6'-алкоксихалкон-трансферазной (6'-AO-CT) активности, более конкретно с помощью повторных инкубаций с 5-алкоксифлавоноидом, таким как 5-метоксипренилфлавоноид.
Еще одно конкретное воплощение изобретения включает композиции, включающие 5-метокси(пренил)флавоноид метилтрансферазу и/или 6'-метокси(пренил)халкон метилтрансферазу из гомоацетогенного бактериального штамма, более конкретно из Eubacterium sp., и еще более конкретно из Eubacterium limosum.
Конкретное воплощение композиций по настоящему изобретению относится к композициям, включающим обогащенную активность 5-алкоксифлавоноид трансферазы (5-AO-FT) и/или 6'-алкоксихалкон трансферазы (6'-AO-CT), полученной из бактериального штамма Eubacterium limosum, депонированного в Бельгийских Координированных коллекциях Микроорганизмов (BCCM) в BCCM/LMG коллекции под депозитным номером LMG P-23546.
В следующем аспекте в настоящем изобретении предлагаются способы продукции фитоэстрогенов, включающие деалкилирование 5-алкоксифлавоноидов по положению 5 или деалкилирование 6'-алкоксихалконов по соответствующему положению 6', отличающиеся тем, что их осуществляют in vitro с применением эукариотического или прокариотического материала не животного происхождения. В конкретном воплощении способы применяются для получения 8-PN. Согласно конкретному воплощению деалкилирование в способах по изобретению представляет собой деметилирование и осуществляется с применением эукариотического или прокариотического материала не животного происхождения. Более конкретно не животный материал представляет собой бактериальный штамм, более конкретно гомоацетогенную бактерию или очищенные, или частично очищенные фракции или компоненты на его основе, такие как частично очищенные или выделенные ферменты. Конкретное воплощение относится к деалкилированию с применением материала из Eubacterium sp. или Peptostreptococcus sp., такого как Eubacterium limosum. Следующие конкретные воплощения способа по изобретению включают способы деалкилирования пренилированных 5-алкоксифлавоноидов и/или пренилированных 6'-алкоксихалконов.
Согласно следующему конкретному воплощению предлагаются способы деалкилирования 5-алкоксифлавоноидов и/или 6'-алкоксихалконов растительного происхождения, более конкретно с происхождением из хмеля. Согласно конкретным воплощениям предлагаются способы деалкилирования 6'-алкоксихалкона ксантогумола и/или 5-алкоксифлавоноида изоксантогумола.
Следующий аспект изобретения представляет собой применение бактериальной клеточной линии для in vitro деалкилирования 5-алкоксифлавоноидов и/или 6'-алкоксихалконов, более конкретно для деметилирования 5-метоксифлавоноидов и/или 6'-метоксихалконов. Более конкретно бактериальные клетки являются клетками из гомоацетогенного бактериального штамма, такого как Eubacterium limosum. Следующее конкретное воплощение представляет собой применение бактериальных клеток, в которых увеличена продукция 5-алкоксифлавоноид трансферазной (5-AO-FT) и/или 6'-алкоксихалкон-трансферазной (6'-AO-CT) активности, например, с помощью повторных инкубаций с 5-алкоксифлавоноидом, таким как 5-метоксипренилфлавоноид.
Еще в одном аспекте изобретения предлагаются способы продукции фитоэстрогенов in vitro, которые включают стадии а) предоставления бактериального штамма бактерии, более конкретно гомоацетогенной бактерии или экстракта на его основе и b) введение в контакт композиции, включающей 5-алкоксифлавоноиды, более конкретно 5-метоксифлавоноиды и/или 6'-алкоксихалконы, более конкретно 6'-метоксихалконы с бактериальным штаммом или экстрактом на его основе, так чтобы дать возможность деалкилирования 5-алкоксифлавоноидов и/или 6'-алкоксихалконов с помощью бактериального штамма или экстракта на его основе. Необязательно способы дополнительно включают идентификацию и/или очистку полученного деалкилированного флавоноида.
Конкретные воплощения этих способов представляют собой способы, которые включают приготовление экстракта бактериального штамма, который дополнительно включает стадию обогащения и необязательно очистки бактериального экстракта для того, чтобы содержать обогащенную или очищенную 5-алкоксифлавоноид-трансферазную (5-AO-FT) активность и/или обогащенную или очищенную 6'-алкоксихалкон-трансферазную (6'-AO-CT) активность.
Дополнительно или альтернативно способы по настоящему изобретению включают стадию обогащения продукции бактериального штамма 5-AO-FT и/или 6'-AO-CT активностью с помощью повторных инкубаций с 5-алкоксифлавоноидом, таким как 5-метоксипренилфлавоноид.
Еще в одном аспекте изобретения предлагается 5-метоксипренилфлавоноид метилтрансфераза или 6'-метоксипренилхалкон метилтрансфераза из Eubacterium limosum.
Еще в одном аспекте изобретения предлагаются фармацевтические композиции и пищевые добавки, включающие биоактивные фитоэстрогены, полученные с помощью способов по настоящему изобретению.
В другом аспекте изобретения предлагаются фармацевтические композиции и пищевые добавки, включающие два компонента для одновременного или последовательного введения, где первый компонент включает гомоацетогенную бактерию, или экстракт, или компонент на ее основе, имеющий 5-алкоксифлавоноид-трансферазную (5-AO-FT) и/или 6'-алкоксихалкон-трансферазную (6'-AO-CT) активность, и второй компонент, включающий 5-алкоксифлавоноиды или 6'-алкоксихалконы или их источник, такой как экстракт хмеля. Согласно конкретным воплощениям флавоноид представляет собой 6'-алкоксихалкон ксантогумол или 5-алкоксифлавоноид изоксантогумол. Следующие конкретные воплощения относятся к фармацевтическим композициям и пищевым добавкам согласно изобретению, где гомоацетогенной бактерией является Eubacterium limosum. Необязательно бактерии в фармацевтической композиции по изобретению представлены в виде состава для специфической доставки в прямую кишку.
В настоящем изобретении описано, что IX может быть деметилирован до 8-PN с помощью живых организмов не животного происхождения, таких как бактерии кишечника человека или животных, особенно позвоночных или млекопитающих, и что IX может, таким образом, действовать как проэстроген. В настоящем изобретении дополнительно идентифицированы микроорганизмы, способные осуществлять превращение IX в 8-PN, например, in vitro продукцией 8-PN с применением культур таких микроорганизмов. Дополнительно в настоящем изобретении предлагается способ селекции других штаммов, способных количественно получать 8-PN из IX.
В настоящем изобретении дополнительно продемонстрировано, что процесс превращения метилированных предшественников флавоноидных фитоэстрогенов in vivo с помощью микробной флоры является очень вариабельным и зависит от композиции микробной флоры индивидуума (между индивидуумами или у одного и того же индивидуума в различные моменты). Вероятно это имеет важные последствия при воздействии фитоэстрогенов на индивидуумов. Действительно в экстрактах хмеля, в пиве и в пищевых продуктах или добавках менее эстрогенный IX присутствует в более высоких концентрациях, чем 8-PN.
С помощью представленных способов продукции активированных фитоэстрогенов (in vitro или in vivo) в настоящем изобретении дополнительно предлагается интересная альтернатива или дополнение современным пищевым экстрактам хмеля. Непредсказуемый выход при превращении метилированных предшественников флавоноидных фитоэстрогенов (например, IX) в их активные деметилированные соединения можно контролировать с помощью in vitro предварительного превращения или in vivo/in situ деалкилирования. Это дает возможность осуществления контроля за воздействием активного компонента на каждого индивидуума, несмотря на индивидуальные различия в кишечной микрофлоре, или конкретно принимать эти различия во внимание.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Подразумевается, что чертежи иллюстрируют настоящее изобретение, но не следует считать, что имеются в виду какие-либо ограничения изобретения представленными здесь воплощениями.
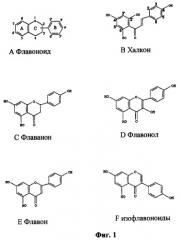
Фиг.1: Основные структуры флавоноидов.
Фиг.2: Структуры пренилфлавоноидов хмеля и их превращение.
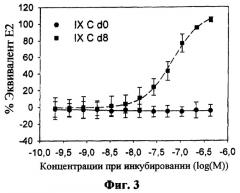
Фиг.3: Реакция на эстроген (среднее + ст. откл.) фекальной культуры (С), инкубированной с IX (0 и 8 дней инкубации) (n=3).
Фиг.4: Трансформация IX (25 мг/л) человеческими фекальными культурами (E-L) в 8-PN через 3 дня [среднее + ст. откл. (n=3)].
Фиг.5: Превращение изоксантогумола (IX) в 8-пренилнарингенин (8-PN) с помощью кишечных бактерий от 51 человеческого индивидуума. Индивидуумы были распределены по возрастанию продукции 8-PN, и результаты представлены как величина, выражающая % превращения IX в 8-PN (n=3) (+/- станд. откл.).
Фиг.6: Превращение IX (25 мг/л) в 8-PN с помощью P. productus (три культуры: Inc 1, Inc 2 и Inc 3). Исчезновение IX (закрашенные символы) и продукцию 8-PN
(незакрашенные символы) детектировали в течение 13 дней.
Фиг.7: Превращение IX в 8-PN после добавления культуры E. Limosum к фекальной культуре В (E. Limosum в процентном выражении от 0% (только фекальный образец) до 100% (не зараженная культура E. Limosum)) (n=3).
Фиг.8: Превращение IX в 8-PN в микробной экосистеме, моделирующей человеческий кишечник, при условиях, дающих возможность активации метилированных метилфлавоноидов. PF+ отделение TWIN SHIME.
Фиг.9: Превращение IX в 8-PN в микробной экосистеме, моделирующей человеческий кишечник, при условиях, не дающих возможности активации метилированных метилфлавоноидов.
Определения
На протяжении настоящей заявки использовались следующие сокращения:
Х: ксантогумол;
DMX: дезметилксантогумол;
IX: изоксантогумол;
8-PN: 8-пренилнарингенин;
6-PN: 6-пренилнарингенин;
5-AO-FT: 5-алкоксифлавоноид алкилтрансфераза;
5-MO-FMT: 5-метоксифлавоноид метилтрансфераза;
6'-AO-CT: 6'-алкоксихалкон алкилтрансфераза;
6'-MO-CMT: 6'-метоксихалкон метилтрансфераза.
Термин «флавоноиды» обозначает группу органических молекул, на основе остова из 15 атомов углерода, содержащего хромановое кольцо и имеющего второе ароматическое кольцо В в положении 2, 3 или 4 (Фиг.1А). Фиг.1А демонстрирует традиционную нумерацию для заместителей, которая также применяется в настоящем изобретении. Подгруппами флавоноидов являются халконы, флаваноны, флавоны, флаванолы и изофлавоноиды. Халконы (Фиг.1В) являются изомерами флаванонов (Фиг.1С). Фиг.1В и 2 демонстрируют традиционную нумерацию халконов. Флаваноны отличаются от флавонов (Фиг.1Е) тем, что они лишены двойной связи в положениях 2, 3. Флавоны (Фиг.1Е) являются флавоноидами, лишенными 3-ОН группы флаванолов (Фиг.1Е). Изофлавоноиды являются флавоноидами, где фенильное кольцо В локализовано в положении 3 (Фиг.1F). Все эти подгруппы имеют кетоновую функцию в положении 4.
Термин «пренилфлавоноид», использованный в настоящем изобретении, относится к флавоноидам, содержащим неполярную пренильную боковую цепь, присоединенную к одному из фенольных колец. Пренильная цепь чаще находится в положении 8, но может также быть в положении 6, или в обоих положениях 6 и 8 [в халконах пренильная цепь локализована в положении 3' и/или 5']. В хмеле пренилфлавоноиды, главным образом, находятся в лупулиновых железах, располагающихся в основании брактеолей в хмелевых шишках женского растения. Другие натуральные источники пренилфлавоноидов представляют собой, например, Dendrolobium lanceolatum, Sophora flavescens, Sophora tomentosa, Artocarpus communus и Marshallia grandiflora. Примерами пренилфлавоноидов являются халконы (такие как ксантогумол (Х) и дезметилксантогумол (DMX), дегидроциклоксантогумол) и флаваноны (такие как изоксантогумол (IX), 8-пренилнарингенин (8-PN) и 6-пренилнарингенин (6-PN)).
Термин «геранилфлавоноид» относится к флавоноиду, содержащему неполярную геранильную боковую цепь, присоединенную к одному из фенольных колец. Примерами являются тетрагидроксигеранилхалкон, 6-геранилнарингенин, 3'-геранилхалконарингенин и 8-геранилнарингенин. Все эти геранилированные соединения были выделены из хмелевых шишек и 8-геранилнарингенину была приписана эстрогенная активность (Milligan et al. (2000) J. Clin. Endocrinol. Metab. 85, 4912-4915).
Термин «ферментативное деалкилирование или деметилирование», использованный здесь, обозначает удаление из соединения с применением фермента алкильной или метильной группы, соответственно.
Термин «5-алкокси деалкилирование» или «5-метокси деметилирование», использованный здесь, обозначает удаление алкильной группы из алкокси группы или метильной из метокси (-OCH3) группы, соответственно, локализованной в положении 5 флавоноида (нумерацию кольца смотри в Фиг.1А). В этом контексте «5-метокси» и «5-О-метил» имеют одно и тоже значение.
Термин «5-алкокси(пренил)флавоноид трансфераза (5-AO-(P)FT)» обозначает фермент, способный обеспечить 5-алкокси деалкилирование 5-алкокси(пренил)флавоноидов.
Конкретной группой флавоноидов являются халконы, где нумерация кольца отличается. Таким образом, что касается халконов, настоящее изобретение относится к удалению алкильной группы из халконового соединения, более конкретно к 6'-алкокси деметилированию, т.е. к удалению метильной группы из алкокси группы, такой как метокси (-OCH3), локализованной в 6' положении халкона (нумерацию кольца смотри в Фиг.1В). Здесь «6'-метокси» и «6'-О-метил-» имеют одно и то же значение. Ферменты, обеспечивающие 6'-алкокси деалкилирование и, более конкретно, 6'-метокси деметилирование также обозначены здесь как «6'-алкокси(пренил)халкон трансфераза (6'-AO-(P)CT)» и «6'-метокси(пренил)халкон метилтрансфераза (6'-MO-(P)CMT)», соответственно.
Термин «микроорганизм», использованный здесь, включает и бактерии, и грибы. Он относится к штаммам индивидуальных микроорганизмов, микробным консорциумам или микробным сообществам, таким как микробное сообщество кишечника животных или любой другой части тела животных (включая человека), или из любого источника в окружающей среде.
Термин «in vitro способ», использованный в контексте настоящего изобретения, относится к способам, осуществленным вне многоклеточных организмов, и включает как способы, осуществленные в отсутствии живых клеток (применяя, например, лизированные клетки, белковые экстракты или рекомбинантные белки), так и процессы, осуществленные с применением живых клеток, более конкретно культур выделенных клеток. Когда ссылаются на in vitro способы, то, таким образом подразумевается, что исключаются такие процессы, как встречающиеся в природе в интактных шишках хмеля или в кишечнике живых животых.
Когда ссылаются на «in situ» деалкилирующую, деметилирующую активность in vivo, то подразумевается, что это происходит в одном или более конкретном органе тела.
Когда здесь ссылаются на «бактерии», то подразумеваются и аэробные, и анаэробные бактерии.
«Гомоацетогены», по отношению к бактериям, являются анаэробными бактериями, которые восстанавливают СО2 до ацетата или до окисленного ацетата через путь ацетил-CoA. Характерными гомоацетогенными бактериями являются, например, Acetoanaerobium noterae, Acetobacterium woodii, Acetobacterium wieringae, Acetogenum kivui, Acetitomaculum ruminis, Clostridium aceticum, Clostridium thermoaceticum, Clostridium formicoaceticum, Desulfotomaculum orientis, Sporomusa paucivorans, Peptostreptococcus sp. и Eubacteum sp.
Термины первый, второй, третий и подобные в описании и в формуле изобретения используются для обозначения различий между похожими элементами и не являются необходимыми для описания последовательного или хронологического порядка. Следует понимать, что используемые таким образом термины являются заменяемыми при соответствующих обстоятельствах, и описанные здесь воплощения по изобретению способны действовать в другом порядке, по сравнению с описанным или иллюстрированным здесь.
Согласно настоящему изобретению ферментативное деалкилирование и, более конкретно, 5-алкокси деалкилирование флавоноидов можно осуществить с помощью ферментов, в основном обозначенных как 5-алкокси-трансферазы, более конкретно с помощью 5-метоксифлавоноид метилтрансферазы (5-МО-FMT) и/или 6'-метоксихалкон метилтрансферазы (6'-МО-CMT), так же как с помощью интактной живой или инактивированной клетки (или клеточного материала), производящей 5-алкоксифлавоноид алкилтрансферазу или фермент 6'-алкоксихалкон алкилтрансферазу, с помощью лизата такой клетки, с помощью фракции лизата такой клетки (например, мембраны или цитоплазмы), с помощью обогащенной или очищенной белковой фракции, включающей указанную 5-алкоксифлавоноид алкилтрансферазу и/или 6'-алкоксихалкон алкилтрансферазу, или с помощью экспрессирующейся рекомбинантной 5-алкоксифлавоноид алкилтрансферазы и/или 6'-алкоксихалкон алкилтрансферазы. В случае, если рекомбинантный деалкилированный фермент секретируется клетками, то может быть использована подходящая среда. В случае, если рекомбинантный фермент локализован в цитоплазме, то сигналы секреции могут быть добавлены к рекомбинантной ДНК, чтобы получить белок, который может быть выделен из ростовой среды.
В изобретении предлагаются алкокси-деалкилазы, более конкретно ферменты, способные к удалению алкильной группы у алкоксифлавоноидов. Алкильная группа может представлять собой линейный или разветвленный алкил. Более конкретно алкильная группа представляет собой С1-С6 алкил. В конкретном воплощении алкил является метилом.
Согласно настоящему изобретению предлагаются 5-алкокси-алкилтрансферазы, более конкретно 5-алкоксифлавоноид алкилтрансферазы, которые имеют прокариотическое или эукариотическое не животное происхождение, включая 5-алкокси-алкилтрансферазы, имеющие происхождение из растительной клетки или микроорганизма.
Первый аспект настоящего изобретения относится к клеткам, экстрактам и обогащенным частично очищенным или очищенным белкам (так же, как к композициям, включающим один из этих компонентов или более), способных к деалкилированию 5-алкоксифлавоноидов, более конкретно способных к деметилированию 5-метоксифлавоноидов и/или 6'-метоксихалконов. Согласно конкретному воплощению настоящего изобретения клетки, экстракты и белки, включающие активность 5-AO-FMT (и/или 6'-AO-CMT), имеют бактериальное происхождение. Более конкретно бактерии представляют собой гомоацетогенные бактерии. Следующее воплощение изобретения относится к гомоацетогенным бактериям, выбранным из видов Eubacterium и Peptostreptococcus. Гомоацетогенные бактерии можно культивировать в анаэробных условиях с сахарами, одноуглеродными соединениями, такими как формиат, метанол, СО и СО2 плюс Н2, также как с алкоксилированными ароматическими соединениями в качестве источника углерода. Бактериальные штаммы с увеличенной или обогащенной пренилфлавоноид деалкилирующей или деметилирующей активностью могут быть получены с помощью селекции, основанной на повторной инкубации с соответствующим субстратом, как здесь описано в разделе примеров. Обогащение активности, как здесь обозначено, относится к активности, примерно от 1,5 до 10 раз превышающей активность в исходном штамме, более конкретно до ~3 раз превышающей активность в исходном штамме. Дополнительно или альтернативно способ обогащения по настоящему изобретению обеспечивает ферментативную активность, которая достигает 90-100% превращения субстрата (используя, например, 25 мг/л IX). Таким образом, настоящее изобретение также относится к способам обогащения 5-алкоксифлавоноид трансферазной (5-AO-FT) и/или 6'-алкоксихалкон трансферазной (6'-АО-CT) активностью бактериальных штаммов, включающим стадию инкубации штамма на среде с 5-алкоксифлавоноидом, таким как 5-метоксипренилфлавоноид (или 6'-метоксихалкон), более конкретно включающим стадию рассеивания бактерий на среде, включающей IX (или X), с последующей селекцией колонии с наивысшим продуцированием. Более конкретно штамм несколько раз высевают на среде, включающей субстрат, как, например, 2-10 раз, более конкретно 3-4 раза, с последующей селекцией колонии с наивысшей 5-алкоксифлавоноид-трансферазной (5-AO-FT) и/или 6'-алкоксихалкон-трансферазной (6'-АО-CT) активностью. Эту активность можно измерить, например, на основании продукции конечного продукта реакции. Согласно конкретному воплощению этот способ обогащения осуществляют на гомоацетогенном бактериальном штамме, более конкретно на штамме Eubacterium или Peptostreptococcus, более конкретно E. limosum или P. productus. Конкретный пример обогащенного бактериального штамма Eubacterium limosum депонирован Willy Verstraete 15 марта 2006 года в Бельгийских Координированных коллекциях Микроорганизмов (BCCM) в BCCM/LMG коллекции под депозитным номером LMG P-23546, Laboratorium voor Microbiologie, Universiteit Gent (UGent), K.L. Ledeganckstraat 35, B-9000 Gent, Belgium.
Таким образом, в настоящем изобретении предлагается способ получения обогащенной частично очищенной и/или очищенной 5-алкоксифлавоноид трансферазы, более конкретно 5-метоксипренилфлавоноид метилтрансферазы, который включает стадии получения бактериального штамма, более конкретно гомоацетогенного штамма, такого как Eubacterium limosum с увеличенной/обогащенной 5AO-FT активностью, более конкретно с увеличенной 5MO-FMT активностью, и обогащение, частичную очистку или очистку фермента проводили с использованием классических методов очистки, включая осаждение сульфатом аммония, ионно-обменную хроматографию и гель-фильтрационную хроматографию.
В настоящем изобретении предлагаются бактериальные штаммы в качестве источника, где алкил- или метилтрансфераза присутствует в высоких концентрациях и/или где присутствует природный мутант с высокой активностью. В обоих случаях ссылаются на «обогащенный» бактериальный штамм.
Согласно еще одному воплощению изобретения клетка, включающая 5-алкокси деалкилирующую активность, более конкретно 5-метоксифлавоноид деметилирующую активность (и/или 6'-метоксихалкон деметилирующую активность), является трансгенной клеткой, полученной путем введения в микроорганизм или в растительную клетку последовательности ДНК, кодирующей 5-алкокси-алкилтрансферазу, более конкретно 5-MO-FMT (и/или 6'-MO-CMT). Генетически модифицированные растительные клетки с обогащенной 5-MO-FMT (и/или 6'-MO-CMT) активностью, которая может быть объединена с высоким природным или искусственно индуцированным уровнем флавоноидов (например, метилфлавоноидов), полученным в результате “in planta” продукции фитоэстрогенов. Таким образом, в настоящем изобретении предлагаются, но не ограничиваются ими, генетически модифицированные растения с увеличенным содержанием фитоэстрогенов, такие как хмелевые растения.
Согласно другому воплощению клетки, экстракты и белки, включающие 5-алкокси деалкилирующую активность, более конкретно 5-метокси деметилирующую активность, представляют собой растительные клетки Humulus lupulus или других растений, где синтезируется 8-PN, таких как Marshallia grandiflora и Sophora tomentosa. Для крупномасштабного превращения можно провести скрининг растений, где повышенное природное превращение X или IX в 8-PN, для того чтобы обнаружить природные мутанты по 5-MO-FMT (и/или 6'-MO-CMT) или суперэкспрессию 5-MO-FMT (и/или 6'-MO-CMT).
Клетки или композиции можно протестировать на предмет наличия активности 5-AO-FT (и/или 6'-AO-CT), более конкретно 5-MO-FMT (и/или 6'-MO-CMT), испо