Рентгеновская установка для формирования изображения исследуемого объекта и ее применение
Иллюстрации
Показать всеИзобретение относится к медицинской технике, а именно к устройствам для формирования изображений исследуемого объекта. Рентгеновская установка содержит по меньшей мере один рентгеновский источник, испускающий полихроматическое рентгеновское излучение, первый приемник или первый блок приемников определения значений первой интенсивности проходящего рентгеновского излучения, второй приемник или второй блок приемников определения значений второй интенсивности испускаемого исследуемым объектом флуоресцентного рентгеновского излучения, блок корреляции, а также устройство вывода для отображения исследуемого объекта на основе сигналов элементов изображения. Применение рентгеновской установки для формирования изображения исследуемого объекта, содержащего по меньшей мере один рентгеноконтрастный химический элемент, осуществляется посредством рентгеновского излучения, проходящего через исследуемый объект, и флуоресцентного рентгеновского излучения, испускаемого указанным объектом. Использование изобретения позволяет обеспечить изображение малых патологических изменений с высоким пространственным разрешением при меньшей дозе облучения. 2 н. и 20 з.п. ф-лы, 7 ил.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к рентгеновской установке для формирования изображения исследуемого объекта, содержащего по меньшей мере один рентгеноконтрастный химический элемент, посредством рентгеновского излучения, к применению рентгеновской установки, а также к способу рентгеноконтрастного формирования изображения исследуемого объекта, например млекопитающего, прежде всего человека.
Уровень техники
Медицинская диагностика с помощью рентгеновского излучения - это технически высокоразвитый раздел диагностики заболеваний, например, для их своевременного распознавания, рентгенографического подтверждения, характеристики и локализации опухолей, заболеваний сосудов и других патологических изменений человеческого организма. Техника весьма эффективна и отличается высокой степенью доступности.
Для генерирования рентгеновского излучения используются рентгеновские трубки с вольфрамовыми, молибденовыми или родиевыми вращающимися анодами и алюминиевыми, медными, титановыми, молибденовыми и родиевыми фильтрами. Соответствующие фильтры позволяют отфильтровывать часть тормозного излучения, поэтому в благоприятных случаях на выход рентгеновской трубки поступает по существу характеристическое излучение.
В качестве приемников (детекторов) используются обычные рентгеновские пленки, гибкие диски накопителей или цифровые плоскостные приемники. В компьютерных томографах применяются одни однострочные приемники или приемники с несколькими строками. Возможно также параллельное включение нескольких приемников. Для непосредственного преобразования рентгеновских лучей в электрические сигналы используются полупроводниковые приемники (детекторы), выполненные на основе теллурида кадмия (СТ), теллурида кадмия-цинка (CZT), аморфного селена или же аморфного или кристаллического кремния (M.J.Yaffe, J.A.Rowlands, “X-Ray Detectors for Digital Radiography”, Med. Biol, 42(1) (1997) 1-39).
Пример конструкции таких приемников приведен в патенте US 5434417 А. Чтобы обеспечить энергочувствительность приемника, он набирается из нескольких слоев. Рентгеновские лучи с различной энергией проникают в этот приемник на разную глубину и за счет фотоэлектрического эффекта генерируют в соответствующем слое электрический сигнал, который можно непосредственно считывать как импульс тока с идентификацией по слою и, следовательно, по энергии рентгеновских фотонов.
Компьютерная томография (КТ) уже давно используется в повседневной клинической практике. КТ позволяет получать снимки тела в разрезе с улучшенным пространственным разрешением по сравнению с обычной проекционной радиографией. Несмотря на то, что и разрешение по плотности при КТ значительно выше, чем разрешение по плотности при обычной рентгеновской технике, для более надежного распознавания многих болезненных изменений требуются рентгеноконтрастные препараты. Они улучшают качество морфологической информации. При этом контрастное средство позволяет, с одной стороны, представить функциональные процессы в организме (выделение, перфузия, проницаемость), с другой стороны, подчеркнуть морфологию путем создания контрастов (различная концентрация рентгеноконтрастных веществ в различных тканях).
Во многих случаях обычную рентгенотехнику нельзя было использовать, так как контраст исследуемой ткани был недостаточным. Для этой цели были разработаны рентгеноконтрастные вещества, создающие высокую рентгенографическую плотность в ткани, в которой они скапливаются. Типичными примерами являются йод, бром, элементы с порядковыми номерами 34, 42, 44-52, 54-60, 62-79, 82 и 83 в качестве рентгеноконтрастных элементов, а также внутрикомплексные соединения с порядковыми номерами 56-60, 62-79, 82 и 83. Из соединений йода можно использовать, например, меглумин-натрий- или лизин-диатризоат, йоталамат, йокситаламат, йопромид, йогексол, йомепрол, йопамидол, йоверсол, йобитридол, йопентол, йотролан, йодиксанол и йоксилан (INN) (ЕР 0885616 А1).
В определенных случаях, несмотря на введение рентгеноконтрастных веществ, не удавалось добиться достаточного контраста тканей. Для дальнейшего усиления контраста была введена цифровая субтрактивная ангиография (DSA), при которой преконтрастные и постконтрастные снимки (логарифмически) вычитаются друг из друга. Метод вычитания для применения в маммографии описан в ЕР 0885616 А1: Для проекционной маммографии там предлагается сначала снять преконтрастную маммограмму, затем быстро ввести пациентке внутривенно распространенный урографический рентгеноконтрастный препарат и примерно через 30 с-1 мин по окончании инъекции снять постконтрастную маммограмму. Полученные данные обоих снимков соотносят друг с другом, предпочтительно вычитают один из другого.
Новые разработки в области компьютерной томографии, что касается возбуждения излучения, относятся, например, к применению в КТ синхротронного излучения (F.A.Dilmanian “Computed Tomography with Monochromatic X-Rays”, Am. J. Physiol. Imaging, 314 (1992) 175-193). Хорошие рентгеновские снимки можно получить, например, посредством так называемой “К-краевой субтрактивной компьютерной томографии” (F.A.Dilmanian, р.179), причем используется сильное нарастание коэффициента поглощения в энергии связи К-электронов атома. Элемент йод имеет К-линию при энергии 33,17 кэВ. К сожалению, этот способ функционирует только с помощью синхротронного излучения, получаемого на больших накопительных кольцах, например DESY, так как это излучение имеет благоприятные для способа монохроматичность и интенсивность. Обычные рентгеновские трубки дают не монохроматическое излучение, а непрерывный спектр. Поэтому они мало пригодны для подобного рода дифференциальных измерений.
Альтернативная возможность описана в документе DE 10118792 А1. Здесь для снятия проекционных маммограмм предлагается способ, при котором используются источники рентгеновского излучения с двумя рентгеновскими анодами из различных материалов. Для снятия маммограмм пациентке сначала вводится рентгеноконтрастное вещество. Затем делается первый проекционный снимок с использованием первого из двух рентгеновских анодов, после чего - второй проекционный снимок с использованием второго рентгеновского анода. Путем наложения каждого отдельного элемента изображения первого снимка на каждый отдельный элемент изображения второго снимка изготавливается корреляционное изображение. Характеристическое излучение обоих рентгеновских анодов согласуется со спектром поглощения рентгеноконтрастного вещества. Энергия излучения первого рентгеновского анода несколько ниже энергии поглощения контрастирующего элемента в рентгеноконтрастном веществе, а энергия излучения второго анода несколько выше энергии поглощения контрастирующего элемента. Недостатком этого способа является то, что обычные рентгеновские трубки с одним рентгеновским анодом приходится заменять двуханодными трубками.
Дополнительно к трансмиссионной радиографии описывается эмиссионная радиография.
Так, в документе WO 2004/041060 А2 описано устройство для неинвазивного определения in vivo химического элемента в простате человека, состоящее из зонда, системы облучения, способной возбуждать лучевую эмиссию химического элемента, приемника излучения внутри зонда, позволяющего отображать обнаруженное излучение, а также системы регистрации, обработки и индикации сигналов, позволяющей определять количество химического элемента в различных зонах простаты в соответствии с отображением обнаруженного излучения. Испускаемое излучение представляет собой в основном флуоресцентное излучение. В случае исследования простаты определяется предпочтительно распределение цинка в тканях.
Далее в DE 3608965 А1 описан способ определения доли различных химических элементов в слое исследуемой зоны посредством гамма- или рентгеновского излучения. При этом отдельно регистрируются комптоновское и рэлеевское рассеянное излучение. Характер определенного по данным измерения дифференциального коэффициента рассеяния зависит от долей различных химических элементов в отдельных элементах изображения. Поэтому он позволяет определять долю этих химических элементов. Для этого исследуемая зона просвечивается первичным лучом из большого числа направлений, и излучение, исходящее под различными углами из исследуемой зоны, регистрируется приемным (детекторным) устройством в различных положениях за пределами исследуемой зоны, после чего по полученным в результате результатам измерения определяется разностный коэффициент рассеяния для различных переданных импульсов каждого элемента изображения в слое.
Наряду с этим Quanwen Yu и др. в работе “Preliminary Experiment of Fluorescent X-Ray Computed Tomography to Detect Dual Agents for Biological Study”, см. J. Synchrotron Rad. (2001), 8 1030-1034, предлагают использовать метод рентгеновской флуоресценции для определения очень малых концентраций нерадиоактивных веществ при биомедицинских исследованиях. С помощью этого метода можно получать изображения, позволяющие с использованием линии Кα флуоресценции в одном исследовании одновременно обнаруживать мультиагенты, чтобы, например, количественно регистрировать кровоток в мозгу и плотность клеток головного мозга. В представленном исследовании изображения, полученные по этому методу, сравнивались с изображениями, полученными с помощью рентгеновской трансмиссионной томографии.
Правда, метод рентгеновской флуоресценции или рентгеновского рассеянного света, описанный в указанных выше публикациях, имеет тот недостаток, что представление мелких деталей в исследуемом объекте довольно сложно из-за трудностей отображения. Более того, изображения получаются только с грубым разрешением, что не позволяет представить на снимке мелкие детали.
Раскрытие изобретения
Исходя из вышеизложенного, задача изобретения состоит в том, чтобы избежать указанных недостатков и, прежде всего, создать установки и способы, позволяющие получать снимки с различными рентгеноконтрастными химическими элементами. Далее получение рентгеновских снимков также должно быть простым, удобным и экономичным. Техника исследования должна быть доступной на широкой основе. Следует обеспечить отображение даже малых патологических изменений в исследуемом объекте с высоким пространственным разрешением при как можно меньшей дозе облучения. Необходимо избежать дефектов изображения, обусловленных движением объекта.
Проблема решается с помощью рентгеновской установки для формирования изображения исследуемого объекта, содержащего по меньшей мере один рентгеноконтрастный химический элемент, посредством рентгеновского излучения по п.1 формулы изобретения, применения этой установки по п.11 и способа рентгеноконтрастного формирования изображений по п.25. Предпочтительные варианты изобретения описаны в зависимых пунктах формулы изобретения.
Если в описании изобретения и в пунктах формулы изобретения используются термины “испускаемое излучение” и “испускать”, то под этим следует понимать, во-первых, рентгеновскую флуоресценцию, т.е. эмиссию излучения после возбуждения облученной материи электромагнитным излучением и, во-вторых, предпочтительно, рэлеевское рассеяние. В последнем случае излучение без передачи импульса снова испускается (переизлучение) облученной материей, при этом, однако, в результате облучения электроны оболочки в атомах этой материи не переходят в возбужденное состояние, как при флуоресценции.
Для формирования изображения рентгеновская установка использует проходящее через исследуемый объект и испускаемое им рентгеновское излучение. Для этого предлагаемая в изобретении рентгеновская установка содержит:
а) по меньшей мере один рентгеновский источник, испускающий по существу полихроматическое рентгеновское излучение,
б) первый приемник или первый блок приемников, выполненный с возможностью определения значений первой интенсивности проходящего через исследуемый объект рентгеновского излучения,
в) второй приемник или второй блок приемников, выполненный с возможностью определения значений второй интенсивности испускаемого исследуемым объектом рентгеновского излучения,
г) по меньшей мере один блок корреляции, выполненный с возможностью соотнесения, по элементам изображения, значений первой интенсивности проходящего рентгеновского излучения со значениями второй интенсивности испускаемого рентгеновского излучения, а также
д) по меньшей мере одно устройство вывода для отображения исследуемого объекта на основе сигналов элементов изображения, получаемого путем соотнесения значений первой интенсивности со значениями второй интенсивности.
Проходящее рентгеновское излучение и испускаемое рентгеновское излучение можно обнаруживать (детектировать) одновременно или последовательно одно за другим.
Эта рентгеновская установка может использоваться для формирования изображения исследуемого объекта, содержащего по меньшей мере один рентгеноконтрастный химический элемент, посредством рентгеновского излучения. Рентгеноконтрастный химический элемент предпочтительно вводится в исследуемый объект с рентгеноконтрастным веществом, которое для этого вводится в объект исследования, например в организм человека или животного.
Рентгеноконтрастные химические элементы с низким порядковым числом, которые естественно присутствуют в исследуемом объекте, дают лишь незначительный выход рентгеновской флуоресценции, поэтому формирование изображений с использованием этих элементов представляется практически нецелесообразным. Кроме того, энергия фотонов рентгеновской флуоресценции в этом случае мала, так что и их распространение в тканях организма незначительно. В частности, начиная с элемента йод (порядковый номер - 53) с линиями испускания 28,6 и 32,3 кэВ, в распоряжении имеются линии флуоресценции, которые достаточно интенсивно покидают исследуемый объект и могут регистрироваться приемником, расположенным вне объекта. В случаях более низкого порядкового числа химического элемента следует выбрать расположение второго приемника по возможности ближе к исследуемой зоне (или интересующей зоне).
Эта рентгеновская установка применяется для осуществления предлагаемого в изобретении рентгеноконтрастного способа исследования. Способ включает в себя следующие операции:
а) предпочтительно выполняемое введение в организм по меньшей мере одного обеспечивающего рентгеновский контраст химического элемента,
б) просвечивание исследуемого объекта по существу полихроматическим рентгеновским излучением,
в) определение значений первой интенсивности проходящего через исследуемый объект рентгеновского излучения,
г) определение значений второй интенсивности испускаемого исследуемым объектом рентгеновского излучения,
д) выполняемое по элементам изображения соотнесение значений первой интенсивности проходящего рентгеновского излучения со значениями второй интенсивности испускаемого рентгеновского излучения, а также
е) отображение исследуемого объекта на основе сигналов элементов изображения, полученных путем соотнесения значений первой интенсивности со значениями второй интенсивности.
В отличие от известных способов, при которых или только проводится трансмиссионная рентгеновская компьютерная томография (ТРКТ), или обнаруживается рентгеновская флуоресценция (флуоресцентная рентгеновская компьютерная томография - ФРКТ), в настоящем изобретении проходящее и испускаемое излучение измеряются одновременно или последовательно и комбинируются друг с другом согласно настоящему изобретению, причем полученные изображения путем соответствующего способа корреляции (соотнесения) накладываются одно на другое. Такой подход позволяет использовать преимущества обеих технологий.
Преимуществом трансмиссионной рентгеновской томографии является высокое временное и пространственное разрешение, что позволяет обнаружить даже мельчайшие патологические изменения или другие детали в исследуемом человеческом организме. Однако полученный контраст зачастую не достаточен, чтобы наглядно представить эти детали. Это прежде всего относится к исследованию мягких тканей. Кроме того, исследование определенных участков тела методом ТРКТ затруднено костным скелетом.
С другой стороны, флуоресцентная рентгеновская томография имеет преимущество чрезвычайно контрастного представления, поскольку исключительно определенные химические элементы при их соответствующем возбуждении испускают электромагнитное излучение, поэтому находящиеся в исследуемой зоне элементы могут служить чрезвычайно чувствительными измерительными зондами. Однако метод ФРКТ имеет тот недостаток, что он обеспечивает лишь небольшое пространственное разрешение и не позволяет отобразить мелкие патологические изменения.
Только соотнесение (коррелирование) значений интенсивности проходящего рентгеновского излучения по элементам изобретения (от одного элемента изображения к другому) со значениями интенсивности испускаемого рентгеновского излучения и представление исследуемого объекта на основе сигналов элементов изображения, полученных путем такого соотнесения, позволяет создать контрастное и детальное изображение исследуемой зоны. Правда, часть изображения, обеспечивающая контраст, имеет малое разрешение. Путем соотнесения соответствующих значений друг с другом можно практически полностью устранить этот недостаток, так как необходимая детальная информация определяется значениями интенсивности излучения, измеренного методом ТРКТ.
Изобретение в особенности предназначено для исследований человека. Его можно использовать для получения радиографических снимков для отображения пространственных требований, сосудов и перфузии, например пищеводо-желудочно-кишечного тракта, для бронхографии, холеграфии, ангио- и кардиоангиографии, для церебральной ангиографии и перфузионных измерений, для маммографии, а также для лимфографии. Основным направлением использования изобретения является компьютерная томография (многосрезовая компьютерная томография - МСКТ, компьютерная микротомография КМКТ) и ее разновидности ПЭТ (позитронно-эмиссионная томография), ОФЭКТ (однофотонная эмиссионная компьютерная томография), сонография и другие методы оптического формирования изображения. В принципе изобретение можно использовать также для исследования неживой материи, например, в области контроля материалов.
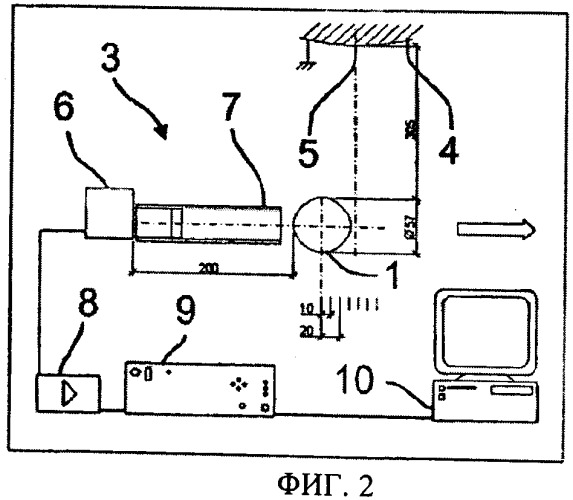
Для проведения исследования проходящее излучение регистрируется посредством первого приемника, находящегося на пути хода лучей рентгеновской трубки, ослабленных исследуемым объектом. Испускаемое излучение измеряется посредством второго приемника, расположенного вне хода лучей, предпочтительно под углом 90° к ходу лучей. Этот второй приемник можно в принципе устанавливать и под любым другим углом к рентгеновскому лучу, например под углом 45° или 135° к лучу источника рентгеновского излучения, однако он не должен находиться на пути луча, проходящего через исследуемый объект. Если рентгеновская трубка находится в положении на 12 часов, то обычные компьютерные томографы оснащаются рядом приемников, установленных в противоположное положение, на 6 часов. Предпочтительнее располагать второй приемник в положении на 3 часа или на 9 часов. Посредством этого второго приемника можно регистрировать как рентгеновскую флуоресценцию, так и рентгеновское рассеяние (рэлеевское, комптоновское рассеяние).
Для селективной регистрации изображений вторым приемником с использованием испускаемого рентгеновского излучения можно измерять энергию испускаемого рентгеновского излучения с хорошим разрешением. В частности, предпочтительно при наличии заданного излучающего химического элемента в исследуемом объекте отличать (дискриминировать, или выделять) воспринятое вторым приемником рентгеновское излучение, исходящее от рентгеноконтрастного элемента, от другого испускаемого рентгеновского излучения, например рассеянного излучения (комптоновского, рэлеевского излучения) и от флуоресцентного излучения других химических элементов. Это позволяет очень четко представлять определенные зоны исследования с использованием, например, скопления рентгеноконтрастных химических элементов в определенных органах человеческого тела, используя большой контраст между высвеченной излучением ткани и окружающими тканями. Даже обусловленная костным скелетом структура в полученном изображении в этом случае отступает на задний план по сравнению с изображением ткани, так что костный скелет практически не мешает изображению.
Для обнаружения и определения характеристик испускаемого излучения предпочтительно использовать энергодисперсионный приемник. Однако можно использовать для этого и более простые приемники и определять характеристики излучения посредством рентгенооптических модулей (комбинации фильтров, монохроматоров).
Кроме того, этот принцип таким же образом можно переносить на измерение значений интенсивности проходящего рентгеновского излучения первым приемником. В таком случае достигается селективное изображение зон в исследуемом объекте, в которых скапливаются рентгеноконтрастные химические элементы.
Таким образом, изобретение также позволяет контрастно отображать мягкие ткани, например, в организме человека. Путем согласования энергии или энергетического интервала зарегистрированного приемниками проходящего и испускаемого рентгеновского излучения с видом рентгеноконтрастного химического элемента можно достигнуть эффективного усиления контраста по сравнению с другими способами.
Для генерирования рентгеновских лучей можно использовать обычную, предлагаемую на рынке рентгеновскую трубку с непрерывным спектром, например трубку с молибденовым, вольфрамовым или родиевым анодом. В зависимости от вида содержащегося в исследуемом объекте рентгеноконтрастного химического элемента на анод подается напряжение, обеспечивающее непрерывное излучение, например в диапазоне свыше 100 кэВ.
В принципе источник рентгеновского излучения может работать без исходящего излучения, в результате чего полихроматическое излучение попадает на исследуемый объект во всей области спектра. Однако для снижения лучевой нагрузки на исследуемый объект можно также отфильтровывать такое рентгеновское излучение из спектра полихроматического источника рентгеновских лучей, энергия которого не требуется или не желательна для детектирования. Для этого используется, например, алюминиевый или медный фильтр, который отфильтровывает энергию в диапазоне ≤20 кэВ (мягкое излучение). Таким образом, под непрерывным спектром следует понимать рентгеновское излучение в диапазоне ≥0 кэВ, предпочтительнее ≥15 кэВ, еще предпочтительнее ≥17 кэВ и особенно предпочтительно ≥20 кэВ, например до 100 кэВ, причем никакой спектральный диапазон в этих пределах не выделяется относительно других и не исключается. Верхний предел спектра излучения определяется напряжением, приложенным к рентгеновскому аноду.
Низкоэнергетическая область излучения предпочтительно отфильтровывается, чтобы исключить опасную для человеческого организма дозу облучения.
Обычно для исследования объекта с полихроматическим рентгеновским излучением используется соответствующий приемник. В качестве варианта можно использовать энергодисперсионный приемник, чтобы определить энергию попадающих на объект фотонов.
Существуют два принципиально различных варианта исполнения энергодисперсионных приемников и блоков приемников:
а) Описание энергодисперсионных приемников по типу кадмиево-(цинко-)технециевых приемников содержится во вступительной части. Такой серийный ряд приемников позволяет по элементам изображения измерять рентгеновские спектры рентгеновского излучения.
б) Используются простые рентгеновские приемники. Перед приемником устанавливается дискриминатор, который в простейшем случае представляет собой соответствующую комбинацию фильтров. Однако для энергетической селекции можно использовать также монохроматоры, настраиваемые, например, на рентгеновскую флуоресценцию введенного в организм рентгеноконтрастного вещества.
в) Вместе с тем, технически вполне возможно настраивать приемник непосредственно на рентгеноконтрастное вещество. Так, можно использовать гаделиново-(цинко-)технециевые или диспрозиево-(цинко-)технециевые приемники.
Во всех случаях приемник по возможности располагается таким образом, чтобы измерять минимум комптоновского рассеяния.
Для определения значений интенсивности, а также энергии испускаемого исследуемым объектом рентгеновского излучения обнаруженные фотоны подразделяются по меньшей мере на два различных энергетических диапазона, содержащих, например, линии испускания Кα и Кβ. Для повышения специфичности элементов в некоторых случаях можно ввести поправку на комптоновское рассеяние. Однако, как показывают приведенные ниже примеры, это не всегда требуется.
Если отказаться от присущего рентгеновским снимкам контраста, можно для осуществления предлагаемого в изобретении способа ввести в исследуемый объект, например организм человека, рентгеноконтрастное вещество. Рентгеноконтрастное вещество можно вводить, например, энтерально или парентерально, прежде всего в виде внутривенной, внутримышечной или подкожной инъекции или вливания. После этого делается рентгеновский снимок. Пригодны такие рентгеноконтрастные вещества, которые в выбранной области спектра сами по себе имеют высокий коэффициент ослабления. Рентгеноконтрастные вещества, поглощающий элемент которых имеет К-край спектра поглощения в выбранном спектральном диапазоне, также вполне пригодны. Такие рентгеноконтрастные вещества содержат рентгеноконтрастные химические элементы с порядковым числом 35 или больше 35 (при этом речь идет, например, о содержащих бром рентгеноконтрастных веществах), с порядковым числом 47 или больше 47 (при этом речь идет, например, о содержащих йод рентгеноконтрастных веществах), с порядковым числом 57 или больше 57 (при этом речь идет, например, о рентгеноконтрастных веществах, содержащих лантаниды, прежде всего о рентгеноконтрастных веществах, содержащих гадолиний), или с порядковым числом 83 (здесь речь идет о рентгеноконтрастных веществах, содержащих висмут). Поэтому используются рентгеноконтрастные вещества, содержащие рентгеноконтрастные химические элементы с порядковыми числами от 35 (бром) до 83 (висмут). Пригодны также рентгеноконтрастные вещества с рентгеноконтрастными химическими элементами, имеющими порядковые числа от 53 (йод) до 83 (висмут), а также с порядковым числом от 57 или больше 57 (лантаниды) до 83 (висмут), а особенно предпочтительны вещества с рентгеноконтрастными химическими элементами, имеющими порядковые числа 57-70 (лантаниды: La, Се, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb).
Пригодными содержащими йод рентгеноконтрастными веществами являются, например, соединения, содержащие трийодные ароматические углеводороды, прежде всего амидотризоат, йогексол, йопамидол, йопановая кислота, йопадиновая кислота, йопромид, йопроновая кислота, йопидон, йоталаминовая кислота, йопентол, йоверсол, йоксаглат, йотролан, йодиксанол, йотроксиновая кислота, йоксаглиновая кислота, йокситаламиновая кислотна и йосименол (INN). Фирменными наименованиями для рентгеноконтрастных веществ, содержащих йод, являются Urografin® (ф. Шеринг), Gastrografin® (ф. Шеринг), Biliscopin® (ф. Шеринг), Ultravist® (ф. Шеринг) и Isovist® (ф. Шеринг).
В качестве рентгеноконтрастных веществ используются также металлокомплексные соединения, например Gd-DTPA (Magnevist® (ф. Шеринг)), Gd-DOTA (Gadoterate, Dotarem), Gd-HP-DO3A (Gadoteridol, Prohance® (ф. Бракко)), Gd-EOB-DTPA (Gadoxrtat, Primavist), Gd-BOPTA (Gadobenat, MultiHance), Gd-DTPA-BMA (Gadodiamide, Omniscan® (ф. Амершам Хелс)), Dy-DTPA-BMA, Gd-DTPA-Polylysin, каскадные полимеры Gd-DTPA и др., причем DTPA = диэтилентриаминпентауксусная кислота, DOTA = 1,4,7,10-тетраазациклододекан, HP-DO3A = 10-(гидроксипропил)-1,4,7,10-тетраазациклодекан-1,4,7-триуксусная кислота), EOB-DTPA = 3,6,9-триаза-3,6,9-трис(карбоксилметил)-4-(4-этоксибензил)ундекандикрабоновая кислота, ВОРТА = (4-карбокси-5,8,11-трис(карбоксиметил)-1-фенил-2-окса-5,8,11-триазатридекан-130-оис, беник-оксид), DTPA-BMA = диэтилентриаминпентаацетат-бис(метиламид), DTPA-полилизин = даэтилентриаминпентаацетат-полилизин, каскадные полимеры DTPA.
Рентгеноконтрастные вещества могут применяться энтерально или парентерально. При парентеральном применении предпочтение отдается внутривенному введению (i.v.). Предпочтительными дозировками для содержащих йод неионных рентгеноконтрастных веществ являются дозы до 0,75 г/кг веса тела. Это соответствует примерно 6 ммоль/кг веса тела. В дальнейшем дозу можно предпочтительно увеличивать до 1,5 г/кг веса тела (что соответствует примерно 12 ммоль/кг веса тела), а в исключительных случаях - до 2 г (т.е. 16 ммоль) или до 5 г (39 ммоль) на 1 кг веса тела. Для лантанидных комплексных соединений предпочтительная доза составляет 0,1 ммоль/кг веса тела. Целесообразны и также предпочтительны дозы до 0,3 ммоль/кг веса тела или до 1 ммоль/кг веса тела.
Спектральные линии испускания гадолиния соответствуют 43,0 и 48,7 кэВ, т.е. эти значения выше, чем для йода, для которого они составляют 28,6 и 32,3 кэВ. Комплексные соединения металлов могут вместо атомов гадолиния включать в себя, например, также все другие лантаниды, прежде всего лантан или иттербий.
Цифровые приемники уже в течение некоторого времени выпускаются различными изготовителями (например: The BBI Newsletter, февраль 1999, с.34; H.G.Chotas, J.T.Dobbins, C.E.Ravin “Principles of Digital Radiography with Large-Area, Electronically Readable Detectors: A Review of the Basics”, Radiol, 210 (1999) 595-599). Зачастую они состоят из аморфного кремния или других полупроводниковых материалов. В предлагаемой в изобретении рентгеновской установке используются, прежде всего, следующие приемники: приемники с фосфорными пластинками (например, ф. Fuji Chemical, Konica), с аморфным кремнием (например, ф. GE Medical, Philips Medical, Siemens Medical), с селеном (например, ф. Philips Medical, Toshiba), с гипосульфитом гадолиния (например, ф. Kodak), с полупроводниковыми элементами из теллурида кадмия (СТ) или теллурида кадмия-цинка CZT), с оксиортосиликатом иттрия, оксиортосиликатом лютеция, йодидом натрия или германатом висмута. Особенно хорошие результаты достигаются с так называемыми С(Z)Т-приемниками, т.е. с приемниками, выполненными из полупроводникового материала теллурида кадмия - (C(Z)T).
Подробное описание конструкции энергодисперсионного приемника из полупроводникового материала приведено в патенте US 5434417 А. В этом случае предусмотрены сегментированные полупроводниковые ленты, облучаемые рентгеновскими лучами с торцовой стороны. Излучение проходит в полупроводниковый материал и начинает взаимодействовать с полупроводниковым материалом. Глубина проникновения зависит от энергии рентгеновских фотонов. При большей энергии рентгеновских фотонов излучение проникает глубже, чем при меньшей энергии рентгеновских фотонов, пока не начнет взаимодействовать с материалом приемника и под действием фотоэлектрического эффекта генерировать импульс тока. Импульсы тока в отдельных сегментах приемника могут сниматься с установленных там электрических контактов. Импульсы тока обрабатываются в предварительном усилителе.
Приемник, во-первых, может быть выполнен плоскостного типа. В этом варианте исполнения все элементы изображения регистрируются одновременно и направляются для анализа в блок корреляции. В этом случае приемник представляет собой плоскую схему из отдельных детекторных чувствительных элементов (датчиков) предпочтительно в виде матрицы, в которой детекторные чувствительные элементы расположены в строках и столбцах.
Во-вторых, может быть предусмотрен блок приемников, который служит для определения испускаемого рентгеновского излучения и выполнен с возможностью формирования изображения в испускаемых лучах, а для этого выполнен с рентгенооптическим модулем для энергетической селекции.
Вместо плоскостного приемника могут использоваться также строчные приемники или матрица из нескольких приемников для съемки отдельного элемента изображения. В таких приемниках рентгеновское излучение от исследуемого объекта одновременно направляется по рентгеновским световодам. Множество таких световодов объединяется в планарный приемник.
Помимо этого, приемник может быть выполнен с возможностью регистрации одного отдельного элемента изображения и установлен с возможностью перемещения для регистрации всех элементов изображения. В этом варианте приемник при измерении может регистрировать только энергозависимые интенсивности в отдельном элементе изображения. Значения интенсивности отдельных элементов изображения регистрируются последовательно, например построчно, и для дальнейшей обработки направляются в блок корреляции.
Кроме того, приемник может содержать матрицу детекторных чувствительных элементов содержит матрицу детекторных чувствительных элементов, каждый из которых выполнен с возможностью регистрации соответствующего элемента изображения, установленную с возможностью перемещения для регистрации всех элементов изображения. Под матрицей детекторных чувствительных элементов согласно настоящему изобретению понимается как строка детекторных чувствительных элементов, так и другая схема детекторных чувствительных элементов, например табличная. В этом варианте исполнения приемник регистрирует значения интенсивности в отдельных элементах изображения построчно или в некоторых случаях поблочно. Для регистрации всех значений интенсивности приемник во время измерения перемещается предпочтительно перпендикулярно к главной оси матрицы. Определенные при измерении значения интенсивности передаются для обработки в блок корреляции.
Для формирования изображения, например распределения рентгеноконтрастных химических элементов в исследуемом объекте, целесообразно регистрировать интенсивности излучения, испускаемого соответствующими пространственными элементами с одинаковой значимостью. Далее для этой цели целесообразно также воздействовать на пространственные элементы излучением одинаковой интенсивности от рентгеновского источника. Однако на практике оказывается, что эти посылки существуют лишь условно, так как, с одной стороны, падающее рентгеновское излучение в исследуемом объекте в различной степени ослабляется поглощением в зависимости от пути, пройденного лучами до приемника, а, с другой стороны, излучение, испускаемое пространственными элементами в исследуемом объекте в зависимости от того, какой путь лучи в исследуемом объекте еще должны пройти до приемника, в различной степени ослабляется собственным поглощением.
Эта проблема присуща всем эмиссионно-спектроскопическим методам. Для того чтобы решить эту проблему, значения второй интенсивности сначала корректируют с учетом поглощения падающего рентгеновского излучения и/или собственного поглощения испускаемого рентгеновского излучения в исследуемом объекте, и только после этой корректировки выполняется осуществляемое по элементам изображения соотнесение значений первой и второй интенсивности. Такую коррекцию можно выполнить с помощью цифровых методов с учетом геометрической формы исследуемого объекта и по меньшей мере приближенно пространственно зависимой плотности рентгеновского излучения. Для определения пространственно зависимой плотности рентгеновского излучения можно использовать изображения, полученные по значениям первой интенсивности. Для определения пространственно зависимого поглощения и собственного поглощения можно в первом приближении брать за основу полученную путем измерения пространственно зависимую плотность рентгеновского излучения, так как коэффициенты поглощения проходящего и испускаемого рентгеновского излучения идентичны.
Далее с учетом собственного поглощения испускаемого излучения может оказаться целесообразным изменение положения и угла установки второго приемника относительно исследуемой зоны во время измерения, например по дуговой траектории, чтобы компенсировать структурные неоднородност