Способ получения окислителя энергетических конденсированных систем
Иллюстрации
Показать всеИзобретение относится к окислителям твердотопливных энергетических конденсированных систем на основе двойного окислителя перхлорат - нитрат аммония. Способ заключается в смешении безводных солей нитрата аммония и перхлората аммония в виде кристаллов фракции менее 50 мкм при соотношении компонентов в смеси НА:ПХА=0,9-0,1:0,1-0,9 в термостойком сосуде и нагреве до 185°С в течение 20-30 минут, после чего температуру поднимают до 200-250°С и термостатируют смесь в течение 8-12 часов. Разработанный способ позволяет безопасно получать термически стабильный экологически чистый окислитель, содержащий нитрат аммония и не менее 10% перхлората аммония с улучшенными физико-химическими свойствами: фазостабильный, термически стабильный, обладающий более высокими энергетическими характеристиками. 3 ил., 4 пр.
Реферат
Изобретение относится к области энергетических конденсированных систем (ЭКС). Окислитель, полученный по данному способу, может быть использован в твердотопливных составах газогенерирующих устройств нового поколения, например, в автомобильных подушках безопасности, твердотопливных огнетушителях, спасательных шлюпках, ракетных топливах и др.
Известен способ получения окислителя энергетических конденсированных систем, заключающийся в смешении перхлората аммония NH4ClO4 (ПХА) и нитрата аммония NH4NO3 (НА) с модифицирующими добавками (катализаторами термического разложения, фазовыми стабилизаторами и др.). (1. Gas-generating compositions. Пат. 6846373 США, МПК 7 C06B 31/28. NOF Corp., Takayama Shinsuke, Serizawa Kazuya, Takahashi Katsuhiko. N 10/027136; Заявл. 26.12.2001; Опубл. 25.01.2005; Приор. 27.12.2000, N 2000-397718 (Япония).
2. De Luca L.Т., Galfetti L., Severini F., Taiariol P., Babuk V.A., Kondrikov B.N., Vorozhtsov А.В., Klyakin G. Ballistic properties of solid rocket propellants based on dual-oxidizer (ammonium perchlorate and ammonium nitrate) mixtures // Progress in Combustion and Detonation: Proceedings of the International Conference on Combustion and Detonation (Zel'dovich Memorial), Moscow, Aug.30-Sept.3, 2004: Abstracts of Papers. Moscow: TORUS PRESS. 2004, с.151-152.
3. Баллистические свойства твердых ракетных топлив, основанных на смесях двух окислителей - перхлорат аммония - нитрат аммония Yoshida Saeko, Kohga Makoto (National Defense Academy, 1-10-20 Hashirimizu, Yokosuka, Kanagawa 239-8686, Japan) Sci. and Technol. Energ. Mater. 2006. 67, N 4, с.117-123.)
Основной причиной, препятствующей достижению технического результата, который обеспечивается нашим изобретением, является неравномерное распределение компонентов, входящих в состав окислителя, в объеме горючего-связующего.
Наиболее близким к предлагаемому изобретению по технической сущности и достигаемому результату и принятому за прототип является изобретение «Окислители с улучшенной термической стабильностью и метод их изготовления» (патент США №3708357, зарег. 21.04.1971 г., опубл. 02.01.1973 г. Morrow; Scott I. (Morris Plains, NJ) Oxidizers With Improved Thermal Stability And Method Of Making Same The United States of America as represented by the Secretary of the Army), заключающийся в смешивании НА и ПХА и нагревании этой смеси до температуры не выше 185°C. Основной причиной, препятствующей достижению технического результата, который обеспечивает наше изобретение, является то, что согласно прототипу «…смесь компонентов, нагретая до вышеназванной температуры, будет плавиться без окисления, т.е. ПХА будет растворяться в образующейся жидкости (расплаве НА)». Исследования, проведенные нами и авторами (Посыпайко В.И., Алексеева Е.А., Васина Л.А. Диаграммы плавкости солевых систем. / Справочник, ч.III. - М.: Металлургия, 1979. - С.125; Трунин А.С., Макаров А.Ф., Юлина И.В., Зипаев Д.В. Физико-химические исследования систем на основе перхлората натрия и аммония. // Изв. Томского политехн. ун-та, 2007. - Т.310. №1), показывают, что ПХА может растворяться в плаве НА в количестве не более 8% с образованием эвтектики, а большее количество не растворяется в расплаве НА, а образует механическую смесь. Содержание НА в смеси до 8% не позволяет получить ожидаемого технического результата: фазовой стабильности до 50°C (замена полиморфного перехода IY-III на переход IY-II*), термической стабильности (температура начала интенсивного разложения системы повышается на 20°С), экзотермическим разложением в одну стадию, ростом энергетических характеристик системы (площадь экзотермического пика увеличивается более чем в 1,5 раза), отсутствием фазового превращения ПХА.
Ссылка авторов на возможность использовать другие методы для получения «совместных кристаллов НА и ПХА» неправомочна, так как из водных растворов в данной системе кристаллизуются только механические смеси исходных компонентов (Карнаухов А.С., Ганина Г.И., Заворуева Г.Н., Васильева С.И. Характеристика жидких и твердых фаз системы NH4NO3-NH4ClO4-H2O при 25°C. // Сб. научн. тр. Ярославского гос. пед. ин-т. - 1978. - №169. - С.20-22; Карнаухов А.С. Водная взаимная система из хлорнокислых и азотнокислых солей аммония и калия при 25°C. // Ж. неорг. химии. - 1957. - Т.2, вып.4. - С.915-927).
Основная задача, решаемая предлагаемым изобретением, заключается в разработке безопасного способа получения дешевого и экологически чистого окислителя ЭКС, представляющего собой совместные кристаллы перхлората и нитрата аммония с новыми физико-химическими свойствами.
Технический результат, на достижение которого направлено настоящее изобретение, состоит в следующем: при сохранении основных преимуществ системы НА - ПХА, разработать безопасный способ получения совместных кристаллов НА и ПХА, представляющих собой устойчивую равновесную фазу с содержанием ПХА от 10-90% и обладающих новыми физико-химическими свойствами: фазовой стабильностью до 50°C (замена полиморфного перехода IY-III на переход IY-II*), термической стабильностью (температура начала интенсивного разложения системы повышается на 20°С), экзотермическим разложением в одну стадию, ростом энергетических характеристик системы (площадь экзотермического пика увеличивается более чем в 1,5 раза), отсутствием фазового превращения ПХА. Технический результат, достигаемый в результате описанного способа, обеспечивается проведением твердофазного процесса между кристаллами НА и ПХА в процессе длительного нагрева системы.
Поставленная задача решается разработкой способа проведением твердофазной реакции между кристаллами НА и ПХА:
способ получения окислителя энергетических конденсированных систем, включающий смешение безводных солей - НА и ПХА в соотношении НА:ПХА=0,9-0,1:0,1-0,9 в термостойком сосуде, нагреве смеси при интенсивном перемешивании до 185°C, причем для смешения берут фракцию кристаллов менее 50 мкм, а нагрев до температуры 185°C осуществляется в течение 20-30 мин, затем температуру поднимают до 200-250°C и образовавшуюся смесь термостатируют в течение 8-12 часов в стационарных условиях.
Контроль процесса осуществляют по дифференциально-термическому (ЛТА) и рентгено-фазовому анализам (РФА).
Авторами впервые установлено, что совокупность вышеназванных технологических операций позволяет решить техническую задачу за счет образования в результате термостатирования совместных кристаллов НА и ПХА в виде устойчивой системы, обладающей новыми физико-химическими свойствами. Особенность проведения данного процесса состоит в том, что нагреву подвергаются лабильные соли, причем температура нагрева близка к температуре разложения системы. Ингибирование термораспада системы в процессе нагрева обеспечивает наличие ионов NH4 + образующихся в процессе диссоциации НА.
Сущность изобретения поясняется примерами его реализации.
Пример 1 (прототип)
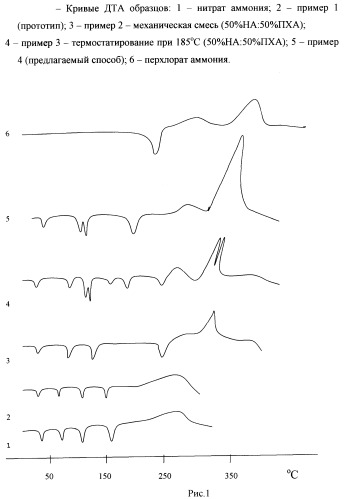
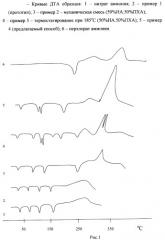
Процесс осуществлен по патенту США №3708357. НА марки «чда» в количестве 9 г и ПХА марки «хч» в количестве 1 г после смешения загружают в термостойкий стеклянный сосуд с регулируемым нагревом и смесь нагревают до 185°C (расплавляют до полного растворения твердой фазы). После завершения процесса смесь охлаждают, измельчают, при необходимости фракционируют и исследуют методом ДТА. Результаты представлены на рисунке 1.
Пример 2 (50:50) (механическая смесь-аналог)
НА марки «чда» в количестве 1 г и ПХА марки «хч» в количестве 1 г после смешения и механического истирания в фарфоровой ступке исследуют методом дифференциально-термического анализа (рис.1).
Пример 3 (50:50)
НА марки «чда» в количестве 1 г и ПХА в количестве 1 г после смешения загружают в стеклянный сосуд с регулируемым нагревом и при температуре 185°C нагревают в течение 20-30 мин, постоянно перемешивая систему стеклянной мешалкой. После завершения процесса смесь охлаждают, измельчают, при необходимости фракционируют и исследуют методом дифференциально-термического анализа (рис.1).
Пример 4 (50:50) (предлагаемый способ)
Процесс ведут по примеру 3, но со следующими отличиями: после нагрева системы до 185°C в течение 20-30 мин при интенсивном перемешивании температуру поднимают до 200-250°C и выдерживают при этой температуре в стационарных условиях в течение 8 ч. Полученный образец исследуют методом ДТА (рис.1).
Образец, полученный по предлагаемому способу (пример 4) имеет набор термоэффектов, отличающихся от механической смеси исходных компонентов и от образцов, полученных по примеру 2 и 3 (рисунок 1). В образце отсутствует полиморфный переход IY-III НА, а имеется переход IY-II* при температуре 56°C (что увеличивает фазовую стабильность смеси). Кроме этого, появляется новый термоэффект при 130°C (инконгруэнтное плавление двойной соли), а также отсутствует полиморфный переход ПХА при 240°C (из орторомбической модификации в кубическую). Экзоэффект термораспада системы превышает по площади таковой для примеров 2 и 3 в 1,5 раза и происходит в 1 стадию (что подтверждено дериватографическими исследованиями).
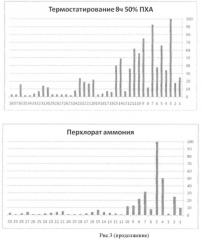
Основной проблемой при проведении данного процесса получения совместных кристаллов является безопасность, так как оба соединения лабильны, причем НА начинает разлагаться при температуре 220°C. Действительно, в процессе нагрева системы при температуре 200-250°C наблюдается потеря массы образца (рисунок 2), которая зависит от времени термостатирования. При нагреве системы до 1 ч потеря массы не превышает 1-2%, что можно отнести к потере влаги (адсорбционной и внутрикристаллической). Дальнейшее термостатирование приводит к росту потери массы образца до 3-5%, что можно отнести к возгонке ПХА. При термостатировании образцов более 8 ч начинается более активное разложение, что может привести к автокаталитическому распаду системы, поэтому оптимальным временем проведения твердофазного процесса является 8 ч. Удачное соотношение двух лабильных солей и предварительный нагрев системы до температуры 185°C позволяет провести твердофазный процесс при температурах 200-2 50°C без разложения системы за счет аммиака, который ингибирует термораспад аммониевых солей.
Плотность образца состава 50:50 1,76 г/см3, что близко к плотности ПХА высокотемпературной (кубической) модификации, что является подтверждением предположения об образовании в системе сложной композиции.
Основным достоинством разработанного способа является безопасность проведения твердофазного процесса, так как НА - лабильное соединение, диссоциирующее на аммиак и азотную кислоту уже при температуре более 160°C.
На рисунке 3 представлены штрихрентгенограммы образцов, подтверждающие индивидуальность соединения, полученного после 8 ч нагрева при температуре 200-250°C.
Способ получения окислителя энергетических конденсированных систем, включающий смешение безводных солей - нитрата аммония (НА) и перхлората аммония (ПХА) в термостойком сосуде, нагрев до 185°С, отличающийся тем, что смешивают кристаллы фракции менее 50 мкм, соотношение компонентов в смеси НА:ПХА=0,9-0,1:0,1-0,9, а нагрев осуществляется в течение 20-30 мин, после чего температуру поднимают до 200-250°С и термостатируют смесь в течение 8-12 ч.