Способ синтеза макролидов
Иллюстрации
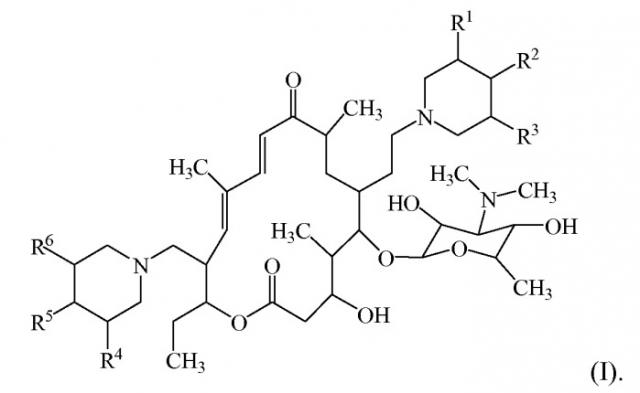
Показать всеНастоящее изобретение относится к способу получения макролида формулы (I)
или его соли, к способу лечения пастереллеза, респираторной болезни свиней и респираторной болезни крупного рогатого скота с использованием соединений формулы (I), а также к способу получения соединения формулы (III)
3 н. и 8 з.п. ф-лы, 3 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ПАТЕНТНЫЕ ЗАЯВКИ
Настоящий патент притязает на приоритет по предварительной патентной заявке США № 60/834067 (поданной 28 июля, 2006) и европейской патентной заявке № 06118159.0 (поданной 31 июля, 2006). Полный текст этих патентных заявок включен в данный патент посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к способу получения макролидов, и, в частности, к способу получения необязательно замещенного 20,23-дипиперидинил-5-О-микаминозил-тилонолида и его производных, а также к способам лечения с использованием таких макролидов, применению таких макролидов для получения лекарственных средств и способам получения промежуточных соединений, которые, inter alia, можно использовать для получения макролидов.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Эффективность макролидов для лечения инфекционных заболеваний людей, домашнего скота, домашней птицы и других животных известна давно. Самые первые макролиды включали 16-членные макролиды, такие как, например, тилозин А:
См., например, патент США № 4920103 (колонка 5, строки 12-38). См. также патент США № 4820695 (колонка 7, строки 1-32) и EP 0103465B1 (страница 5, строка 3). Со временем, для того чтобы увеличить антибактериальное действие и избирательность соединений, были разработаны производные тилозина.
Производные тилозина включают, например, соединения, рассматриваемые в патенте США № 6514946, которые соответствуют по структуре формуле (I):
где:
каждый из R1 и R3 представляет собой метил, а R2 представляет собой водород; каждый из R1 и R3 представляет собой водород, а R2 представляет собой метил; или каждый из R1, R2 и R3 представляет собой водород; и
каждый из R4 и R6 представляет собой метил, а R5 представляет собой водород; каждый из R4 и R6 представляет собой водород, а R5 представляет собой метил; или каждый из R4, R5 и R6 представляет собой водород.
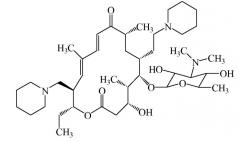
Такие соединения включают, например, 20,23-дипиперидинил-5-О-микаминозил-тилонолид, который имеет следующую структуру:
Полагают, что эти соединения, и, в частности, 20,23-дипиперидинил-5-О-микаминозил-тилонолид обладают фармакокинетическими и фармакодинамическими свойствами для безопасного и эффективного лечения, например, пастереллеза, респираторной болезни крупного рогатого скота и респираторной болезни свиней. Обсуждение, относящееся к применению этих соединений для лечения домашнего скота и домашней птицы, включено в патент США № 6514946. Настоящее обсуждение включено в данный патент посредством ссылки.
В литературе опубликованы различные методы получения макролидов.
Например, в EP 0103465B1 авторы Debono et al. обсуждают различные стадии способа получения соединений, относящихся к данному классу. Эти способы включают, например, следующее восстановление:
где: R, R1, R2, R3, и R4 определены как различные заместители. В частности, R определен как азотсодержащая кольцевая система, имеющая до 3 ненасыщенных или насыщенных колец, необязательно, замещенных. В публикации Debono et al. указано, что цианоборгидрид является «предпочтительным восстановителем». Авторы Debono et al. также утверждают, что обычным растворителем для этой реакции является инертный полярный растворитель, такой как алканол С1-С4. См. строки 7-14 на странице 6. В поданном позднее патенте-аналоге авторы Debono et al., кроме того, описывают восстановительное аминирование различных альдегидных соединений (включая тилозин) амином. В качестве подходящих восстановителей упоминаются цианоборгидрид натрия и боргидрид натрия, а в качестве подходящего растворителя упоминается безводный метанол. См. строки 60-68 в колонке 7 патента США № 4820695.
В патенте США № 6664240 авторами Phan et al. также описано восстановительное аминирование:
где: Rp 2, R4, R7 и R8 определены как различные заместители, в частности, R7 и R8 каждый определен как независимый заместитель, или, в качестве альтернативы, вместе они могут образовать гетероциклическое кольцо с количеством звеньев от 3 до 7. Авторы Phan et al. обсуждают проведение этой реакции с боргидридом в растворителе спирте или ацетонитриле. Боргидрид натрия и цианоборгидрид натрия приведены как примеры боргидридных реагентов; а метанол, этанол и изопропанол приведены как примеры спиртовых растворителей. См., например, начиная со строки 64 в колонке 15 до строки 42 в колонке 16; и строки 41-49 в колонке 22.
В EP 0240264B1 авторы Tao et al. также описывают восстановительное аминирование:
где: R1, R2, R3 и R4 определены как различные заместители. В частности, каждый из R3 и R4 определен как независимый заместитель, или, в качестве альтернативы, вместе они могут образовать гетероциклическую кольцевую систему, имеющую до 3 колец, необязательно замещенных. Авторы Tao et al. сообщают, что это восстановление можно осуществить, используя муравьиную кислоту в качестве восстановителя. Кроме того, авторы Tao et al. описывают, что растворителем обычно является инертный полярный органический растворитель. Амилацетат и ацетонитрил приведены в качестве примеров такого растворителя. См. описание, начиная со строки 57 стр. 4 до строки 10 стр. 5. Также см. патент США № 4921947 со строки 62 в колонке 3 до строки 16 в колонке 4.
В патенте EP 0103465B1 авторы Debono et al. описывают следующую реакцию гидролиза:
где: R1, R2, R3 и R4 определены как различные заместители. Авторы Debono et al. описывают данную реакцию следующим образом: «гидролиз можно осуществить, используя водный раствор сильной минеральной кислоты, такой как соляная или серная кислота, или сильную органическую кислоту, такую как п-толуолсульфоновая кислота». См. строки 3-8 на странице 7. Кроме того, в позднее поданном патенте-аналоге авторами Debono et al. описан гидролиз микарозной группы модифицированных по атому углерода С20 производных тилозина, макроцина и DOMM (О-деметилмакроцина) с применением «хорошо известных» методик кислого гидролиза. См. строки 35-43 в колонке 8 патента США № 4820695.
Принимая во внимание значение макролидов для лечения множества патологических состояний, постоянно необходимы экономически выгодные, с высоким выходом, способы получения макролидов. Нижеследующее описание направлено на решение этой проблемы.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам получения макролидов, и, в частности, необязательно замещенного 20,23-дипиперидинил-5-О-микаминозил-тилонолида и его производных. Такие способы включают способы получения самих макролидов, а также способы получения соединений, которые, inter alia, можно использовать в качестве промежуточных соединений для получения различных макролидов.
Вкратце, изобретение отчасти направлено на способ получения макролида и его солей. Макролид соответствует по структуре формуле (I):
где:
что касается R1, R2 и R3:
каждый из R1 и R3 представляет собой метил, а R2 представляет собой водород,
каждый из R1 и R3 представляет собой водород, а R2 представляет собой метил, или
каждый из R1, R2 и R3 представляет собой водород.
Что касается R4, R5 и R6:
каждый из R4 и R6 представляет собой метил, а R5 представляет собой водород,
каждый из R4 и R6 представляет собой водород, а R5 представляет собой метил, или
каждый из R4, R5 и R6 представляет собой водород.
В некоторых вариантах осуществления изобретения способ включает в себя реакцию тилозина (например, тилозина А или его соли), пиперидинильного соединения формулы (II) и муравьиной кислоты в присутствии неполярного растворителя. В этих вариантах осуществления изобретения пиперидинильное соединение формулы (II) соответствует по структуре:
В некоторых вариантах осуществления изобретения способ включает в себя реакцию соединения 20-пиперидинил-тилозина с кислотой. В этих вариантах осуществления изобретения соединение 20-пиперидинил-тилозин соответствует по структуре формуле (III):
В некоторых вариантах осуществления изобретения способ включает в себя реакцию соединения 23-О-мицинозил-20-пиперидинил-5-О-микаминозил-тилонолида с кислотой. В этих вариантах осуществления изобретения соединение 23-О-мицинозил-20-пиперидинил-5-О-микаминозил-тилонолид соответствует по структуре формуле (IV):
В некоторых вариантах осуществления изобретения способ включает в себя активацию соединения 23-гидрокси-20-пиперидинил-5-О-микаминозил-тилонолида активирующим агентом для получения активированного соединения. В этих вариантах осуществления изобретения соединение 23-гидрокси-20-пиперидинил-5-О-микаминозил-тилонолид по структуре соответствует формуле (V):
Активированное соединение (также именуемое как «соединение 23-L-20-пиперидинил-5-O-микаминозил-тилонолид») соответствует по структуре формуле (VI):
Причем L является уходящей группой.
В других вариантах осуществления изобретения способ включает в себя реакцию активированного соединения формулы (VI) с пиперидинильным соединением формулы (VII). В этих вариантах осуществления изобретения пиперидинильное соединение формулы (VII) соответствует по структуре:
В некоторых вариантах осуществления изобретения способ включает в себя комбинацию перечисленных выше вариантов осуществления для получения макролида формулы (I) или его соли.
В некоторых вариантах осуществления изобретения способ включает в себя один или несколько из перечисленных выше вариантов осуществления для получения макролида формулы (I) или его соли в, например, аморфной, кристаллической, сольватированной форме или в виде сокристаллов.
Настоящее изобретение также отчасти направлено на способ получения соединения 20-пиперидинил-тилозина формулы (III) или его соли. В этих вариантах осуществления изобретения способ включает в себя реакцию тилозина (например, тилозина А), пиперидинильного соединения формулы (II) и муравьиной кислоты в присутствии неполярного растворителя.
Настоящее изобретение также отчасти направлено на способ получения соединения 23-О-мицинозил-20-пиперидинил-5-О-микаминозил-тилонолида формулы (IV) или его соли. В этих вариантах осуществления изобретения способ включает в себя реакцию соединения 20-пиперидинил-тилозина формулы (III) с HBr.
Настоящее изобретение также отчасти направлено на способ получения соединения 23-гидрокси-20-пиперидинил-5-О-микаминозил-тилонолида формулы (V) или его соли. В этих вариантах осуществления изобретения способ включает в себя реакцию соединения 23-О-мицинозил-20-пиперидинил-5-О-микаминозил-тилонолида формулы (IV) с кислотой.
Настоящее изобретение также отчасти направлено на способ получения активированного соединения формулы (VI) или его соли. В этих вариантах осуществления изобретения способ включает в себя активацию соединения 23-гидрокси-20-пиперидинил-5-О-микаминозил-тилонолида формулы (V) активирующим агентом.
Настоящее изобретение также относится к применению соединений формулы (I) (и их фармацевтически приемлемых солей), полученных по этому изобретению, в способах лечения заболевания, такого как пастереллез, респираторная болезнь свиней или респираторная болезнь крупного рогатого скота. Более конкретно, настоящее изобретение отчасти направлено на способ, включающий в себя получение соединения формулы (I) (или его фармацевтически приемлемой соли) по одному или нескольким перечисленным способам; и, затем, введение терапевтически эффективного количества соединения или соли животному, которому необходимо лечение. Настоящее изобретение также отчасти направлено на применение соединения формулы (I) (или его фармацевтически приемлемой соли), полученного по настоящему изобретению, в изготовлении лекарственного препарата, в частности лекарственного препарата для применения в приведенных выше способах лечения.
Дополнительные объекты и выгоды данного изобретения будут очевидны специалисту после ознакомления с настоящим описанием.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ
ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Данное подробное описание предпочтительных вариантов осуществления изобретения подразумевает только ознакомление других специалистов в данной области с изобретением, его принципами и применением его на практике для того, чтобы они могли адаптировать и применить изобретение в различных вариантах, наилучших для конкретного применения. Несмотря на то, что это подробное описание и его примеры указывают предпочтительные варианты осуществления изобретения, они предназначены только для иллюстрации данного изобретения. Поэтому данное изобретение не ограничено предпочтительными вариантами осуществления, описанными в этой спецификации, и можно осуществить различные модификации изобретения.
А. Макролиды, которые можно получить по данному изобретению
Соединения, которые можно получить по способу данного изобретения, включают соединения, соответствующие по структуре формуле (I):
где:
каждый из R1 и R3 представляет собой метил, а R2 представляет собой водород; каждый из R1 и R3 представляет собой водород, а R2 представляет собой метил; или каждый из R1, R2 и R3 представляет собой водород; и
каждый из R4 и R6 представляет собой метил, а R5 представляет собой водород; каждый из R4 и R6 представляет собой водород, а R5 представляет собой метил; или каждый из R4, R5 и R6 представляет собой водород.
В некоторых вариантах осуществления изобретения пиперидинильные заместители в формуле (I) идентичны, а именно:
В некоторых таких вариантах осуществления изобретения, например, оба пиперидинильных заместителя представляют собой пиридин (т.е. каждый из R1, R2, R3, R4, R5 и R6 представляет собой водород), так что соединение представляет собой 20,23-дипиперидинил-5-О-микаминозил-тилонолид:
Такие соединения включают, например:
Другие соединения, имеющие идентичные пиперидинильные заместители, включают:
В некоторых вариантах осуществления изобретения пиперидинильные заместители формулы (I) не являются идентичными, а именно:
Соединения, имеющие разные пиперидинильные заместители, включают:
Б. Синтез макролидов
Настоящее изобретение можно применять для синтеза макролидов из доступных в данной области веществ.
Б-1. Получение соединения 20-пиперидинил-тилозина
В некоторых вариантах осуществления изобретения синтез макролидов начинается с получения или включает получение соединения 20-пиперидинил-тилозина и, в частности, соединения, соответствующего по структуре формуле (III):
В некоторых вариантах осуществления изобретения каждый из R1 и R3 является метилом, а R2 является водородом; или каждый из R1 и R3 является водородом, а R2 является метилом. В других вариантах осуществления изобретения каждый из R1, R2 и R3 является водородом, так что соединение соответствует по структуре:
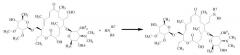
Соединение 20-пиперидинил-тилозин можно получить из тилозина А и пиперидинильного соединения в результате реакции восстановительного аминирования с использованием восстановителя, который содержит муравьиную кислоту (или «НСООН»):
Если каждый из R1, R2 и R3 является водородом, то эта реакция выглядит следующим образом:
Тилозин А, пиперидинильные соединения и муравьиная кислота доступны в продаже.
Реагент тилозин А может, например, представлять собой чистый (или, по меньшей мере, практически чистый) тилозин А. В качестве альтернативы, как отмечено ниже в разделе Б-7, реагент тилозин А может являться частью смеси, такой как, например, смесь, включающая в себя тилозин А, а также одно или несколько производных тилозина А, таких как тилозин В, тилозин С и/или тилозин D.
Тилозин А может находиться в виде свободного основания, или, в качестве альтернативы, может представлять собой соль. Аналогично, производные тилозина А могут, необязательно, находиться в виде одной или нескольких солей. Предполагается, что могут подходить различные соли. Например, в некоторых вариантах осуществления изобретения соль включает в себя фосфат. В других вариантах осуществления изобретения соль включает в себя тартрат. В третьих вариантах осуществления изобретения соль включает в себя цитрат или сульфат. Дальнейшее обсуждение, касающееся солей, можно найти в ниже разделе В.
Растворитель может включать в себя один или несколько растворителей. Хотя растворитель может включать в себя один или несколько полярных растворителей, в некоторых вариантах осуществления изобретения растворитель, предпочтительно, включает в себя один или несколько неполярных растворителей. «Неполярный растворитель» представляет собой растворитель, ионизация которого недостаточна для электрической проводимости и в котором не растворяются (или, по меньшей мере, практически не растворяются) полярные соединения (например, различные неорганические соли), но в котором растворяются неполярные соединения (например, углеводороды и смолы). В общем, предпочтительно, чтоб растворитель не вступал в реакции с реагентами, продуктами и другими компонентами реакционной смеси. Например, растворитель может включать в себя хлороформ (или «CHCl3»); тетрагидрофуран (или «ТГФ»); дихлорметан (или «CH2Cl2» или «ДХМ», или «метиленхлорид»); четыреххлористый углерод (или «CCl4»); этилацетат (или «СН3СООС2Н5»); диэтиловый эфир (или «CH3CH2OCH2CH3»); циклогексан (или «С6Н12»); или ароматические углеводородные растворители, такие как бензол (или «С6Н6»); толуол (или «С6Н5СН3»); ксилол (или «С6Н4(СН3)2» или «диметилбензол» (включая 1,3-диметилбензол (или «м-ксилол»), 1,2-диметилбензол (или «о-ксилол») или 1,4-диметилбензол (или «п-ксилол»)), этилбензол или их смеси (например, смеси м-ксилола, о-ксилола, п-ксилола и/или этилбензола). В некоторых вариантах осуществления изобретения растворитель включает в себя дихлорметан, хлороформ или этилацетат. В других вариантах осуществления изобретения растворитель включает в себя ксилол. В третьих вариантах осуществления изобретения растворитель включает в себя толуол. В некоторых таких вариантах осуществления изобретения особенно предпочтителен толуол, поскольку его легко использовать при обычных температурах проведения реакции.
В некоторых вариантах осуществления изобретения растворитель включает в себя смесь растворителей. Например, в некоторых таких вариантах осуществления изобретения растворитель включает в себя смесь толуола и ДХМ. Где объемное соотношение толуола и ДХМ может, например, составлять от примерно 1:1 до примерно 100:1 или от примерно 5:1 до примерно 8:1. В некоторых из этих вариантов осуществления изобретения соотношение составляет, например, примерно 8:1 (по объему). В других соотношение составляет, например, примерно 5,3:1 (по объему).
Обычно для проведения аминирования в реактор загружают реагент тилозин А, пиперидинильное соединение, муравьиную кислоту (или источник муравьиной кислоты) и растворитель и перемешивают их. В общем, эти компоненты можно загружать в реактор в любой последовательности.
Тип реактора может быть любым. Например, в некоторых вариантах осуществления изобретения реактор представляет собой реакционный аппарат с мешалкой. Часто предпочтительно использовать стеклянные или покрытые внутри эмалью реакторы, хотя можно использовать любой состав, стабильный при воздействии реакционной смеси. Также, например, обычно можно использовать реакторы из нержавеющей стали.
Обычно можно использовать эквимолярные количества реагента тилозина А, пиперидинильного соединения и муравьиной кислоты. Однако, как правило, используют избыточное количество пиперидинильного соединения и муравьиной кислоты относительно молярного количества реагента тилозина А.
В некоторых вариантах осуществления изобретения в реактор загружают от 1 до примерно 3 эквивалентов (или от 1,05 до примерно 3 эквивалентов) пиперидинильного соединения. Например, в некоторых таких вариантах осуществления изобретения в реактор загружают от 1,05 до примерно 1,2 эквивалента пиперидинильного соединения. В других таких вариантах осуществления изобретения в реактор загружают от примерно 1,07 до примерно 1,5 эквивалента пиперидинильного соединения. В которых, например, в реактор можно загрузить примерно 1,3 эквивалента пиперидинильного соединения. В некоторых вариантах осуществления изобретения пиперидинильное соединение загружают в реактор в двух или нескольких загрузках через промежуток времени, причем предпочтительно, чтобы последующая загрузка (последующие загрузки) были меньше первой загрузки. В некоторых вариантах осуществления изобретения, например, пиперидинильное соединение загружают в реактор в двух загрузках, причем количество второй загрузки на 10% меньше количества первой загрузки. Авторы изобретения обнаружили, что это положительно влияет на увеличение степени превращения.
В некоторых вариантах осуществления изобретения используют от 1 до примерно 10 эквивалентов (или от 1,05 до примерно 10 эквивалентов, от примерно 2 до примерно 5 эквивалентов или от примерно 2,5 до примерно 4,5 эквивалентов) муравьиной кислоты. Например, в некоторых вариантах осуществления изобретения используют примерно 4,5 эквивалентов муравьиной кислоты. В других таких вариантах осуществления изобретения используют от примерно 2,5 до примерно 4 эквивалентов муравьиной кислоты. Например, в некоторых таких вариантах осуществления изобретения используют примерно 3,0 эквивалентов муравьиной кислоты.
Обычно растворитель должен быть в количестве, достаточном, например, чтобы предотвратить (или по существу предотвратить) приваривание к реактору реагентов, продуктов и других к реакционной смеси и чтобы обеспечить равномерное распределение реагентов. В некоторых вариантах осуществления изобретения количество растворителя составляет, по меньшей мере, 1 л на кг реагента тилозина А (или, если реагент тилозин А входит в смесь реагента тилозина А и его производных, то на кг общей тилозиновой смеси). Обычно количество растворителя составляет меньше примерно 40 л на кг реагента тилозина А (или тилозиновой смеси). В некоторых вариантах осуществления изобретения количество растворителя составляет от примерно 2 до примерно 15 л (или от примерно 5 до примерно 15 л, от примерно 5 до примерно 12 л, от примерно 5 до примерно 10 л или от примерно 8 до примерно 10 л) на кг реагента тилозина А (или тилозиновой смеси). Для иллюстрации, в некоторых таких вариантах осуществления изобретения растворитель включает толуол или смесь толуола с ДХМ, а количество растворителя составляет от примерно 8 до примерно 10 л на кг реагента тилозина А (или тилозиновой смеси). Где, например, количество растворителя может составлять примерно 8 л на кг реагента тилозина А (или тилозиновой смеси).
Обычно реакцию, по меньшей мере, частично (или полностью) проводят при температуре выше примерно 20°С, выше примерно 25°С или выше примерно 60°С. Обычно реакцию, по меньшей мере, частично (или полностью) проводят при температуре не выше точки кипения растворителя и, чаще всего, при температуре ниже точки кипения. Например, если растворителем является толуол, то обычно реакцию, по меньшей мере, частично (или полностью) проводят при температуре меньше примерно 110°С. В качестве еще одного примера, когда растворителем является ксилол, то, как правило, реакцию, по меньшей мере, частично (или полностью) проводят при температуре меньше примерно 165°С. Обычно реакцию, по меньшей мере, частично (или полностью) проводят при температуре от примерно 60 до примерно 95°С, от примерно 70 до примерно 85°С или от примерно 75 до примерно 80°С. Например, в некоторых вариантах осуществления изобретения температура реакции в течение, по меньшей мере, части времени реакции (или всей реакции) составляет примерно 80°С. Например, в других вариантах осуществления изобретения температура реакции в течение, по меньшей мере, части времени реакции (или всей реакции) составляет примерно 76°С. Хотя можно использовать температуры ниже указанного диапазона, при таких температурах понижается скорость реакции. Аналогично, хотя можно использовать температуры выше указанного диапазона, при таких температурах повышается выход нежелательных побочных продуктов реакции.
Реакцию можно проводить при любом давлении, включая атмосферное давление и давление ниже и выше атмосферного. Однако обычно предпочтительно проводить реакцию при давлении, примерно равным атмосферному. В предпочтительных вариантах осуществления изобретения эту реакцию проводят в инертной атмосфере (например, под азотом).
Время реакции может зависеть от различных факторов, которые включают, например, температуру реакции, свойства растворителя, относительные количества компонентов и желаемую степень превращения. В реакторе периодического действия время реакции, в общем, составляет, по меньшей мере, примерно 1 минуту, обычно, по меньшей мере, примерно 5 минут и чаще всего, по меньшей мере, примерно 1 час. В общем, время реакции составляет меньше 24 часов. Например, в некоторых вариантах осуществления изобретения время реакции составляет от примерно 0,5 до примерно 12 часов или от примерно 1 до примерно 4 часов. В некоторых таких вариантах осуществления изобретения время реакции составляет примерно 3,5 часов. В некоторых других таких вариантах осуществления изобретения время реакции составляет от примерно 1 до примерно 3 часов. В этих вариантах осуществления изобретения время реакции может составлять, например, примерно 2 часа. Хотя можно использовать время реакции короче указанного диапазона, но при этом выход реакции снижается. А также, хотя можно использовать большее время реакции, но при этом получают большее количество примесей и неэффективно используются оборудование и людские ресурсы.
Очистку и выделение продукта реакции можно, например, провести различными способами, известными в данной области. В качестве альтернативы, продукт можно использовать в следующей стадии без дальнейшей очистки или выделения.
Б-2. Получение соединения 23-мицинозил-20-пиперидинил-5-О-микаминозил-тилонолида
(Гидролиз микарозилоксильного заместителя)
В некоторых вариантах осуществления изобретения синтез макролида начинается с получения или включает получение соединения 23-О-мицинозил-20-пиперидинил-5-О-микаминозил-тилонолида и, в частности, соединения, соответствующего по структуре формуле (IV):
В некоторых вариантах осуществления каждый из R1 и R3 является метилом, а R2 является водородом; или каждый из R1 и R3 является водородом, а R2 является метилом. В других вариантах осуществления изобретения каждый из R1, R2 и R3 является водородом, так что соединение соответствует по структуре:
Соединение 23-О-мицинозил-20-пиперидинил-5-О-микаминозил-тилонолид можно получить кислотным гидролизом соединения 20-пиперидинил-тилозина:
Если каждый из R1, R2 и R3 является водородом, то эта реакция выглядит следующим образом:
Соединение 20-пиперидинил-тилозин можно получить способом, описанным выше в разделе Б-1, можно получить другим способом (например, способом, в котором в качестве восстановителя используется боргидрид) или можно приобрести у коммерческого поставщика. В некоторых предпочтительных вариантах осуществления изобретения соединение 20-пиперидинил-тилозин получают способом, описанным выше в разделе Б-1.
Кислотой может быть, например, сильная минеральная кислота, такая как соляная кислота (или «HCl»), азотная кислота (или «HNO3»), фтороборная кислота(или «HBF4»), серная кислота (или «H2SO4»), фосфорная кислота (или «Н3РО4»), полифосфорная кислота (или «РРА») или бромоводородная кислота (или «HBr»); или сильная органическая кислота, такая как п-толуолсульфоновая кислота или трифторуксусная кислота («CF3COOH»). В некоторых вариантах осуществления изобретения кислота включает в себя HCl. В других вариантах осуществления изобретения кислота включает в себя HBr. Использование HBr дает меньше примесей в смеси продуктов реакции по сравнению, например, с HCl. В некоторых вариантах осуществления изобретения используется смесь кислот (в частности, сильной кислоты с другой кислотой).
В общем, достаточное количество кислоты смешивают с соединением 20-пиперидинил-тилозином для гидролиза (т.е. отщепления) микарозилоксильного заместителя, при этом образуется гидроксильная группа. Обычно количество кислоты будет составлять, по меньшей мере, один эквивалент исходя из количества соединения 20-пиперидинил-тилозина. Обычно кислоту добавляют в реакционную смесь в концентрированном виде. Концентрация обычно не превышает примерно 50% (масса/объем), не превышает примерно 48% (масса/объем), составляет от примерно 1 до примерно 30% (масса/объем) или от примерно 1 до примерно 24% (масса/объем). В некоторых вариантах осуществления изобретения кислотой является HBr, и концентрация раствора кислоты, добавленного к реакционной смеси, составляет примерно 24% (масса/объем). В некоторых вариантах осуществления изобретения концентрированная кислота включает в себя смесь кислот, такую как, например, смесь HBr с другой кислотой.
В общем, компоненты реакционной смеси можно загружать в реактор в любой последовательности. Тип реактора может быть любым. В некоторых вариантах осуществления изобретения, например, реактор представляет собой реакционный аппарат с мешалкой. Часто, предпочтительно, использовать стеклянные или покрытые внутри эмалью реакторы, хотя можно использовать любой состав, стабильный при воздействии кислой реакционной смеси.
Как правило, гидролиз, по меньшей мере, частично (или полностью) проводят при температуре выше точки затвердевания смеси, чтобы смесь можно было перемешивать, и смесь была гомогенной. Обычно предпочтительная температура, по меньшей мере, составляет примерно 10°С (или выше примерно 15°С, или выше примерно 25°С). Обычно температура реакции не превышает точку кипения растворителя (например, воды), и, обычно, она ниже точки кипения. В некоторых вариантах осуществления изобретения реакцию, по меньшей мере, частично (или полностью) проводят при температуре, не превышающей примерно 100°С (или не превышающей примерно 65°С). В некоторых вариантах осуществления изобретения, если кислотой являются HCl или HBr, то температура реакции на протяжении ее части (или всей реакции) составляет от примерно 20 до примерно 60°С. В некоторых таких вариантах осуществления изобретения температура реакции на протяжении ее части (или всей реакции) не превышает 40°С. В некоторых примерах температура реакции на протяжении ее части (или всей реакции) может составлять от примерно 20 до примерно 40°С, от примерно 25 до примерно 40°С или от примерно 30 до примерно 40°С. В других вариантах осуществления изобретения, если кислотой являются HCl или HBr, температура реакции на протяжении ее части (или всей реакции) составляет от примерно 45 до примерно 60°С или от примерно 50 до примерно 56°С. Для иллюстрации, в таких вариантах осуществления изобретения температура реакции на протяжении ее части (или всей реакции) может быть, например, примерно 56°С. Хотя можно использовать температуры выше указанного диапазона, при использовании таких температур повышается количество нежелательных побочных продуктов. А также, хотя можно использовать температуры ниже указанного диапазона, они приводят к замедлению скорости реакции. Однако такая скорость может оказаться подходящей, если принять во внимание легкость прохождения реакции гидролиза.
При загрузке кислоты в реактор температуру реакционной смеси можно поддерживать немного ниже желаемой температуры реакции. В таких вариантах осуществления изобретения температура обычно увеличивается после загрузки кислоты в реактор.
Реакцию можно проводить при любом давлении, включая атмосферное давление, давление ниже атмосферного и давление выше атмосферного. Однако обычно предпочтительно проводить реакцию при давлении, примерно равным атмосферному.
Время реакции может зависеть от различных факторов, которые включают, например, температуру реакции, относительные количества компонентов и желаемую степень превращения. В реакторе периодического действия время реакции может быть меньше минуты, т.е. реакция может быть практически самопроизвольной или самопроизвольной. Однако обычно время реакции составляет, по меньшей мере, примерно 1 минуту, обычно, по меньшей мере, примерно 5 минут и, чаще всего, по меньшей мере, примерно 15 минут. Как правило, время реакции составляет меньше 3 часов. В некоторых вариантах осуществления изобретения, например, время реакции составляет от примерно 0,25 до примерно 2 часов, от примерно 0,25 до примерно 1,5 часов или от примерно 0,25 до примерно 1,1 часов. Хотя можно использовать время реакции короче указанного диапазона, но при этом выход реакции снижается. А также, хотя можно использовать большее время реакции, но при этом получается большее количество примесей, и неэффективно используются оборудование и людские ресурсы.
Очистку и выделение продукта реакции можно, например, провести различными способами, известными в данной области. В качестве альтернативы, продукт можно использовать в следующей стадии без дальнейшей очистки или выделения.
Б-3. Получение соединения 23-гидрокси-20-пиперидинил-5-О-микаминозил-тилонолида
(гидролиз мицинозилоксильного заместителя)
В некоторых вариантах осуществления изобретения синтез макролида начинается с получения или включает получение соединения 23-гидрокси-20-пиперидинил-5-О-микаминозил-тилонолида и, в частности, соединения, соответствующего по структуре формуле (V):
В некоторых вариантах осуществления каждый из R1 и R3 является метилом, а R2 является водородом; или каждый из R1 и R3 является водородом, а R2 является метилом. В других вариантах осуществления изобретения каждый из R1, R2 и R3 является водородом:
Соединение 23-гидрокси-20-пиперидинил-5-О-микаминозил-тилонолид можно получить реакцией кислотного гидролиза из сое