Технологический режим для pt-re биметаллических катализаторов конверсии водяного газа, катализаторы
Иллюстрации
Показать всеИзобретения относятся к области химии и могут быть использованы в способах образования водорода. По первому варианту проводят реакцию конверсии водяного газа при температуре от 150 до 450°C в присутствии катализатора на основе Pt-Re. Сырьевой газ включает до приблизительно 20 об.% CO и пар. Газовая объемная скорость сырьевого газа составляет от 4500 до 50000 ч-1. Контроль температуры, объемных % CO, газовой объемной скорости осуществляют таким образом, чтобы ΔТ(50)20ч, означающее разницу температур при 50% конверсии CO, т.е. Т(50)изношенный 20 ч-Т(50)свежий, имело значение менее 7,0. По второму варианту реакцию конверсии водяного газа ведут при температуре более 330°C при газовой объемной скорости сырьевого газа, от менее чем 20000 ч-1×Pt(г/л)/7,4. По третьему варианту реакцию конверсии водяного газа ведут при температуре 280-320°C при газовой объемной скорости сырьевого газа менее чем 15000 ч-1×Pt(г/л)/7,4. По четвертому варианту реакцию конверсии водяного газа ведут при температуре 200-250°C при газовой объемной скорости сырьевого газа менее чем 2500 ч-1×Pt(г/л)/7,4. Сырьевой газ содержит приблизительно 2-6 об.% CO и пара. Изобретения позволяют обеспечить стабильный процесс образования водорода. 4 н. и 6 з.п. ф-лы, 4 ил., 2 табл., 1 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к оптимизации условий эксплуатации платиново (Pt) - рениевых (Re) биметаллических катализаторов конверсии водяного газа с целью продления срока службы катализаторов.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Топливные элементы непосредственно преобразовывают химическую энергию в электричество, таким образом, исключая этапы механического способа, которые ограничивают термодинамическую эффективность, и были предложены как энергетический источник для многих применений. Топливный элемент может быть в два или три раза эффективнее двигателя внутреннего сгорания - с небольшим, если таковое вообще имеется, выделением первичных загрязняющих веществ, таких как монооксид углерода, углеводороды и NOx. Приводимые в движение при помощи топливного элемента транспортные средства преобразует углеводороды, служащие источником энергии для топливного элемента, генерируют меньше углекислого газа (парникового газа) и имеют больший коэффициент полезного действия топлива.
Топливные элементы, включая РЕМ топливные элементы (топливные элементы на протонных мембранах) [также называемые твердотельным полимерным электролитом или (SPE) топливными элементами], производят электроэнергию на основе химической реакции между восстанавливающим агентом (водород) и окисляющим агентом (кислород), которые питают топливные элементы. РЕМ топливный элемент включает анод и катод, разделенные мембраной, которая обычно является мембраной из ионообменной смолы. Анод и катод обычно состоят из частиц углеродного порошка, нанесенных на частицы углерода каталитических частиц и протонпроводящей смолы, перемешанной с каталитическими и углеродными частицами. В обычном способе в РЕМ топливном элементе водород электролитически окисляется до ионов водорода на аноде, состоящем из реакционного платинового катализатора, нанесенного на проводящий углеродный электрод. Протоны проходят через мембрану из ионообменной смолы, которая может быть фторполимером сульфоновой кислоты, названной протонообменной мембраной. Когда затем протоны соединяются с кислородом, который электролитически восстанавливается на катоде, образуется H2O. В этом способе электроны текут через внешнюю цепь для выполнения работы, создавая разность потенциалов на концах электродов.
Топливные процессоры (также известные как топливные преобразователи) производят водородсодержащий газовый поток, который может использоваться для питания топливного элемента или производить водород для особого химического применения или для хранения на водородной заправочной станции. Топливные процессоры включают реакторы, которые преобразуют углеводородное исходное сырье (например, природный газ, сжиженный нефтяной газ (LPG)) и углеводородные производные (например, спирты) в виде пара для получения технологического потока, обогащенного водородом. Другим приемлемым способом риформинга углеводородов является так называемый способ автотермического риформинга, который комбинирует частичное окисление с паровым риформингом. Другие побочные продукты риформинга углеводородов включают монооксид и диоксид углерода. Например, метан преобразуется в водород, монооксид углерода и диоксид углерода согласно трем реакциям ниже:
CH4+H2O→3H2+CO
CH4+2H2O→4H2+CO2
CH4+½O2→2H2+CO
Получающийся газ реагирует далее в реакторе конверсии водяного газа, где технологический поток дополнительно обогащается при реакции монооксида углерода с паром в реакторе конверсии водяного газа:
CO+H2O↔CO2+H2
В топливных процессорах реакция часто проводится в две стадии с целью контроля теплоты и минимизации концентрации выхода CO. Первая стадия оптимизирована для взаимодействия при повышенных температурах (приблизительно 350°C) и обычно производится при использовании катализаторов, основанных на комбинации оксида железа с хромом. Вторая стадия проводится при низшей температуре (приблизительно 200°C) и обычно проводится при использовании катализаторов, основанных на смесях медных и цинковых материалов.
Другие катализаторы, которые могут быть использованы для проведения реакции конверсии водяного газа, включают катализаторы на основе платины (Pt), такие как платина на оксиде алюминия или платина на оксиде церия, содержащем подложку. Несмотря на эффективное образование водорода при применении реакции конверсии водяного газа, в которой применяются температуры выше приблизительно 300°C, катализаторы реакции конверсии водяного газа, кроме того, обусловливают образование метана (CH4) посредством катализа реакции CO с водородом, как показано ниже:
CO+3H2→CH4+H2O
Эта нежелательная побочная реакция жертвует тремя молями водорода на каждый моль монооксида углерода, преобразованного в метан. Метанизация может также иметь место при этих условиях с диоксидом углерода согласно уравнению, показанному ниже:
CO2+4H2→CH4+2H2O
В этой побочной реакции четыре моля водорода жертвуются на каждый моль диоксида углерода, преобразованного в метан. Производство метана во время реакции конверсии водяного газа (называемое здесь как "метанизация") является побочной реакцией, которая расходует водород в экзотермической реакции, в конечном счете понижая выход водорода в реакции конверсии водяного газа. Более того, реакция метанизации ускоряется при увеличении температуры слоя катализатора. Это свойство представляет помеху, поскольку экзотермическая реакция может привести к неконтролируемому взаимодействию с диоксидом углерода, в дополнение к монооксиду углерода, будучи метанизированными. Может произойти потеря основного количества водорода, и катализатор может быть разрушен высокой температурой. К тому же метан является парниковым газом. Топливный элемент позиционируется как источник питания без выбросов, и выделение метана является нежелательным. Метан является трудносгораемым веществом при нормальных условиях эксплуатации топливного элемента, поэтому образование значительных количеств метана является экологически неблагоприятным.
Катализаторы на основе Pt являются сейчас лучшим выбором для замещения основы в металлокатализаторах бытовых топливных процессоров и водородных генераторов для локального производства водорода и низкотемпературных РЕМ топливных элементов. Однако старение катализаторов на основе Pt является отрицательным свойством этого типа катализаторов. Вследствие проблем старения Pt катализаторы рассматриваются как нестабильные в различных способах.
Металлы, такие как кобальт (Со), рутений (Ru), палладий (Pd), родий (Rh) и никель (Ni) также используются как катализаторы конверсии водяного газа, но не являются достаточно активными для селективной реакции конверсии водяного газа и активации реакции метанизации CO в CH4 при стандартных условиях реакции. Другими словами, водород, произведенный при реакции конверсии водяного газа, расходуется, когда вступает в реакцию с подаваемым CO в присутствии таких катализаторов с образованием метана. Эта активность в реакции метанизации ограничивает практическую применимость металлов, таких как Co, Ru, Pd, Rh и Ni как катализаторов конверсии водяного газа.
Недавно были предложены Pt-Re биметаллические катализаторы для использования в реакциях конверсии водяного газа. Например, Pt-Re на подложке из диоксида церия-диоксида циркония показывает увеличение степени конверсии водяного газа в сравнении со степенью, наблюдаемой для одной лишь Pt на подложке из диоксида церия-диоксида циркония, "Pt-Re bimetallic supported CeO2-ZrCr2 mixed oxides as water-gas shift catalyst", Choung et al., Catalysis Today 99 (2005) 257-262. U.S. Patent No.6,777,117 issued August 17, 2004 и U.S. Pat. Pub. No.2003/0186804 published October 2, 2003 раскрывают подобные Pt-Re катализаторы конверсии водяного газа.
Существует необходимость в управлении катализатором конверсии водяного газа на биметаллической Pt-Re основе при условиях, которые уменьшают способ старения такого катализатора и обеспечивают устойчивый режим для производства эффективного количества водорода для использования в топливных элементах.
КРАТКОЕ ИЗЛОЖЕНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение направлено на новый способ, который значительно снижает старение Pt-Re биметаллического катализатора конверсии водяного газа. Неожиданно было найдено, что стабильность и продление эффективной Pt-Re биметаллического катализатора конверсии водяного газа зависит от 1) содержания CO в подаваемом газе, 2) объемной скорости подачи газа, 3) содержания Pt катализатора и 4) температуры. Был найден относительно узкий интервал условий эксплуатации, что в результате значительно уменьшило старение Pt-Re биметаллического катализатора во время проведения конверсии водяного газа.
Удивительно, что Pt-Re катализатор эффективно работает при определенных условиях, но непрерывно стареет в условиях эксплуатации вне диапазона изобретения. Это удивительно, учитывая то, что обычно старение катализатора зависит или от рабочей температуры, или изменяется линейно со скоростью оборота реагентов. В настоящем изобретении старение значительно уменьшается при определенных условиях, включающих повышение температуры, низкую объемную скорость и от низкого до среднего значение концентрации подачи CO.
Было найдено, что в основном Pt-Re биметаллический катализатор конверсии водяного газа работает стабильно при 1) низкой объемной скорости, 2) высокой температуре и 3) низком содержании CO в подаваемом газе при данной концентрации Pt на катализаторе. Чем выше содержание Pt (при равной степени дисперсности) катализатора, тем выше может быть объемная скорость для устойчивой работы без старения катализатора.
КРАТКОЕ ОПИСАНИЕ ФИГУР
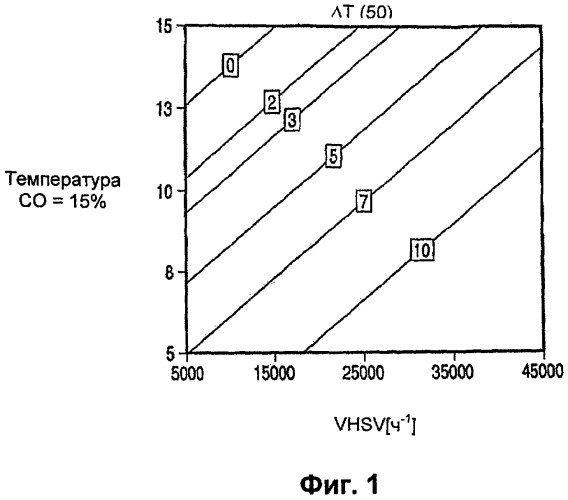
Фиг.1 показывает точки одинаковой стабильности Pt-Re катализатора в зависимости от объемной скорости и температуры при высокой концентрации CO.
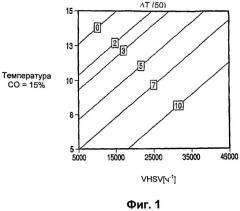
Фиг.2 показывает точки одинаковой стабильности Pt-Re катализатора в зависимости от объемной скорости и температуры при низкой концентрации CO.
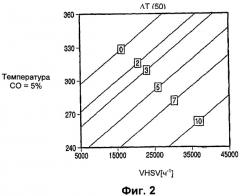
Фиг.3 показывает точки одинаковой стабильности Pt-Re катализатора в зависимости от объемной скорости и концентрации CO при умеренной температуре.
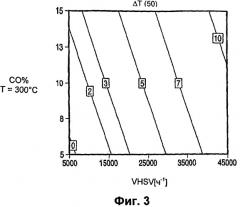
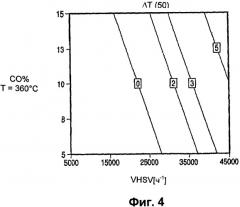
Фиг.4 показывает точки одинаковой стабильности Pt-Re катализатора в зависимости от объемной скорости и концентрации CO при высокой температуре.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение обеспечивает способ использования Pt-Re каталитического состава конверсии водяного газа ("КВГ") при заданных условиях эксплуатации, что минимизирует старение каталитического состава.
Катализатор содержит по меньшей мере Pt и Re и, необязательно, палладий, родий, рутений, иридий и осмий. Как правило, содержание платинового металла в каталитическом составе в дополнение к дополнительным металлам составляет по меньшей мере 0.1 мас.%. Предпочтительно от 0.5 до 10 мас.% и более предпочтительно от 0.75 до 8 мас.% платинового металла в каталитическом составе. Содержание платинового металла от 1.0 до 10 мас.% также представлено в качестве примера. В основном массовое соотношение Pt:Re составляет от 10:1 до 1:5. Также представлено в качестве примера соотношение Pt:Re от 5:1 до 1:1 и, как правило, от 5:1 до 2:1.
В основном биметаллический Pt-Re катализатор обеспечен неорганической оксидной подложкой. Пригодные неорганические оксидные подложки носителей включают неорганические оксидные подложки с большой поверхностной площадью. Эти неорганические оксидные подложки включают, например, активированный оксид алюминия, диоксид циркония, диоксид титана, диоксид кремния и оксиды редкоземельных металлов и их смешанные оксиды. Особенно пригодные подложки включают диоксид циркония, смешанный оксид диоксида циркония-диоксида церия, легированный редкоземельными металлами диоксид циркония или диоксид циркония-диоксид церия. В основном неорганическая оксидная подложка имеет удельную площадь поверхности по меньшей мере 10 м2/г. Более предпочтительно неорганическая оксидная подложка имеет удельную площадь поверхности по меньшей мере 50 м2/г.
Во всех осуществлениях настоящего изобретения катализатор предпочтительно сформирован нанесением платины и рения на неорганическую оксидную подложку. Платину и рений предпочтительно наносят на неорганическую оксидную подложку посредством контакта подложки с водорастворимыми или вододиспергируемыми солями платины и рения в течение достаточного времени для пропитывания неорганической оксидной подложки с последующей стадией сушки. Пропитывание может быть достигнуто при использовании начального влажного пропитывания, в котором для пропитывания неорганической оксидной подложки используются минимальные количества растворов соли металла. В других вариантах воплощения изобретения пропитывание может быть достигнуто при использовании большего соотношения растворов солей платиновых и рениевых металлов. Пригодные соли платиновых и рениевых металлов включают, но не ограничиваются ними, нитрат платины, аминорастворимый гидроксид платины, перренат аммония, перренатная кислота и т.п. Подложка, содержащая компоненты платиновой и рениевой групп металлов, может быть обожжена для формирования металлов или оксидов предпочтительно при температуре выше приблизительно 400°C.
Неорганическая оксидная подложка может быть модифицирована добавлением к ней оксидов редкоземельных металлов. Редкоземельные металлы имеют атомные номера 57-71 в Периодической таблице элементов. Предпочтительно редкоземельные элементы, которые могут быть включены в неорганическую оксидную подложку, включают оксиды лантана, церия, празеодима, неодима, прометия, самария, европия и гадолиния. Также пригодными являются оксиды иттербия. Оксид редкоземельного металла предпочтительно нанесен на неорганическую оксидную подложку посредством контакта неорганической оксидной подложки с водорастворимой или вододиспергируемой солью редкоземельного металла в течение достаточного времени для пропитывания неорганической оксидной подложки с последующей стадией сушки. Пропитывание может быть достигнуто при использовании начального влажного пропитывания, в котором для пропитывания неорганической оксидной подложки используются минимальные количества растворов соли редкоземельного металла. В других вариантах воплощения изобретения пропитывание может быть достигнуто при использовании большего соотношения растворов соли редкоземельного металла. Пригодные соли редкоземельных металлов включают, но не ограничиваются ними, хлориды, сульфаты, нитраты, ацетаты редкоземельных металлов и т.п. После сушки соль редкоземельного металла преобразуется в оксид обжигом на воздухе при температурах выше приблизительно 300°C. Оксид редкоземельного металла, если присутствует, обычно составляет от 2 до 20 мас.% по отношению к катализатору. Также представлены в качестве примера катализаторы с содержанием оксида редкоземельного металла от 3 до 15 мас.%.
Pt-Re биметаллический катализатор может быть модифицирован путем добавления молибденового промотора катализатора. Такой промотор обычно находится в форме оксида, например МоО3. Могут использоваться молибдаты, такие как BaMoO4, Се2(MoO4)3, La2(МоО4)3, Y2(MoO4)3. В основном такие промоторы, если используются, присутствуют в количествах от приблизительно 0.1 до 10 мас.% от катализатора. Содержание оксидов Mo также составляет от 1 до 5% от массы катализатора.
Необязательно катализатор, включающий неорганическую оксидную подложку, металл платиновой группы и рениевый металл, может быть усилен прибавлением соединений щелочных металлов. В частности, было найдено, что прибавление соединений лития, натрия, калия, рубидия и цезия увеличивает первоначальную каталитическую активность. В основном компонент щелочного металла может быть добавлен к катализатору диспергированием соединения щелочного металла в воде и пропитыванием модифицированной неорганической оксидной подложки, высушиванием и обжигом на воздухе с образованием оксида щелочного металла. Соединение щелочного металла может быть добавлено одновременно с пропитыванием платиной или в отдельной стадии. Для внедрения в катализатор путем пропитывания компонент щелочного металла может быть в форме, например, гидроксида или хлорида, нитрата, сульфата, карбоната и т.п., или в виде соли щелочного металла с низшими органическими кислотами, такой как ацетат щелочного металла. В основном количество компонента щелочного металла, если внедрен в катализатор, в перерасчете на щелочной металл составляет от приблизительно 0.1 до 15 мас.% относительно подложки, также с приведением в качестве примера содержания от 0.5 до 10 мас.%.
Наносные покрывающим слоем композиции, экструдаты и таблетки катализатора предпочтительно формируются из измельченных каталитических составов, содержащих платиновые и рениевые металлы. С другой стороны, платиновые и рениевые металлы могут быть добавлены после образования каталитического состава в любой пригодной форме.
Наносные покрывающим слоем композиции (или "взвеси") катализатора для нанесения покрытия на подложки являются особенно пригодными формами каталитического состава в настоящей заявке. Такие наносные покрывающим слоем композиции приготавливаются при помощи методов, известных в уровне техники. Предпочтительно катализатор, измельченный в шаровой мельнице, представляет собой суспензию с использованием достаточного количества воды для приготовления жидкого раствора с необходимой концентрацией. Концентрация твердых частиц в наносной покрывающим слоем суспензии может использоваться в качестве метода контроля толщины слоя катализатора, нанесенного в конечном итоге на подложку. Например, увеличение массового содержания твердых частиц в водном жидком растворе приведет к более толстому каталитическому слою.
Также предпочтительней приготовить суспензию, содержащую частицы маленького размера, например менее чем 10 мкм, чтобы привязать катализатор к подложке. Поэтому обычно измеряется распределение частиц по размерам, и перемалывание продолжают до достижения необходимого размера частиц. И здесь, связующие вещества, такие как гидратированные формы оксида алюминия, например псевдобемит, необязательно включены во взвеси для улучшения адгезии наносного покрывающего слоя к стенкам подложки.
Наносной покрывающий слой взвеси наносят на подложку методами, хорошо известными в обычной практике. Так, например, при обычном приготовлении сотового носителя катализатора слой нанесенного Pt-Re катализатора может быть приготовлен погружением подложки в емкость, содержащую достаточный объем суспензии так, чтобы подложка была полностью погружена. Покрытая подложка может затем быть высушена и обожжена. С другой стороны, подложка может быть покрыта с использованием катализатора, который содержит только Pt, и Re добавляется после стадии покрытия погружением подложки в раствор растворимого Re соединения.
Как указанное выше, наносной покрывающим слоем катализатор может быть распределен на подложке с образованием монолитной покрытой подложки. Хотя могут быть использованы множество подложек, подложка представляет собой предпочтительно одно или более монолитных тел, имеющих множество протянутых через них тонких отверстий для прохода газа (каналов). Предпочтительно монолитная подложка имеет множество тонких параллельных отверстий для прохода газа, тянущихся поперек продольной оси подложки от входной или выходной поверхности, так чтобы каналы были открыты для потока жидкости через них (часто называемая как "сотовый носитель катализатора"). Отверстия, которые являются преимущественно прямыми между входной и выходной поверхностями подложек, определены стенками, на которых каталитическая композиция может быть покрыта наносными покрывающим слоем композициями таким образом, что газы, текущие через отверстия, контактируют с материалом катализатора.
Монолитные сотовые носители катализаторов являются коммерчески доступными в различных размерах и конфигурациях. Проточные каналы монолитной подложки с тонкостенными каналами, которые могут быть любой соответствующей поперечной формы и размера, такой как трапецеидальной, прямоугольной, квадратной, синусоидальной, гексагональной, овальной, круговой. Такие монолитные подложки могут содержать до приблизительно 700 или более проточных каналов ("ячеек") на квадратный дюйм поперечного сечения, хотя могут использоваться значительно меньшие количества. Например, подложка может содержать от приблизительно 60 до 600, более часто от приблизительно 200 до 400 ячеек на квадратный дюйм ("cpsi").
Известны различные типы материалов для получения сотовых носителей катализаторов. Сотовый носитель катализатора может быть приготовлен из различных материалов, включая металлические или керамические материалы. В некоторых вариантах осуществления изобретения монолитная подложка может быть изготовлена из керамического пористого материала, образованного одним или более оксидами металлов, например оксидом алюминия, оксидом алюминия-диоксидом кремния, оксидом алюминия-диоксидом кремния-диоксидом титана, муллитом, кордиеритом, диоксидом циркония, диоксидом циркония-диоксидом церия, диоксидом циркония-шпинелью, диоксидом циркония-муллитом, карборундом и т.п. Некоторые неопределенные образцы керамических монолитных подложек могут включать сделанные из: циркония, титаната бария, фарфора, оксида тория, оксида магния, стеатита, карбонатов бора или кремния, кордиерита-альфа оксида алюминия, нитрида кремния, сподумена, оксида алюминия-диоксида кремния-оксида магния, силиката циркония, силлиманита, силикатов магния, циркона, петалита, альфа оксида алюминия и алюмосиликатов. Одним из примеров коммерчески доступного материала для использования в качестве подложки в настоящем изобретении является кордиерит, который является оксидом алюминия-оксидом магния-диоксидом кремния.
Металлическая монолитная подложка может быть сотовым носителем катализатора, изготовленным из тугоплавкого металла, такого как нержавеющая сталь или другой коррозионно-устойчивый сплав на железной основе (например, железохромовый сплав). Металлическими монолитными подложками могут быть изготовленные, например, из сплавов хрома, алюминия и кобальта, такие как поставляемые под торговой маркой KANTHAL, или изготовленные из сплавов железа, хрома, алюминия и иттрия, поставляемые под торговой маркой FECRALLOY. Металл может также быть углеродистой сталью или простым чугуном. Монолитные подложки обычно изготавливают из таких материалов путем размещения плоского и гофрированного металлических листов один на другой и скручивания листов, уложенных в стопку, в цилиндрическую конструкцию параллельно оси конструкции, с образованием подложки, имеющей множество мелких параллельных отверстий для прохода газа, количество которых обычно может изменяться в пределах от приблизительно 200 до приблизительно 1,200 на квадратный дюйм фронтального сечения. Теплообменники, которые обычно формируются из металлических материалов, могут также использоваться как монолитные структуры.
Подложка может быть изготовлена из керамической или металлической пены. Подложки в форме пены хорошо известны в предыдущем уровне техники, например, см. U.S. Patent No.3,111,396, включенный здесь посредством ссылки.
Катализатор может быть в форме экструдатов. Обожженный измельченный в порошок катализатор, содержащий неорганическую оксидную подложку и платиновые и рениевые металлы, обычно смешивается со связующим веществом и экструдируется через головку требуемой формы, сушится и обжигается. С другой стороны, может быть экструдирована, высушена и обожжена неорганическая оксидная подложка. Обожженный экструдат может затем быть пропитан платиновыми и рениевыми металлами и другими дополнительными компонентами, рассмотренными выше. Обычно пригодные связующие вещества включают гидратированные формы оксида алюминия (например, псевдобемит), кремнеземистые связующие вещества, глинистые связующие вещества, циркониевые связующие вещества и т.п. Последующий обжиг приводит к желательным каталитически активным металлическим частицам на подложке.
Настоящее изобретение относится, в частности, к способам использования катализаторов в настоящем изобретении. В предпочтительном варианте воплощения изобретения катализаторы в настоящем изобретении могут быть использованы в способах получения водорода посредством реакции конверсии водяного газа при различных условиях в пределах определенных условий эксплуатации. Например, катализаторы конверсии водяного газа в настоящем изобретении могут быть включены в реактор, наполненный входящим газовым потоком, содержащим монооксид углерода и пар, с образованием водорода и диоксида углерода в качестве продуктов в выходящем газовом потоке.
Состав входящего газового потока для способа может изменяться в зависимости от источника реагирующего монооксида углерода. Способ в настоящем изобретении является особенно эффективным, когда концентрация монооксида углерода составляет вплоть до 20% по объему. Как правило, используются молярные избытки пара по отношению к количеству монооксида углерода, введенного во входящий газовый поток. В основном молярные соотношения H2O:СО между 1:1 (т.е. "1.0") и
20:1 (т.е. "20.0") являются предпочтительными во входящем газовом потоке, для значительной конверсии монооксида углерода особенно предпочтительны большие соотношения диапазона.
В локальных генераторах водорода и/или устройствах топливного элемента в способе в настоящем изобретении входящие газовые потоки обычно содержат по меньшей мере 10% по объему водорода в дополнение к монооксиду углерода и пару. Большее содержание водорода, например более чем 30-50% по объему, часто используются в устройствах топливного элемента. Входящий газовый поток обычно содержит 10-25% по объему диоксид углерода.
В дополнение к монооксиду углерода, диоксиду углерода, пару и водороду входящий газовый поток может содержать азот и незначительные количества олефинов, спиртов, альдегидов и/или других углеводородов. Предпочтительно входящий газовый поток содержит не более чем 4-5% по объему углеводородов.
Давление в реакционной зоне предпочтительно поддерживается ниже значения давления конденсации реакционной смеси. Следует осознавать, что могут быть использованы более низкие или более высокие значения давления в реакционной зоне, такие как от атмосферного вплоть до 500 фунтов на кв. дюйм.
Предпочтительно способ конверсии водяного газа осуществляется в непрерывном режиме с реагентами, передающимися по всей поверхности катализатора, содержащегося в одной или более реакционных зонах. В основном газовая почасовая объемная скорость VHSV (volume hourly space velocities) составляет от 500 до приблизительно 50000 ч-1, измеренная для монолитного катализатора на основании влажного газа при стандартных условиях является особенно подходящей для большинства режимов работы топливного элемента. Пригодная рабочая температура способа конверсии водяного газа составляет от 150 до 450°C. Предпочтительный рабочий диапазон составляет от 200 до 400°C.
Экстремальные интервалы температур для этих катализаторов делают их идеальными кандидатами для внедрения в топливно-процессорные реакторы, которые служат в качестве "высокотемпературного" компонента в реакторах конверсии водяного газа. Как будет показано ниже, рабочий интервал объемной скорости и температуры для Pt-Re катализаторов в настоящем изобретении выбраны в отношении концентрации подачи CO так, чтобы значительно уменьшить старение катализатора. Вне интервала рабочих параметров наблюдается старение катализатора. Напротив, интуитивно было найдено, в общем, что уменьшение объемных скоростей, уменьшение концентрации CO и увеличение температур приводят к значительному уменьшению старения Pt-Re катализаторов конверсии водяного газа.
Не будучи связанным, в соответствии с этой теорией, по нашему мнению экспериментальные результаты могут объяснить следующий механизм, как найдено в примерах ниже. Есть два конкурирующих способа, которые определяют устойчивость катализатора против спекания каталитически активных частичек Pt, сопровождающегося понижением каталитической активности. Один способ - формирование поверхностной разновидности частиц карбонила платины вследствие накопления CO, связанного с поверхностью Pt, что ослабляет взаимодействие Pt подложки и делает атомы Pt "подвижными" на поверхности и облегчает спекание частичек Pt. Другой способ - перемещение молекул CO, связанных с Pt. Этот последний способ, состоящий из каталитической конверсии CO, связанного на поверхности Pt, в CO2 и десорбции связанных молекул CO в газовую фазу. Этот способ обеспечивает "очистительный" механизм для поверхности Pt. Равновесие этих двух способов определяет, остается ли активность катализатора стабильной. Если скорость реакции очистки превышает скорость реакции дезактивации (накопления CO), то катализатор работает стабильно. Скорости этих двух реакций зависят от температуры, объемной скорости и концентрации CO (т.е. вытекания CO за единицу времени).
Чем больше расход CO (концентрация CO и объемная скорость) на единицу поверхности Pt, тем выше вероятность образования карбонилов Pt, а значит и спекания Pt. Чем выше температура, тем ниже вероятность, что CO свяжется с поверхностью Pt (т.е. уменьшится рабочая поверхность), а значит уменьшится и вероятность образования подвижных частиц карбонила Pt. Кроме того, при более высоких температурах очищающий механизм, т.е. превращение молекул CO в молекулы СО2 или десорбция CO более быстрые. Поэтому связанный CO преобразовывается или удаляется прежде, чем будет достигнута критическая поверхностная концентрация, необходимая для образования неустойчивых частиц карбонила.
Если образование поверхностного неустойчивого карбонила происходит быстрее, чем конкурентная реакция конверсии водяного газа, то катализатор спекается. Если преобладает каталитическая реакция пара и CO с образованием CO2 и Н2, то катализатор остается стабильным. Данные, приведенные в таблице 2 ниже, показывают, что регулирование условий протекания реакции может изменять относительные скорости реакции и, следовательно, стабильность катализатора, эксплуатируемого в этих условиях. Например, если проводить способ при объемной скорости 15000 ч-1 и 15% концентрации CO при 360°C, то катализатор работает стабильно (ΔТ(50)=-0.6). Однако при увеличении объемной скорости в 3 раза (45000 ч-1) при той же температуре и концентрации CO катализатор стареет со скоростью ΔТ(50)=10°C за 20 часов. Следовательно, старение не является линейным относительно потока CO над катализатором (т.е. в 3 раза выше при 3-кратном повышении объемной скорости).
Точнее, при анализе экспериментальных результатов при помощи пакета программ "Design Expert" (Stat-ease Inc.) было найдено, что согласно следующему уравнению может осуществляться понижение активности катализатора.
ΔТ(50)20 ч=(5,51+4,40×10-5×VHSV-0,015×T+0,049×%CO)2-1,65
где:
Т означает температуру в градусах C.
(% CO) означает содержание CO в сухом способе (без пара) в объемных процентах.
VHSV означает ежечасную объемную скорость газа для катализатора, содержащего 7.4 г Pt на литр. Этот член заменяется на [VHSV×(Pt(г/л)/7,4)] для катализаторов с другим содержанием Pt.
ΔТ(50)20 ч означает разницу температур при 50% конверсии CO, т.е. Т(50)изношенного 20 ч - T(50)свежего.
В настоящем изобретении значение ΔТ(50)20 ч менее чем 3 показывает стабильность использования катализатора. Значения ΔТ(50)20 ч ≤2 являются особенно пригодными для значительного уменьшения старения. Среднее отклонение между экспериментальными данными и предсказанными (вычисленными) на основе уравнения значениями дельта-Т(50) составляет 3.5. Следовательно, вычислено, что значения менее чем 7.0 и ≤5.0 в уравнении могут все еще уменьшаться в желаемом диапазоне Т(50)20 ч<3 способа и поэтому находятся в пределах границ настоящего изобретения. См. таблицу 2 ниже.
Кроме того, было найдено, что старение Pt-Re катализатора конверсии водяного газа уменьшается при рассмотренных ранее нагрузках катализатора и при следующих условиях: CO (от 5 до 15 об.%); VHSV (<20000 ч-1×Pt(г/л)/7,4) и Т (>330°C). Также служащими примером являются следующие параметры: CO (от 5 до 15 об.%), VHSV (8000-15000 ч-1×Pt(г/л)/7,4) и Т (360°C). Помимо непосредственно выраженного "высоко" температурного режима было найдено, что "низко" и "умеренно" температурные режимы значительно понижают старение катализатора. Например, могут использоваться следующие условия эксплуатации:
Средний: Т=280-320°C, CO=10-20%, VHSV×Pt(г/л)/7.4<15000 ч-1
Низкий: Т=200-250°C, CO=2-6%, VHSV×Pt(г/л)/7,4<2500 ч-1
Хотя катализаторы конверсии водяного газа и способы в настоящем изобретении могут быть использованы в любом применении, где необходимо образование водорода, особенно пригодным применением являются аппараты, такие как топливные процессоры, которые снабжают водородом топливные элементы. Как рассмотрено выше, эти системы обычно включают ряд реакторов, которые преобразуют углеводородное топливо (например, природный газ, бензин, дизельное топливо, сжиженный нефтяной газ и т.п.) в водородное топливо. Преобразования, которые имеют место в реакторах, включают реакции риформинга и реакции конверсии водяного газа с образованием водорода. Другие реакторы и улавливающие устройства могут также быть включены в аппараты, которые уменьшают содержание нежелательных компонентов в водородном сырьевом потоке (например, монооксида углерода и серосодержащих компонентов), которыми в конечном итоге снабжается топливный элемент.
ПРИМЕР 1
Катализатор конверсии водяного газа, как описано ниже, использовался для проверки на старение.
Приготовление порошка 2%Re/4%Pt/2%La2(MoO4)3ZrO2:La2O3:Gd2O3
Был приготовлен раствор 1.023 мл раствора La(NO3)3 (d=1.74 г/мл; 27 мас.% La2O3) в 600 мл деионизированной воды. К раствору добавили 50 г порошка ZrO2:La2O3:Gd2O3 и перемешивали 15 мин. Затем к суспензии добавили в течение 30 мин раствор 0.79 г (NH4)2MoO4 и перемешивали дополнительно 30 мин. Затем добавили 1 М раствор NH4OH до достижения рН 9. Осадок отфильтровывали и промывали дважды при помощи 200 мл разбавленного NH4OH. Промытый осадок сушили 8 ч при 120°C и обжигали 4 ч при 500°C.
50 г полученного выше порошка суспендировали в 500 мл деионизированной воды при перемешивании. Прикапывали раствор аминосодержащей Pt соли, содержащий 2.08 г Pt, и перемешивали в течение 30 мин. Добавляли уксусную кислоту до достижения рН 6. Суспензию фильтровали, сушили и обжигали, как описано выше.
10 г полученного порошка пропитывали раствором 0.3 г NH4ReO4 в воде до образования кашицы. Порошок сушили и обжигали, как описано выше.
Приготовление монолитов:
Для приготовления монолитов катализатора порошок катализатора 6%Pt/2%La2(MoO4)3/ZrO2:La2O3:Gd2O3 смешивали с глиноземистым связующим веществом и получали суспензию. Монолитная подложка погружалась в суспензию до тех пор, пока не была достигнута ее желаемая масса. Катализатор затем сушили и обжигали 2 ч при 200°C и 2 ч при 500°C.
Монолит был пропитан Re посредством погружения в раствор NH4ReO4 до отложения 3% Re в перерасчете на мас.% наносного покрывающего слоя. Катализатор затем сушили и обжигали, как описано выше.
В таблице 1 приведены некоторые из условий испытаний, которые приводят к открытию настоящего изобретения. CO в сырьевом газе меняется между 5, 10 и 15 об.%, объемная скорость сырьевого газа (VHSV) меняется между 5000, 15000, 25000 и 45000 ч-1 (на монолитной подложке), и температуры изменяются между 240, 300 и 360°C. Все эксперименты были выполнены с содержанием катализаторов 7,4 г/л. Эксперименты проанализированы при помощи пакета программ "Design Expert" (Stat-ease Inc.), чтобы согласовать экспериментальные результаты с полиноминальным уравнением. Контурное изображение на Фиг.1-4 показывает равновесные значения дельта Т(50). Например, все значения на