Sparc-производные антигенные пептиды отторжения опухоли и лекарственные средства, содержащие их
Иллюстрации
Показать всеИзобретение относится к биотехнологии. Описан пептид, который обладает способностью индуцировать цитотоксические (киллерные) Т-клетки. Представлены средства, содержащие описанный пептид, для индукции иммунитета, направленного против злокачественных опухолей, для лечения и/или профилактики опухолей, индукции антиген-презентирующих клеток, обладающих высокой способностью индуцировать Т-клетки, реакционноспособные в отношении опухоли, для индукции Т-клеток, реакционноспособных в отношении опухолей. Представлено антитело, которое специфически связывается с описанным пептидом. Описаны выделенные Т-клетка киллер, реакционноспособная в отношении опухолей, которая индуцируется in vitro стимуляцией описанным пептидом, хелперная Т-клетка, реакцонноспособная в отношении опухолей, которая индуцируется in vitro стимуляцией описанным пептидом, антиген-презентирующая клетка, которая представляет комплекс молекулы HLA и описанного пептида. Изобретение позволяет усилить иммунитет пациента, страдающего метастазирующим раком или резистентным раком, у которого хирургическое лечение, химеотерапия и лучевая терапия практически не применимы. 10 н.п. ф-лы, 4 ил., 1 табл., 3 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к новым пептидам, которые являются эффективными в качестве вакцины для злокачественных новообразований, высоко экспрессирующих SPARC, таких как рак желудка, рак поджелудочной железы или злокачественная меланома (меланома), и к лекарственным средствам, содержащим вышеуказанные пептиды, используемым для лечения и/или профилактики опухолей.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
По сравнению с западными странами заболеваемость раком желудка выше в азиатских странах, таких как Япония и Китай. В результате распространения медицинских осмотров, широкого применения эндоскопов для исследования пищеварительного тракта и разработки методик проверки, стало возможным выявлять рак желудка на ранней стадии, и, таким образом, число пациентов, страдающих от этого вида рака, снизилось. Тем не менее, рак желудка остается второй причиной смерти в результате злокачественных новообразований в Японии. Таким образом, рак желудка остается основной причиной смертности. Среди нескольких типов рака желудка, диффузный (скиррозный) рак желудка чаще встречается у молодых людей по сравнению с другим типом рака желудка (аденокарциномой). Такой диффузный (скиррозный) рак желудка имеет тенденцию к быстрому прогрессированию, и часто возникают отдаленные метастазы или перитонеальные метастазы, что дает плохой прогноз. Во многих случаях скиррозного рака желудка уже стало невозможным проводить хирургическое удаление опухоли на момент постановки диагноза. Даже если сохраняется возможность удалить опухоль, то после лечения рак зачастую рецидивирует. В связи этим крайне необходимо создать новый способ лечения.
Количество смертей от рака поджелудочной железы в Японии имеет тенденцию к увеличению. В 2003 году из-за рака поджелудочной железы умерло 21148 человек. В настоящее время рак поджелудочной железы составляет 6,8% злокачественных опухолей, которые являются причиной смерти в Японии. То есть, рак поджелудочной железы занимает пятое место среди причин смерти после рака легких, рака желудка, рака толстой кишки и рака печени. Были проанализированы демографические данные по всему миру, и был подсчитан возрастной уровень смертности, используемый для сравнения уровней смертности в разнородных возрастных популяциях. В результате, в 2000 году на 100000 мужчин, 8,6 человек умерло из-за рака поджелудочной железы в Японии, тогда как 7,3 человека умерло в Соединенных Штатах и 6,3-7,0 человек умерло в Соединенном Королевстве из-за рака того же типа. На 100000 женщин 4,9 человека умерло из-за рака поджелудочной железы в Японии, тогда как 5,3 человека умерло в Соединенных Штатах и 4,8-5,1 человек умерло в Соединенном Королевстве из-за рака того же типа. Таким образом, уровень смертности из-за рака поджелудочной железы в Японии стал таким же, как и уровень в западных странах.
С учетом возрастного показателя в 2000 (100000 человек мировой популяции), в отношении мужчин, 8,6 человек умерло из-за рака поджелудочной железы в Японии, тогда как 7,3 человека умерло в Соединенных Штатах и 6,3-7,0 человек умерло в Соединенном Королевстве из-за рака того же типа. Кроме того, в отношении женщин, 4,9 человек умерло из-за рака поджелудочной железы в Японии, тогда как 5,3 человека умерло в Соединенных Штатах и 4,8-5,1 человек умерло в Соединенном Королевстве из-за рака того же типа. Таким образом, уровень смертности из-за рака поджелудочной железы в Японии стал таким же, что и уровень в западных странах. Несмотря на развитие диагностической визуализации, в настоящее время, приблизительно 40% всех японцев, больных раком поджелудочной железы, страдает от прогрессирующего рака поджелудочной железы, приводящего к отдаленным метастазам, и, в дальнейшем, имеется много случаев, при которых рак обнаруживается после достижения местно распространенной стадии рака, при которой опухоль не может быть удалена. Относительная 5-летняя выживаемость всех пациентов с раком поджелудочной железы составляет 43% в диагностированных случаях в 1996 году. Хотя этот уровень обычно бывает выше, чем обычный уровень выживаемости (2-3%), он все еще остается низким. В отношении факторов развития рака поджелудочной железы было высказано предположение, что различные факторы, в том числе образ жизни, например, курение, ожирение, питание, алкогольные напитки и кофе, а также хронический панкреатит, диабет, генетический фактор и т.д. приводят к возникновению рака поджелудочной железы.
Рак поджелудочной железы не имеет особых симптомов, и, следовательно, во многих случаях, когда появляются определенные симптомы, рак уже прогрессировал. В результате, 5-летняя выживаемость всех пациентов составляет 5% или менее, и прогноз после постановки диагноза является крайне негативным. Из-за трудности диагностики рака поджелудочной железы, процент этого типа рака как причины смерти от рака постепенно увеличивается в развитых странах. В настоящее время проводится многопрофильное лечение, в том числе хирургическое удаление, в качестве основного лечения, лучевая терапия и химиотерапия. Однако, не было получено существенного улучшения терапевтических эффектов, и, следовательно, крайне необходимо разработать новую терапевтическую стратегию.
Меланома представляет собой тип рака кожи, который зачастую называют злокачественной меланомой. Среди нескольких типов рака кожи, у меланомы высока вероятность инфильтрации и метастазирования и у нее наиболее высокая степень злокачественности, и, следовательно, меланома вызывает серьезные опасения. Среди клеток, которые составляют кожу, некоторые клетки продуцируют пигмент меланин. Такие клетки называются меланоцитами. Когда такие меланоциты становятся злокачественными, возникает меланома. Кроме того, частота встречаемости меланомы увеличилась, в частности среди лиц белой расы, как результат увеличения воздействия ультрафиолетовых лучей вследствие уменьшения озонового слоя в атмосфере, вызванного резким ухудшением состояния окружающей среды.
В Японии, случаи меланомы варьируют от 1,5 до 2 человек на 100000 в общей популяции. Следовательно, по оценкам, приблизительно у 1500-2000 человек в год развивается меланома. С другой стороны, в западных странах, более чем у двенадцати человек развивается меланома на 100000 в общей популяции. В частности, в Австралии, у двадцати или более человек развивается такая меланома на 100000 в общей популяции, и, следовательно, известно, что заболеваемость меланомой в Австралии наиболее высокая в мире. В этих условиях, люди, проживающие в Европе, Соединенных Штатах и в Австралии обращают особое внимание на симптомы меланомы. Более того, неожиданно было отмечено что, возникновение меланомы имеет тенденцию к увеличению год от года в Японии, также как и в зарубежных странах. В соответствии с данными последних исследований, ежегодное число смертельных исходов от меланомы приблизительно составляет 450 в Японии. Меланома развивается независимо от возраста. Однако частота случаев этого заболевания увеличивается у людей старше 40, и является наиболее высокой у людей 60 и 70 лет. Появление этого заболевания в детстве является чрезвычайно редким, но это не означает, что это заболевание никогда не развивается в детстве. В последнее время, возникновение меланомы имеет тенденцию к увеличению у молодых пациентов в возрасте 20 и 30 лет. Меланома развивается независимо от пола, и этим заболеванием страдают как мужчины, так и женщины. В случае пациентов-японцев местом, в котором наиболее вероятно развивается меланома, является подошва ступни, и насчитывает 30% всех случаев меланомы. Как характеристика пациентов-японцев, меланома также развивается на ступне и ногтевых фалангах пальцев. Кроме того, в случае пациентов западных стран, меланома развивается в любых участках кожи, таких как туловище, рука, ступня, лицо и голова.
В настоящее время, способы, которые могут использоваться для лечения меланомы, включают хирургическое лечение, химиотерапию и лучевую терапию. Однако в качестве терапии для облегчения симптомов метастазирующего рака или резистентного рака, при котором вышеупомянутые способы лечения применяться не могут, центром внимания стала иммунотерапия для повышения иммунитета пациентов, страдающих раком, к злокачественной опухоли, с тем, чтобы подавить рост злокачественной опухоли. Такая иммунотерапия является фактически эффективной для некоторых пациентов.
С другой стороны, с развитием молекулярной биологии и иммунологии опухолей в последние годы, было показано, что цитотоксические (киллерные) Т-клетки и хелперные Т-клетки распознают пептиды, образованные при разрушении белков, высоко и специфически экспрессируемых на злокачественных клетках, которые представлены на поверхностях злокачественных клеток или антиген-презентирующих клеток через молекулы HLA, и что они проявляют иммунологическую реактивность для разрушения таких злокачественных клеток. Более того, было идентифицировано огромное количество опухолевых антигенных белков и пептидов, происходящих от них, которые стимулируют иммунную реакцию для разрушения злокачественных опухолей, и было предложено клиническое применение антиген-специфичной иммунотерапии опухолей.
Молекулы HLA I класса экспрессируются на поверхностях всех ядросодержащих клеток организма. Белки, образованные в цитоплазме и ядре, предоставляют пептиды, образованные в результате разрушения в клетках, и они экспрессируются на поверхностях таких клеток. На поверхностях здоровых клеток пептиды, происходящие от нормальных аутологичных белков, связываются с молекулами HLA I класса, а Т-клетки иммунной системы не распознают и не разрушают такие пептиды, связанные с молекулами HLA I класса. С другой стороны, в процессе, при котором злокачественные клетки превращаются в злокачественную опухоль, такие злокачественные клетки могут экспрессировать огромное количество белков, которые практически не экспрессируются или экспрессируются только в небольших количествах на здоровых клетках. Если пептид, образованный при разрушении в цитоплазме такого белка, который высоко специфически экспрессируется в злокачественной клетке, связывается с молекулой HLA I класса и экспрессируется на поверхности такой злокачественной клетки, Т-клетка киллер распознает этот пептид и разрушает только злокачественную клетку. Кроме того, путем иммунизации организма пациента таким антигеном, специфичным для злокачественной опухоли, или пептидом можно разрушить злокачественные клетки и подавить рост злокачественной опухоли без причинения вреда здоровым клеткам. Это называется иммунотерапией злокачественных опухолей с использованием антигена, специфичного для злокачественной опухоли. Более того, молекулы HLA II класса преимущественно экспрессируются на поверхности антиген-презентирующих клеток. Такие молекулы HLA II класса связываются с пептидами, происходящими из антигена, специфичного для злокачественной опухоли, образованными включением антигена, специфичного к злокачественной опухоли, с наружной стороны клетки и разрушения его в клетке, и он экспрессируется на поверхности клетки. Т-клетка хелпер, которая распознала пептиды, связанные с молекулой HLA II класса, активируется для продукции различных цитокинов, которые активируют другие иммунокомпетентные клетки, с тем, чтобы индуцировать или усилить иммунную реакцию против опухоли.
Таким образом, если может быть разработана иммунотерапия, направленная на антиген, специфически экспрессирующийся на высоком уровне в такой злокачественной опухоли, она может обеспечить терапевтический способ эффективного устранения только злокачественной опухоли, не нанося вреда здоровым аутологичным органам. Более того, ожидается, что такая иммунотерапия может обеспечить терапевтический способ, который может использоваться у пациентов, страдающих терминальной стадией рака, у которых другие способы лечения проводиться не могут. Кроме того, если антиген, специфичный для злокачественной опухоли, и пептид вводить в форме вакцины людям с высоким риском развития такого типа рака, то будет получена возможность предотвращения возникновения злокачественной опухоли.
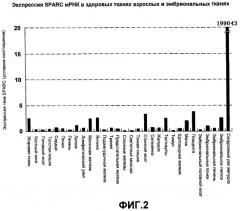
Сначала авторы настоящего изобретения провели анализ экспрессии генов всего генома. Авторы изобретения проанализировали 23040 типов генов в тканях рака желудка и здоровых тканях, используя микроматрицу кДНК. В результате в 11 из 20 случаев у пациентов с диффузным инфильтрирующим раком желудка авторы изобретения идентифицировали секретируемый кислый и богатый цистеином белок (SPARC), который представляет собой продукт гена, высокоэкспрессирующегося в тканях рака желудка, и уровень экспрессии которого в 5 или более раз выше уровня экспрессии в здоровых тканях (в среднем в 130000 раз выше в среднем) (Фигура 1). Ген SPARC экспрессируется на низких уровнях в нормальных жировых тканях, молочной железе, яичниках, спинном мозге, тестикулах, матке, плаценте и т.д. Однако уровень экспрессии гена SPARC в любом из вышеупомянутых органов ниже уровня экспрессии в здоровой слизистой оболочке желудка в 5 раз или менее (Фигура 2).
Другие исследователи сообщили, что SPARC не только экспрессируется при диффузном инфильтрирующем раке желудка, но также экспрессируется при раке поджелудочной железы и при меланоме. Более того, авторы настоящего изобретения обнаружили, что SPARC секретируется в сыворотке пациентов, страдающих меланомой, и что SPARC может быть подходящим опухолевым маркером, особенно для раннего обнаружения меланомы (японская патентная заявка № 2004-303688; и Clinical Cancer Research 11: 8079-8088, 2005).
SPARC представляет собой кислый секреторный белок размером 43-кДа, состоящий из 286 аминокислот. Этот белок богат цистеином и двигается к ядру во время фазы деления клетки. Кроме того, SPARC контролирует взаимодействие между белками внеклеточного матрикса и клеткой, поэтому он также может быть связан с контролем за клеточным ростом. Поскольку SPARC экспрессируется в остеобластах, тромбоцитах и раневых областях, считается, что этот белок связан с репарацией и восстановлением тканей. Более того, также сообщалось, что SPARC высоко экспрессируется в злокачественных опухолях, таких как меланома или остеосаркома, и в интерситциальных клетках опухолей, и что экспрессия SPARC коррелирует с прогнозом, инфильтрацией или метастазированием опухолей.
[Непатентный документ 1] Icuta Y et al, Clinical Cancer Research 11: 8079-8088, 2005.
[Патентный документ 1] японская патентная заявка № 2004-303688
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Проблемы, решаемые настоящим изобретением
Целью настоящего изобретения является разработка способа усиления иммунитета пациента, страдающего метастазирующим раком или резистентным раком, у которого хирургическое лечение, химиотерапия и лучевая терапия, используемые в качестве способа лечения опухолей, высокоэкспрессирующих SPARC, таких как диффузный инфильтрирующий рак желудка, рак поджелудочной железы или меланома, практически не применимы, для облегчения симптомов таких злокачественных опухолей и для проведения иммунотерапии, подавляющей рост таких злокачественных опухолей. Другими словами, целью настоящего изобретения является идентификация пептида, происходящего из белка SPARC, гиперэкспрессирующая в злокачественной ткани, который способен индуцировать сильный иммунный ответ на вышеупомянутые злокачественные опухоли, не вызывая вредных эффектов у больных злокачественным заболеванием, и применение идентифицированного пептида для иммунотерапии опухолей. То есть, целью настоящего изобретения является идентификация пептида, производного белка SPARC, способного индуцировать Т-клетки киллеры и Т-клетки хелперы человека, реакционноспособные в отношении опухолей, и получение средства для проведения иммунотерапии опухолей у пациентов с различными типами рака, выскоэкспрессирующими SPARC.
Способы решения этих задач
Авторы настоящего изобретения идентифицировали ген, SPARC, который высоко экспрессируется при диффузном инфильтрирующем раке желудка, путем проведения анализа с использованием кДНК микроматрицы с указанным выше раком желудка и различными здоровыми тканями. Экспрессия SPARC также наблюдается в некоторых типах здоровых тканей. Однако уровень экспрессии SPARC в нормальных тканях существенно ниже уровня экспрессии в злокачественных тканях. Для того, чтобы проверить наличие или отсутствие индукции противоопухолевого иммунитета SPARC- специфичными Т-клетками киллерами, были использованы мыши BALB/c, которые экспрессируют мышиные молекулы Kd, характеристики аминокислотной последовательности связанного пептида которых идентичны таковым HLA-A24, который является наиболее частым аллелем HLA I класса у населения Японии. Гомология аминокислотной последовательности SPARC человека и мыши составляет 95%. Таким образом, были синтезированы пептиды, состоящие из аминокислотных последовательностей, общих для людей и мышей, имеющие связывающий мотив, общий для HLA-A24 человека и Kd мыши. После чего, мышей BALB/c (Kd-экспрессирующих) иммунизировали дендритными клетками, полученными из костного мозга, на которые была нагружена эта смесь пептидов, и авторы изобретения исследовали, индуцируются ли или нет Т-клетки киллеры, реакционноспособные в отношении злокачественных клеток, экспрессирующих SPARC. Более того, в отношении мышей, которых предварительно подвергали тому же способу иммунизации, как описано выше, авторы настоящего изобретения исследовали, подавляется ли рост трансплантированных злокачественных клеток, экспрессирующих мышиный SPARC, и удлиняется или нет время выживания мышей. Кроме того, также проверили, появляются ли или нет негативные эффекты вместе с возникновением аутоиммунного феномена у мышей, иммунизированных пептидом. В результате было обнаружено, что пептид с любой аминокислотной последовательностью SEQ ID NO: 1-3 способен индуцировать Т-клетки киллеры, которые разрушают злокачественные клетки, экспрессирующие SPARC. Более того, рост трансплантированных мышиных злокачественных клеток, экспрессирующих SPARC, подавляется у мышей, иммунизированных вышеупомянутым пептидом, и, следовательно, время выживания мышей удлиняется. Настоящее изобретение было выполнено на основании полученных результатов.
Настоящее изобретение относится к следующему:
(1) Пептиду, выбранному из:
(А) пептида, который состоит из любой аминокислотной последовательности SEQ ID NO: 1-3; или
(В) пептида, который состоит из аминокислотной последовательности, содержащей замену или добавление одной или нескольких аминокислот в отношении пептида, состоящего из любой аминокислотной последовательности SEQ ID NO: 1-3, и который обладает способностью индуцировать цитотоксические (киллерные) Т-клетки.
(2) Средству, индуцирующему иммунитет в отношении злокачественных опухолей, который содержит по меньшей мере один тип пептида по пункту (1).
(3) Лекарственному средству для лечения и/или профилактики опухолей, которое содержит по меньшей мере один тип пептида по пункту (1).
(4) Средству для индукции антиген-презентирующих клеток, обладающих высокой способностью индуцировать Т-клетки, реакционноспособные в отношении опухоли, которое содержит по меньшей мере один тип пептида по пункту (1).
(5) Средству для индукции Т-клеток, реакционноспособных в отношении опухолей, которое содержит по меньшей мере один тип пептида по пункту (1).
(6) Средству для индукции антиген-презентирующих клеток, обладающему высокой способностью индуцировать Т-клетки, реакционноспособные в отношении опухоли, которое содержит ген, кодирующий пептид, выбранный из:
(А) пептида, состоящего из любой аминокислотной последовательности SEQ ID NO: 1-3; или
(В) пептида, состоящего из аминокислотной последовательности, содержащей замену или добавление одной или нескольких аминокислот в отношении пептида, состоящего из любой аминокислотной последовательности SEQ ID NO: 1-3, и который обладает способностью индуцировать Т-клетки киллеры.
(7) Антителу против пептида по пункту (1).
(8) Т-клетке киллеру, хелперной Т-клетке, или популяции иммуноцитов, содержащих такие клетки, которые индуцируется пептидом по пункту (1).
(9) Антиген-презентирующей клетке, которая представляет комплекс молекулы HLA и пептида по пункту (1).
(10) Антиген-презентирующей клетке по пункту (9), которая индуцируется средством по пункту (4) или (6).
НАИЛУЧШИЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
(1) Пептид по настоящему изобретению и содержащее его средство, индуцирующее противоопухолевый иммунитет
Пептид по настоящему изобретению описывается следующим:
(А) пептид, который состоит из любой аминокислотной последовательности SEQ ID NO: 1-3; или
(В) пептид, который состоит из аминокислотной последовательности, содержащей замену или добавление одной или нескольких аминокислот в отношении пептида, состоящего из любой аминокислотной последовательности SEQ ID NO: 1-3, и который обладает способностью индуцировать Т-клетки киллеры.
Термин «пептид, обладающий способностью индуцировать цитотоксические Т-клетки» используется в настоящем описании для обозначения пептида, обладающего активностью стимулировать Т-клетки киллеры, реакционноспособные в отношении опухолей.
Способ получения/продукции пептида по настоящему изобретению не ограничен особым образом. Может быть использован либо химически синтезированный пептид, либо рекомбинантный пептид, полученный с помощью генной рекомбинации.
При получении химически синтезированного пептида пептид по настоящему изобретению может быть синтезирован способом химического синтеза, таким как метод Fmoc (фторэнилметилоксикарбонильный метод) или метод tBoc (t-бутилоксикарбонильный метод), например.
Кроме того, пептид по настоящему изобретению также может быть синтезирован различными видами коммерчески доступных пептидных синтезаторов.
В тех случаях, когда пептид по настоящему изобретению продуцируется в форме рекомбинантного белка, получают ДНК, имеющую нуклеотидную последовательность, кодирующую упомянутый выше белок, ее мутированную форму или ее гомолог, а затем ее вводят в предпочтительную систему экспрессии, для получения пептида по настоящему изобретению.
В качестве вектора экспрессии, предпочтительно, может быть использован вектор, способный к автономной репликации в клетке-хозяине, или способный встраиваться в хромосому клетки-хозяина. Используют вектор экспрессии, содержащий промотор в положении, способном экспрессировать ген, кодирующий пептид. Кроме того, трансформант, имеющий ген, кодирующий пептид по настоящему изобретению, может быть получен путем встраивания вышеупомянутого экспрессионного вектора в хозяина. В качестве хозяина может быть использована любая из бактериальных, дрожжевых клеток, клеток животного и насекомого. Вектор экспрессии может быть введен в хозяина в соответствии с известным способом, в зависимости от типа такого хозяина.
В настоящем изобретении, трансформант, полученный выше, культивируют, а пептид по настоящему изобретению затем продуцируется и накапливается в культуре. После этого, пептид по настоящему изобретению собирают из культуры для выделения рекомбинантного пептида.
В тех случаях, когда такой трансформант является прокариотической клеткой, таким как Escherichia coli, или эукариотом, таким как дрожжи, средой, используемой для культивирования таких микроорганизмов может быть любая природная или синтетическая среда, при условии, что она содержит источник углерода, источник азота, неорганические соли и подобное, что может ассимилироваться вышеупомянутыми микроорганизмами, способная эффективно осуществлять культивирование трансформанта. Более того, такое культивирование можно проводить в условиях, которые обычно применяются для культивирования вышеупомянутых микроорганизмов. После завершения культивирования, пептид по настоящему изобретению может быть выделен и очищен из культуры трансформанта в соответствии с общепринятым способом выделения и очистки пептидов.
Термин «одна или несколько аминокислот», используется в настоящем описании для обозначения в основном от 1 до 10 аминокислот, предпочтительно от 1 до 8 аминокислот, более предпочтительно от 1 до 5 аминокислот, и особенно предпочтительно от 1 до 3 аминокислот (например, 1, 2, или 3 аминокислот).
Пептид, состоящий из аминокислотной последовательности, содержащей замену или добавление одной или нескольких аминокислот в отношении пептида, состоящего из любой аминокислотной последовательности SEQ ID NO: 1-3, может быть соответствующим образом получен или приобретен специалистами в данной области на основании информации, касающейся любой аминокислотной последовательности SEQ ID NO: 1-3. Другими словами, пептид, который состоит из аминокислотной последовательности, содержащей замену или добавление одной или нескольких аминокислот в отношении любой аминокислотной последовательности SEQ ID NO: 1-3, и который обладает способностью индуцировать цитотоксические Т-клетки, может быть получен любым заданным способом, известным специалистам в данной области, например, упомянутым выше химическим синтезом, способами генной инженерии или мутагенезом. Например, подходит сайт-направленный мутагенез, который представляет собой генно-инженерный способ, поскольку представляет собой способ введения специфической мутации в конкретное положение. Такой сайт-направленный мутагенез можно выполнить с помощью способа, описанного в Molecular Cloning: A laboratory Manual, 2nd Ed, Cold Spring Harbor Laboratory, Cold Spring Harbor, NY, 1989 (здесь и далее сокращенно Molecular Cloning 2nd Ed), Current Protocols in Molecular Biology, Supplement 1-38, John Wiley & Sons (1987-1997) (здесь и далее сокращенно Current Protocols in Molecular Biology), и т.д.
Как описано далее в примерах, упомянутый выше пептид по настоящему изобретению способен индуцировать иммунный ответ против злокачественных опухолей. Таким образом, настоящее изобретение относится к средству, индуцирующему иммунный ответ против злокачественных опухолей, которое содержит пептид по настоящему изобретению.
Средство, индуцирующее иммунный ответ по настоящему изобретению, используемое против злокачественных опухолей, применяется in vitro, ex vivo или in vivo, и, предпочтительно, ex vivo, так, чтобы оно могло индуцировать Т-клетки киллеры, хелперные Т-клетки или популяцию иммуноцитов, содержащую такие клетки, тем самым обеспечивая противоопухолевый иммунитет.
(2) Антитело по настоящему изобретению
Настоящее изобретение также относится к антителу, которое распознает часть упомянутого выше пептида по настоящему изобретению, или пептид целиком как эпитоп (антиген), и Т-клеткам киллерам, индуцированным посредством ex vivo или in vitro стимуляции с использованием упомянутого выше пептида. В основном, известно, что такие Т-клетки киллеры проявляют противоопухолевую активность, которая сильнее активности антитела.
Антитело по настоящему изобретению может быть либо поликлональным антителом, либо моноклональным антителом. Такое антитело может быть получено общепринятым способом.
Например, поликлональное антитело может быть получено путем иммунизации млекопитающего или птиц пептидом по настоящему изобретению, используемому в качестве антигена, затем получения крови этого млекопитающего или птицы, а затем отделением и очисткой антитела из полученной крови. Например, могут быть иммунизированы млекопитающие или птицы, например, мыши, хомяки, морские свинки, цыплята, крысы, кролики, псовые, козы, овцы, были или лошади. Такой способ иммунизации известен специалистам в данной области. Например, антиген можно вводить 2 или 3 раза с интервалами от 7 до 30 дней. В дозе приблизительно от 0,05 до 2 мг антигена, например, можно вводить однократно. Путь введения особым образом не ограничен и в зависимости от ситуации может быть выбрано подкожное введение, внутрикожное введение, внутрибрюшинное введение, внутривенное введение, внутримышечное введение и т.д. Кроме того, антиген можно растворить в подходящем буфере, содержащем адъювант, например, в подходящем буфере, содержащем обычно используемый адъювант, такой как полный адъювант Фрейнда или гидроксид алюминия, и может быть использован такой антиген.
Иммунизированных таким образом млекопитающих или птиц выращивают в течение определенного периода времени. После этого, если титр антител повышается, можно провести повторную иммунизацию с использованием от 100 до 1000 мкг антигена, например. Через один или два месяца после последней иммунизации у иммунизированного млекопитающего или птицы берут кровь. Полученную таким образом кровь (поликлональную антисыворотку) затем отделяют и очищают обычным способом, включающим в себя центрифугирование, преципитацию с использованием сульфата аммония или полиэтиленгликоля, хроматографию, такую как гель-фильтрационная хроматография, ионообменная хроматография или аффинная хроматография и т.д., для получения поликлонального антитела, которое распознает пептид по настоящему изобретению.
С другой стороны, моноклональное антитело может быть получено с помощью гибридомы. Например, такая гибридома может быть получена путем клеточного слияния клетки, продуцирующей антитела, и миеломной клетки. Гибридома, которая генерирует моноклональное антитело по настоящему изобретению, может быть получена следующим способом слияния клеток.
В качестве антителопродуцирующей клетки использую Т-клетку селезенки, клетку лимфатического узла, В лимфоцит или подобные, полученные от иммунизированного животного. В качестве антигена, используют пептид по настоящему изобретению. В качестве иммунизированного животного можно использовать мышь, крысу или подобное. Антиген вводят этому животному в соответствии с обычным способом. Например, суспензию или эмульгированную жидкость, содержащую адъювант, такой как полный адъювант Фрейнда или неполный адъювант Фрейнда, и пептид по настоящему изобретению, используемый в качестве антигена, вводят животному посредством внутривенного введения, подкожного введения, внутрикожного введения, внутрибрюшинного введения и т.д., несколько раз для иммунизации животного. После этого антителопродуцирующую клетку, такую как клетка селезенки, получают от иммунизированного животного, и полученную таким образом клетку селезенки затем сливают с миеломной клеткой в соответствии с известным способом (G Kohler et al., Nature, 256 495 (1975)), получая, таким образом, гибридому.
Примеры штаммов миеломных клеток, используемых в слиянии клеток, включают штамм P3X63Ag8, штамм P3U1 и штамм Sp2/0, в случае мышей. При проведении такого слияния клеток, используют активатор слияния, такой как полиэтиленгликоль или вирус Сендай. Для селекции гибридомы после завершения клеточного слияния, используют среду с гипоксантин-аминоптерин-тимидином (HAT) в соответствии с обычным способом. Гибридому, полученную как результат слияния клеток, клонируют с помощью метода предельных разведений. Далее, при необходимости, проводят скрининг иммуноферментным анализом с использованием пептида по настоящему изобретению, с получением штамма клеток, продуцирующих моноклональное антитело, специфически распознающего пептид по настоящему изобретению.
Для получения моноклонального антитела, представляющего интерес, из полученной таким образом гибридомы, эту гибридому можно культивировать, обычным способом культивирования клеток или способом получения асцитической жидкости, и моноклональное антитело, представляющее интерес, может быть очищено из культурального супернатанта или асцитической жидкости в соответствии с обычным способом. Например, фракционирование с использованием сульфата аммония, гель-фильтрация, ионообменная хроматография, аффинная хроматография и другие способы могут быть объединены, в зависимости от ситуации, и использованы.
Более того, фрагменты вышеупомянутого антитела также включены в объем настоящего изобретения. Примеры таких фрагментов антител включают фрагмент F(ab')2 и фрагмент Fab'.
(3) Т-клетки киллеры, хелперные Т-клетки или популяция иммуноцитов, содержащая такие клетки
Настоящее изобретение также относится к Т-клетке киллеру, хелперной Т-клетке или популяции иммуноцитов, содержащей такие клетки, которые индуцируются путем стимуляции in vitro с использованием пептида по настоящему изобретению. Например, когда лимфоциты периферической крови или лимфоциты, инфильтрирующие опухоль стимулируют in vitro пептидом по настоящему изобретению, индуцируются активированные Т-клетки, демонстрирующие реакционную способность в отношении опухоли. Таким образом, активированные Т-клетки могут эффективно использоваться для адоптивной иммунотерапии рака. Более того, пептид по настоящему изобретению имеет возможность экспрессироваться в дентдритных клетках, которые являются мощными антиген-презентирующими клетками in vivo или in vitro, и дендритные клетки, экспрессирующие антигенный пептид затем вводят для индукции иммунного ответа на опухоли.
Предпочтительно, Т-клетки киллеры, хелперные Т-клетки или популяция иммуноцитов, содержащая такие клетки, могут быть индуцированы путем стимуляции ex vivo или in vitro с использованием пептида по настоящему изобретению и иммуностимулятора. Примеры такого иммуностимулятора, используемого в настоящем изобретении, включают Т-клеточный фактор роста и цитокин.
Полученные таким образом Т-клетки киллеры, хелперные Т-клетки или популяцию иммуноцитов, содержащую такие клетки, переносят в организм таким образом, чтобы опухоль могла быть суппрессирована и чтобы можно было предупредить и/или лечить злокачественную опухоль.
Далее, используя пептид по настоящему изобретению, можно получить Т-клетки киллеры, хелперные Т-клетки или популяцию иммуноцитов, содержащую такие клетки, которые способы подавлять рост опухоли, как описано выше. В связи с этим, настоящее изобретение относится к клеточному культуральному раствору, содержащему Т-клетки, реационноспособные в отношении опухоли, и пептид по настоящему изобретению. Используя такой клеточный культуральный раствор, могут быть получены Т-клетки киллеры, хелперные Т-клетки или популяция иммуноцитов, содержащая такие клетки, которые способны подавлять рост опухоли. Более того, настоящее изобретение также относится к клеточному культуральному набору для получения Т-клеток киллеров, хелперных Т-клеток или популяции иммуноцитов, содержащей такие клетки, который содержит вышеупомянутый клеточный культуральный раствор и флакон для клеточной культуры.
(4) Лекарственное средство по настоящему изобретению для лечения и/или профилактики опухоли (противораковая вакцина)
Поскольку пептид по настоящему изобретению способен индуцировать Т-клетки киллеры, специфичные к злокачественным клеткам, его можно предложить в качестве средства для лечения и/или профилактики злокачественных опухолей. Например, бактерии, такие как BCG (Bacillus Calmette-GuErin), которые были трансформированы рекомбинантной ДНК, полученной путем внесения гена, кодирующего пептид по настоящему изобретению, в подходящий вектор, или вирусы, такие как вирус коровьей оспы, в геном которого ДНК, кодирующая пептид по настоящему изобретению, была включена, могут эффективно использоваться в качестве живой вакцины для лечения и/или профилактики злокачественных опухолей человека. Следует отметить, что доза и способ введения противораковой вакцины такие же, что и дозы и способы введения в случае обычной противооспенной вакцинации или вакцинации BCG.
Другими словами, ДНК, кодирующая пептид по настоящему изобретению (которая используется как есть, или в форме плазмидной ДНК, встроенной в вектор экспрессии), или рекомбинантный вирус или рекомбинантная бактерия, содержащая вышеупомянутую ДНК, можно вводить в качестве противораковой вакцины млекопитающим, в том числе людям, непосредственно или в диспергированном в адъюванте виде. Подобным образом, пептид по настоящему изобретению также можно вводить в качестве противораковой вакцины в диспергированном в адъюванте виде.
Примеры адъюванта, используемого в настоящем изобретении, включают в себя неполный адъювант Фрейнда, BCG, димиколат трегалозы (TDM), липополисахарид (LPS), алюминиевый адъювант и кремниевый адъювант. С точки зрения способности индуцировать антитела, предп