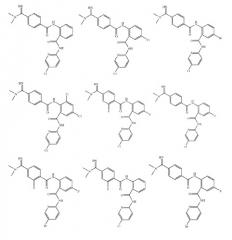
Стандартные лекарственные препараты и способы лечения тромбоза пероральным введением ингибитора фактора ха
Иллюстрации
Показать всеГруппа изобретений относится к медицине и предназначена для ингибирования коагуляции крови у пациента-человека. Применяют бетриксабан или его фармацевтически приемлемые соли. Совокупная суточная доза от 0,01 до 2,0 мг/кг. Группа изобретений позволяет воздействовать на ингибирование образования тромбина и анти-Ха активность. 2 н. и 9 з.п. ф-лы, 6 табл., 12 ил., 9 пр.
Реферат
Перекрестная ссылка на родственные заявки
По данной заявке испрашивается приоритет согласно 35 U.S.A. § 119(e) на основании предварительных патентных заявок US № 60/873792, поданной 8 декабря 2006 г., и US № 60/947629, поданной 2 июля 2007 г., которые включены в настоящее описание в полном объеме.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Область изобретения
Данное изобретение относится к способам ингибирования коагуляции с использованием конкретной дозы ингибитора фактора Ха. Изобретение также относится к анализу, который позволяет определять образование тромбина в крови, чтобы оценить антитромботическую активность испытуемого соединения.
Уровень техники
Гемостаз, остановка кровотечения, происходит в результате хирургического вмешательства или за счет физиологических свойств вазоконстрикции и коагуляции. Хотя и тромбоциты, и коагуляция крови вовлечены в восстанавливающий гемостаз и в тромботические заболевания, в основном конкретные компоненты каскада коагуляции являются ответственными за амплификацию и ускорение процессов, вовлекаемых в агрегацию тромбоцитов и отложение фибрина, которые являются главными событиями в тромбозе и гемостазе.
Образование сгустка вызывает превращение фибриногена в фибрин, который полимеризуется в сетчатую структуру для восстановления гемостаза после повреждения. Подобный процесс приводит к закупоренным кровеносным сосудам при тромботических заболеваниях. Превращение фибриногена в фибрин катализируется тромбином, конечным продуктом ряда реакций в каскаде коагуляции крови. Тромбин также играет ключевую роль в активации тромбоцитов, внося тем самым свой вклад в тромбоз в условиях как артериального, так и венозного кровяного потока. По этим причинам теоретически допустимо, что эффективное регулирование тромбина может приводить к эффективному регулированию тромбоза. Некоторые классы применяемых в настоящее время антикоагулянтов непосредственно или косвенно воздействуют на тромбин (например, нефракционированные гепарины, низкомолекулярные гепарины, гепариноподобные соединения, пентасахарид и варфарин). Непосредственному или косвенному ингибированию активности тромбина уделяется главное внимание при клинических разработках различных антикоагулянтов (обзор, выполненный Eriksson and Quinlan, Drugs 11: 1411-1429, 2006).
Протромбин, предшественник тромбина, превращается в активный фермент фактором Ха (fXa). Локализованная активация генерации тканевый фактор/опосредуемый фактором VIIa фактор Ха амплифицируется комплексом фактор IXa/фактор VIIIa и ведет к сборке протромбиназы на активированных тромбоцитах. Фактор Ха как часть комплекса протромбиназы является единственным ферментом, ответственным за продолжительное образование тромбина в сосудистой системе. Фактор Ха является серин-протеазой, активированной формой его предшественника фактора Х, и членом связывающих ион кальция, содержащих гамма-карбоксиглутаминовую кислоту (GLA), зависимых от витамина К и участвующих в коагуляции крови факторов. В отличие от тромбина, который действует на различных белковых субстратах, включая фибриноген и рецепторы PAR (активируемые протеазой рецепторы, Coughlin, J. Thrombosis Haemostasis 3: 1800-1814, 2005), фактор Ха, по-видимому, имеет единственный физиологический субстрат, а именно протромбин. Так как одна молекула фактора Ха может быть способна генерировать более чем 1000 молекул тромбина (Mann, et al., J. Thrombosis Haemostasis 1: 1504-1514, 2003), непосредственное ингибирование фактора Ха, как путь косвенного ингибирования образования тромбина, может быть эффективной антикоагулянтной стратегией. Это суждение основано на ключевой роли протромбиназы в синтезе тромбина и на том факте, что ингибирование протромбиназы будет иметь явное воздействие на все пути агрегации тромбоцитов и свертывания крови.
Активированные протеазы, такие как фактор VIIa, фактор IXa или фактор Xa, сами по себе имеют слабую протеолитическую активность. Однако их сборка в зависимые от кофактора, связанные с мембраной комплексы значительно повышает их каталитические эффективности. Этот эффект наиболее драматичен для фактора Ха, когда эффективность увеличивается множителем 105 (Mann, et al., Blood 76(1):1-16, 1990). Благодаря более высокой концентрации зимогенов, присутствующих в крови (1,4 мкМ протромбина против 150 нМ фактора Ха), и кинетике активации меньшее количество фактора Ха, чем требуется для ингибирования тромбина, необходимо для достижения антикоагулянтного эффекта. Косвенное подтверждение гипотезы превосходства фактора Ха в качестве терапевтической мишени по сравнению с тромбином может быть также найдено в клинических исследованиях по предотвращению тромбоза глубоких вен. Фондапаринукс, зависимый от антитромбина III ингибитор фактора Ха, превосходит эноксапарин (низкомолекулярный гепарин, который ингибирует и тромбин, и фактор Ха), как было доказано в четырех широких исследованиях по ортопедической хирургии (Turpie, et al., Archives Internal Medicine 162(16):1833-1840, 2002). Следовательно, подтверждено, что соединения, которые избирательно ингибируют фактор Ха, могут быть применимы в качестве диагностических агентов in vitro или для терапевтического введения при некоторых тромботических расстройствах, см., например, WO 94/13693.
Сущность изобретения
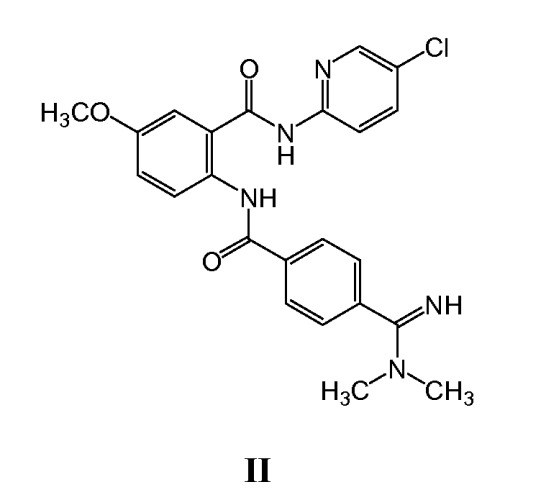
Сравнительное моделирование степени изменений активности протромбиназы до уровней антитромботической эффективности привело к обнаружению терапевтической активности ингибиторов фактора Ха в отношении людей. Данное изобретение относится к способу ингибирования коагуляции у пациента-человека с использованием ингибирующего коагуляцию количества ингибитора фактора Ха. Конкретно, перорально доступные непосредственные ингибиторы фактора Ха эффективны для ингибирования коагуляции у пациента-человека, когда их вводят пациенту в совокупном суточном количестве между около 0,01 и около 2,0 миллиграммов на килограмм на основе общей массы пациента ("мг/кг"). Предполагается, что такая доза будет эффективной для любого соединения, которое специфически ингибирует фактор Ха, и особенно эффективна для ингибиторов фактора Ха формул I, II, III, IV или V, которые описаны ниже.
Изобретение также относится к способу определения статуса коагуляции у пациента. Предполагается, что этот способ определения статуса коагуляции может быть использован для испытания многих различных классов антикоагулянтов в дополнение к ингибиторам фактора Ха.
В одном аспекте изобретения способ содержит введение пациенту ингибирующего коагуляцию количества соединения формулы I:
где
А выбран из таких групп, как
(а) С1-С6-алкил;
(b) С3-С8-циклоалкил;
(c) -N(R1,R2), N(R1,R2)-С(=NR3)-, N(R1,R2)-С(=NR3)-N(R4)-, R1-С(=NR3)-, R1-С(=NR3)-N(R4)-;
(d) фенил, который независимо замещен 0-2 заместителями R;
(e) нафтил, который независимо замещен 0-2 заместителями R, и моноциклическая или конденсированная бициклическая гетероциклическая кольцевая система, имеющая от 5 до 10 атомов в кольце, где 1-4 атома кольца кольцевой системы выбраны из N, O и S и где кольцевая система может быть замещенной 0-2 заместителями R;
R выбран из
Н, галогена, -CN, -CO2R1, -C(=O)-N(R1,R2), -(CH2)m-CO2R1, -(CH2)m-C(=O)-N(R1,R2), -NO2, -SO2N(R1,R2), -SO2R1, -(CH2)m-NR1,R2, -(CH2)m-C(=NR3)-R1, -(CH2)m-C(=NR3)-N(R1,R2), -(CH2)m-N(R4)-C(=NR3)-N(R1,R2), -(CH2)m-NR1-группы, прикрепленной к 3-6-членному гетероциклическому кольцу, содержащему 1-4 гетероатома, выбранных из N, O и S, -С1-4 алкила, -С2-6 алкенила, -С2-6 алкинила, -С3-8 циклоалкила, -С0-4 алкил-С3-8 циклоалкила, -CF3, OR2 и 5-6-членной гетероциклической системы, содержащей 1-4 гетероатома, выбранных из N, O и S, где 1-4 атома водорода гетероциклической системы могут быть независимо заменены заместителем, выбранным из группы, состоящей из таких заместителей, как галоген, -С1-4 алкил, -С1-4 алкил-CN, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил и -NO2;
m представляет собой целое число 0-2;
R1, R2, R3 и R4 независимо выбраны из группы, состоящей из таких заместителей, как Н, -OR5, -N(-R5,-R6), -С1-4 алкил, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил, -С0-4 алкилфенил и -С0-4 алкилнафтил, где 1-4 атома водорода на кольцевых атомах фенильной и нафтильной частей молекулы могут быть независимо заменены заместителем, выбранным из группы, состоящей из таких заместителей, как галоген, -С1-4 алкил, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил, -CN и -NO2; или R1 и R2, или R2 и R3, взятые вместе, могут образовывать 3-8-членный циклоалкил или гетероциклическую кольцевую систему, где гетероциклическая кольцевая система может иметь от 3 до 10 кольцевых атомов с 1-2 кольцами в кольцевой системе и содержать 1-4 гетероатома, выбранных из N, O и S, где 1-4 атома водорода гетероциклической кольцевой системы могут быть независимо заменены заместителем, выбранным из группы, состоящей из таких заместителей, как галоген, С1-4 алкил, -CN, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил и -NO2;
R5 и R6 независимо выбраны из группы, состоящей из таких заместителей, как
Н, -С1-4 алкил, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил, -С0-4 алкилфенил и -С0-4 алкилнафтил, где 1-4 атома водорода на кольцевых атомах фенильной и нафтильной частей молекулы могут быть независимо заменены заместителем, выбранным из группы, состоящей из таких заместителей, как галоген, -С1-4 алкил, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил, -CN и -NO2; или R5 и R6, взятые вместе, могут образовывать 3-8-членный циклоалкил или гетероциклическую кольцевую систему, где гетероциклическая кольцевая система может иметь от 3 до 10 кольцевых атомов с 1-2 кольцами в кольцевой системе и содержать 1-4 гетероатома, выбранных из N, O и S, где 1-4 атома водорода гетероциклической кольцевой системы могут быть независимо заменены заместителем, выбранным из группы, состоящей из таких заместителей, как галоген, -С1-4 алкил, -CN, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил и -NO2;
Q представляет заместитель, выбранный из группы, состоящей из таких заместителей, как
непосредственная связь, -СН2-, -С(=О)-, -О-, -N(R7)-, -N(R7)СН2-, -CH2N(R7)-, -С(=NR7)-, -С(=О)-N(R7)-, -N(R7)-С(=О)-, -S-, -SO-, -SO2-, -SO2-N(R7)- и -N(R7)-SO2-;
R7 выбран из группы, состоящей из таких заместителей, как
Н, -С1-4 алкил, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил, -С0-4 алкиленфенил и -С0-4 алкиленнафтил, где 1-4 атома водорода на кольцевых атомах фенильной и нафтильной частей молекулы могут быть независимо заменены заместителем, выбранным из группы, состоящей из таких заместителей, как галоген, -С1-4 алкил, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил, -CN и -NO2;
D представляет непосредственную связь или заместитель, выбранный из группы, состоящей из таких заместителей, как
(а) фенил, который независимо замещен 0-2 заместителями R1a;
(b) нафтил, который независимо замещен 0-2 заместителями R1a, и
(c) моноциклическая или конденсированная бициклическая гетероциклическая кольцевая система, имеющая от 5 до 10 атомов в кольце, где 1-4 атома кольца кольцевой системы выбраны из N, O и S и где кольцевая система может быть замещенной 0-2 заместителями R1a;
R1a выбран из
галогена, -С1-4 алкила, -С2-6 алкенила, -С2-6 алкинила, -С3-8 циклоалкила, -С0-4 алкилен-С3-8 циклоалкила, -CN, -NO2, -(CH2)n-NR2a,R3a, -(CH2)n-CO2R2a, -(CH2)n-CONR2aR3a, -SO2NR2aR3a), -SO2R2a, -CF3, -OR2a и 5-6-членной ароматической гетероциклической системы, содержащей 1-4 гетероатома, выбранных из N, O и S, где 1-4 атома водорода ароматической гетероциклической системы могут быть независимо заменены заместителем, выбранным из группы, состоящей из таких заместителей, как галоген, -С1-4 алкил, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил, -CN и -NO2;
R2a и R3a независимо выбраны из группы, состоящей из таких заместителей, как
Н, -С1-4 алкил, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил, -С0-4 алкиленфенил и -С0-4 алкиленнафтил, где 1-4 атома водорода на кольцевых атомах фенильной и нафтильной частей молекулы могут быть независимо заменены заместителем, выбранным из группы, состоящей из таких заместителей, как галоген, -С1-4 алкил, -С2-6 алкенил, -С2-6 алкинил, -С3-8 циклоалкил, -С0-4 алкилен-С3-8 циклоалкил, -CN и -NO2;
n представляет собой целое число 0-2;
Е представляет непосредственную связь или заместитель, выбранный из группы, состоящей из таких заместителей, как
-С1-2 алкилен, -О-, -S-, -SO-, -SO2-, -С0-1 алкилен-С(=О), -С0-1 алкилен-С(=О)-N(-R8)-С0-1 алкилен-, -С0-1 алкилен-N(R8)-С(=О)-С0-1 алкилен-, -N(-R8)-С(=О)-N(-R8)- и С0-1 алкилен-N(-R8)-;
R8 выбран из группы, состоящей из таких заместителей, как
Н, -С1-4 алкил, -С0-4 алкиленарил, -С0-4 алкиленгетероарил, -С1-4 алкилен-С(=О)-ОН, -С1-4 алкилен-С(=О)-О-С1-4 алкил и -С1-4 алкилен-С(=О)-N(-R2b,-R3b);
R2b и R3b независимо выбраны из группы, состоящей из таких заместителей, как
Н, -С1-4 алкил, -С0-4 алкилен-арил, -С0-4 алкилен-гетероциклическая группа, и R2b и R3d вместе с атомом N, к которому они присоединены, могут образовывать 5-8-членное гетероциклическое кольцо, содержащее 1-4 гетероатома, выбранных из N, O и S, где гетероциклическое кольцо может быть замещенным 0-2 группами R1c;
R1c выбран из группы, состоящей из таких заместителей, как
галоген, -С1-4 алкил, -CN, -NO2, -C(=O)-N(-R2c,-R3c), -C(=O)- OR2c, -(CH2)q-N(-R2c,-R3c), -SO2-N(-R2c,-R3c), -SO2R2c, -CF3 и -(CH2)q-OR2c,
R2c и R3c независимо выбраны из группы, состоящей из таких заместителей, как
Н, -С1-4 алкил и -С1-4 алкилен-арил;
q представляет собой целое число 0-2;
G выбран из группы, состоящей из таких заместителей, как
(а) С2 алкенил или С3-8 циклоалкенил, где точками присоединения алкенила и циклоалкенила являются атомы углерода алкенила и где -С2 алкенил или -С3-8 циклоалкенил замещены 0-4 группами R1d;
(b) фенильная группа, где кольцевые атомы углерода фениленовой группы замещены 0-4 группами R1d;
(с) 3-8-членная гетероциклическая кольцевая система, содержащая 1-4 гетероатома, выбранных из N, O и S, где 0-2 атома кольца могут быть замещены 0-4 группами R1d; и
(с) 8-10-членная конденсированная гетероциклическая бициклическая кольцевая система, содержащая 1-4 гетероатома, выбранных из N, O и S, где 0-2 атома кольца конденсированной бициклической кольцевой системы могут быть замещены 0-4 группами R1d;
R1d выбран из группы, состоящей из
Н, галогена, -С1-6 алкила, арила, -CN, -NO2, -(CH2)0-6-NR2dR3d, -SO2NR2dR3d, -SO2R2d, -CF3, -(CH2)0-6-OR2d, -О-(CH2)1-6OR2d, -О-(CH2)1-6-С(=О)-O-R2d, -О-(CH2)1-6-С(=О)-N(R2d,R3d), -N(R5a)-(CH2)1-6-OR2d, -N(R5a)-(CH2)1-6-N(R2d,R3d), -С(=О)-N(R2d,R3d), -N(R5a)-(CH2)1-6-С(=О)-N(R2d,R3d), -N(-(CH2)1-6-OR2d)2, -N(R5a)-(CH2)1-6-OR2d, -N(R5a)-C(=O)-R2d, -N(R5a)-SO2-R2d, -(CH2)0-6-С(=О)-O-R2d, -(CH2)0-6-С(=О)-N(R2d,R3d), -(CH2)0-6-С(=NR2d)-N(R3d,R4d), -(CH2)0-6-N(R5a)C(=NR2d)-N(R3d,R4d), -(CH2)0-6-N(R3d)C5-6-членного гетероциклического кольца, содержащего 1-4 гетероатома, выбранных из N, O и S и -(CH2)0-6-5-6-членное гетероциклическое кольцо, содержащее 1-4 гетероатома, выбранных из N, O и S;
R5a, R2d, R3d и R4d независимо выбраны из группы, состоящей из
Н, -С1-6 алкила, -С1-6 алкиларила, -CN, -NO2; карбоциклического арила, -CN, -NO2; или R2d и R3d, взятые вместе с атомами N, к которым они независимо присоединены, образуют 5-7-членное гетероциклическое кольцо, или R3d и R4d, взятые вместе с атомами N, к которым они присоединены, образуют 5-8-членное гетероциклическое кольцо, содержащее 1-4 гетероатома, выбранных из N, O и S;
J представляет непосредственную связь или выбран из группы, состоящей из
-N(-R9)-С(=О)-, -С(=О)-N(-R9)-, -O-, -S-, -SO-, -SO2-, -СН2-, -N(-R9)- и -N(-R9)-SO2-;
R9, независимо выбран из группы, состоящей из
Н, -С1-4 алкила, -С0-4 алкил-карбоциклического арила, -(CH2)0-4-5-6-членного гетероциклического кольца, содержащего 1-4 гетероатома, выбранных из N, O и S; -(CH2)1-6-С(=О)-О-С1-4 алкила и -(CH2)1-6-С(=О)-N(R6a,R6b);
R6a и R6b, каждый независимо, выбран из группы, состоящей из
Н и -С1-6 алкила;
Х выбран из группы, состоящей из таких заместителей, как
(а) фенил, замещенный 0-3 группами R1e;
(b) нафтил, замещенный 0-3 группами R1e, и
(c) 6-членная ароматическая гетероциклическая кольцевая система, содержащая 1-3 атома N и имеющая 0-3 атома в кольце, замещенные 0-3 группами R1e, и
(d) 8-10-членная конденсированная ароматическая гетероциклическая бициклическая кольцевая система, содержащая 1-4 гетероатома, выбранных из N, O и S, и 0-3 атома кольца конденсированной гетероциклической бициклической кольцевой системы замещены 0-3 группами R1e;
R1e независимо выбран из группы, состоящей из таких заместителей, как
галоген, -CF3, -С1-4 алкил, карбоциклический арил, -C0-2-алкилен-CN, -O-R2e, -C0-2-алкилен-С(=О)-О-R2e, -C0-2-алкилен-С(=О)-N(R2e,R3e), -C0-2-алкилен-NO2, -C0-2-алкилен-N(R2e,R3e), -C0-2-алкилен-SO2-N(R2e,R3e), -C0-2-алкилен-SO2-R2e, тригалогеналкил, -О-C0-2-алкилен-О-R2e, -C0-2-алкилен-О-R2e, -О-C1-4-алкилен-С(=О)-N(R2e,R3e), -О-C1-4-алкилен-С(=О)-О-R2e, -C0-2-алкилен-N(R2e)-С(=О)-R3e, -C0-2-алкилен-N(-R2e)-SO2-R3e, -CH2-N(R2e)-С(=О)-R3e, -CH2-N(R2e)-SO2-R3e, -(CH2)0-6-NR2eR3e, -С(=О)-N(R2e,R3e), -N(-(CH2)1-6-OR2e)2, -N(R10)-(CH2)1-6-OR2e, -N(R10)-С(=О)-R2e, -N(R10)-SO2-R2e, -С(=N(R10))-N(R2e,R3e) и -(CH2)0-6-5-6-членное гетероциклическое кольцо, содержащее 1-4 гетероатома, выбранных из N, O и S;
R10, R2e и R3e независимо выбраны из группы, состоящей из
Н, -С1-4 алкила, -С0-2 алкилен-O-R1g, -С0-2 алкилен-N(-R1g,-R2g), -С1-4 алкилен-карбоциклического арила, -С1-4 алкилен-гетероциклической группы, и R10 и R2e или R2e и R3e вместе с атомом N, к которому они присоединены, могут образовывать 5-8-членное гетероциклическое кольцо, содержащее 1-4 гетероатома, выбранных из N, O и S, которое может быть замещенным 0-2 группами R1g;
R1g и R2g независимо выбраны из группы, состоящей из таких заместителей, как
Н, галоген, -С1-4 алкил, карбоциклическая арильная группа, гетероциклическая группа, -CN, -С(=О)-N(R3g)R4g, -С(=О)-OR3g, -NO2, -(CH2)p-NR3gR4g, -SO2NR3gR4g, -SO2R3g, -CF3 и -(CH2)pOR3g;
p означает целое число 0-2 и
R3g и R4g независимо выбраны из группы, состоящей из таких заместителей, как
Н, С1-4 алкил и -C0-4-алкилен-карбоциклический арил;
или его фармацевтически приемлемой соли.
В одном варианте осуществления ингибирующее коагуляцию количество соединения ингибитора фактора Ха является совокупной суточной дозой между около 0,01 и около 2,0 мг/кг. В другом варианте осуществления ингибирующее коагуляцию количество соединения ингибитора фактора Ха является совокупной суточной дозой между около 0,1 и около 1,5 мг/кг. В еще одном варианте осуществления ингибирующее коагуляцию количество между около 0,4 и около 1,2 мг/кг.
В одном варианте осуществления ингибирующее коагуляцию количество вводят пациенту один раз в сутки. В другом варианте осуществления ингибирующее коагуляцию количество вводят пациенту за одни сутки, но дают порциями несколько раз в сутки, т.е. дважды ("BID") или три раза в сутки ("TID").
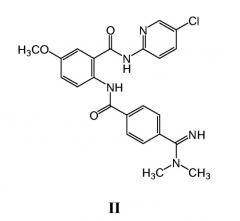
В одном варианте осуществления фармацевтически приемлемой солью соединения ингибитора фактора Ха является соль малеат. В другом варианте осуществления соединение формулы I является соединением формулы II:
или его фармацевтически приемлемой солью. В некоторых вариантах осуществления соль является малеатом. В одном варианте осуществления ингибирующее коагуляцию количество является совокупной суточной дозой между около 0,01 и около 2,0 мг/кг, или между около 0,1 и около 1,5 мг/кг, или между около 0,4 и около 1,2 мг/кг.
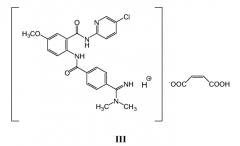
В другом варианте осуществления соединение, ингибитор фактора Ха, является солью малеатом, имеющим структуру формулы III:
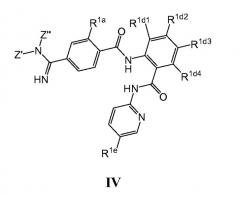
Изобретение также относится к стандартному препарату, содержащему фармацевтическую композицию, содержащую фармацевтически приемлемый носитель и ингибирующее коагуляцию количество соединения ингибитора фактора Ха формулы I, II, IV или V (как описано ниже) или его фармацевтически приемлемой соли или соли формулы III. В некоторых вариантах осуществления ингибирующее коагуляцию количество находится между около 0,01 и около 2,0 мг/кг. В других вариантах осуществления доза находится между около 0,1 и около 1,5 мг/кг или между около 0,4 и около 1,2 мг/кг.
Изобретение также относится к анализу in vitro для определения антитромботических свойств соединения in vivo. Анализ содержит следующие стадии:
а) введение испытуемого соединения в образец in vitro цельной крови или плазмы, содержащей тканевый фактор (TF) и обнаружимо меченный тромбиновый субстрат для формирования испытуемого образца;
(b) определение степени активности тромбина в испытуемом образце путем отслеживания расщепления обнаружимо меченного тромбинового субстрата в испытуемом образце как функцию времени;
с) определение степени активности тромбина в контрольном образце путем отслеживания расщепления обнаружимо меченного тромбинового субстрата в контрольном образце как функцию времени, где контрольный образец содержит цельную кровь или плазму, содержащую тканевый фактор (TF) и обнаружимо меченный тромбиновый субстрат;
d) сравнение степени активности тромбина в испытуемом образце и в контрольном образце, где степень активности тромбина в испытуемом образце является показателем того, что испытуемое соединение имеет in vivo антитромботическую активность.
Кровь и плазма могут быть предохранены от коагуляции или не предохранены от коагуляции.
В некоторых вариантах осуществления изобретения обнаружимо меченным тромбиновым субстратом является Z-Gly-Gly-Arg-AMC.
Краткое описание чертежей
На фиг. 1А показана корреляция образования тромбина с международным нормализованным отношением (INR) у пациентов, прошедших антикоагулянтную терапию варфарином. Образование тромбина измеряли на 10 минуте в образцах плазмы от пациентов, получающих стабильную терапию варфарином (n=137). Данные от пациентов, получающих стабильную терапию варфарином, представлены как квинтили результатов ЯМР. Планки погрешностей показывают стандартные ошибки.
На фиг. 1В показана корреляция образования тромбина с активированным парциальным тромбопластиновым временем (аРТТ) у пациентов, прошедших антикоагулянтную терапию эноксапарином. Образование тромбина плазмы измеряли у 16 пациентов, прошедших антикоагулянтную терапию эноксапарином. Единицы анти-fXa измеряли путем анализа COATEST LMW согласно инструкциям производителя. Группы сравнивали путем t-теста Стъюдента.
На фиг. 1С показана корреляция образования тромбина с аРТТ у пациентов, прошедших антикоагулянтную терапию нефракционированным гепарином (UFN). Образование тромбина плазмы измеряли у 15 пациентов. Единицы анти-fXa измеряли путем анализа COATEST LMW согласно инструкциям производителя. Группы сравнивали путем t-теста Стъюдента.
На фиг. 2 показано зависимое от дозы ингибирование тромбоза in vivo на модели обезьяны и дает основание полагать, что анализ in vitro позволяет судить об антитромботической активности in vivo. Оседание меченных индием тромбоцитов в камере в течение времени после инфузии носителя или бетриксабана. Число меченых тромбоцитов в камере нормализовали для подсчетов прединфузионных тромбоцитов для отдельных животных. Данные представляют среднее значение ± стандартное отклонение. Оседание тромбоцитов за 140 минут анализировали путем ANOVA с последующим тестом Dunnet. Доза 3 (26-38 нг/мл) давала значительное снижение по сравнению с контролем (Р<0,05) и доза 4 (54-88 нг/мл) давала значительное снижение по сравнению с контролем (величина Р<0,01).
На фиг. 3 показано зависимое от дозы ингибирование образования тромбина в цельной крови от здоровых людей-добровольцев. Цельную кровь обрабатывали бетриксабаном установленной концентрации (в нМ) перед началом испытания. Показаны относительные единицы флуоресценции, являющиеся результатом расщепления меченого тромбинового субстрата.
На фиг. 4А и 4В показано зависимое от дозы ингибирование образования тромбина в цельной крови от здоровых людей-добровольцев. Цельную кровь обрабатывали фондапаринуксом установленной концентрации (в нМ) перед началом испытания. Диапазон концентрации фондапаринукса, изображенный на фиг. 4В, соответствует уровням терапевтической антикоагуляции, применяемым в ортопедической хирургии и у пациентов с острым коронарным синдромом. Показаны относительные единицы флуоресценции, являющиеся результатом расщепления меченого тромбинового субстрата.
На фиг. 5 показаны данные анализов in vitro, проводимых с плазмой от здоровых людей-добровольцев, получавших перорально бетриксабан. Это более подробно обсуждается в примере 8.
На фиг. 6 показана процентная доля пациентов с венозной тромбоэмболией (VTE) и 95% доверительными интервалами для бетриксабана и эноксапарина, как определено путем исследования в примере 9 с применением односторонней венографии между днями 10 и 14 и для эноксапариновых исторических контролей (В и С) из исследований с использованием двусторонней венографии, проводимой между днями 10 и 14 после ортопедической хирургии (полная замена колена). Это более тщательно обсуждается в примере 9. Подробности исследования, соответствующего Enox B, сообщаются в Blood 102 (11); 2003. Подробности исследования, соответствующего Enox C, сообщаются в ссылке Lassen et al. (J. Thromb Haemostasis 2007, сентябрь 15).
На фиг. 7 показано уменьшение от базисной линии образования тромбина при лечении различными дозами бетриксабана и эноксапарина на день 2, при выписывании и флебограмме. Показано среднее изменение от базисной линии относительных единиц флуоресценции (± стандартная ошибка от среднего значения) при образовании тромбина плазмы, путем осмотра и лечения. Пациенты, выписанные на день 2, также представлены средней величиной на этот день исследования.
На фиг. 8 показаны изменения активности анти-fXa изменяющихся доз бетриксабана и эноксапарина на день 2, при выписывании и при флебограмме. Показано среднее значение (± стандартная ошибка от среднего значения) активности анти-fXa (ед./мл), как измерено гепариновым анализом Coatest LMW, путем осмотра и лечения. Поддающийся определению предел анти-fXa был 0,05 ед./мл; величины ниже поддающегося определению предела были установлены до 0,025. Пациенты, выписанные на день 2, также представлены средней величиной на этот день исследования.
На фиг. 9 показана концентрация бетриксабана в плазме (нг/мл) изменяющихся доз бетриксабана на день 2, при выписывании и при флебограмме.
Подробное описание изобретения
Прежде чем будут описаны композиции и способы, должно быть понятно, что изобретение не ограничивается описанными конкретными методиками, протоколами, клеточными линиями, анализами и реагентами, так как они могут изменяться. Следует также понимать, что используемая здесь терминология предназначается для описания конкретных вариантов осуществления данного изобретения и не предназначается для какого-либо ограничения сферы действия данного изобретения, которая сформулирована в прилагаемой формуле изобретения.
Если не определено иначе, все используемые здесь технические и научные термины имеют те же значения, которые обычно понятны специалисту в области техники, к которой данное изобретение принадлежит. Хотя любые способы и материалы, подобные или эквивалентные тем, которые описаны здесь, могут быть использованы при применении на практике или испытании данного изобретения, теперь будут описаны предпочтительные способы, устройства и материалы. Все технические и патентные публикации, цитируемые здесь, приобщены ссылкой во всей их полноте. Ничто здесь не должно быть истолковано как допущение, что изобретению не дано право датировать более ранним числом такое раскрытие на основании предшествующего изобретения.
При осуществлении на практике данного изобретения будут использованы, если не указано иное, традиционные методики тканевой культуры, иммунологии, молекулярной биологии, клеточной биологии и рекомбинантной DNA, которые относятся к компетенции специалиста. См., например, Sambrook and Russell eds. (2001) Molecular Cloning: A Laboratory Manual, 3rd edition; the series Ausubel et al. eds. (2007) Current Protocols in Molecular Biology; the series Methods in Enzymology (Academic Press, Inc., N.Y.); MacPherson et al. (1991) PCR 1: A Practical Approach (IRL Press at Oxford University Press); MacPherson et al. (1995) PCR 2: A Practical Approach; Harlow and Lane eds. (1999) Antibodies, A Laboratory Manual; Freshney (2005) Culture of Animal Cells: A Manual of Basic Techique, 5th edition; Gait ed. (1984) Oligonucleotide Synthesis; U.S. Patent No. 4,683,195; Hames and Higgins eds. (1984) Nucleic Acid Hybridization; Anderson (1999) Nucleic Acid Hybridization; Hames and Higgins eds. (1984) Transcription and Translation; Immobilized Cells and Enzymes (IRL Press (1986)); Perbal (1984) A Practical Guide to Molecular Cloning; Miller and Calos eds. (1987) Gene Transfer Vectors for Mammalian Cells (Cold Spring Harbor Laboratory); Makrides ed. (2003) Gene Transfer and Expression in Mammalian Cells; Mayer and Walker eds. (1987) Immunochemical Methods in Cell and Molecular Biology (Academic Press, London); Herzenberg et al. eds (1996) Weir's Handbook of Experimental Immunology; Manipulating the Mouse Embryo: A Laboratory Manual, 3rd edition (Cold Spring Harbor Laboratory Press (2002)).
Все цифровые обозначения, например, рН, температуры, времени, концентрации и молекулярной массы, включая пределы, являются приближенными значениями, которые изменяются (+) или (-) приращениями 0,1. Следует понимать, что, хотя это и не всегда эксплицитно установлено, описанные здесь реагенты являются только примерными и их эквиваленты известны в технике.
1. Определения
В соответствии с данным изобретением и тем, как использованы здесь, следующие термины определены следующими значениями, если эксплицитно не установлено иное.
Используемая в описании и формуле изобретения форма единственного числа с артиклями "а", "an" и "the" имеет отношение и к множественному числу, если из контекста четко не следует иное. Например, термин "клетка" включает множество клеток, включая их смеси.
Используемый здесь термин "содержащий" или "содержит" предназначается для обозначения того, что композиции и способы включают упомянутые элементы, но не исключают другие. Выражение "состоящий по существу из", используемое здесь для определения композиций и способов, будет означать исключение других элементов какой-либо существенной значимости для комбинации для установленной цели. Так, композиция, состоящая по существу из элементов, которые определены здесь, не будет исключать следовые количества загрязняющих примесей после способа изоляции и очистки и фармацевтически приемлемые носители, такие как забуференный фосфатом физиологический раствор, консерванты и тому подобное. Выражение "состоящий из" будет означать исключение более чем следовых количеств элементов других ингредиентов и существенных стадий способа введения композиций по данному изобретению или стадий процесса получения композиции или достижения планируемого результата. Варианты осуществления, характеризуемые каждым из указанных переходных терминов, входят в сферу действия данного изобретения.
Термин "совокупная суточная доза" относится к количеству лекарства или соединения, вводимому в течение 24-часового периода.
Термин "испытуемый образец" или "раствор для анализа" содержит цельную кровь или плазму крови (предохраненные от свертывания или не предохраненные от свертывания), тканевый фактор ("TF"), обнаружимо меченный тромбиновый субстрат и испытуемое соединение. Раствор может также содержать некоторое количество подходящих растворителей, таких как диметилсульфоксид (DMSO). В одном варианте осуществления кровь или плазму в испытуемом образце не обрабатывают или не титруют с ферментами, включающими ферменты ядов рептилий, такими как Reptilase®. В другом варианте осуществления кровь или плазма не обогащены тромбоцитами.
Термин "тканевый фактор", или TF, означает фактор, который присутствует в субэндотелиальной ткани, тромбоцитах и лейкоцитах и является необходимым для инициирования образования тромбина из зимогенного протромбина. TF упоминается также как тромбопластин, фактор III или CD142. TF, используемый в способах по изобретению, - это предпочтительно рекомбинантный TF человека, такой TF коммерчески доступен от Dade Behring Pharmaceuticals или American Diagnostica, Inc. TF, испольуемый в анализах, может быть также эндогенным или сочетанием эндогенного и экзогенного.
Используемый здесь термин "испытуемое соединение" относится к непептидному соединению, имеющему молекулярную массу менее чем 1500 Дальтон. Этот термин также относится к малым гепариноидным и сахаридным частям молекул, имеющим молекулярную массу менее чем 5000 Дальтон.
Термин "контрольный образец" относится к испытуемому образцу или раствору для анализа, в которых отсутствует испытуемое соединение.
Термин "не предохраненная от коагуляции цельная кровь" относится к крови, отобранной у пациента, который не подвергался антикоагулянтной терапии антитромботическим агентом. Он также относится к крови от пациента, который мог подвергаться антикоагулянтной терапии, но какое-либо полезное воздействие или эффект больше не реализуется.
Термин "предохраненная от коагуляции цельная кровь" или "предохраненная от коагуляции плазма" относится к крови или плазме, взятой у пациентов, которые недавно подвергались антикоагулянтной терапии или проходят такое лечение в настоящее время. Он также относится к крови от людей-доноров, которую получают венепункцией и собирают в среду, содержащую экзогенно добавленный антикоагулянт, такой как цитрат, EDTA или гепарин.
Термин "обнаружимо меченный тромбиновый субстрат" относится к тромбиновому субстрату, который помечен чем-либо из хорошо известных меток. К таким меткам относятся, но без ограничения перечисленным, флуоресцентные метки, фосфоресцентные метки, хемилюминесцентные метки, электрохемилюминесцентные метки и радиоактивные метки. В одном варианте осуществления изобретения меченым субстратом является Z-Gly-Gly-Arg-AMC, коммерчески доступный от Bachem.
Термин "антитромботическая активность" относится к способности соединений ингибировать образование тромба с приемлемыми эффектами по классическим единицам измерения параметров коагуляции, тромбоцитов и функции тромбоцитов. Состояния, характеризуемые нежелательным тромбозом, включают те, которые вовлекают артериальную и венозную сосудистую сеть. Что касается артериальной сосудистой сети, аном